Обратная транскрипция вируса гепатита с
Вирусы гепатитов поражают прежде всего печень, почему болезнь и получила своё название : hepatitis (лат.) - воспаление печени . Путь передачи обоих вирусов - парентеральный , то есть через кровь и половым путём. Если раньше самой распространённой причиной заражения было переливание крови, то в настоящее время инфицирование чаще всего происходит в группах высокого риска (проститутки, наркоманы).

Какой из гепатитов опаснее - В или С? Ответить можно только по-одесски - оба.
Гепатит В встречается гораздо чаще протекает более остро, но чаще всего заканчивается без осложнений. Последнее мало утешает те 10% больных, у которых болезнь переходит в хроническое течение, а при хроническом гепатите, в свою очередь, в 1 % случаев развивается цирроз и первичный рак печени.
Гепатит С называют "убийцей с мягкими лапами". Протекая не столь остро, как гепатит В, он переходит в хронический процесс в 30-70% случаев. Цирроз печени развивается у 10-30% больных, велик процент первичного рака печени.

Рис.1 Расспространенность гепатита С
Специфического лечения гепатитов не существует, терапия интерфероном (при гепатите С), крайне дорогостояща и недостаточно эффективна.
Вирус гепатита С
Вирус гепатита С содержит однонитевую РНК и относится к семейству флавивирусов. Электроннооптических изображений вируса гепатита С не существует, это связано с низким содержанием вируса в крови. По понятным причинам не может быть и фотографий, сделанных с помощью светового микроскопа. Вирус идентифицирован и охарактеризован молекулярно-биологическими методами.
Однонитевая РНК вируса содержит около 10.000 нуклеотидов. Идентифицированы три структурных белка: структурный белок нуклеокапсида (белок C), а также - мембранный (белок М) и поверхностный (белок E). Белки обладают сходными антигенными свойствами, поэтому их общим маркером являются иммуноглобулины анти-HCV-core-Ig . Выделены также 5 неструктурных (NS) белков, принимающие участие в репликации вируса.
Диагностика гепатита C

| Динамика специфического маркера вирусного гепатита С (суммарного анти-HCV) по стадиям инфекционного процесса |  |
Обнаружение антигена .
Непосредственное обнаружение антигена в крови не представляется возможным. Это обусловлено малым количеством вирусных частиц в сыворотке больного, не превышающим 10 5 /мл, что ниже предела чувствительности иммунологических методов.
Антитела .
В скрининговых исследованиях используют метод ИФА для определения суммарных (IgM+IgG) анти-HCV или анти-HCV класса IgG . В качестве подтверждающих тестов применяют иммуноблот на основе рекомбинантных и синтетических пептидов. Для уточнения стадии заболевания существуют тест-системы для определения анти-HCV класса IgM , а также анти-NS-IgG (антитела к не-структурным белкам) . В типичных случаях анти-HCV появляются в конце инфекционного процесса, т.е. через 4 - 9 мес. после заражения. Однако, в некоторых случаях антитела обнаруживались уже на 2 - 4 неделе после переливания заражённой крови , а в других случаях сероконверсия происходила через год после заражения . В соответствии с тенденцией гепатита С к хронизации - антитела обнаруживаются в течение длительного периода. Учитывая задержку в выработке антител, отрицательный результат исследования на анти-HCV не исключает инфекционности сыворотки. В то же время, все сыворотки, в которых была обнаружена РНК вируса гепатита С, оказались "заразными".
HCV-RNA (определение РНК вируса гепатита С ) .
РНК вируса гепатита С может быть обнаружена в сыворотке крови или в биоптате печени с помощью ПЦР с обратной транскрипцией. Теоретически чувствительность ПЦР позволяет определить одну (!) вирусную частицу в пробе. Существующие в настоящее время тест-системы ПЦР позволяют не только выявлять наличие вируса гепатита С, но и устанавливать его тип, определяя тем самым тактику и прогноз лечения.
Фазы течения заболевания гепатитом С и результаты лабораторного исследования
Острая фаза
Инкубационный период длится в среднем 6 - 8 нед. (от 2 - 4-х недель до 4 -6 месяцев и более). В этот момент регистрируется первый пик повышения печёночных ферментов. Сероконверсия наступает через 15 - 20 нед. (варьирует от 5 до 50 недель) от момента заражения. Анти-HCV класса IgM обнаруживают на 3 - 4 недели раньше, чем анти-HCV класса IgG. РНК вируса с помощью ПЦР определяется через 1 - 3 недели после инфицирования.
Критерии острой фазы:
Признаки благоприятного исхода острого гепатита С с выздоровлением
Желтуха является хорошим прогностическим признаком, а длительная циркуляция анти-HCV-IgM (более 2-х мес.) — плохим, свидетельствующим о возможной хронизации процесса.
Соответствует хроническому персистирующему гепатиту при полном или почти полном отсутствии клинических проявлений. Может продолжаться многие годы, в среднем 15-20 лет. Важно отметить существенные отличия хронического носительства вирусного гепатита В (ВГВ) и вирусного гепатита С (ВГС). Латентная (скрытая) стадия ГС является предстадией фазы реактивации инфекционного процесса с развитием клинических проявлений хронического гепатита. В то время как хроническое носительство HBsAg (при отсутствии повторного инфицирования), крайне редко предшествует обострению хронического ГВ.
Критерии латентной фазы:
Важнейшим критерием оценки хронического ВГС является динамический контроль за анти-HCV IgM. Они всегда регистрируются в фазу обострении
Критерии перехода в фазу реактивации:
Типичные сочетания маркеров гепатита C и соответствующее клиническое значение (диагноз)
Интерпретация результатов ИФА
Возможно, острый гепатит С
2. Стадия перехода в ХГС (латентную фазу)
2. Латентная фаза ХГС
1. Обострение в латентную фазу ХГС
2. Фаза реактивации
Критерии разграничения фаз заболевания необходимо рассматривать только в совокупности и в динамике, так как близкие результаты разовых исследований могут соответствовать как острой, так и хронической стадии инфекционного процесса. Важное значение имеет предположительный учёт давности болезни.
Вспомогательные методы диагностики и контроля лечения гепатитов.
Печень выполняет в организме многочисленные задачи, она - "рекордсмен" по количеству выполняемых функций. Инфекционные гепатиты, нарушая функции печени, вызывают изменения практически всех лабораторных показателей состояния организма. Некоторые из этих изменений неспецифичны, т. е. возникают и при других заболеваниях. Есть и признаки, характерные именно для вирусных гепатитов (ВГ). Так, возникающее при ВГ массивное повреждение клеток печени - гепатоцитов - влечёт за собой выход в кровь содержащихся в этих клетках ферментов. Содержание аланиламинотрансферазы ( АлАт ) и аспартатаминотрансферазы ( АсАт ) при остром гепатите возрастает в крови в десятки раз, причём преобладает возрастание АлАт - это характерный признак гепатита. Активность аминотрансфераз увеличивается ещё до возникновения желтухи - пожелтения кожных покровов и слизистых, что делает выявление АлАт и АсАт ценным диагностическим признаком. Нарушается также т.н. пигментный обмен - возрастает количество билирубина (именно его избыток, откладываясь в тканях, и даёт желтушность). Следует отметить, что при вирусных гепатитах возрастает, в основном, содержание т.н. прямого билирубина ; это отличает их от других заболеваний печени. В моче ещё в дожелтушном периоде увеличивается количество уробилиногена (которое легко определяется с помощью тест-полосок, что делает этот метод очень ценным для экспресс-диагностики в очагах вирусного гепатита).
При хронических гепатитах ценным методом является цитологическое исследование материала, полученного при биопсии печени. Этот метод позволяет оценить степень и характер повреждения клеток печени
Вирус гепатита В
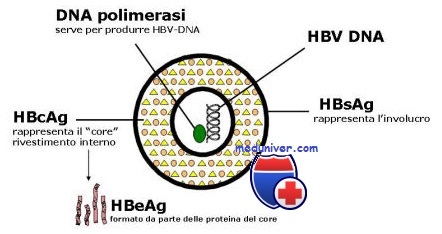
Вирус гепатита В является ДНК-содержащим вирусом, относится к семейству гепаднавирусов. Его диаметр- 42 nm.
Центральное положение занимает нуклеокапсид или "ядро" - "core". Нуклеокапсид имеет 27 nm в диаметре, в его состав входит т.н. "серцевинный антиген" HBcAg , а также - антиген HBeAg. Нуклеокапсид окружен оболочкой толщиной около 4 nm, белок которой назван "поверхностным" или HBsAg . Широко распространён синоним его названия - "австралийский антиген".
Иногда оболочка вирусной частицы (она же - поверхностный антиген HBsAg ) простирается в виде длинного "цоколя лампы" по одну сторону от нуклеокапсида (НК) . Поверхностный антиген производится в большом избытке, в крови инфицированных людей его нитевидные и сферические частицы обнаруживаются даже в отсутствие нуклеокапсида. Нитевидные частицы имеют различную длину, их средний диаметр 22nm. Нередко можно различить поперечную регулярную их исчерченность, не имеющую спирального характера.

 |
| Динамика специфических маркеров вирусного гепатита В |  |
Обнаружение антигена* .
HBsAg обнаруживается в крови через 2 - 8 недель после заражения и в большинстве случаев через 4 месяца после заражения исчезает из сыворотки. HBeAg появляется в острый период болезни в течение короткого промежутка времени. Его обнаружение при хроническом гепатите или циррозе печени свидетельствует о продолжающемся развитии и размножении вируса.
Антитела** .
Антитела к HBsAg ( Анти-HBs антитела) обычно появляются сыворотке крови после исчезновения HBsAg. Однако, в ряде случаев HBsAg перестает определяться раньше, чем появляются антитела. В этой ситуации необходимо протестировать сыворотку на наличие анти-НВс антител, которые появляются на ранней стадии заболевания. Диагноз острой инфекции может быть окончательно подтвержден при обнаружении анти-НВс антител класса IgM. Это необходимо для дифференциальной диагностики острой инфекции и хронического активного гепатита, сопровождающегося персистенцией вируса. Обнаружение анти-НВе антител является показателем наличия НВеAg.
HBV-ДНК (ДНК вируса гепатита В) *** :
Определение ДНК в сыворотке или ткани рекомендуется в тех случаях, когда нужно подтвердить наличие остаточного инфекционного процесса. Это бывает важно у больных, положительных по HBsAg, но отрицательных по НВеAg при наличии анти-НВс антител. Такие больные, вопреки существовавшему до недавнего времени мнению - представляют инфекционную угрозу, т.е. заразны.
Среди вирусов, вызывающих гепатит у людей, HBV — единственный ДНК-содержащий вирус. Размер его генома всего 3,2 Кб, т. е. это мельчайший из ДНК-содержащих вирусов, вызывающих инфекционные заболевания у человека. Кольцевая ДНК вируса имеет двухцепочечную структуру лишь на протяжении части своей длины, тогда как значительный участок ДНК варьирующего размера остается одноцепочечным. Эндогенная ДНК-полимераза позволяет вирусу достраивать недостающий участок второй цепи из присутствующих в клетке нуклеотидов на основе вирусной матрицы.
Перед репликацией генома вирус синтезирует прегеном, представляющий собой полномерную одноцепочечную РНК-копию DNA HBV. Далее, используя эту РНК-копию в качестве матрицы, вирусная ДНК-полимераза (обратная транскриптаза) синтезирует ДНК-геном. Таким образом, HBV обладает главным свойством ретровирусов — способностью к обратной транскрипции. Полномерная прегеномная РНК выполняет также и вторую функцию: она служит матрицей для трансляции вирусных белков. Вирион состоит из белково-нуклеинового комплекса — нуклеокапсида, окруженного оболочкой — липопротеиновой мембраной.
Липиды оболочки представлены триглицеридами, фосфолипидами и холестерином, причем все они являются продуктами клетки хозяина. Нуклеокапсид имеет форму икосаэдра, присущую белку core (HBcAg) и содержит вирусную ДНК и полимеразу. Оболочка тесно связана с поверхностным (S-) антигеном (HBsAg) — трансмембранным белком, существующим в трех сходных формах. Все три формы белка являются продуктами одного гена, транслируемыми в S-OPC (открытую рамку считывания), но имеют три разных сайта начала трансляции (ATG). Общий стоп-кодон (ТАА) объясняет идентичность карбокситерминальной части всех трех форм белка.
Эти все формы, охарактеризованные пока неполностью и все вместе, называют поверхностным антигеном вируса гепатита В (HBsAg). HBsAg первоначально называли антигеном гепатита, или антигеном, связанным с гепатитом или австралийским антигеном.
Геном HBV содержит 4 взаимно перекрывающихся открытых рамки считывания. По конечным продуктам экспрессии 4 ОРС названы: S (поверхностные белки), Р (полимераза), С (core) и X. В участке генома S выделяют области S, преSl и преS2. Область S кодирует основную, наименьшую по размеру форму HBsAg, состоящую из 226 аминокислот. Это наиболее обильно экспрессируемый белок вириона, составляющий также основную часть сферических и тубулярных частиц. Аббревиатуру HBsAg иногда применяют в узком смысле именно для обозначения этого белка.
Важным элементом стабилизации его трехмерной структуры служат дисульфидные связи. HBsAg — важнейший антиген HBV, так как именно он содержит эпитопы, к которым вырабатывается защищающий от HBV иммунитет и служит основным компонентом коммерческих вакцин. Установлено, что присутствие в сыворотке одних только антител к HBsAg достаточно для защиты от HBV-инфекции [5, 10]. Средняя по размеру форма HBsAg кодируется областями S и preS2 и содержит дополнительные 55 аминокислот, а максимальная по размеру форма кодируется областями S, preS2 и preSl и содержит еще 119 или 108 аминокислот в зависимости от субтипа (генотипа) вируса. Мембрана ьириона содержит смесь всех трех форм HBsAg как в гликозилированной, так и негликозилированной форме. Известно 6 генотипов HBV, обозначаемых латинскими буквами A-F. В основе разделения HBV на различные генотипы лежат отличия в последовательности нуклеотидов S-гена в сегменте между позициями 256 и 796.
Белок core (HBcAg) и секретируемый е-белок (HBeAg) являются продуктами гена pre-core и core и имеют примерно 160 общих аминокислот. HBeAg представляет собой полипептидный фрагмент HBcAg, подвергшийся посттрансляционному процессингу. HBeAg экспрессирован также на поверхности гепатоцитов и, по-видимому, служит важной мишенью для механизмов иммунитета, разрушающих гепатоциты. HBeAg индуцирует иммунологигескую толерантность и, таким образом, связан с хронической инфекцией.
Он также способен модулировать репликацию HBV, супрессируя инкапсулирование прегеномной РНК в нуклеокапсиды. Корпускулярный нуклеокапсидный антиген (HBeAg) в свободной форме может быть обнаружен в ядрах инфицированных гепатоцитов. В сыворотке крови его выявляют только в частицах Дейна.
Помимо структурных и секретируемых белков вирус способен синтезировать различные неструктурные белки. Ген Р кодирует вирусную ДНК-полимеразу (обратную транскриптазу). Р-ОРС перекрывает все другие ОРС вируса ГВ. Ген X кодирует Х-антиген (HBxAg), белок, биологические функции которого пока еще охарактеризованы неполностью. Известно, однако, что он играет регуляторную роль в процессе размножения вируса и способен активировать транскрипцию ДНК вируса при помощи ряда клеточных промоторов.
Исследование для выявления возбудителя гепатита C (HCV), в ходе которого с помощью метода полимеразной цепной реакции в реальном времени (РТ-ПЦР) определяется наличие генетического материала (РНК) вируса в крови.
Вирус гепатита С (ВГС), качественное определение РНК.
Синонимы английские
Hepatitis С Virus, RNA, Blood, HCV RNA, Real-Time PCR, Qualitative.
Полимеразная цепная реакция с обратной транскрипцией в режиме реального времени.
Выявляет генотипы HCV: 1a, 1b, 2a, 2b, 2c, 2i, 3, 4, 5a, 6.
Специфичность определения: 100 %.
Чувствительность определения: 50 МЕ/мл.
Линейный диапазон концентраций РНК вируса гепатита С, определяемых тест-системой: 150-1*10^8 МЕ/мл.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Вирус гепатита С (HCV) – РНК-содержащий вирус из семейства Flaviviridae, который поражает печень. Он способен размножаться в клетках крови (нейтрофилах, моноцитах и макрофагах, В-лимфоцитах) и вызывать криоглобулинемию, болезнь Шегрена и В-клеточные лимфопролиферативные заболевания. HCV благодаря высокой мутационной активности может избегать воздействия защитных механизмов иммунной системы. Существует 6 генотипов и множество субтипов вируса, которые имеют разные значения для прогноза развития заболевания и эффективности противовирусной терапии.
Основной путь передачи инфекции – через кровь (препараты для переливания элементов крови и плазмы, донорские органы, нестерильные шприцы, иглы, инструменты для татуирования, пирсинга). Вероятно заражение при половом контакте и ребенка от матери во время родов, но это случается нечасто.
Острый вирусный гепатит, как правило, характеризуется бессимптомным течением и остается невыявленным в большинстве случаев. Только у 15 % инфицированных заболевание протекает остро – с тошнотой, ломотой в теле, отсутствием аппетита и потерей веса (редко сопровождается желтухой). У 60-85 % инфицированных развивается хроническая инфекция, что в 15 раз превышает частоту хронизации при гепатите В. Хронический вирусный гепатит С протекает с повышением печеночных ферментов и скудным проявлением симптомов. У 20-30 % больных заболевание приводит к циррозу печени, увеличивая риск развития печеночной недостаточности и гепатоцеллюлярной карциномы.
Выявление РНК HCV свидетельствует о размножении вируса в организме и помогает диагностировать заболевание. Генетический материал вируса можно обнаружить методом ПЦР через 10-12 дней после инфицирования – в этот период специфические антитела, которые образуются через несколько месяцев после заражения, отсутствуют и биохимические показатели функции печени находятся в пределах референсных значений. РНК вируса гепатита С с высокой специфичностью и чувствительностью определяют качественно или количественно. Благодаря качественному методу подтверждается факт инфицирования или гибели вируса. Это особенно важно в ранней диагностике вирусного гепатита у людей, подвергшихся риску заражения, а также при контроле за противовирусной терапией. При лечении альфа-интерфероном отсутствие РНК вируса через 24 недели после завершения терапии служит критерием ее эффективности.
Для чего используется исследование?
- Для раннего выявления вирусного гепатита С.
- Для дифференциальной диагностики гепатитов.
- Для контроля за эффективностью противовирусного лечения.
- Для мониторинга течения вирусного гепатита С.
- Для проверки донорской крови.
Когда назначается исследование?
- При сомнительных результатах серологического исследования.
- При обследовании людей из группы риска по заражению вирусным гепатитом С.
- Если ребенок родился от инфицированной матери.
- При симптомах гепатита и повышенных биохимических показателях функции печени.
- До лечения и в конце терапии, затем через 6 и 24 месяца наблюдения.
Что означают результаты?
Референсные значения: не обнаружено.
Причины положительного результата
Причины отрицательного результата
- Отсутствие вируса гепатита С в крови исследуемого.
Что может влиять на результат?
Причины ложноотрицательного результата:
- минимальная вирусная нагрузка крови (50 МЕ/мл);
- наличие в образце ингибиторов – химических и белковых субстанций, влияющих на различные компоненты ПЦР;
- присутствие в крови гепарина;
- высокий уровень криоглобулинов в крови.
- Само по себе наличие РНК вируса гепатита С при отсутствии изменений других лабораторных показателей не позволяет диагностировать инфекцию со стопроцентной уверенностью. При этом необходимо повторное выявление РНК вируса методом ПЦР и комплексная оценка всех исследований. При хроническом гепатите С концентрация вирусного РНК меняется волнообразно – положительные и отрицательные результаты могут чередоваться, что требует проведения биопсии печени для уточнения диагноза и тактики лечения.
- Прямой зависимости между активностью размножения вируса и изменением биохимических показателей функции печени нет.
Кто назначает исследование?
Литература
- Возианова Ж.И. Инфекционные и паразитарные болезни: В 3х т. - К.: Здоровье, 2000 – Т.1.: 600-690.
- Кишкун А.А. Иммунологические и серологические исследования в клинической практике. - М.:ООО МИА, 2006 – 471-476 с.
- Harrison's Principles of Internal Medicine. 16 th ed. NY: McGraw-Hill; 2005: 1822-1855.
- Lerat H, Rumin S, Habersetzer F, and others. In vivo tropism of hepatitis C virus genomic sequences in hematopoietic cells: influence of viral load, viral genotype, and cell phenotype. Blood. 1998 May 15;91(10):3841-9.PMID:9573022.
- Revie D, Salahuddin SZ. Human cell types important for hepatitis C virus replication in vivo and in vitro: old assertions and current evidence. Virol J. 2011 Jul 11;8:346. doi: 10.1186/1743-422X-8-346. PMID:21745397.
Вирус гепатита В — один из мельчайших оболочечных вирусов человека. Его вирион (частица Дейна) имеет сферическую форму диаметром 40—45 нм. Под электронным микроскопом в вирионах отчетливо видны сердцевина (кор, т.е. нуклеокапсид) и наружная липопротеиновая оболочка (суперкапсид) (рис. 2).
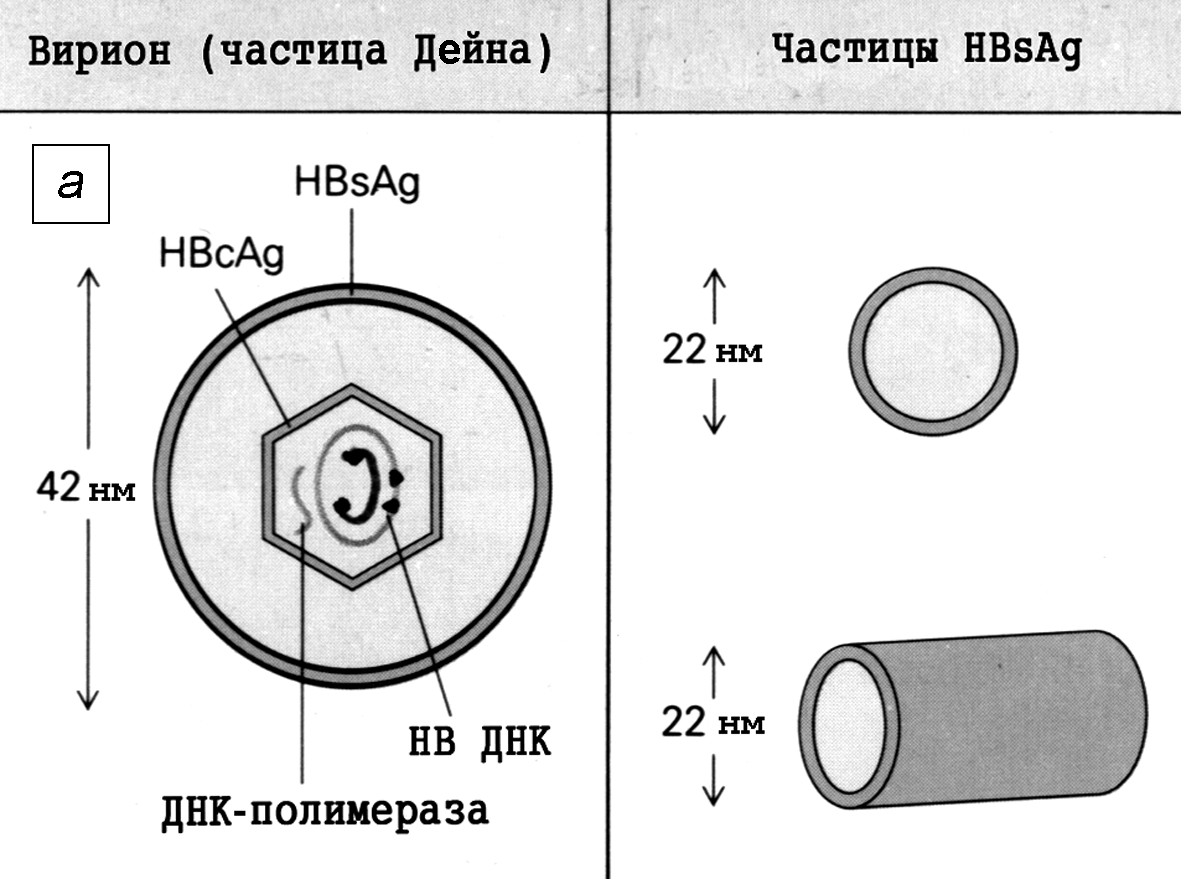
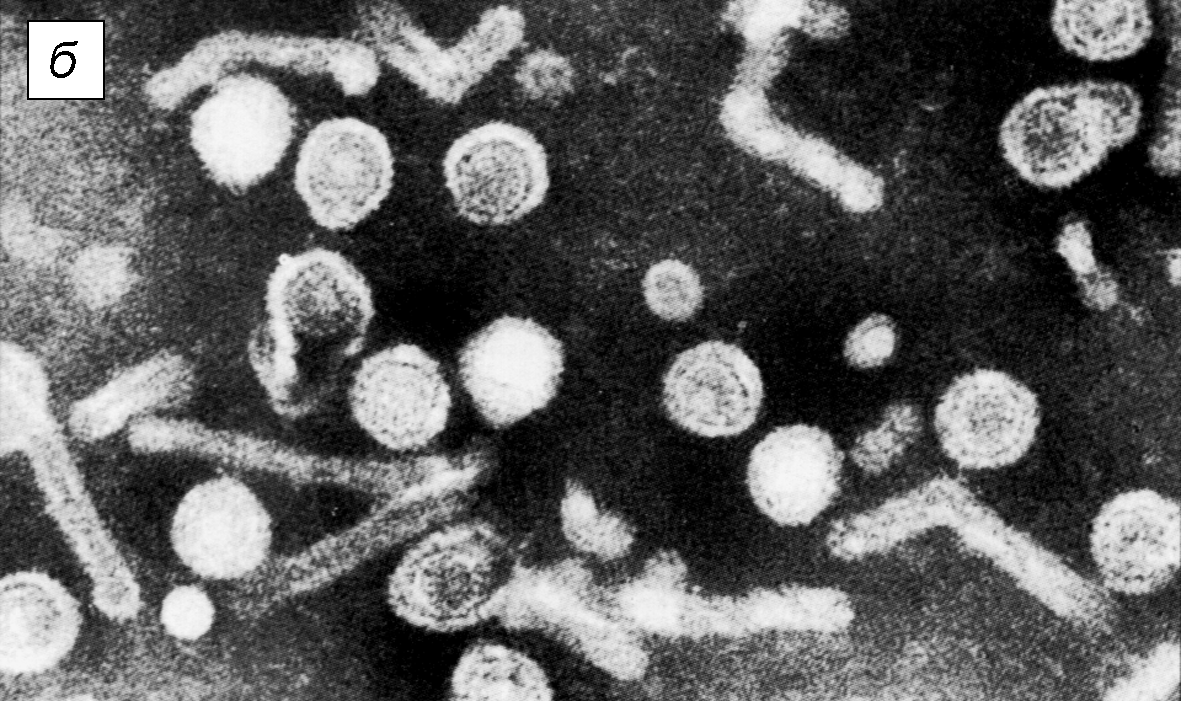
Рис. 2. Вирион вируса гепатита В (частица Дейна) и HВsAg-частицы:
а — принцип строения; б — электронограмма крови больного
Вирусные белки. Вирус обладает пятью белковыми антигенами: HBsAg, HbcAg, HBeAg, HBxAg и HBpol.
HBsAg (устар. австралийский антиген) — поверхностный антиген (s от англ. surface — поверхность). Обеспечивает избирательное прикрепление вируса к мембране гепатоцитов, возможно за счет связывания с полимеризованным сывороточным альбумином.
HBsAg cодержит протективные В-эпитопы и индуцирует синтез антител, блокирующих прикрепление вируса к рецепторам гепатоцитов. Синтезируется в избытке (особенно при интегративной инфекции — см. ниже) и в значительных количествах секретируется в кровь, где определяется не только в структуре вирионов, но и в виде свободных агрегатов (сферические частицы, филаменты), состоящих из S- и L-белков. Их количество во много раз превосходит число полноценных вирионов, достигая 10 12 в 1 мкл сыворотки (см. рис. 2).
По HВsAg-эпитопным особенностям дифференцируют четыре основных HBV-серовара, которые используются как эпидмаркеры. По меньшей мере один из эпитопов (a) является общим для всех штаммов вируса, что обеспечивает возможность универсальной диагностики, основанной на выявлении HВsAg в сыворотке, а также применение стандартной HВsAg-вакцины для профилактики гепатита В.
HВcAg, или кор-антиген — главный белок HBV-нуклеокапсида, или сердцевины (англ. core — сердцевина). Кодируется c-геном, к которому прилежит небольшой, но функционально значимый фрагмент ДНК — пре-c. От того, с какого участка пре-c начинается транскрипция мРНК, зависит качество и судьба НВсAg. Один из его вариантов входит в состав вирионного нуклеокапсида, другой (гидрофобный) включается в клеточные мембраны и служит объектом для распознания и атаки Т-лимфоцитами. В кровь не секретируется и в свободном состоянии не определяется.
HBeAg — важный для диагностики (и, по-видимому, для репликации вируса) продукт c-гена (англ. envelope — оболочка). Образуется в результате протеолиза (возможно, аутопротеолиза) кор-антигена, встроенного в клеточные мембраны. Отличается от последнего по В-эпитопам (т.е. к каждому из них образуются собственные антитела), но содержит общие с ним Т-эпитопы. Не входит в состав вириона, а выделяется в кровь, где его содержание коррелирует с активностью вирусной репликации.
HBхAg — неструктурный белок. Определяется в сыворотке и печени при высоком уровне вирусной репликации. Выполняет функции трансактиватора вирусных и клеточных генов, способствуя развитию патологического процесса в печени. Его производные определяются в мембране гепатоцитов почти у половины больных хроническим гепатитом, являясь объектом для цитотоксических Т-лимфоцитов. Полагают, что наряду с инсерционным мутагенезом (результат внедрения/инсерции вирусного генома в хромосомы клетки) HBxAg участвует в индукции злокачественного перерождения HBV-инфицированных гепатоцитов, активируя клеточные онкогены и блокируя антионкогенные (апоптозиндуцирующие) белки, в частности р53.
HBVpol (полимераза) — полифункциональный фермент, входящий в состав HBV-сердцевины. Продукт самого крупного, р-гена, перекрывающего s- и c-локусы. Обладает активностью ДНК-полимеразы, обратной транскриптазы и РНК-азы (см. ниже). Играет ключевую роль на всех этапах репликации вируса.
Геном. Геном гепаднавирусов устроен своеобразно. Он состоит из двух ковалентно незамкнутых нитей ДНК, одна из которых (плюс-нить) не достроена, т.е. короче другой (минус-нити) на 20—30%. Ликвидация этого дефекта является обязательным этапом репликации вируса и обеспечивается вирионной ДНК-полимеразой после проникновения вируса в ядро гепатоцитов. Каждому из главных вирусных белков соответствует открытая рамка считывания (фактически ген), но небольшой размер генома (3,2 кбайт, т.е. меньше, чем у любого из известных вирусов с двухспиральной ДНК) не позволяет синтезировать даже столь скромный набор антигенов без дополнительных ухищрений, нацеленных на увеличение генетической емкости ДНК. Это достигается путем транскрипции с перекрывающихся областей ДНК (перехлест генов) и сдвига рамок трансляции мРНК-транскриптов. Кроме того, синтезированные полипептиды подвергаются посттрансляционным модификациям (ограниченному протеолизу, гликозилированию), меняющим их структуру и функции.
Репликативная инфекция. Репликация HBV происходит необычно. Это единственный из ДНК-вирусов человека, который реплицируется с подключением механизма обратной транскрипции по схеме ДНК—РНК—ДНК (рис. 3). После достраивания в ядре дефектной ДНК-нити она используется клеточной РНК-полимеразой в качестве матрицы для синтеза полной РНК-копии — прегенома (pgRNA). Одновременно образуются и более короткие РНК, которые подвергаются трансляции, обеспечивая синтез вирусных белков. pgRNA транспортируется в цитоплазму и после объединения с капсидом переписывается в ДНК, т.е. подвергается обратной транскрипции. РНК разрушается, и на свободных участках ДНК строится вторая (дефектная) ДНК-нить.
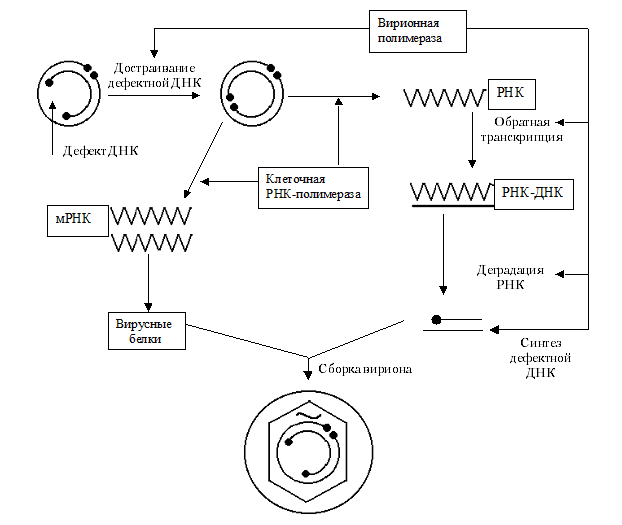
Рис. 3. Репликация вируса гепатита В. После вхождения в клетку ДНК-геном подвергается созреванию (достраивание дефектной ДНК) и транскрипции минус-нити в ядре гепатоцита. Короткие РНК-транскрипты транслируются в цитоплазме с образованием вирусных антигенов. Полный РНК-транскрипт включается в состав созревающего нуклеокапсида (кора) с образованием репликативных комплексов. Вслед за обратной транскрипцией прегеномной РНК следует синтез второй ДНК-нити, сборка и высвобождение вируса из инфицированной клетки
Все перечисленные этапы (достраивание дефектной ДНК-нити, обратная транскрипция, разрушение pgRNA, синтез дефектной ДНК-нити) обеспечиваются общим ферментом — вирионной полимеразой. Полифункциональность снижает точность ферментативных реакций. Весомость ошибок возрастает, если они (как в данном случае) допускаются при репликации. С этим, в частности, может быть связана высокая мутационная изменчивость HBV, которая накладывает серьезный отпечаток на взаимоотношения с хозяином. Механизм обратной транскрипции сближает гепаднавирусы с ретровирусами. По этой причине их даже предложено называть параретровирусами.
Процесс репликации заканчивается сборкой суперкапсида. Кор одевается наружной оболочкой, используя для этого внутриклеточные мембраны аппарата Гольджи с встроенными в них HВsAg (S, L и М), и высвобождается из клетки.
Интегративная инфекция. Кроме репликативной инфекции, которая ведет к воспроизведению вирионов, вирус гепатита В имеет в арсенале еще одну стратегию — он охотно встраивает свою ДНК в геном зараженной клетки, используя ее как прикрытие. Этот механизм, хорошо известный в вирусологии, носит название интегративной вирогении. Не обеспечивая репродукции (хотя такая возможность остается), он способствует длительному сохранению (персистенции) вируса в инфицированных клетках, что поддерживает его патогенетический потенциал. Экспрессия вирусных генов блокируется; исключение составляют s- и, по-видимому, x-гены. Транскрипция s-гена даже усиливается, если он попадает под контроль клеточных генов-промоторов. Образующийся в избытке HBsAg не накапливается в гепатоцитах, а в больших количествах выделяется в кровь. При хроническом гепатите репликативная и интегративная инфекции развиваются параллельно, но со временем верх берет интегративный компонент, который существенно влияет на развитие цирроза печени и первичной гепатомы.
Читайте также:
- Вирус пятнистости у растений
- Антикор анализы при гепатите с
- Вакцинация от гепатита а в таджикистане
- Рвота с кровью при ротавирусе
- Вакциной гриппозной инактивированной субъединичной совигрипп
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

