Механизм интеграции днк и рнк вирусов в геном клетки
1. Классификация и характеристика ДНК-геномных вирусов
2. Вирус папилломы человека. Характеристика. Онкогенность. Лабораторная диагностика
3. Вирус полиомы человека. Характеристика. Онкогенность
1. Классификация и характеристика ДНК-геномных вирусов
ДНК-содержащие вирусы – вирусы, геном которых представлен дезоксирибонуклеиновой кислотой и репликация идет посредством ДНК-зависимой ДНК-полимеразы, без использования промежуточного звена-посредника РНК.
Геномная ДНК этих вирусов может быть двуцепочечной или одноцепочечной и иметь линейную или кольцевую форму.
| ДНК-содержащие вирусы | Наличие суперкапсида | Размер вириона в нанометрах | Типовые представители |
| Аденовирусы | Отсутствует | 70-90 | Аденовирусы человека 42 типов |
| Гепаднавирусы | Имеется | 45-50 | Вирус гепатита В |
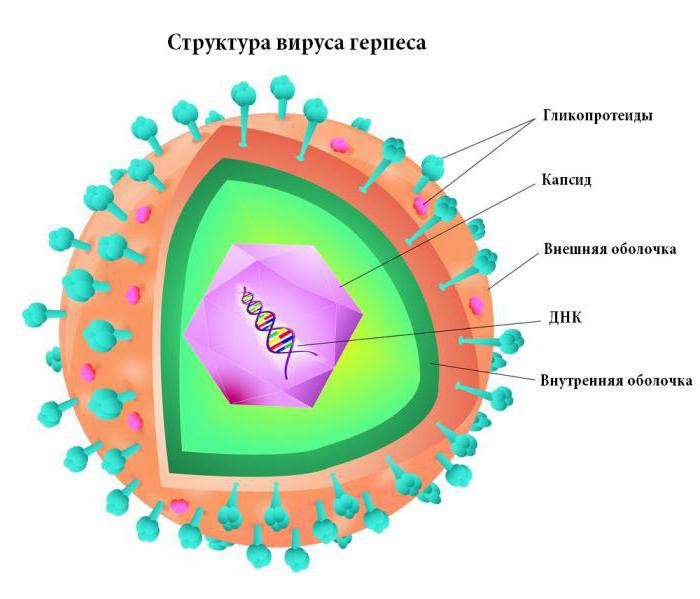
| Герпесвирусы | Имеется | 200 | Вирусы простого герпеса, цитомегалии, Эпстайна-Барр |
| Паповавирусы | Отсутствует | 45-55 | Вирусы папилломы, полиомы |
| Парвовирусы | Отсутствует | 18-26 | Аденоассоциированный вирус |
| Поксвирусы | Имеется | 130-240 | Вирусы осповакцины |
Геномы большинства ДНК-содержащих вирусов (за исключением поксвирусов) транскрибируются в ядре клетки-хозяина с помощью клеточной РНК-полимеразы II . Синтез и процессинг мРНК у этих вирусов практически полностью осуществляется за счет клеточных механизмов (несколько вирусных белков участвуют только в регуляции транскрипции).
У многих ДНК-содержащих вирусов транскрипция происходит в три этапа, во время которых избирательно считываются сверхранние, ранние и поздние гены.
Нуклеокапсиды герпесвирусов проникают в цитоплазму вместе с белками матрикса, затем этот комплекс транспортируется вдоль микротрубочек к порам ядерной оболочки и далее в ядро. Белки матрикса вместе с клеточными факторами транскрипции запускают транскрипцию сверхранних генов. У герпесвирусов продукты сверхранних генов, так называемые сверхранние белки, играют роль трансактиваторов и необходимы для начала транскрипции ранних генов. Однако у других ДНК-содержащих вирусов транскрипция ранних генов может происходить и без участия сверхранних белков.
Большинство ранних генов кодируют белки, осуществляющие репликацию вирусной ДНК и запуск транскрипции поздних генов. Поздние гены кодируют главным образом структурные белки, необходимые для сборки вирусов и их выхода из зараженной клетки. Транскрипция поздних генов зависит от репликации ДНК и прекращается в присутствии ингибиторов репликации.
Для каждого семейства ДНК-содержащих вирусов характерен уникальный механизм репликации ДНК.
Геном герпесвирусов представлен линейной ДНК, которая в зараженной клетке замыкается в кольцо. Кольцевые молекулы вирусной ДНК реплицируются по механизму "катящегося кольца" с образованием длинных линейных конкатемерных молекул, состоящих из многих копий генома. Затем конкатемерные молекулы расщепляются на полноценные геномы. В репродукции герпесвирусов участвуют вирусные ДНК-полимераза и ферменты, увеличивающие внутриклеточную концентрацию дезоксинуклеозидтрифосфатов - структурных элементов ДНК.
Репликация линейных геномов аденовирусов происходит при участии вирусной ДНК-полимеразы и нуклеотид-белкового комплекса, выполняющего роль праймера.
Двухцепочечные кольцевые геномы паповавирусов реплицируются с сохранением кольцевой структуры. Репликация осуществляется клеточными ферментами, а для запуска репликации необходим ранний вирусный белок - Т-антиген.
Изредка геномы паповавирусов (например, папилломавирусов) встраиваются в хромосому зараженной клетки, что приводит к усиленной экспрессии вирусных белков и неконтролируемому делению клетки. Интеграция паповавирусов в клеточный геном может стать причиной злокачественного новообразования, например рака шейки матки.
В отличие от репродукции других ДНК-содержащих вирусов, репродукция поксвирусов полностью происходит в цитоплазме. Эти вирусы содержат факторы транскрипции, РНК-полимеразу, а также набор ферментов, обеспечивающих процессинг мРНК (присоединение 7-метилгуанозина, полиаденилирование). Геном поксвирусов имеет уникальное строение: комплементарные цепи двухцепочечной ДНК на обоих концах ковалентно соединены между собой, так что в действительности геном состоит из одноцепочечной кольцевой молекулы ДНК. Кроме того, в геноме имеются инвертированные концевые повторы. Репликация вирусной ДНК начинается с расщепления одной из цепей в области инвертированных концевых повторов; затем одновременно на обоих концах генома начинается синтез комплементарной цепи, который осуществляет вирусная ДНК-полимераза. Праймером служит прилегающий к месту расщепления короткий участок расщепленной цепи (самозатраванный механизм). Поксвирусы, как и герпесвирусы, кодируют несколько ферментов, способствующих репликации ДНК путем увеличения концентрации дезоксирибонуклеозидтрифосфатов.
2. Вирус папилломы человека. Характеристика. Онкогенность. Лабораторная диагностика
Папилломавирус человека (HPV – Human Papillomavirus) – вирус из рода папилломавирусов, семейства паповавирусов. Передаётся только от человека к человеку и приводит к изменению характера роста тканей. Известно более 100 видов ВПЧ. Из них более 40 – могут вызвать поражение аногенитального тракта (половые органы и задний проход) мужчин и женщин и появление остроконечных кондилом. Некоторые из них безвредны, другие вызывают бородавки, некоторые вызывают рак.
HPV – одна из наиболее распространённых болезней, передаваемых половым путём.
Жизненный цикл вируса:
Характерные проявления инфекции - простые бородавки.
В настоящее время известно уже более 100 типов (штаммов) папилломавируса, обнаруженных у человека. Большинство представителей обладает онкогенными свойствами и вызывает доброкачественные или злокачественные опухоли (папилломы). Доказана этиологическая роль папилломавируса в развитии рака шейки матки. Папилломавирусы имеют видоспецифические и некоторые типоспецифические антигены. Не культивируются в клеточных системах.
Вирус папилломы человека выявляется в кератоцитах в виде эписомы, 50 – 200 копий на пораженную клетку. Процессы продуктивной инфекции и интеграции не наблюдаются.
Папилломавирус человека (ВПЧ) известен достаточно давно, именно он вызывает бородавки. Однако в 80-е годы XX века стали появляться сообщения о связи инфицирования папилломавирусами и онкологическими заболеваниями шейки матки у женщин, которые вскоре были доказаны убедительной статистикой.
Папилломавирусы являются антропонозными возбудителями – то есть передача их возможна только от человека к человеку.
Есть вероятность сохранения вирусов в отшелушивающих клетках кожи определенное время – поэтому для некоторых заболеваний, вызываемых вирусом, вероятен контактно-бытовой путь заражения (бородавки) при условии микроповреждений кожи.
Основным путем заражения аногенитальными бородавками (остроконечными кондилломами) является половой путь заражения (включая орально – генитальные контакты (крайне редко) и анальный секс).
Возможно заражение папилломавирусом новорожденных при родах, что является причиной возникновения ларингеального папилломатоза у детей и аногенитальных бородавок у младенцев.
Попав в организм, вирусы папиллом инфицируют базальный слой эпителия, причем наиболее пораженным участком является зона перехода многослойного плоского эпителия в цилиндрический эпителий. В зараженной клетке вирус существует в двух формах: эписомальной (вне хромосом клетки), которая считается доброкачественной формой, и интросомальной – интегрированной (встраиваясь в геном клетки) – которую определяют как злокачественную форму паразитирования вируса.
Условно все известные папилломавирусы можно разбить на три основные группы:
1) Неонкогенные папилломавирусы (HPV 1,2,3,5)
2) Онкогенные папилломавирусы низкого онкогенного риска (в основном HPV 6,11,42,43,44)
3) Онкогенные папилломавирусы высокого онкогенного риска (HPV 16,18,31,33,35,39,45,51,52,56,58,59 и 68)
Диагностика папилломавирусной инфекции
1. Клинический осмотр.
По характерной клинической картине выявляются все виды бородавок, остроконечные кондиломы. При наличии аногенитальных бородавок обязателен осмотр шейки матки, по показаниям – для исключения эндоуретральных кондилом – уретроскопия
2. Кольпоскопия. Кольпоскопия и биопсия показаны всем женщинам с цервикальной интраэпителиальной неоплазией класса II(CIN II) или класса III(CIN III), независимо от подтверждения у них наличия ВПЧ-инфекции Тест с уксусной кислотой (Acetic Acid Test). В настоящее время специфическим кольпоскопическим признаком ПВИ шейки матки считается неравномерное поглощение йодного раствора Люголя беловатым после уксуса участком эпителия (в виде йодпозитивных пунктации и мозаики). Признаками ПВИ шейки матки могут также быть ацетобелый эпителий, лейкоплакия, пунктация, белые выросты и мозаика, атипичная зона трансформации, жемчужная поверхность после обработки уксусом.
3. Цитологическое исследование шеечных мазков по Папаниколау.
Цитологическое исследование шеечных мазков по Папаниколау (PAP – smear test) выделяет следующие результаты:
1-й класс – атипические клетки отсутствуют, нормальная цитологическая картина.
2-й класс – изменение клеточных элементов обусловлено воспалительным процессом во влагалище и (или) шейки матки.
- 6572
- 5,5
- 0
- 5

Вопрос о происхождении вирусов
Существует три основные теории возникновения вирусов [1]:
Зарождение жизни. Идея последнего универсального общего предка: каким он мог бы быть и что ему предшествовало?

Рисунок 1. Схема трехдоменной классификации, предложенная Вёзе. В основании этой схемы должен находиться последний универсальный общий предок (англ. last universal common ancestor, LUCA). Рисунок из Википедии.
Самый сильный аргумент в пользу существования LUCA — сохранившаяся общая система экспрессии генов (передачи наследственной информации от гена с образованием РНК или белков), одинаковая для всех живущих организмов. Все известные клеточные формы жизни используют один и тот же генетический код из 20 универсальных аминокислот и стоп-сигналов, закодированных в 64 кодонах (единицах генетического кода). Трансляция генетической информации в процессе синтеза белков по заданной матрице выполняется рибосомами, состоящими из трех универсальных молекул РНК и примерно 50 белков, из которых 20 так же одинаковы для всех организмов.
В 2010 году американский биохимик Даглас Теобальд математически проверил вероятность существования LUCA [6]. Он выбрал 23 белка, встречающихся у организмов из всех трех доменов, но имеющих разную структуру у различных видов. И исследовал эти белки у 12 различных видов (по четыре из каждого домена), после чего использовал компьютерное моделирование различных эволюционных сценариев, чтобы понять, при каком из них наблюдаемая картина будет наиболее вероятной. Оказалось, что концепция, включающая существование универсального предка, значительно вероятнее концепций, где его нет. Еще более вероятна модель, основанная на существовании общего предка, но допускающая обмен генами между видами [7].
Предположение о том, что LUCA был прокариотической клеткой, похожей на современные, часто принимается по умолчанию. Однако мембраны архей и бактерий имеют разное строение (рис. 2). Получается, что общий предок должен был обладать комбинаторной мембраной. Новая информация о мембранах LUCA появилась в 2012 году, когда несколько групп ученых подробно проанализировали историю генов всех ферментов биосинтеза компонентов липидов у бактерий, архей и эукариот [8].

Родственными у архей и бактерий оказались ферменты для синтеза терпеновых спиртов и пришивания полярных голов к спиртам. Значит, эти реакции мог проводить и LUCA. Проще всего было предположить, что липиды LUCA состояли из одного остатка терпенового спирта, остатка фосфата и полярной группы (серина или инозитола). Подобные липиды были синтезированы искусственно. Образующиеся из них мембраны обладают высокой подвижностью по сравнению с современными мембранами, хорошо пропускают ионы металлов и малые органические молекулы. Это могло позволять древним протоклеткам поглощать готовую органику из внешней среды даже без транспортных белков.
Реконструкции LUCA методами сравнительной геномики указывают на то, что это должен быть сложный организм без обширного ДНК-генома (геном, состоящий из нескольких сотен РНК-сегментов или ДНК провирусного типа). Но даже если считать возможность существования общего предка доказанной, остается загадкой, в какой среде он мог бы появиться.
Предполагается, что идеальные условия для формирования жизни существовали вблизи термальных геоисточников (морских или наземных) в виде сети неорганических ячеек, обеспечивающих градиенты температуры и рН, способствующих первичным реакциям, и предоставляющих универсальные каталитические поверхности для примитивной биохимии [10].
Эти отсеки могли быть населены разнородной популяцией генетических элементов. Вначале сегментами РНК. Затем более крупными и сложными молекулами РНК (один или несколько белок-кодирующих генов). А позднее и сегментами ДНК, которые постепенно увеличивались (рис. 3).

Такие простейшие генетические системы использовали неорганические соединения из раствора и продукты деятельности других генетических систем. Сначала они должны были подчиняться индивидуальному отбору ввиду большого разнообразия. Но ясно, что важным фактором такого отбора была способность передавать генетическую информацию, то есть, копировать себя. Присутствие одновременно в одной ячейке молекул, способных копировать РНК, кодировать полезные белки и управлять синтезом новых молекул, давало больше шансов выживать в каждой отдельной ячейке. И в такой системе рано или поздно должны были появиться паразитирующие элементы. А если это так, то вирусные элементы стоят у самых истоков эволюции [11].
Возникновение паразитов — неизбежное последствие эволюционного процесса

Рисунок 4. Схематическое представление структуры модели эволюции РНК-подобной системы. На втором этапе цепочки последовательностей начинают соединяться комплементарными связями сами с собой. В результате у двух видов (cat-C и cat-A) возникает вторичная структура молекулы, которая обладает каталитическим свойством. Она ускоряет собственную репликацию (или репликацию несвернувшихся соседей). Два вида при этом приобретают паразитические свойства (par-G и par-U). Пояснения в тексте. Рисунок из [12].
Таким образом, паразитарные репликаторы способствуют эволюции разнообразия, вместо того, чтобы мешать этому разнообразию. Это также делает существующую систему репликатора чрезвычайно стабильной при эволюции паразитов.
Согласно гипотезе Черной Королевы, чтобы поддержать свое существование в постоянно эволюционирующем мире, вид должен реагировать на эти эволюционные изменения и должным образом приспосабливаться к среде. Поэтому, если мы говорим о вирусах как о паразитах, мы обязаны представлять себе взаимоотношения вируса с хозяином. В борьбе с вирусом хозяева развивают новые защитные механизмы, а паразиты отвечают, развивая механизмы для атаки и взлома защиты. Этот процесс может длиться бесконечно либо до вымирания одной из противоборствующих сторон. Так множественные системы защиты составляют существенную часть геномов всех клеточных организмов, а взлом защиты — одна из основных функций генов у вирусов с большими геномами*.
Механизмы клеточной защиты против вирусов
Механизмы защиты от вирусов стандартны, поскольку все вирусы уникальны, и приспособиться к каждому не представляется возможным. Это такие механизмы как:
- Деградация РНК (вирусных и клеточных) — РНК-интерференция;
- Угнетение синтеза белков (вирусных и клеточных);
- Ликвидация зараженных клеток — апоптоз (программируемая клеточная смерть);
- Воспаление.
Получается, что клетка борется с вирусом, нарушая собственные обмен веществ и/или структуру. Защитные реакции клетки — это в основном самоповреждающие механизмы.
Вирус заражает конкретную клетку потому, что его механизмы нападения направлены именно против данного типа клеток. Это такие механизмы как:
- Угнетение синтеза клеточной РНК;
- Угнетение синтеза клеточных белков;
- Нарушение клеточной инфраструктуры и транспорта;
- Подавление/включение апоптоза и других видов клеточной смерти.
Схемы защитных приемов клетки и противозащиты вирусов во многом идентичны. Вирусы и клетки применяют одни и те же приемы. Для подавления синтеза вирусных белков клетка использует интерферон, а чтобы подавить образование интерферона, вирус угнетает синтез белков.
Поскольку узнавание вируса неспецифическое, клетка не может знать намерения конкретного вируса. Она может бороться с вирусом лишь стандартными приемами, поэтому ее оборонные действия часто могут быть чрезмерными.
Понятие о вирусном геноме, типы вирусных генов, концепция генов-сигнатур
В исследовании, проведенном вирусологом Евгением Куниным и его коллегами [16], анализ последовательностей вирусных геномов выявил несколько категорий вирусных генов, принципиально отличающихся по происхождению. Можно обсуждать, какая степень дробности классификации оптимальна, но четко различаются пять классов, укладывающихся в две более крупные категории.
Гены с четко опознаваемыми гомологами у клеточных форм жизни:
- Гены, присутствующие у узких групп вирусов (обычно это гены, гомологичные генам хозяев этих вирусов).
- Гены, консервативные среди большой группы вирусов или даже нескольких групп и имеющие относительно отдаленные клеточные гомологи.
Таким образом, отличительные особенности генов-сигнатур:
- Происхождение из первичного пула генов;
- Наличие лишь очень отдаленных гомологов среди генов клеточных форм жизни, из чего можно сделать вывод, что они никогда не входили в геномы клеточных форм;
- Необходимость для репродукции вирусов.
Из всего вышесказанного следует, что эти гены переходили от вируса к вирусу (или к элементу, подобному вирусу) на протяжении четырех миллиардов лет эволюции жизни, а вирусные геномы появились благодаря перемешиванию и подгонке друг к другу генов в гигантской генетической сети, которую представляет собой мир вирусов. Многочисленные гены клеточных форм жизни также пронизывают эту сеть, прежде всего благодаря геномам крупных вирусов, таких как NCDLV и крупным бактериофагам, которые позаимствовали множество генов от своих хозяев на разных этапах эволюции. Однако большинство заимствованных генов сами по себе не критичны для репликации и экспрессии вирусного генома (исключая некоторые случаи возможного неортологичного замещения генов-сигнатур); обычно эти гены участвуют во взаимодействии между вирусом и хозяином. Таким образом, несмотря на интенсивный взаимообмен генами с хозяевами, вирусы всегда происходят от других вирусов.
Вирусы, встроенные в геном, и горизонтальный перенос генов
В процессе эволюции многие вирусы встроились в геномы клеточных форм жизни путем горизонтального переноса генов (ГПГ). Впервые горизонтальный перенос был описан в 1959 году, когда ученые продемонстрировали передачу резистентности к антибиотикам между разными видами бактерий. В 1999 году Рави Джайн, Мария Ривера и Джеймс Лейк в своей статье писали о произошедшей значительной передаче генов между прокариотами [17]. Этот процесс, по-видимому, оказал некоторое влияние также и на одноклеточные эукариоты. В 2004 году Карл Вёзе опубликовал статью, в которой утверждал, что между древними группами живых организмов происходил массивный перенос генетической информации. В древнейшие времена преобладал процесс, который он называет горизонтальным переносом генов. Причем, чем дальше в прошлое, тем это преобладание сильнее [18].
Горизонтальный перенос генов — процесс, в котором организм передаёт генетический материал другому организму, не являющемуся его потомком. Горизонтальная передача генов реализуется через различные каналы генетической коммуникации — процессы конъюгации, трансдукции, трансформации, переноса генов в составе плазмидных векторов, вирусов, мобильных генетических элементов (МГЭ).
Трансдукция — перенос бактериофагом (агентами переноса генов, АПГ) в заражаемую клетку фрагментов генетического материала клетки, исходно содержавшей бактериофаг [19]. Такой бактериофаг обычно переносит лишь небольшой фрагмент ДНК хозяина от одной клетки (донор) к другой (реципиент). В зависимости от типа трансдукции — неспецифической (общей), специфической или абортивной, геном фага или хозяина-бактерии может быть изменен тем или иным образом:
- При неспецифической трансдукции (рис. 5) ДНК клетки-хозяина включаются в частицу фага (дополнительно к его собственному геному или вместо него);
- При специфической трансдукции гены фага замещаются генами хозяина;
- При абортивной трансдукции внесённый фрагмент ДНК донора не встраивается в ДНК хозяина-реципиента, а остаётся в цитоплазме и не реплицируется. Это приводит к тому, что при клеточном делении он передаётся только одной из дочерних клеток и затем теряется в потомстве.

Рисунок 5. Схема общей трансдукции. Фото с сайта vkjournal.ru.
Наиболее известным примером специфической трансдукции служит трансдукция, осуществляемая фагом λ. Поскольку этот фаг при переходе в состояние профага включается в хромосому бактерий между генами, кодирующими синтез галактозы и биотина, именно эти гены он может переносить при трансдукции.
Вот несколько примеров важных эволюционных событий, связанных с молекулярным одомашниванием:
- Ферменты теломеразы, служащие для восстановления концевых участков хромосом, возможно, ведут свое происхождение от обратных транскриптаз, кодируемых ретровирусами и ретротранспозонами [22];
- Белки RAG, играющие ключевую роль в системе адаптивного иммунитета, по-видимому, происходят от прирученных транспозаз — ферментов, кодируемых транспозонами;
- Ген Peg10, необходимый для развития плаценты, был позаимствован древними млекопитающими у ретротранспозона (рис. 6) [23].

Рисунок 6. Роль гена Peg10 в эмбриональном развитии. Ученые под руководством Рюичи Оно из Токийского медицинского университета Японии показали, что у мышей с выключенным геном Peg10 нарушается развитие плаценты, от чего эмбрион погибает через 10 дней после зачатия [24]. Фото с сайта flickr.com.
В 2008 году в ходе целенаправленного поиска неиспорченных вирусных генов в геноме человека исследователи нашли два очень похожих друг на друга ретровирусных гена (их назвали ENVV1 и ENVV2), которые, по всей видимости, находятся в рабочем состоянии [25]. Это гены белков оболочки ретровируса. Каждый из них входит в состав своего эндогенного ретровируса (ЭРВ), причем все остальные части этих ЭРВ давно не функционируют.
Вирусные гены ENVV1 и ENVV2 у человека и обезьян работают в плаценте и, скорее всего, выполняют следующие функции:
Таким образом, как минимум три полезных применения нашли себе вирусные гены в плаценте приматов. Это показывает, что генетические модификации, которым ретровирусы подвергают организмы, в долгосрочной перспективе могут оказаться полезными или даже определить развитие вида. И с учетом всего вышесказанного древо доменов должно выглядеть как на схеме ниже (рис. 7).

Рисунок 7. Горизонтальный перенос генов в рамках трехдоменного дерева. Рисунок из [26].
Заключение
Возникновение паразитов — обязательная черта эволюционирующих систем репликаторов, а соревнование хозяев и паразитов движет эволюцию тех и других. Любой организм является результатом миллионов лет борьбы клеток с невероятно разнообразным миром вирусов. Их действия и их эволюция пронизывают всю историю клеточной эволюции, и сейчас меняется само наше представление о них. Когда-то вирусы считали деградировавшими клетками, но чем больше мы узнаем о вирусах, тем очевиднее, что их роль в общей эволюции значительна. И невероятно много нам еще предстоит узнать.
Статья написана в соавторстве с Евгенией Щепенок.
Вирусы представляют собой форму жизни, которая погибает через некоторое время после попадания в окружающую организм среду, то есть не может существовать вне тела носителя. По факту их можно назвать паразитами внутриклеточного уровня, которые размножаются в клетках, вызывая тем самым различные заболевания. Вирусы способны поражать как РНК (рибонуклеиновую кислоту), так и ДНК (дезоксирибонуклеиновую кислоту). ДНК-содержащие вирусы признаются более консервативными с точки зрения генетики и наименее подверженными каким-либо изменениям.
Теории о происхождении
Существует несколько теорий о происхождении вирусов. Приверженцы одной теории утверждают, что зарождение вирусов происходит спонтанно и обусловлено рядом факторов. Другие считают вирусы потомками простейших форм. Однако эта теория бездоказательна и необоснованна, так как сама паразитарная суть вирусов предполагает наличие более высокоорганизованных существ, в клетках которых они могли бы существовать.
Еще одна версия происхождения вирусов предполагает преобразование более сложных форм. Эта теория говорит о вторичности простоты вируса, так она является следствием адаптации к паразитическому образу жизни. Подобное упрощение свойственно всем паразитирующим микроорганизмам. Они утрачивают способность к самостоятельному питанию, приобретая при этом склонность к быстрому размножению.
Устройство и размеры ДНК-содержащих вирусов
Самые простые вирусы имеют в составе нуклеиновую кислоту, которая выступает в качестве генетического материала как самого микроорганизма, так и его капсида, представляющего собой чехол из белка. Состав некоторых вирусов дополнен жирами и углеводами. У вирусов отсутствует часть ферментов, которая отвечает за репродуктивную функцию, поэтому размножаться они могут, только попав в клетку живого организма. Метаболизм зараженной клетки после этого перестраивается на производство вирусных, а не собственных компонентов. В каждую клетку заложена определенная генетическая информация, которая при определенных обстоятельствах может рассматриваться в качестве инструкции по синтезу конкретного вида белка внутри клетки. Зараженная клетка воспринимает данную информацию как руководство к действию.
Размеры
Что касается размеров ДНК- и РНК-содержащих вирусов, то он находится в пределах 20-300 нм. Вирусы в большинстве своем имеют меньший размер, чем бактерии. Эритроцитные клетки, например, на порядок больше вирусных. Способная к заражению, полноценная инфекционная вирусная частица вне здорового организма носит название вирион. В ядро вириона входят одна или несколько молекул нуклеиновой кислоты. Капсид представляет собой оболочку из белка, которая покрывает вирионовую нуклеиновую кислоту, обеспечивая защиту от пагубного воздействия окружающей среды. Нуклеиновая кислота, входящая в вирион, считается геномом вируса и выражается в дезоксирибонуклеиновой кислоте, или ДНК, а также рибонуклеиновой (РНК). В отличие от бактерий, у вирусов не встречается комбинация этих двух видов кислоты.
Рассмотрим основные стадии размножения ДНК-содержащих вирусов.
Размножение вирусов
Чтобы иметь возможность размножаться, вирусам необходимо внедриться в клетки носителя. Некоторые вирусы могут существовать у большого количества хозяев, у других имеется склонность к конкретным видам. На первоначальной стадии заражения вирус внедряет в клетку генетический материал в виде ДНК или РНК. Репродуктивная его функция, а также дальнейшее развитие клеток напрямую зависят от деятельности и выработки генов и белков вируса.
Для производства клеток ДНК-содержащим вирусам бывает недостаточно собственных белков, поэтому используются аналогичные вещества носителя. Спустя некоторое время после заражения в клетке остается только небольшая часть изначальных вирусов. Данная фаза называется эклипсной. Геном вируса в этот период тесно взаимодействует с носителем. Затем, спустя несколько этапов, начинается накопление во внутриклеточном пространстве потомства вируса. Это называется фазой созревания. Рассмотрим последовательность стадий размножения ДНК-содержащих вирусов.
Цикл жизни
Цикл жизни вирусов состоит из нескольких этапов, являющихся обязательными:
1. Адсорбция на клетке носителя. Это первоначальный и важный этап распознания клеток-мишеней по рецепторам. Адсорбция может происходить на клетках органов или тканей. Процесс запускает механизм дальнейшей интеграции вируса в клетку. Для связывания клеток требуется определенное количество ионов. Это необходимо для снижения электростатического отталкивания. Если проникновение в клетку не удается, вирус ищет новую мишень для интеграции и процесс повторяется. Это явление объясняет определенность в путях проникновения вируса в организм человека.
Так, например, слизистая оболочка верхних дыхательных путей обладает рецепторами к вирусу гриппа. Клетки кожи, напротив, таковых не имеют. По этой причине невозможно заразиться гриппом через кожный покров, это возможно только при вдыхании частиц вируса. Бактериальные вирусы в форме нитей или не имеющие отростков не могут прикрепляться на стенках клетки, поэтому они адсорбируются на фимфибриях. На начальном этапе адсорбция происходит за счет электростатического взаимодействия. Данная фаза обратима, так как частица вируса легко отделяется от клетки, выбранной в качестве мишени. Начиная со второй фазы, отделение не представляется возможным.
2. Следующая стадия размножения ДНК-содержащих вирусов характеризуется попаданием целого вириона или нуклеиновой кислоты, им выделяемой внутри клетки носителя. В организм животного вирус интегрируется проще, так как клетки в данном случае не снабжены оболочкой. Если у вириона есть снаружи липопротеидная мембрана, то она сталкивается при контакте с аналогичной защитой клетки носителя и вирус попадает в цитоплазму. Вирусы, проникающие в бактерии, растения и грибы интегрируются сложнее, так как в данном случае они вынуждены проходить сквозь жесткую стенку клетки. Для этого бактериофаги, к примеру, обеспечены ферментом лизоцимом, который помогает растворить твердые клеточные стенки. Примеры ДНК-содержащих вирусов рассмотрим ниже.
3. Третья стадия именуется депротеинизацией. Она характеризуется высвобождением нуклеиновой кислоты, являющейся носителем генетической информации. У некоторых вирусов, например, бактериофагов, данный процесс сочетается со второй стадией, так как белковая оболочка вириона остается за пределами клетки носителя. Вирион способен проникать в клетку путем захвата последней. При этом возникает вакуоль-фагосома, которая вбирает в себя первичные лизосомы. При этом расщепление на ферменты происходит только у белковой части вирусной клетки, а нуклеиновая кислота остается в неизменном состоянии. Именно она в дальнейшем существенно переформирует функционирование здоровой клетки, вынуждая ее производить нужные вирусу вещества. Сам вирус необходимыми для таких процедур механизмами не обеспечен. Существует такое понятие, как стратегия вирусного генома, которая подразумевает реализацию генетической информации.
4. Четвертая стадия размножения ДНК-содержащих вирусов сопровождается выработкой нужных для жизнедеятельности вируса веществ, которая осуществляется под влиянием нуклеиновой кислоты. Сначала вырабатывается ранняя мРНК, которая станет основой для белков вируса. Ранними называются молекулы, которые возникли до высвобождения нуклеиновой кислоты. Молекулы, возникшие после репликации кислоты, называют поздними. Важно понимать, что выработка молекул напрямую зависит от вида нуклеиновой кислоты конкретного вируса. ДНК-содержащие вирусы во время биосинтеза придерживаются определенной схемы, включающей конкретные этапы – ДНК-РНК-белок. Мелкие вирусы используют в процессе транскрипции РНК-полимеразы. Крупные, такие как оспяной вирус, синтезируются не в клеточном ядре, а в цитоплазме.
К ДНК-содержащим вирусам относятся вирусы гепатита В, герпес, вирусы оспы, паповавирусы, гепаднавирусы, парвовирусы.
Группы РНК-вирусов
Вирусы, содержащие РНК, подразделяются на несколько групп:
1. Первая группа устроена наиболее просто. В нее входят корона-, тога- и пикорнавирусы. Транскрипция у этих видов вируса не осуществляется, поскольку однонитчатая РНК вириона самостоятельно реализует функцию матричной кислоты, то есть представляет собой основу для выработки белков на уровне клеточных рибосом. Таким образом, схема биовыработки у них выглядит как РНК-белок. Вирусы данной группы называют также позитивно геномными или плюснитевыми.
2. Вторая группа ДНК и РНК-содержащих вирусов включает в себя минуснитевые вирусы, то есть они обладают негативным геномом. Это вирусы кори, гриппа, паротита и многие другие. В них также содержится однонитчатая РНК, но она не подходит для непосредственной трансляции. По этой причине сначала происходит перенос данных на РНК вириона, а полученная матричная кислота будет служить в дальнейшем основой для выработки белков вируса. Транскрипция в данном случае определяется зависимой от рибонуклеиновой кислоты полимеразой РНК. Данный фермент приносится вирионом, так как он отсутствует в клетке изначально. Это связано с тем, что у клетки не возникает необходимости перерабатывать РНК для получения другого РНК. Так, схема биовыработки в данном случае будет выглядеть как РНК-РНК-белок.
3. Третью группу составляют так называемые ретровирусы. Они же входят в разряд онковирусов. Биосинтез у них происходит по более сложному пути. В исходной матричной РНК однонитчатого типа на начальном этапе происходит выработка ДНК, что является уникальным явлением, аналогов которому нет в природе. Процесс находится под контролем специального фермента, а именно зависимой от РНК полимеразой ДНК. Данный фермент также носит название ревертазы или обратной транкриптазы. Молекула ДНК, полученная в результате биосинтеза, получает форму кольца и обозначается как провирус. Далее молекула внедряется в клетки хромосом носителя и транскрибируется несколько раз посредством полимеразы РНК. Созданные копии совершают следующие действия: представляют собой матрицу РНК, с помощью которой вырабатывается вирусный белок, а также вирион РНК. Схема синтеза представляется таким образом: РНК-ДНК-РНК-белок.
4. Четвертая группа образуется из вирусов, РНК которых имеет двухнитчатую форму. Их транскрипция реализуется посредством фермента вируса зависимой РНК полимеразы РНК.
5. В пятой группе выработка составляющих частицы вируса, а именно капсидных белков и нуклеиновой кислоты происходит многократно.
6. Шестая группа включает в себя вирионы, которые возникают как результат самосборки на основе множества копий белков и кислоты. С этой целью концентрация вирионов должна достичь критического значения. При этом компоненты частицы вируса вырабатываются отдельно друг от друга в разных областях клетки. Сложные вирусы также создают защитную оболочку из веществ, входящих в плазменную клеточную мембрану.
7. На заключительном этапе новые частицы вируса высвобождаются из клетки носителя. Данный процесс происходит разными способами в зависимости от вида вируса. Некоторые клетки после этого погибают, так как клеточный лизис освобождается. В других вариантах возможно отпочковывание от клетки, однако и этот способ не предотвращает ее дальнейшее отмирание, так как повреждается мембрана плазмы.

Период до момента выхода вируса из клетки называют латентным. Продолжительность данного промежутка может находиться в пределах от нескольких часов до пары дней.
Геномные вирусы, содержащие ДНК
Вирусы, содержание ДНК геномного вида подразделяются на четыре группы:
1. Такие геномы, как адено-, папова- и герпесвирусов, переносятся и копируются в клеточном ядре носителя. Это вирусы, содержащие двухцепочечную ДНК. Капсиды, попав в клетку, переносятся к мембране клеточного ядра, чтобы потом, под воздействием определенных факторов, ДНК вируса перешло в нуклеоплазму и накопилось там. Вирусы при этом пользуются матрицей РНК и клеточными ферментами носителя. А-белки переносятся первыми, за ними следуют b-белки и g-белки. Матрица РНК возникает на основе а-22 и а-47. Полимераза РНК реализует перенос ДНК, который размножается по принципу перекатывающегося кольца. Капсид, в свою очередь, возникает из g-5 белка. Какие еще существуют геномы ДНК-содержащих вирусов?
2. Поксивирусы входят во вторую группу. На начальном этапе действия осуществляются в цитоплазме. Там происходит высвобождение нуклеотидов и начало транскрипции. Затем образуется матрица РНК. На ранних стадиях выработки создается полимераза ДНК и около 70 белков, а также двухцепочная ДНК расщепляется полимеразой. С обоих сторон генома начинается репликация в тех местах, где на начальном этапе осуществлялось расплетение и расщепление цепей ДНК.
3. В третью группу включены парвовирусы. Размножение осуществляется в клеточном ядре носителя и находится в зависимости от функций клетки. В данном случае ДНК образует так называемую шпилечную структуру и выступает в роли затравки. 125 первых пар оснований переходят с начальной цепи на смежную, которая и служит матрицей. Таким образом, происходит инверсия. Для синтезирования нужна полимераза ДНК, благодаря которой происходит транскрипция вирусного генома.
8. В четвертую группу входят гепаднавирусы. Сюда относится ДНК-содержащий вирус гепатита. ДНК вируса кольцевого типа работает в качестве основы для выработки мРНК вируса и плюс-цепи РНК. Она, в свою очередь, становится матрицей для синтеза минус-цепи ДНК.
Методы борьбы
ДНК - содержащие вирусы, безусловно, представляют опасность для здоровья человека. Основным методом борьбы с ними может стать проведение профилактических мер, направленное на укрепление иммунитета, а также регулярная вакцинация.
Как правило, антитела, направленные на борьбу с теми или иными вирусами вырабатываются как результат вторжения вредоносных микроорганизмов в систему носителя. Однако усилить выработку антител можно заранее, сделав профилактическую прививку.
Виды вакцинации
Существует несколько основных видов вакцинации, включающих:
1. Введение в организм ослабленных клеток вируса. Это провоцирует выработку увеличенного количества антител, что позволяет бороться с нормальным вирусным штаммом.
2. Введение уже мертвого вируса. Принцип действия аналогичен первому варианту.
3. Пассивная иммунизация. Данный метод заключается в введении уже синтезированных антител. Это может быть как кровь человека, перенесшего заболевание, против которого делается прививка, так и животного, например, лошадей. Последовательность размножения ДНК-содержащих вирусов мы рассмотрели.
Чтобы избежать заражения организма различными видами вирусов, опасных для здоровья человека, следует беречь тело от потенциального контакта с патогенными микроорганизмами. Вполне по силам избежать токсоплазмы, микоплазмы, герпеса, хламидий и других распространенных форм вируса, просто соблюдая определенные рекомендации. Это особенно касается детей до 15 лет.
Если тело ребенка не было заражено вышеперечисленными штаммами вирусов, то у него вырабатывается в подростковом периоде здоровый и усиленный иммунитет. Главная опасность вирусов - не всегда в том, как они выражаются, а в том, какое влияние оказывают на защитные свойства нашего организма. Примеры ДНК- и РНК-содержащих вирусов интересуют многих.
Герпесный вирус, который присутствует в теле 9 из 10 жителей Земли, снижает иммунные свойства примерно на 10 процентов в течение всей жизни, хотя может и никак не проявлять себя.
Заключение
Помимо подобной вирусной нагрузки, которая подчас не ограничивается только герпесом, условия современной жизни далеки от идеала, что также сказывается на защитных барьерах организма. В данный пункт можно отнести форсированный городской ритм жизни, плохую экологию, неправильное питание и т.д. На фоне снижения общего состояния здоровья человека его организм становится менее резистентным к различным вирусам и, соответственно, частым болезням.
Читайте также:


