Как называется вирус способный поражать бактериальную клетку
Вирус (лат. virus - яд) - неклеточная форма жизни, мельчайшие болезнетворные микроорганизмы, не видимые в микроскоп. Они значительно меньше бактерий: легко проходят через бактериальные фильтры.
Вирусы способны размножаться только внутри живых клеток, до проникновения в них вирусы не имеют признаков жизни: пассивно перемещаются во внешней среде, ожидая встречи с клеткой-мишенью.
В 1892 году Ивановский Д.И. в ходе изучения мозаичной болезни табака обнаружил, что болезнь вызывается мельчайшими субстанциями, которые проходят через бактериальный фильтр, то есть были меньше бактерий. Вирусы впервые увидели в электронный микроскоп в 1939 году (спустя 19 лет со смерти Ивановского), однако считается, что именно Ивановский положил начало вирусологии как науке.

Вирусы выделяют в отдельное, пятое царство. Несмотря на их кажущуюся безжизненность, от неживой материи их отличают следующие черты:
- Наличие наследственности и изменчивости
- Способность к репродукции (воспроизведению себе подобных)
Рекомендую обратить особое внимание на черты, которые отличают вирусы от живых организмов:
-
Неживое (инертное) состояние
Вне клетки хозяина находятся в неживом состоянии, ожидая внедрения. Вирусы - облигатные внутриклеточные паразиты.
У вирусов отсутствует обмен веществ с внешней средой (метаболизм).
Не имеют клеточной мембраны, ограничивающих их от внешней среды, и, соответственно, клеточного строения.
Не делятся, не размножаются половым путем
У вирусов отсутствует половое размножение и деление. Попав в живую клетку, вирус встраивает свою нуклеиновую кислоту (РНК/ДНК) в наследственный материал клетки-мишени. В результате клетка начинает синтезировать вирусные белки (новые вирусы): так увеличивается численность вирусов.
Вирусы не растут, не увеличиваются в размерах. Стратегия их жизни - безудержное размножение.
Если мы заглянем в клетку, инфицированную вирусом, то от вируса мы увидим только один элемент - его нуклеиновую кислоту (ДНК/РНК). Во внешней среде вирусы существуют в виде вирионов - полностью сформированных вирусных частиц, состоящих из белковой оболочки (капсида) и нуклеиновой кислоты внутри.
Носителем наследственной информации у вирусов может быть ДНК, РНК. В связи с этим все вирусы подразделяются на ДНК- и РНК-содержащие.
Найдя клетку, на поверхности которой есть подходящий рецептор, вирус взаимодействует с ним и прикрепляется к мембране клетки. Путем эндоцитоза (образование вакуоли) вирус проникает внутрь клетки, выходит из вакуоли в цитоплазму. Наследственный материал (ДНК/РНК) вируса реализуется по схеме: ДНК ↔ РНК → белок.
Проникнув внутрь клетки (инфицировав ее), вирус реализует собственный генетический материал (ДНК/РНК) путем синтеза вирусного белка на рибосомах клетки хозяина. Клетка даже и не подозревает, что вирус встроил в ее РНК/ДНК свой генетический код - она принимает его как свой собственный, а в результате синтезирует вирусные белки.
Образовавшиеся белки объединяются в вирусные частицы, которые могут выходить из клетки разными путями. Вирионы вирусов гепатита C выходят из клетки путем почкования (экзоцитозом), при таком варианте клетка долгое время остается живой и служит для продукции новых вирионов.
Известен и другой механизм выхода вирионов из клетки: взрывной, при котором оболочка клетки разрывается, и тысячи вирионов отправляются инфицировать новые клетки. Такой способ характерен для аденовирусов, ротавирусов.
Это уникальная группа вирусов, инфицирующая только бактерии. Бактериофаг имеет капсид, с содержащимся внутри наследственным материалом - ДНК (реже РНК), протеиновым хвостом. Бактериофаги открыты в 1915 году и с тех пор активно применяются в ходе генетических исследований.
Ниже вы можете видеть типичное строение бактериофага. Бактериофаг напоминает шприц, который протыкает стенку бактерии и впрыскивает внутрь нее свою нуклеиновую кислоту.
Бактериофаги успешно применяются в медицине для лечения многих заболеваний. Это высокоэффективные, дорогостоящие препараты, которые помогают, например, нормализовать микрофлору кишечника при бактериальных инфекциях.
Вирусы вызывают множество заболеваний человека и животных. Некоторые из них неизлечимы даже на современном этапе развития медицины, например бешенство. К вирусным инфекциям относятся грипп, корь, свинка, СПИД (вызванный ВИЧ), полиомиелит, желтая лихорадка, онковирусы.
Такая группа, как онковирусы, потенцируют развитие опухолей в организме. К ВИЧ и онкогенным вирусам не существует специфических антител, что затрудняет процесс создания вакцины. В то же время против ряда вирусных инфекций: корь, ветряная оспа созданы вакцины, создающие стойкий пожизненный иммунитет.
Клетки вырабатывают защитный белок - интерферон. Это вещество подавляет синтез новых вирусных частиц, приводит к повышению температуры тела (например, при гриппе).

Вирус иммунодефицита человека (ВИЧ) представляет для организма большую опасность. Он размножается в T-лимфоцитах - клетках крови, которые выполняют иммунную функцию. С гибелью T-лимфоцитов разрушается иммунная система, становится невозможным сопротивление организма бактериями, вирусам и грибам, что в отсутствии лечения приводит к вторичным инфекциям.
Риск заражения ВИЧ присутствует при гемотрансфузии (переливании крови), половом акте. Инфекция также может быть передана от ВИЧ инфицированной матери к плоду.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
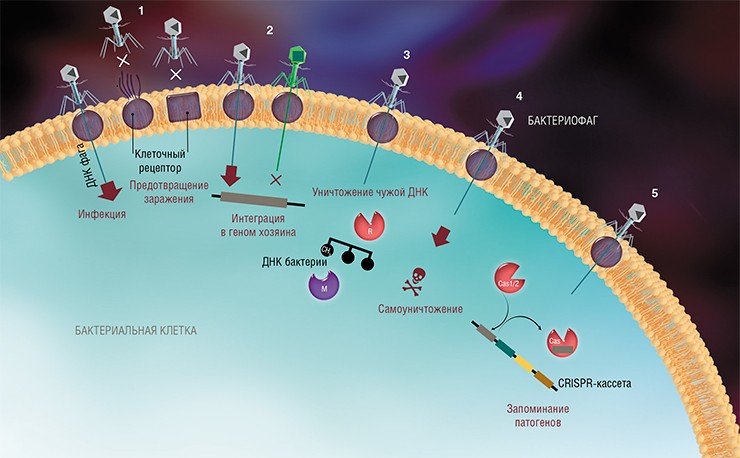
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
Врага нужно знать в лицо
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
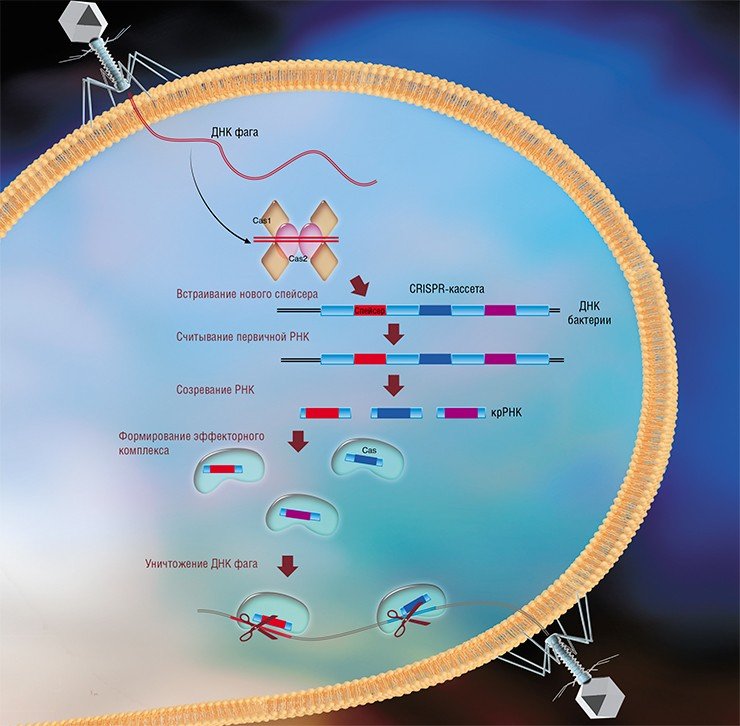
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
Гонка вооружений
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
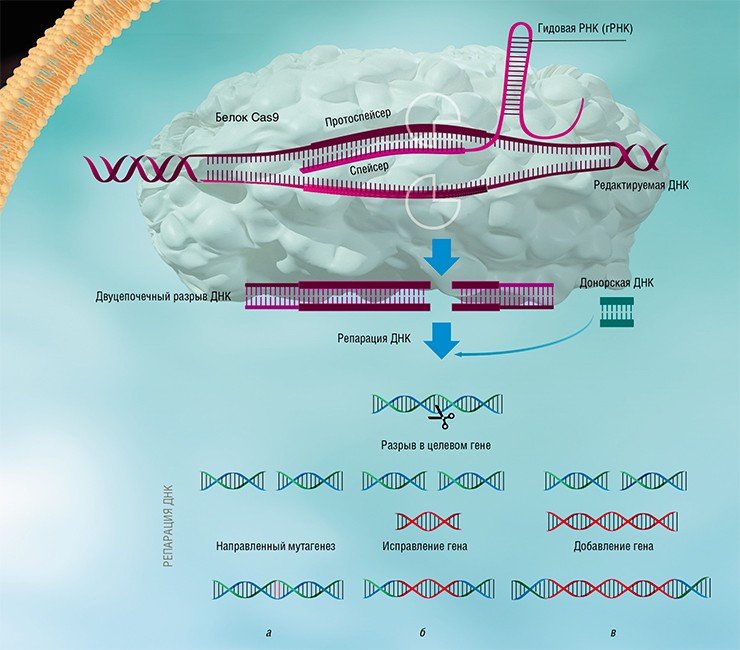
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)

Вирусы. Бактериофаги. Вирусные заболевания.
Вирусы (от лат. вирус – яд) – представляют собой мельчайшие неклеточные формы жизни. Вирусы имеют размеры 2-5*10 -7 см, что значительно меньше, чем бактериальная клетка (от 0,2 до 10 мкм). Рассмотреть вирусы возможно только с помощью электронного микроскопа, увеличивающий в 100 тысяч и более раз. Вирусы относятся к отдельному царству.
Вирусология – наука изучающая вирусы. Становление вирусологии как науки начинается с 30-х годов 20 века.
Впервые вирус табачной мозаики (рис.1) был открыт русским ученым Д.И.Ивановским (1892г.) (рис.2).

Рис.1 Листья табака (слева) пораженные вирусом табачной мозаики (справа)
Рис.2 Д.И.Ивановский – первооткрыватель вирусов
Первый вирус животных (вирус ящура) был описан в 1897 году Лёффером и Фрошем. В 1901 году вирус желтой лихорадки был открыт англичанами У. Ридом и Д. Кэрроллом.
В 1917 году Ф.д’Эррелем был открыт бактериофаг – вирус, поражающий бактерии.
Удивительно то, что первая вакцина от оспы была предложена за 100 лет до открытия вирусов, в 1796 году английским врачом Э.Дженнером. Второй по открытию стала – антирабическая вакцина, представленная французским ученым микробиологом Л.Пастером в 1885 году.
Вирусы – неклеточные частицы, состоящие из белковой оболочки (капсид) и собственного генетического материала в виде нуклеиновой кислоты (ДНК или РНК) (рис.3).
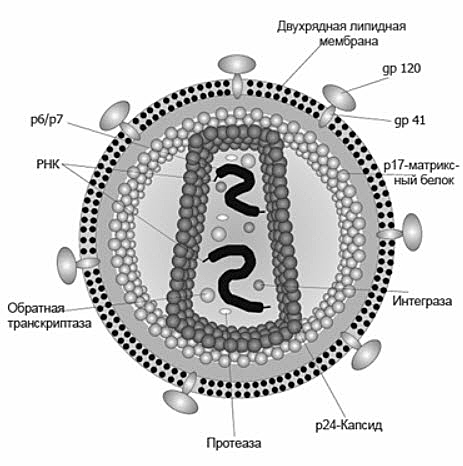
Рис.3 Строение вируса иммунодефицита человека (ВИЧ)
Вирусы могут обладать разнообразными формами: шаровидные, овальные, палочковидные, нитевидные, цилиндры, тетраэдры, октаэдры и др.(рис.4).
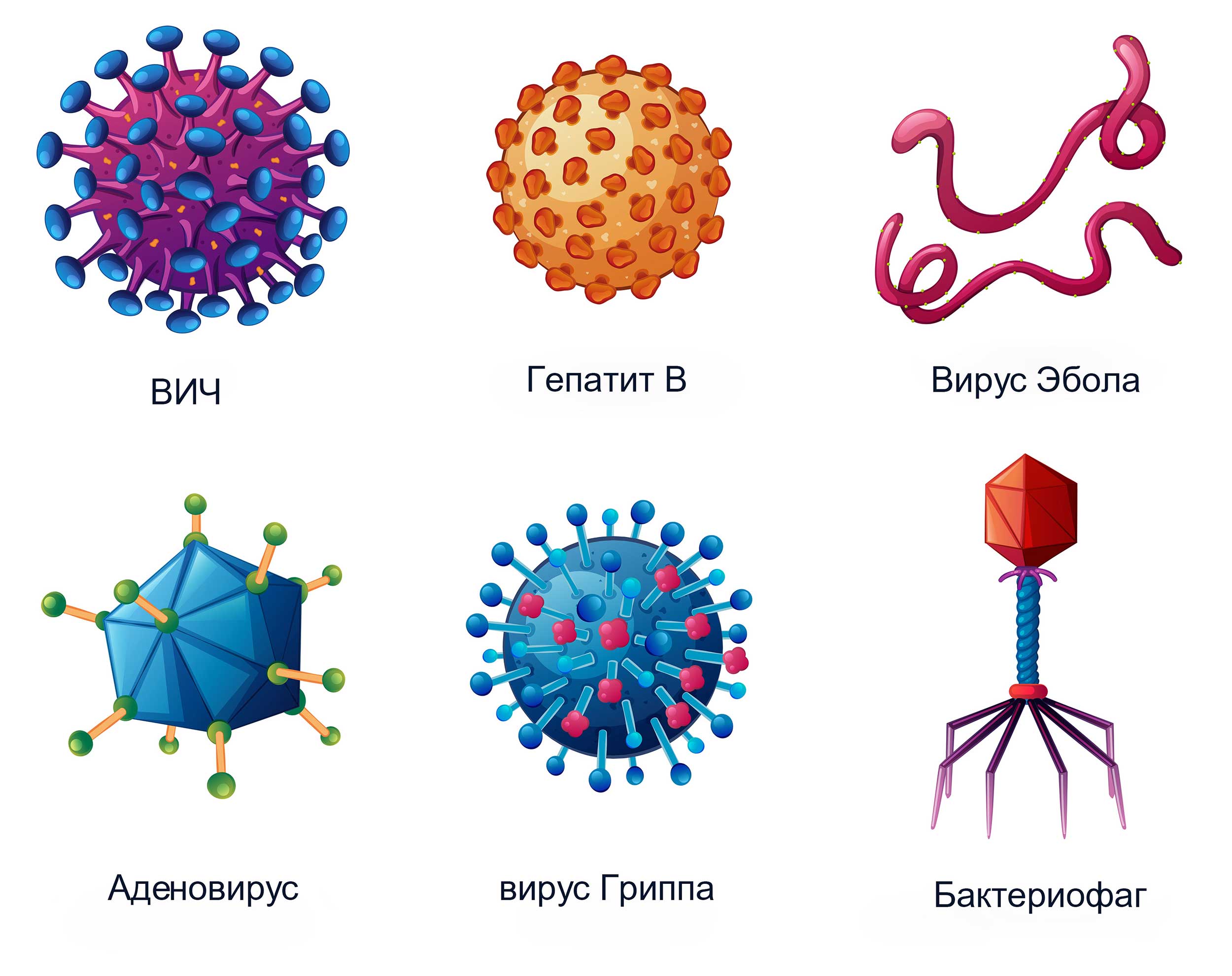
Рис.4 Разнообразные формы и виды вирусов
Более сложные вирусы имеют в своем составе дополнительные белковые или липопротеидные оболочки. Вирусы гриппа и герпеса кроме белковой оболочки могут содержать и углеводы.
| ДНК-содержащие вирусы | РНК-содержащие вирусы |
|---|---|
| оспы | бешенства |
| герпеса | кори |
| бактериофаги Т-группы | СПИДа и лейкоза |
| гепатита В | гепатита А |
| паповавирусы | гриппа |
| аденовирусы | полимиелита |
| цитомегаловирус | ОРЗ |
| Эпштейн-Бара | желтой лихорадки |
| и др. | краснухи и др. |
Геном вирусов может быть представлен однонитчатыми и двунитчатыми молекулами ДНК (вирус оспы человека, овец, свиней, аденовирус человека) и РНК (матрица для вирусов насекомых и других животных). Вирусы с однонитчатой молекулой РНК (энцефалит, краснуха, корь, бешенство, грипп и др.).
Вне живой клетки вирус не питается, не передвигается, не растет, не размножается и не проявляет других свойств живого.
Вирусы способны размножаться только внутри живой клетки. Вирус проникает внутрь клетки путем связывания его с особым протеином – рецептором, расположенным на поверхности клетки. На поверхности чувствительной клетки происходит связывание с рецептором, после чего присоединившейся участок погружается в цитоплазму и превращается в вакуоль. Стенки вакуоли, состоящей из цитоплазматической мембраны способны сливаться с другими вакуолями или даже ядром. В результате вирус достигает любой участок клетки.
Данный процесс до конца не изучен, и возможно именно он мог бы решить вопрос возникновения онкологических заболеваний.
Быстрая способность адаптироваться и видоизменяться, подстраиваясь к геному клетки, делает некоторые вирусные заболевания практически неизлечимыми. Таким образом, вирусы представляют паразитизм на генетическом уровне (рис.5).
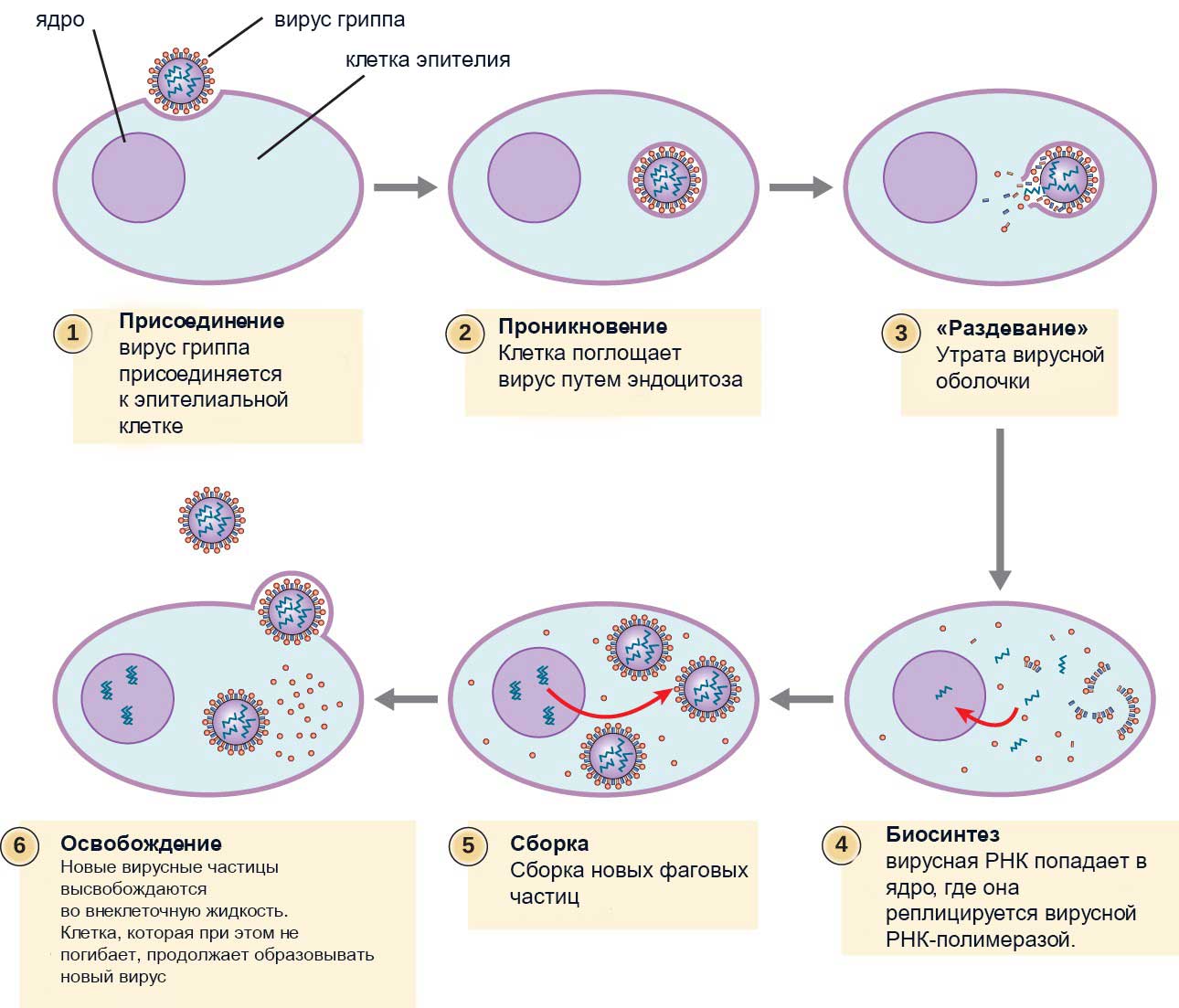
Рис.5 Размножение вируса гриппа
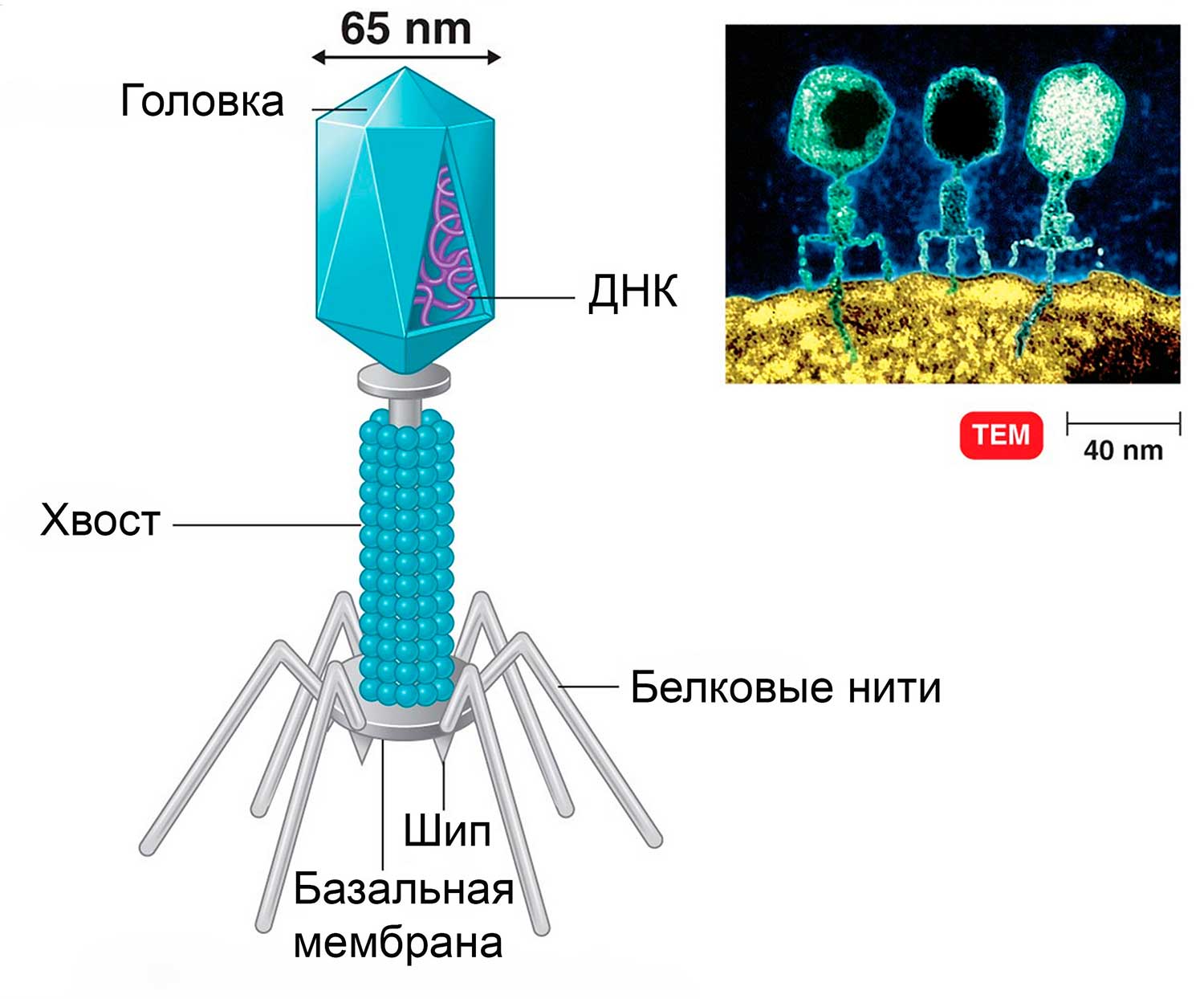
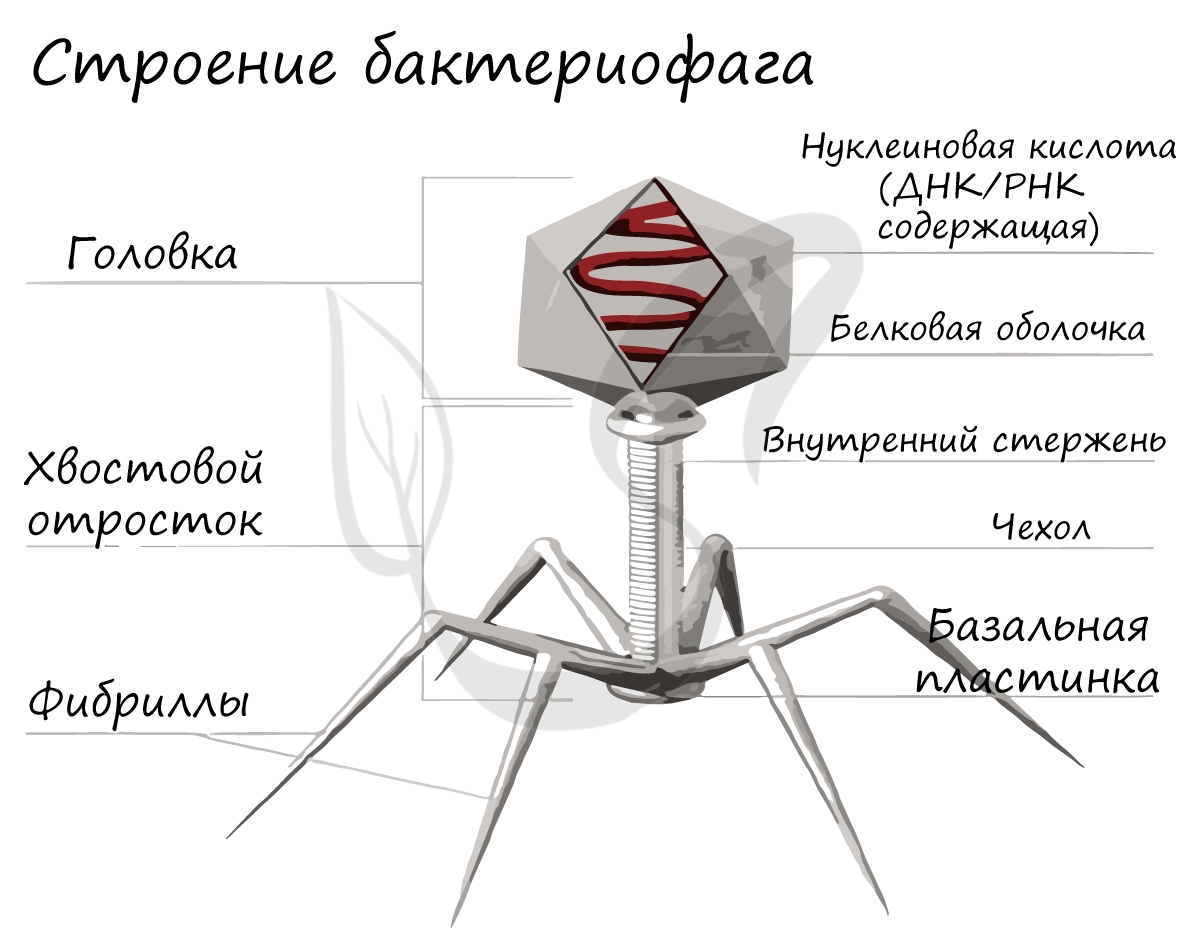
Рис.6 Строение бактериофага
Бактериофаг состоит из головки, хвостика и нескольких хвостовых отростков (белковых нитей). Наружная часть головки покрыта белковой оболочкой. Во внутренней части головки расположена ДНК, а внутри хвоста проходит центральный канал. Из-за толстых клеточных стенок бактерий белок-рецептор бактериофага не может погрузиться в цитоплазму.
Удерживаясь на поверхности клетки за счет шипов, расположенных под базальной мембраной, бактериофаг пронзает стенку бактерии и вводит внутрь полый стержень. По этому стержню в цитоплазму поступает ДНК (или РНК). Геном бактериофага проникает внутрь клетки, а оболочка остается снаружи. Спустя время, сформировавшиеся зрелые фаговые частицы разрушают бактерию изнутри и выходят наружу (рис.7).
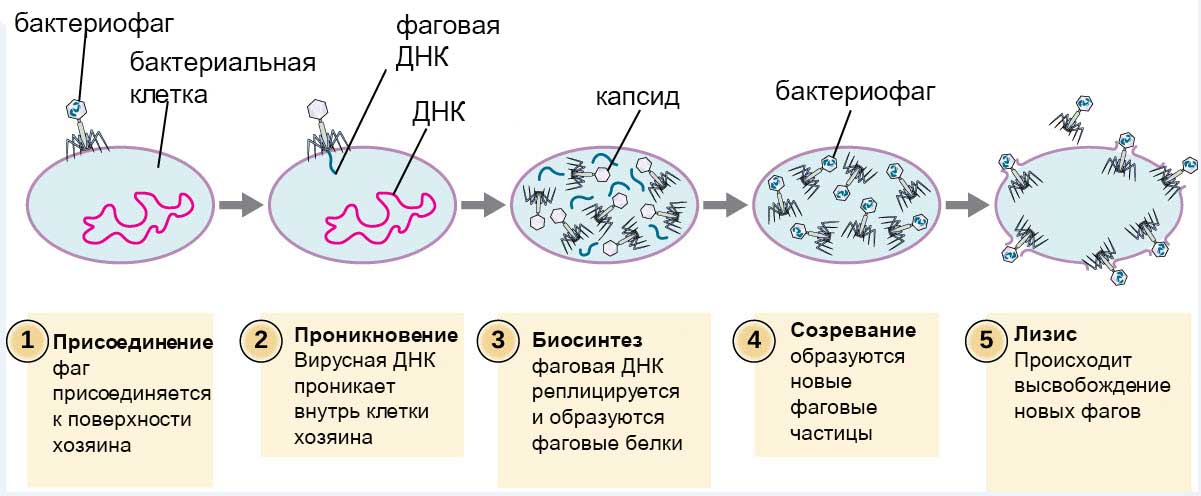
Рис.7 Размножение бактериофага
Обладая способностью полного уничтожения бактериальной клетки, бактериофаги могут быть использованы для лечения разнообразных бактериальных заболеваний (холеры, дизентерии, брюшного тифа и др.).
Отмечено, что отделение от вирусной частицы нуклеиновой кислоты приводит к потере инфекционной способности к репродукции. Это говорит о том, что нуклеиновая кислота играет важную роль в размножении вируса.
При благоприятных условиях вирус очень быстро размножается. Так, за 30 минут в одной клетке появляются сотни новых вирусов.
Вирусы могут продолжительно сохраняться в почве, воде и другим средах. Некоторые представители устойчивы к высоким температурам (свыше +100С) и высушиванию.
В настоящее время известно около 400 видов вирусов растений и около 500 видов вирусов животных.Вирусы растений вызывают поражение листьев и других органов, вызывая появление разноцветных или бесцветных пятен и полосок. Вирусы вызывают замедление роста растений, изменяет их форму и снижает урожайность.
Наиболее опасными для человека являются вирусы гепатита – А, В, С. Вирус способен сильно повреждать ткани печени, вызвав необратимые последствия.
Более опасную для человечества форму представляет вирус иммунодефицита человека или сокращенно ВИЧ (HIV). Попав в кровь, ВИЧ, поражает иммунную систему человека, приводя к развитию болезни под названием СПИД (синдром приобретенного иммунодефицита человека). РНК-содержащий ВИЧ атакует белые кровяные клетки – лимфоциты, отвечающие за иммунитет, делая человека уязвимым для других болезней.
Внедренный в лимфоциты РНК вирус начинает синтезировать фермент – ревертазу. Этот фермент служит матрицей для последующего синтеза молекулы ДНК. Синтезированная вирусная ДНК встраивается в хромосому лимфоцита. После чего вирус долгое время может не проявлять себя. Это может длиться от 1 до 2 лет, а иногда и более. Спустя время вирусная ДНК начинает проявлять себя, синтезируя сотни тысяч вирусов, что в итоге приводит к разрушению лимфоцита.
Вероятность заражения ВИЧ увеличивается при прямом контакте с кровью больного человека. Распространенные пути передачи вируса; незащищенный половой контакт с инфицированным человеком, инъекции шприцом, переливание крови. ВИЧ не передается воздушно-капельным путем, через укусы насекомых, посуду, при рукопожатиях и пользовании общественными местами (туалеты, бассейны, бани и т.п.).
В настоящее время вакцины против СПИДа нет, но существуют медицинские препараты на основе азотимидина и ингибиторов протеаз, способные подавить синтез вирусной ДНК. Это облегчает течение болезни и значительно удлиняет жизнь человека.
Симптомами СПИДа является температура, постоянный озноб, легкая простужаемость, резкое похудение.
Чтобы предупредить СПИД необходимо соблюдать следующие правила;
– избегать прямого контакта с кровью неизвестного человека (зараженными так же могут быть лимфа, сперма, влагалищные выделения, грудное молоко и др.);
– избегать случайные половые связи;
– использовать презервативы;
– пользоваться одноразовыми шприцами;
– пользоваться личными бритвенными приборами, при этом не разрешать пользоваться своими.
Природным очагом СПИДа по мнению ученых считается Центральная Африка, а носителем вируса являются зеленые мартышки.
Всем известный вирус гриппа не менее опасный, наряду с корью, гепатитом и полиомиелитом.
Грипп – болезнь, угрожающая человеческой жизни. В 1918-1919 годах весь земной шар трижды был охвачен волнами гриппа, во время которых погибли 20 млн человек. В США в зиму 1968-1969 годов 50 млн человек перенесли грипп, 70 тыс. из них скончались.
либо инфекции, вызываемые как бактериями так и вирусами
Эпидемия – прогрессируемое во времени и пространстве инфекционное заболевание.
Пандемия – инфекционное заболевание захватывающее большие территории (мирового значения). В настоящее время к ряду таких заболеваний относится коронавирусная инфекция (COVID-19) вызванная коронавирусом (SARS-CoV-2).
Основные методы борьбы с вирусными инфекциями – профилактические прививки (вакцины), Ослабленные возбудители болезни, введенные в организм, позволяют выработать иммунитет. Благодаря вакцинам исчезло такое опасное вирусное заболевание, как оспа. Следует помнить, что без оболочки (капсида) вирусная НК сама попасть в клетку не может. Поэтому дезинфекция, вызывающая разрушение белков оболочки вируса (кипячение, хлорирование, обработка карболовой кислотой и др.), – эффективное профилактическое мероприятие. Наш организм тоже обладает защитными механизмами. Так, иммунный белок интерферон способен защищать организм человека от проникновения вирусов гриппа. В целях профилактики воздушно-капельных вирусных инфекций эффективно обрабатывать защитными средствами носовую полость.
Кроме того, сейчас создано несколько видов антивирусных препаратов как на основе неорганических веществ (ремантадин), так и на основе синтетических антител (виферон, биферон и т. д.). Несмотря на то что фармакология и вирусология ведут постоянные успешные исследования, не надо забывать, что соблюдение мер личной гигиены является надежным методом профилактики вирусных инфекций.
Ученые полагают, что вирусы и бактериофаги представляют собой обособившиеся генетические элементы клеток, подвергшиеся эволюции вместе с клеточными формами жизни.
Открытие вирусов
В 1892 году Д.И. Ивановский (см. Рис. 1), изучая мозаичную болезнь табака (см. Рис. 2), установил, что причиной заболевания является некое инфекционное начало, содержащееся в листьях больных растений, которое проходит через фильтр, задерживающий обыкновенные бактерии. Если профильтрованный сок внести в листья здоровых растений, то они также заболевают мозаичной болезнью.

Рис. 1. Д.И. Ивановский

Рис. 2. Мозаичная болезнь табака
В 1898 году независимо от Ивановского аналогичные результаты получил голландский микробиолог М. Бейеринк. Однако он предположил, что мозаичную болезнь табака вызывают не мельчайшие бактерии, а некое жидкое заразное начало, которое он назвал фильтрующим вирусом.
Размеры вирусов определяются нанометрами (20-200 нм), поэтому их изучение началось после открытия электронного микроскопа. В настоящее время описаны вирусы практически всех групп живых организмов.
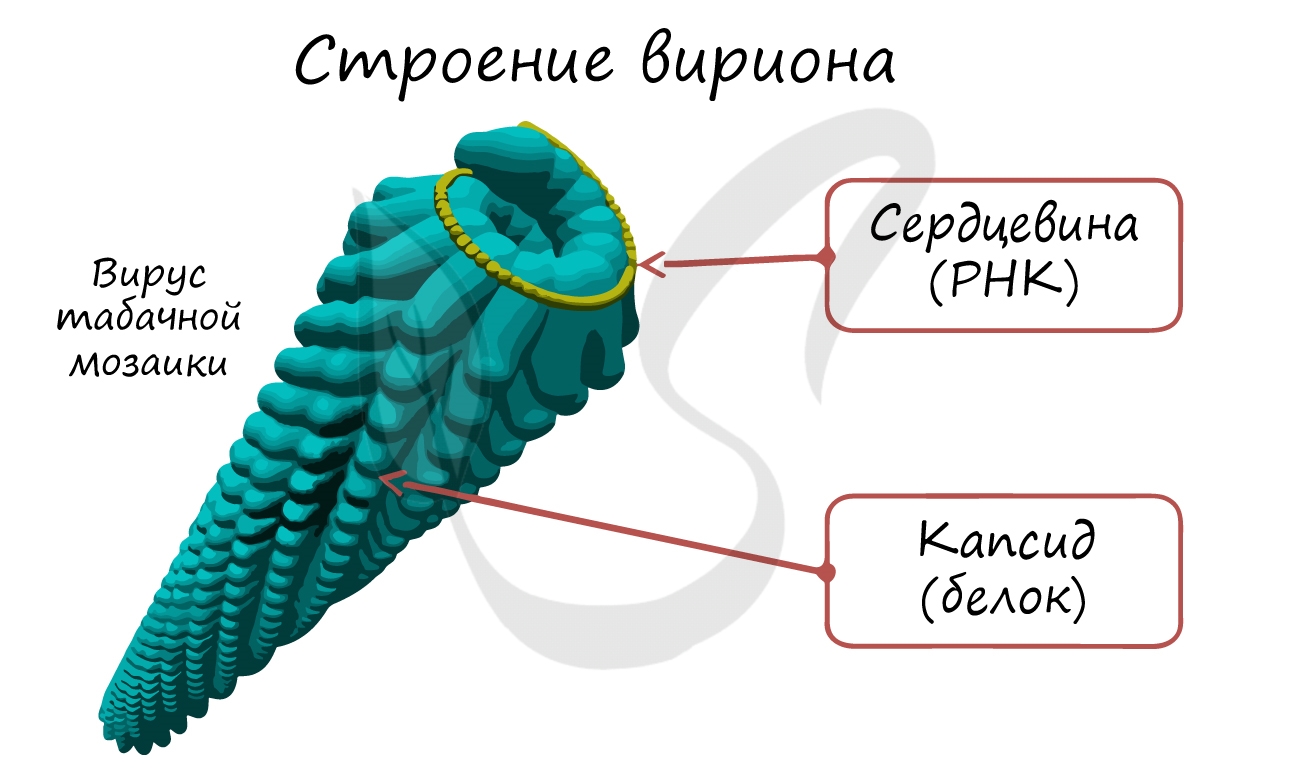
Строение вирусов
Вирусы – неклеточные формы жизни. Они состоят (см. Рис. 3) из фрагмента генетического материала (РНК или ДНК), составляющего сердцевину вируса, и защитной оболочки, которая называется капсид. У некоторых вирусов (герпес, грипп) есть дополнительная липопротеидная оболочка – суперкапсид, которая возникает из плазматической мембраны клетки-хозяина.

Рис. 3. Строение вируса
Вирусы не способны к самостоятельной жизнедеятельности. Они могут проявлять свойства живого, только попав в клетку-хозяина. Они используют потенциал и энергию этой клетки для создания своих новых вирусных частиц, следовательно, вирусы являются внутриклеточными паразитами.
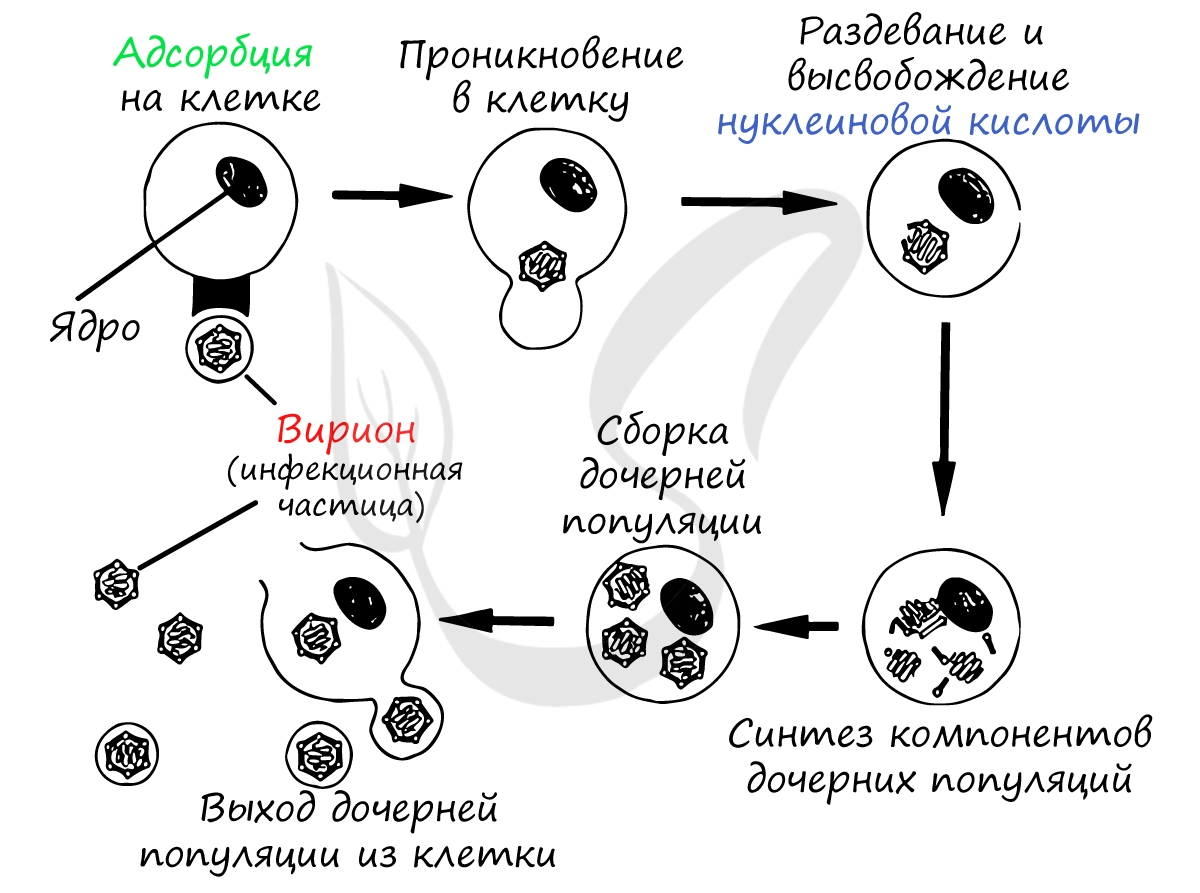
Размножение вирусов
Обычно вирус связывается с поверхностью клетки-хозяина и проникает внутрь. Каждый вирус ищет своего хозяина, то есть клетки строго определенного вида. Например, вирус – возбудитель гепатита (желтуха) проникает и размножается только в клетках печени, а вирус эпидемического паротита (свинка) – только в клетках околоушных слюнных желез человека.
Проникнув внутрь клетки-хозяина, вирусная ДНК или РНК начинает взаимодействовать с ее генетическим аппаратом таким образом, что клетка начинает синтезировать белки, свойственные вирусу (см. Рис. 4).

Рис. 4. Схема репродукции вируса
При заражении ретровирусом (например, вирус иммунодефицита человека (ВИЧ)), у которого в качестве генетического материала используется молекула РНК, наблюдается другая картина. При попадании ретровируса в клетку-хозяина происходит обратная транскрипция. То есть на основе вирусной РНК синтезируется вирусная ДНК, которая встраивается в ДНК человека. Такой тип взаимодействия вируса с клеткой называется интегративным, а встроенная в состав хромосомы клетки ДНК вируса называется провирусом. Далее провирус реплицируется (удваивается) в составе хромосомы и переходит в геном дочерних клеток. Однако под влиянием некоторых физических и химических факторов провирус может выщепляться из хромосомы клетки и переходить к продуктивному типу взаимодействия, то есть синтезировать новые вирусные частицы.
При заражении ВИЧ человек чувствует себя здоровым, пока вирусный генетический материал встроен в хромосому человека. Однако при выщеплении этого вирусного генетического материала из клетки она начинает образовывать новые вирусные частицы, вследствие чего развивается смертельное заболевание – синдром приобретенного иммунодефицита (СПИД).
Вирусы являются возбудителями большого количества заболеваний человека: корь, грипп, оспа, краснуха, энцефалит, свинка, гепатиты, СПИД. Известен также целый ряд заболеваний растений, вызываемых вирусами, например мозаичная болезнь табака, томатов, огурцов или скручивание листьев картофеля. Всего описано около 500 видов вирусов, поражающих клетки позвоночных животных, и около 300 вирусов растений. Некоторые вирусы участвуют в злокачественном перерождении клеток и тем самым провоцируют онкологические заболевания.
ДНК- и РНК-содержащие вирусы
В зависимости от содержащегося генетического материала вирусы подразделяются на ДНК-содержащие и РНК-содержащие.
Одноцепочные РНК-содержащие вирусы подразделяются на:
1. Плюс-нитевые (положительные). Плюс-нить РНК этих вирусов выполняет наследственную (геномную) функцию и функцию информационной РНК (иРНК).
2. Минус-нитевые (отрицательные). Минус-нить РНК этих вирусов выполняет только наследственную функцию.
К РНК-содержащим вирусам относятся более 
вирусов, вызывающих респираторные заболевания, а также вирус гриппа, кори, краснухи, свинки, ВИЧ. Также существует специфическая группа вирусов – арбовирусы, которые переносятся членистоногими.
Двухцепочные ДНК-содержащие вирусы вызывают такие заболевания, как папиллома человека или герпес, гепатит В (гепатит А и гепатит С вызывается РНК-содержащими вирусами).
ДНК-содержащие вирусы поражают также растения. Они вызывают, например, золотую мозаику бобов или полосатость у кукурузы.
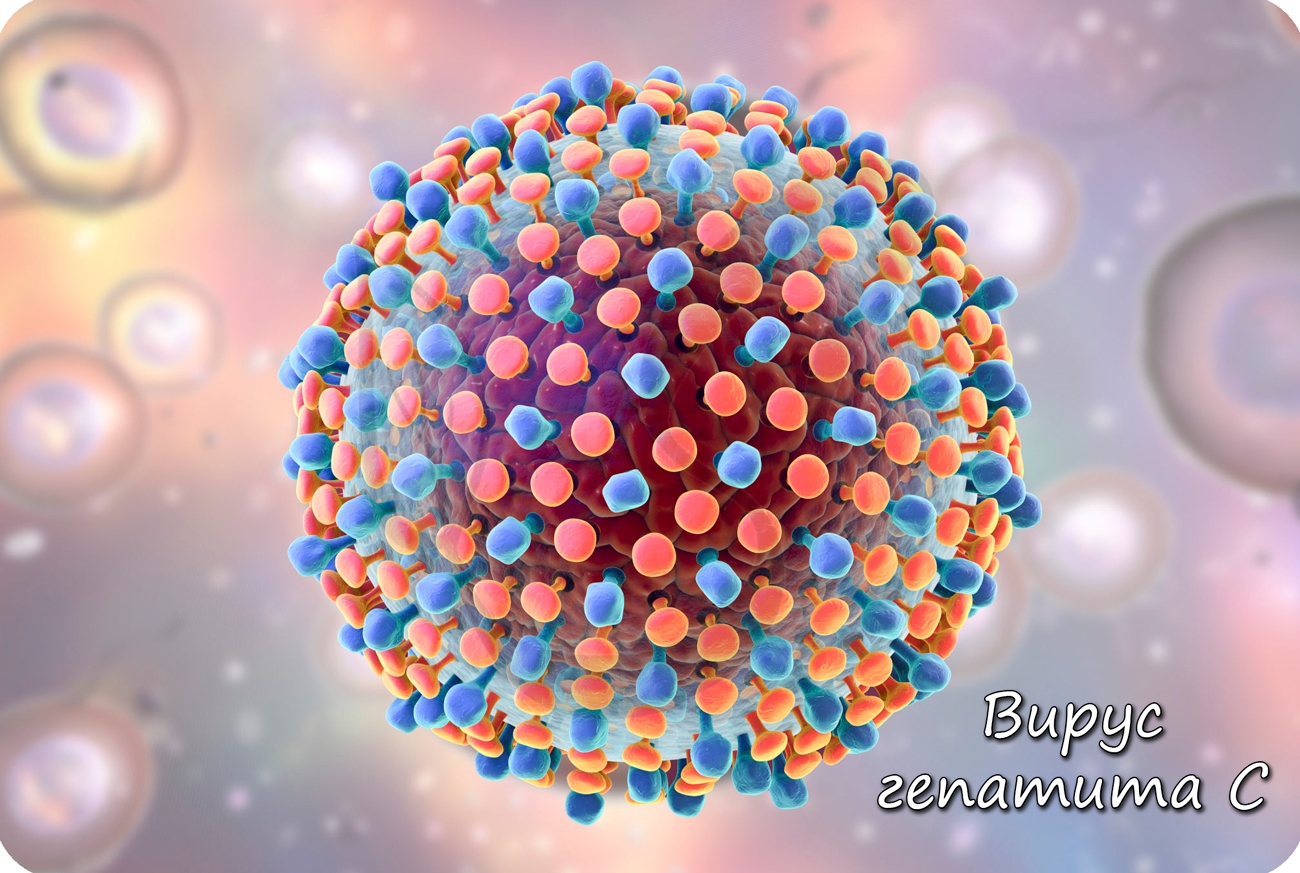
Вирус гепатита С
По своему строению вирус гепатита С – это РНК-содержащий вирус, имеющий сферическую форму, сложно устроенный (см. Рис. 5).
В качестве генетического материала такой вирус содержит линейную однонитчатую молекулу РНК.

Рис. 5. Гепатит С
Вопреки бытующим предрассудкам, подцепить вирус гепатита C невозможно через социальные контакты (поцелуи, объятия), через продукты или воду, через грудное молоко. Вы ничем не рискнете, если разделите с носителем вируса трапезу или напитки. Заразиться гепатитом C можно при контакте с кровью инфицированного человека либо половым путем.
В настоящее время для лечения гепатита С используют два препарата: Интерферон альфа и Рибавирин.
Бактериофаги

Рис. 6. Бактериофаг (Источник)
Особую группу вирусов составляют бактериофаги (или просто фаги), которые заражают бактериальные клетки (см. Рис. 6). Фаг укрепляется на поверхности бактерии при помощи специальных ножек и вводит в ее цитоплазму полый стержень, через который проталкивает внутрь клетки свою ДНК или РНК. Таким образом, генетический материал фага попадает внутрь бактериальной клетки, а капсид остается снаружи. В цитоплазме начинается репликация генетического материала фага, синтез его белков, построение капсида и сборка новых фагов. Уже через 10 мин после заражения в бактерии формируются новые фаги, а через полчаса бактериальная клетка разрушается, и из нее выходят около 200 заново сформированных вирусов – фагов, способных заражать другие бактериальные клетки (см. Рис. 7). Некоторые фаги используются человеком для борьбы с болезнетворными бактериями, вызывающими холеру, дизентерию, брюшной тиф.

Рис. 7. Схема размножения бактериофага (Источник)
Список литературы
- Каменский А.А., Криксунов Е.А., Пасечник В.В. Общая биология 10-11 класс Дрофа, 2005.
- Биология. 10 класс. Общая биология. Базовый уровень / П.В. Ижевский, О.А. Корнилова, Т.Е. Лощилина и др. – 2-е изд., переработанное. – Вентана-Граф, 2010. – 224 стр.
- Беляев Д.К. Биология 10-11 класс. Общая биология. Базовый уровень. – 11-е изд., стереотип. – М.: Просвещение, 2012. – 304 с.
- Агафонова И.Б., Захарова Е.Т., Сивоглазов В.И. Биология 10-11 класс. Общая биология. Базовый уровень. – 6-е изд., доп. – Дрофа, 2010. – 384 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
Домашнее задание
Если вы нашли ошибку или неработающую ссылку, пожалуйста, сообщите нам – сделайте свой вклад в развитие проекта. 

Читайте также:


