Оглавление темы "Методы обнаружения вирусов. Методы диагностики микозов ( грибковых заболеваний ). Методы обнаружения простейших.":
1. Биологические методы диагностики бактерий. Животные при диагностике инфекций. Какие животные используются для диагностики инфекций?.
2. Методы обнаружения вирусов. Лабораторные методы при диагностике вирусных инфекций. Забор материала для выявления вирусов. Культуры клеток для выявления вирусов.
3. Культуры органов для обнаружения вирусов. Куриные эмбрионы при диагностике вирусных инфекций. Заражение вирусом куриного эмбриона. Методы заражения вирусом куриного эмбриона.
4. Животные модели для обнаружения вирусов. Идентификация вирусов. Качественное определение вирусов. Цитопатические эффекты вирусов. Бляшкообразование вируса. Тельца включений вирусов.
5. Отсутствие цитопатического эффекта вируса. Феномен гемадсорбции вирусов. Цветная реакция. Экспресс-диагностика вирусной инфекции.
6. Количественное определение вирусов. Определение инфекционности вирусов. Выявление вирусных антигенов ( Аг ). Выявление вирусных частиц. Морфология вирусов.
7. Серологические методы диагностики вирусных инфекций. Торможение гемагглютинации. Торможение цитопатического эффекта интерференцией вирусов. Прямая иммунофлюоресценция. Иммуноэлектронная микроскопия.
8. Выявление противовирусных антител ( AT ) в сыворотке крови. РТГА. РСК. РИФ. Иммуносорбционные методы выявления противовирусных антител.
9. Выявление вирусных антигенов ( Аг ). ИФА. Гибридизация ДНК. ПЦР. Методы диагностики микозов ( грибковых заболеваний ).
10. Выделение грибов. Неселективные среды для грибов. Селективные среды для грибов. Выявление противогрибковых антител ( AT ). Выявление грибковых антигенов ( Аг ).
11. Методы обнаружения простейших. Микроскопия простейших. Материал для выявления простейших. Выделение простейших. Серологические исследования при диагностике простейших.
Методы обнаружения вирусов. Лабораторные методы при диагностике вирусных инфекций. Забор материала для выявления вирусов. Культуры клеток для выявления вирусов.
Лабораторные методы при диагностике вирусных инфекций включают:
• выделение и идентификацию возбудителя;
• обнаружение и определение титров противовирусных AT;
• обнаружение Аг вирусов в образцах исследуемого материала;
• микроскопическое исследование препаратов исследуемого материала.
При заборе материала для исследований необходимо выполнять следующие условия:
• образцы следует отбирать как можно раньше либо с учётом ритма циркуляции возбудителя;
• материал следует отбирать в объёме, достаточном для всего комплекса исследований;
• образцы следует доставлять в лабораторию незамедлительно (!), при относительно кратковременной транспортировке (не более 5 сут) образцы сохраняют на льду, при более длительной — при температуре -50 С.
![]()
Выделение и идентификация возбудителя — золотой стандарт в диагностике вирусных инфекций.
Вирусы размножаются только в живых клетках, и выделение возбудителя в заражённой культуре клеток — один из основных методов диагностики вирусных инфекций. Поскольку большинство патогенных вирусов отличает тканевая и типовая специфичность, то почти к каждому вирусу можно подобрать соответствующие клеточные или тканевые чультуры, а также создать стандартные условия культивирования (наличие клеток одного типа). Размножение вируса обеспечивают чувствительные (пермиссивные) клетки. Поэтому при выделении неизвестного возбудителя проводят одномоментное заражение 3
4 культур клеток, предполагая, что одна из них может оказаться пермиссивной. Культуры клеток получают диспергированием соответствующих органов и тканей, но чаще используют эмбриональные ткани (человека и животных) либо трансформированные опухолевые клетки. При помещении на соответствующую плоскую поверхность клеточные культуры обычно растут в виде монослоя. Первично-трипсинизированные культуры. Суспензии клеток получают гомогенизированием соответствующих тканей, предварительно обработанных трипсином. Культуры часто представлены клетками смешанного типа и не подлежат повторному культивированию. Жизнеспособность таких культур составляет 2-3 нед.
Полуперевиваемые линии клеток представлены диплоидными клетками человека и животных. Культуры ограниченно пригодны к повторному диспергированию и росту (как правило, не более 20-30 пересевов), сохраняя при этом жизнеспособность и не подвергаясь спонтанной трансформации.
Перевиваемые линии клеток (гетероплоидные культуры) представлены клетками, подвергнутыми длительному культивированию и спонтанным трансформациям. Культуры способны к многократному диспергированию и перевиванию. Работа с ними менее трудоёмка по сравнению с приготовлениями первичных культур; перевиваемые клетки относительно одинаковы по своей морфологии и стабильны по свойствам.
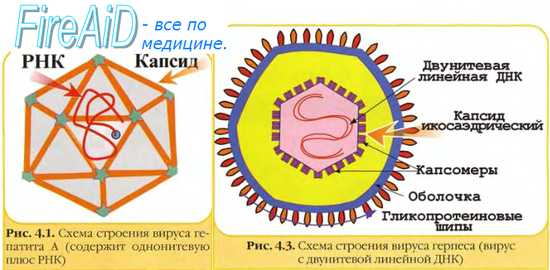
Большинство вирусов обнаруживают при помощи электронной микроскопии. При помощи электронной микроскопии выявлено большое разнообразие морфологии вирусов и изучена ультраструктура вирусных частиц.
В световом микроскопе видны только крупные вирусы (200 нм и больше). Эти вирусы окрашивают по Романовскому-Гимзе и рассматривают при иммерсионной микроскопии.
Вирусы меньше, чем 200 нм окрашивают серебрением по Морозову. Они увеличиваются в размерах и под световым микроскопом вирусы имеют черный цвет и круглую форму. Вирусы оспы, окрашенные по Морозу, - тельца Пашена.
Для диагностики вирусных инфекций в пораженных клетках обнаруживают вирусные тельца или включения. Это скопления вирусных частиц или колонии вирусов в клетке. Они окрашиваются специальными методами и изучаются с помощью светового микроскопа. Образование внутриклеточных включений отмечено при многих вирусных инфекциях. Включения имеют разную величину (от 0,25 до 20-30 нм) и форму (круглая, овальная, грушевидная, веретенообразная, неправильная).
Например, при бешенстве в цитоплазме нервных клеток обнаруживаются тельца Бабеша-Негри. При натуральной оспе в цитоплазме эпителиальных клеток обнаруживаются тельца Гварниери.
Морфология бактериофагов и особенности их взаимодействия с бактериальной клеткой.
Бактериофаги ("пожиратели бактерий") – это вирусы бактерий. Размеры такие же, как у вирусов, – 20 – 200 нм. Как и вирусы, бактериофаги проходят через бактериальные фильтры и размножаются только в живых клетках. Бактериофаги в природе находятся там, где бактерии: в воде, почве, молоке, в организме людей и животных.
С помощью электронного микроскопа показано, что большинство бактериофагов имеют форму головастика или сперматозоида. Они состоят из головки и хвостового отростка. Отросток – стержень с чехлом. Стержень заканчивается шестиугольной пластинкой с короткими шипами, от которых отходят фибриллы. Чехол может сокращаться. Внутри головки находится ДНК. ДНК окружена капсидом. В отростке находятся ферменты – лизоцим и АТФаза. Они участвуют в проникновении фага в клетку.
Взаимодействие бактериофага с бактериальной клеткой называется бактериофагией. Стадии взаимодействия фага с клеткой такие же, как и у вирусов: адсорбция, проникновение в клетку, синтез нуклеиновых кислот и белков, морфогенез, выход из клетки. Но имеются особенности. Фаги обладают строгой специфичностью взаимодействия. Определенный фаг взаимодействует с определенным видом или даже подвидом бактерий. По этому название бактериофагов такие же, как видовые или родовые названия тех бактерий, с которыми они взаимодействуют. Например, стафилофаги, дизентерийные фаги и т.д.
Интересен процесс проникновения фагов с хвостовыми отростками в клетку. Эти фаги адсорбируются при помощи фибрилл, сокращается чехол (при помощи АТФазы), и стержень внедряется в клетку (при помощи фермента лизоцима). ДНК проходит через стержень в цитоплазму клетки. Капсид и отросток остаются вне клетки. Через 5 минут начинается синтез нуклеиновых кислот и белков, а через 30-40 минут бактериальная клетка разрушается (лизируется). В окружающую среду выходит около 200 новых фаговых частиц.
Явление бактериофагии можно обнаружить при выращивании бактерий на жидких и плотных питательных средах. На жидких средах при действии фагов наблюдается просветление жидкости с бактериальной культурой. . На твердых средах на фоне сплошного роста бактерий образуются стерильные пятна круглой или неправильной формы. Они образуются на месте разрушения (лизиса) бактерий. Это "негативные колонии" бактериофага.
Различают: а) поливалентные фаги – взаимодействуют с родственными видами бактерий; б) моновалентные – взаимодействуют с одним определенным видом; в) типовые фаги – взаимодействуют с отдельными вариантами (типами) данного вида бактерий.
Фаги делятся на вирулентные и умеренные. Вирулентные фаги проникают в клетку, размножаются в ней и вызывают ее лизис. Умеренные фаги проникают в клетку и встраиваются в хромосому бактерии. Лизис при этом не происходит. Встроенный в хромосому бактерии фаг называется профагом. Бактериальные клетки, содержащие профаг, называются лизогенными, а само явление – лизогения. Лизогенные бактерии имеют дополнительные свойства (образование токсинов и др). Изменение свойств называется фаговой конверсией. Под влиянием УФ лучей и химических веществ профаг может превращаться в вирулентный фаг. Это явление называется индукцией фага.
Умеренные фаги – мощный фактор изменчивости микроорганизмов и могут нанести вред микробиологическому производству
Получение и применение бактериофагов. Для получения препаратов бактериофагов используют проверенные производственные штаммы фагов и соответствующие им типичные культуры бактерий. В бактериальную культуру в жидкой питательной среде вносят маточную взвесь фага. После просветления (лизиса) культуру фильтруют через бактериальные фильтры, и фильтрат вносят в свежую культуру соответствующих бактерий и т.д. После накопления достаточного количества фага лизированную им культуру бактерий вновь фильтруют, и получают препарат фага.
Таким образом, препараты фагов получают путем многократного пассирования через чувствительную бактериальную культуру, а сами препараты фагов – фильтраты бульонных культур лизированных ими бактерий. Это прозрачные жидкости светло-желтого цвета, а также на их основе готовят другие лекарственные формы - таблетки с кислотоустойчивым покрытием, мази, аэрозоли, свечи.
Применение фагов основано на их строгой специфичности. Они используются для:
а) диагностики инфекционных заболеваний (диагностические препараты): с помощью известного фага можно определить вид или подвид бактериальной культуры;
б) лечения и профилактики заболеваний (лечебно-профилактические препараты).
Относящийся к данному классу атомно-силовой микроскоп оказался инструментом, подходящим для исследования биологических объектов и позволил не только визуализировать наноразмерные структуры, но и манипулировать ими. В частности, принципиально возможной оказалась манипуляция одиночными вирионами и прямое измерение сил, возникающих при их контакте с поверхностью клетки. Такие эксперименты позволяют получать подробные данные о самом первом и во многих случаях еще недостаточно исследованном этапе заражения клетки – адгезии вируса к ее поверхности. Данные исследования представляют и значительный практический интерес, т.к. могут дать ключ к созданию эффективных противовирусных препаратов, защищающих клетки от проникновения вирусов.
Вирусы являются чрезвычайно малыми объектами – их размеры лежат в диапазоне от нескольких десятков до нескольких сотен нанометров. Первым и на долгое время единственным методом прямой визуализации наноразмерных частиц стала электронная микроскопия (ЭМ), которая начала развиваться в 1930-е гг. Метод, оказавшийся очень информативным, позволил не только детально охарактеризовать структуру различных вирусов, но и исследовать процессы, происходящие в зараженной клетке.
Оказалось, что форма вирусных частиц отличается большим разнообразием: от правильных сфер до сложных структур, напоминающих кирпичи, обклеенные трубочками (вирус натуральной оспы), или щетинистых червей (вирус геморрагической лихорадки Эбола).
Вне клетки любой вирус является всего лишь молекулярным контейнером с генетическим материалом (ДНК или РНК) и вряд ли может считаться полноценным живым организмом, хотя по этому вопросу в научной среде до сих пор нет окончательной терминологической определенности.
Так, исследование репликации вируса методом просвечивающей электронной микроскопии на ультратонких срезах выглядит следующим образом: зараженные клетки обрабатывают фиксирующим раствором, обезвоживают спиртом и заливают специальной смолой. После отвердевания смолы с помощью специального прибора – ультратома – делают ультратонкие (≈ 50 нм) срезы, которые затем наносят на специальную сетку и обрабатывают растворами солей тяжелых металлов. Во время самого микроскопического исследования образец находится в вакуумной камере и подвергается действию пучка электронов с энергией в несколько десятков кэВ. Очевидно, что прижизненная визуализация в данном случае принципиально невозможна.
В течение почти полувека электронная микроскопия оставалась единственным методом визуализации наноразмерных объектов. Однако в начале 1980-х гг. эта монополия была нарушена появлением сканирующей зондовой микроскопии (СЗМ). Основным принципом СЗМ является сканирование – прецизионное (с высокой точностью) перемещение зонда вблизи исследуемой поверхности, сопряженное с отслеживанием определенного параметра, характеризующего взаимодействие между зондом и образцом. Результатом такого сканирования является топографическая карта рельефа поверхности образца.
Первым прибором СЗМ стал сканирующий туннельный микроскоп (СТМ), который мог лишь весьма ограниченно использоваться для визуализации биологических объектов, так как для его работы требовалась высокая электрическая проводимость исследуемой поверхности.
В 1986 г. швейцарский физик Г. Бинниг и его коллеги создали новый прибор семейства СЗМ – атомно-силовой микроскоп (АСМ). В основе его работы лежит силовое (Ван-дер-Ваальсово) взаимодействие атомов зонда и поверхности. АСМ не требуется электрическая проводимость поверхности образца, и он может осуществлять съемку в жидкой среде. Поэтому этот прибор оказался удобным инструментом для исследования биологических объектов.
![]()
С момента появления атомно-силового микроскопа было опубликовано огромное число работ, посвященных АСМ-визуализации самых разнообразных биологических образцов. Следует все же признать, что в большинстве случаев в плане визуализации АСМ не дает ничего принципиально нового в сравнении с обычной электронной микроскопией, поэтому зачастую данный метод воспринимается биологами как техническая экзотика, а не как полноценный исследовательский инструмент.
Однако важнейшим, пусть и почти единственным преимуществом визуализации биологических объектов при помощи АСМ по сравнению с электронной микроскопией является возможность выполнения исследований нативных, природных образцов без какой-либо фиксации и специальной пробоподготовки, при физиологических параметрах среды.
Помимо визуализации рельефа поверхности с субнанометровым разрешением АСМ позволяет осуществлять прямое измерение сил, возникающих при взаимо¬действии одиночных наноразмерных объектов.
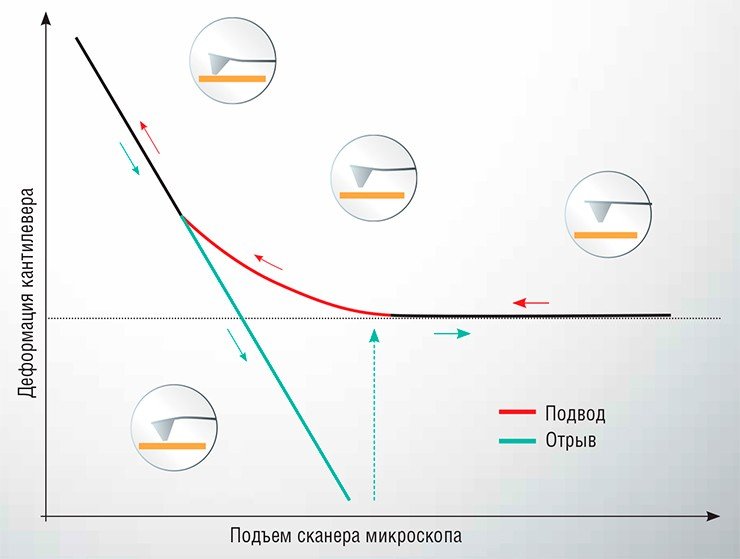
Проводятся такие измерения следующим образом: один объект закрепляется на острие зонда АСМ, а второй фиксируется на подложке, после чего зонд подводится к поверхности подложки до достижения механического контакта, а затем возвращается обратно. В ходе этого перемещения отслеживается деформация упругой консоли (кантилевера). Зависимость этого параметра от расстояния между зондом и подложкой называется силовой кривой. С ее помощью можно определить величину силы, действующей между исследуемыми объектами. Этот метод, названный атомно-силовой спектроскопией (АСС), может использоваться для исследования силовых характеристик взаимодействия самых разнообразных малых объектов: от неорганических наночастиц до вирусов и живых клеток.
![]()
Начальным этапом заражения клетки вирусом является адгезия (прилипание) вирусной частицы (вириона) к клеточной поверхности с последующим проникновением генетического материала вируса внутрь клетки. Этот процесс, определяемый взаимодействием белковых рецепторов, расположенных на поверхности клетки, с поверхностными белками вириона, является критически важным для размножения вируса. И, надо отметить, в большинстве случаев изучен недостаточно.
![]()
Однако фиксация одиночной вирусной частицы на острие зонда атомно-силового микроскопа является весьма непростой задачей. Для успешного проведения эксперимента требуется большая подготовительная работа:
- получить как можно более чистый и концентрированный препарат вируса;
- подготовить на острие зонда площадку подходящего размера для посадки вириона;
- химически активировать поверхность зонда для образования ковалентных связей при контакте с белками вируса;
- убедиться в том, что на зонде закрепился действительно вирион, а не молекулы свободного белка или мелкие фрагменты клеток, всегда присутствующие в препаратах вирусов.
Оценка концентрации и степени чистоты препарата вируса обычно проводится методом просвечивающей электронной микроскопии. Площадку на острие АСМ-зонда, которое обычно изготавливают из кремния или его нитрида, формируют путем длительного сканирования кремниевой или сапфировой подложки при больших значениях развертки и силы прижатия зонда к поверхности. Наиболее наглядной иллюстрацией для этого процесса служит изменение формы острия карандаша в ходе интенсивного рисования.
По меркам микроскопии, клетка высших организмов является относительно крупным (≈ 10 мкм) объектом, поэтому хорошо видна в световом микроскопе, при помощи которого на нее наводится кантилевер атомно-силового микроскопа. Но как быть с самим зондом, на острие которого предполагается наличие вириона? Строго говоря, вместо вириона там может оказаться все, что угодно: монослой белковых молекул, фрагмент клетки или вириона, агрегат из нескольких вирионов, случайное загрязнение и т. д. Кроме того, в процессе измерения вирион может разрушиться или оторваться от зонда. Визуализация же зонда с вирусной частицей методом электронной микроскопии до силовых измерений недопустима, так как под воздействием высушивания, вакуума и пучка электронов вирион приобретет необратимые изменения.
Наиболее эффективным методом решения данной проблемы оказалась визуализация острия зонда АСМ с помощью электронной микроскопии, осуществляемая непосредственно после силовых измерений. Если на острие будет обнаружена вирусная частица, уцелевшая в ходе эксперимента, то все сомнения развеются.
В течение последних пятидесяти лет в результате поистине титанической работы, проделанной электронными микроскопистами всего мира, накоплен огромный багаж знаний в области ультраструктурных аспектов репликации различных вирусов. Создание атомно-силового микроскопа и техники силовой спектроскопии позволило вплотную приблизиться к произвольной механической манипуляции одиночными вирусными частицами. Это выводит изучение взаимодействия вируса с клеткой на принципиально другой уровень – от структурных исследований к функциональным.
При этом атомно-силовая спектроскопия не является конкурентом для электронной микроскопии, а открывает новое самостоятельное направление исследований – наномеханику взаимодействия вирусной частицы с поверхностью клетки. Весьма вероятно, что в самом ближайшем будущем в данном направлении будут совершены фундаментальные открытия, соизмеримые по значимости с достижениями электронной микроскопии в середине прошлого века.
Изучение механизмов связывания вирусных частиц с поверхностью клетки вызывает значительный интерес не только с позиции фундаментальной науки, но и в контексте практических приложений. Более детальное понимание этих механизмов на молекулярном уровне может дать человечеству ключ к созданию эффективных противовирусных препаратов, защищающих клетки от проникновения вирусов.
*Просвечивающая электронная микроскопия с использованием специальной жидкостной ячейки и сканирующая электронная микроскопия при атмосферном давлении позволяют исследовать биологические объекты без фиксации, но из-за ряда технических трудностей и относительно низкого пространственного разрешения эти методы не получили широкого распространения
Корнеев Д. В., Бессуднова Е. В., Зайцев Б. Н. Изучение взаимодействия наночастиц TiO2 и поверхности эритроцитов человека методом атомно-силовой спектроскопии // УНЖ. 2012. № 4. С. 73—77.
Миронов В. Л. Основы сканирующей зондовой микроскопии. Нижний Новгород: ИФМ РАН, 2004. 182 с.
Alsteens D., Pesavent E., Cheuvart G. et al. Controlled manipulation of bacteriophages using single-virus force spectroscopy // ACSNANO. 2009. V. 3(10). P. 3063—3068.
Alsteens D., Trabelsi H., Soumillion P., Dufrene Y. F., Multiparametric atomic force microscopy imaging of single bacteriophages extruding from living bacteria // Nature Communications. V. 4. Article number: 2926.
Binnig G., Quate C. F., Gerber Ch. Atomic force microscope // Phys. Rev. Lett. 1986. V. 56(9). P. 930—933.
Cappella B., Dietler G. Force-distance curves by atomic force microscopy // Surf. Sci. Rep. 1999. V. 34. P. 1—104.
Malkin A.J., Plomp M., McPherson A. Unraveling the architecture of viruses by high-resolution atomic force microscopy // Methods Mol. Biol. 2005. V. 292. P. 85—108.
В публикации использованы фото автора
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
|