Иммуноферментный анализ при ящуре
О . А . Верк о вс кий , доктор биологических наук,
заведующий отделом иммунологии НПО НАР ВАК
Теоретические и практические достижения ветеринарной науки значительно расширили арсенал методов диагностики и средств специфической профилактики инфекционных болезней крупного рогатого скота. При этом развитие новых подходов к предупреждению инфекционных болезней и изучение механизмов иммунологической защиты животных неразрывно связаны с разработкой и внедрением новых методов и технологий, основанных на современных представлениях об эффекторных механизмах иммунитета, среди которых главное место занимает взаимодействие анти ген-антитело.
Иммуноферментный анализ (ИФА) к настоящему времени прошел путь от новейшей научной разработки до рутинного метода в клинической диагностике. С его помощью можно проводить как массовое обследование стад, так и поставить окончательный диагноз у конкретного животного.
По сравнению с другими методами выявления антигенов и антител профессионально разработанные иммуноферментные тест-системы обладают следующими преимуществами:
- высокой чувствительностью, позволяющей выявлять концентрации белка в диапазоне нг/мл, и специфичностью;
- воспроизводимостью полученных результатов;
- стабильностью при хранении всех необходимых реагентов (до года и более);
- простотой проведения реакции и возможностью использования минимальных объемов исследуемого материала;
- наличием инструментального (в качественном и количественном варианте) учета реакции и возможностью автоматизации всех ее этапов.
При инструментальной оценке результат ИФА может быть качественным (позволяет судить о наличии или отсутствии специфических антител) и полуколичественным (позволяет получить информацию об относительном содержании антител в испытуемых пробах). Оба варианта являются приблизительными, однако они намного точнее методов определения титров антител в реакциях с визуальным учетом.
Специалисты НПО НАРВАК в сотрудничестве с ведущими отечественными и зарубежными учеными внедрили в ветеринарную практику нашей страны ИФА-наборы для диагностики лейкоза и ящура, проводят эксперименты по созданию ИФА-набора для диагностики бруцеллеза. Условия применения данных наборов - любые лаборатории, оснащенные стандартным оборудованием для ИФА. ИФА - диагностика лейкоза
"Набор для выявления антител к вирусу лейкоза крупного рогатого скота (ВЛКРС методом им-муноферментного анализа (ИфА)", выпускаемый в двух вариантах:
- И ФА-набор для проведения массовых скри-нинговых исследований - скринирующий тест;
- ИФА-набор (VeriTest) для подтверждения положительных результатов - подтверждающий (конфирмационный или верификационный) тест.
Как и большинство зарубежных аналогов оба варианта ИФА предназначены для выявления антител к поверхностному гликопротеину др51 ВЛКРС в сыворотке крови и молоке животных.
Использование подтверждающего ИфА-набо-ра VeriTest является очень важным моментом при диагностических исследованиях на лейкоз, поскольку одним из наиболее важных вопросов при проведении ИФА является вопрос о специфичности результатов. Так при применении только скриниру-ющего теста, некоторые пробы, взятые от животных с различной патологией, могут давать ложнополо-жительные результаты вследствие синтеза перекрестно-реагирующих антител. Поэтому возможное существование ложнопозитивных результатов ставит перед лабораторным работником задачу их разграничения с истинным выявлением антител к ВЛКРС. Для решения этой задачи и служит ИФА-набор VeriTest, который применяется для подтверждения положительных результатов скринирующего теста.
Таким образом, алгоритм серологического обследования на лейкоз при совместном применении РИД и ИФА следующий.
1) Животные положительные в РИД считаются инфицированными, в ИФА не проверяются и подлежат выбраковке.
2) Отрицательные результаты в РИД, должны быть перепроверены в ИФА и только после этого животные могут считаться серонегативными.
3) Первичное тестирование проб в ИФА проводится в скринирующем тесте и при отсутствии положительной реакции выдается заключение об отсутствии серологических данных инфицирования ВЛКРС. При положительном результате теста проба подлежит исследованию в подтверждающем тесте. При отрицательном результате подтверждающего теста, проба считается серонегативной по ВЛКРС, положительный результат является основанием для окончательного подтверждения серологического диагноза на лейкоз.
Такая схема проведения диагностических исследование за два последних года с успехом апробирована в ряде ветеринарных лабораторий нашей страны и показан ее практический эффект.
Если имеется возможность, то вместо скринирующего ИФА-набора можно сразу же использовать ИФА-набор VeriTest и тем самым упростить алгоритм серологического обследования на лейкоз и сократить число необходимых анализов.
ИФА - диагностика ящура
"Набор для выявления антител к вирусу ящура ЗАВС иммуноферментным методом (ИФА)" предназначен для выявления постинфекционных антител в сыворотке крови крупного рогатого скота.
Набор позволяет обнаружить антитела к неструктурному белку вируса ящура - ЗАВС (в системе используется рекомбинантный белок MSP ЗАВС в качестве антигена), который отсутствует (или скрыт для распознавания клетками иммунной системы) в инактивированных вакцинных препаратах. Поэтому у здоровых или вакцинированных животных антител к ЗАВС белку нет (реакция отрицательная), а у экспериментально зараженных или спонтанно инфицированных животных (даже ранее вакцинированных), в организме которых присутствовал живой вирус ящура - антитела данной специфичности есть (реакция положительная).
Данное заключение демонстрируют результаты, полученные нами при испытании данного набора в профильной лаборатории ФГУ ВНИИЗЖ (табл.1). Для проверки были использованы сыворотки крови крупного рогатого скота, полученные от. а) животных, переболевших ящуром (в динамике с интервалом 3- 5 суток после заражения); б) от животных, вакцинированных против ящура; в) животных сначала вакцинированных против ящура, затем экспериментально зараженных вирулентным вирусом; г) от клинически здоровых неиммунных животных. Исследования проводили в сравнительном аспекте с набором аналогичной направленности и с параллельным определением активности испытуемых сывороток в реакции микронейтрализации и в стандартном варианте непрямого ЙфА, где в качестве антигена используются структурные белки вириона.
Таким образом, отличительной особенностью ИФА-набора для выявления антител к антигену ЗАВС вируса ящура является его способность дифференцировать здоровых и вакцинированных животных от инфицированных и вирусоносите-лей, поэтому его использование незаменимо при проведении оздоровительных и мониторинговых мероприятий.
ИФА - диагностика бруцеллеза
В течение последних лет ряд зарубежных компаний выпускают ИФА-наборы, предназначенные для выявления антител к возбудителям бруцеллеза крупного рогатого скота, овец и коз (Brucella abortus и Brucella melitensis). В настоящее время в НПО проводятся подобные исследования.
В лабораторных исследованиях обычно используют два варианта ИФА: непрямой и конкурентный. Однако на практике наибольшей ценностью обладает конкурентный ИФА, отличительной особенностью которого является возможность дифференцировать животных инфицированных бруцеллами от животных, вакцинированных вакциной из штамма 19 (и возможно из штамма 82). Метод основан на конкурентном взаимодействии моноклональных антител к о-полисахариду S-LPS антигена В. abortus и сывороточных антител к бруцеллам с S-LPS антигеном В. abortus. При отсутствии в исследуемой сыворотке крови антител к В. abortus или В. melitensis, МкА связывается с иммобилизованным S-LPS антигеном, формируя при этом комплекс антиген-антитело. Полученный иммунный комплекс выявляется после взаимодействия с антивидовым конъюгатом, фермент которого после добавления субстрата, вызывает разложение субстрат-индикаторного раствора и образование окрашенного продукта. Если исследуемая сыворотка содержит антитела к бруцеллам, то они конкурируют с МкА за связывание с сайтами антигена и препятствуют взаимодействию МкА с о-полисахаридом S-LPS антигена, в результате чего интенсивность окраски снижается.
Сыворотка крови животных, вакцинированных вакциной из штамма 19, содержит низкоаффинные антитела, которые не конкурируют с МкА за связывание с антигеном, что приводит к отрицательной реакции. Однако в ряде случаев через 6 месяцев после вакцинации животные могут реагировать положительно.
Нами были проведены предварительные испытания двух тест-систем с использованием охарактеризованных в РА сывороток крови крупного рогатого, полученных из ФГУ ВГНКИ (табл.2).
Проведенные исследования показали, что по чувствительности оба варианта ИФА превосходят РА, однако для подтверждения диагностической ценности конкурентного метода проводятся более расширенные испытания с хорошо охарактеризованной панелью сывороток крови, полученных от больных и вакцинированных животных. Есть предположение, что данная тест-система может быть также использована в медицине для выявления антител к бруцеллам у инфицированных людей.

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
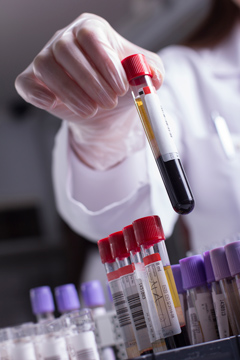
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
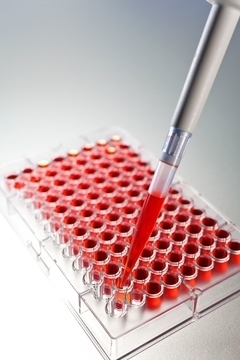
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?
Аннотация научной статьи по ветеринарным наукам, автор научной работы — Афонина Д. Н., Камалова Н. Е., Каньшина А. В., Тимина А. М.
Похожие темы научных работ по ветеринарным наукам , автор научной работы — Афонина Д. Н., Камалова Н. Е., Каньшина А. В., Тимина А. М.
DIAGNOSTIC VALUE OF A TEST FOR DETECTION OF SECRETORY IgA FOR CONFIRMATION OF ABSENCE OF FMD VIRUS CIRCULATION
СЕЛЬСКОХОЗЯЙСТВЕННАЯ БИОЛОГИЯ, 2014, № 6, с. 73-80
Серодиагностика вирусов, иммунология
УДК 619:616.98:578.835.2:616-079.4 doi: 10.15389/agrobiology.2014.6.73rus
О ДИАГНОСТИЧЕСКОЙ ЦЕННОСТИ ТЕСТА ПО ВЫЯВЛЕНИЮ СЕКРЕТОРНЫХ IgA ДЛЯ ПОДТВЕРЖДЕНИЯ ОТСУТСТВИЯ ЦИРКУЛЯЦИИ ВИРУСА ЯЩУРА
Д.Н. АФОНИНА, Н.Е. КАМАЛОВА, А.В. КАНЬШИНА, A.M. ТИМИНА
Ключевые слова: ящур, секреторный иммуноглобулин А, иммуноферментный анализ, вирусоносительство, поствакцинальный контроль.
Известно, что секреторные иммуноглобулины А (sIgA) обеспечивают первую линию защиты против многих возбудителей инфекций (1). В секретах sIgA, связавшись с бактериями и вирусами, предотвращают их адгезию на поверхности слизистой оболочки, а в высоких концентрациях блокируют прикрепление вируса к клеточной стенке. В то же время низкие концентрации полимерных sIgA способны ингибировать внутриклеточную репликацию вируса, не оказывая при этом заметного влияния на
его адгезивные свойства. служат медиатором нейтрализации вирусов (после нейтрализации вируса возможно, способствуют элиминации
вируса), а также стимулируют фагоцитоз, обеспечивая тем самым местную резистентность к инфекции. Предполагается, что увеличение содержания в крови связано не только с повреждением эпителия, но и с усилением его образования в поврежденных органах (2). Информация о разработке тестов, предназначенных для обнаружения специфических свидетельствует о возможности применения этого феномена в комплексе мониторинговых исследований в отношении ящура (3, 4).
В России среди оперативных и превентивных мер борьбы с ящуром как особо опасной для животноводства инфекцией доминирует вакцино-профилактика. Однако не исключены случаи развития субклинической инфекции, вызванной вирусом ящура (ВЯ) у иммунных животных, которые впоследствии становятся вирусоносителями. В связи с этим вирусоно-сители составляют потенциальную угрозу для восприимчивых животных, поэтому возникает необходимость их идентификации и изоляции, чтобы исключить дальнейшее распространение инфекции (5).
Для выявления животных-вирусоносителей референтным считается метод выделения вируса ящура из проб пищеводно-глоточной жидкости (ПГЖ) в чувствительных культурах клеток (6). Однако острая фаза репликации вируса может быть непродолжительной при отсутствии клинических признаков, поэтому вероятность его обнаружения мала. Для выявления вирусного генома в ПГЖ даже в малых количествах используют высокочувствительную и специфичную ПЦР с обратной транскрипцией (ОТ-ПЦР). В то же время у этого метода существует ряд недостатков. Так, возможны ложноположительные результаты из-за наличия неспецифических ингибиторов, кроме того, в ПЦР амплифицируется даже разрушенный геном вируса, утратившего инфекционность (7).
Есть сообщения об обнаружении геномного материала ВЯ в эпителиальных клетках глотки с помощью гибридизации ш 8иШ, но при массовом скрининге после экстренной вакцинации этот трудоемкий подход неудобен для практического использования. Установлено, что при ящуре в организме животного образуются антитела как к структурным, так и к неструктурным белкам ВЯ, тогда как инактивированная вакцина индуцирует антитела только к структурным белкам. В связи с этим практическое применение получил серологический метод по определению антител к неструктурным белкам (НБ), или так называемые НБ-тесты. Однако их точность при определении антител в сыворотках крови животных зависит от качества коммерческой вакцины или от наличия НБ, а также от количества антигена в вакцине и от частоты вакцинации (8-11). Следовательно, сохраняется актуальность разработки альтернативных или дополнительных методов обнаружения субклинической инфекции ящура среди вакцинированных животных (12).
По сообщениям зарубежных авторов, существует возможность идентификации животных-вирусоносителей с помощью экспресс-теста на основе иммуноферментного анализа, выявляющего sIgA (так называемый 8^А-ИФА) (3, 4, 12). Ранее мы определили оптимальные условия ИФА для обнаружения вирусоспецифических в образцах слюны в одном разведении (14).
Целью этой работы стала апробация и сравнительные испытания тест-системы sIgA-ИФА для обнаружения животных-вирусоносителей.
Методика. В эксперименте использовали крупный рогатый скот (КРС) (96 гол., живая масса 200-300 кг, возраст 18-24 мес) из благополучных по ящуру сельскохозяйственных предприятий (Владимирская обл.), в
Антитела к неструктурным белкам ВЯ определяли, как описано (19). Для выделения вируса пользовались методикой, утвержденной Департаментом ветеринарии МСХ РФ (10.11.2002). Реакцию микронейтрализации вируса (РМН) выполняли согласно указаниям (6), полимераз-ную цепную реакцию в реальном времени (ПЦР-РВ) — в соответствии с рекомендациями (20).
Относительную чувствительность, специфичность и точность теста оценивали по формулам, рекомендованным International Epizootic Bureau (IEB — Международное эпизоотическое бюро, МЭБ) (12):
Относительная чувствительность Se = — + — х 100 %, [1]
Относительная специфичность Sp = —^ + ^ х 100 %, [2]
где a — истинно положительные; b — ложноположительные образцы; c — ложноотрицательные; d — истинно отрицательные образцы.
При статистической обработке данных были использованы общепринятые методы, рекомендованные И.П. Ашмариным и соавт. (1975), и компьютерная программа MS Excel 2003.
Результаты. При экспериментальном заражении ящуром вакцинированных животных генерализацию заболевания (вторичные афты на конечностях) не отмечали (имелись лишь первичные афты на языке), у не-вакцинированных во всех случаях наблюдались ящурные поражения на конечностях и образование афт на языке.
Всего исследовали 96 образцов слюны от интактного КРС, 40 — от вакцинированных, 5 — от инфицированных спустя 21 сут после вакцинации и 96 — от инфицированных животных. В слюне от интактных и вакцинированных животных до экспериментального заражения противо-ящурные sIgA не выявили. После инфицирования у КРС с клиническими признаками ящура sIgA обнаруживались спустя 5-6 сут, на 8-е сут и на 1011-е сут, что согласуется с результатами других исследователей (6).
В опыте на КРС, предварительно иммунизированном вакциной из штамма ВЯ O Pan Asia 2 с последующим экспериментальным заражением штаммом ВЯ О № 2108 Забайкальский/10, отобрали также пять особей без
клинических признаков ящура. Было установлено (данные не опубликованы) близкое антигенное родство штамма ВЯ О № 2108/Забайкальский/2010 со штаммом O Pan Asia 2 (показатель антигенного родства ri = 0,420,47). У этих животных выделение ВЯ из образцов ПГЖ в чувствительных культурах клеток — первичной (почка поросенка СП) и перевиваемых (почка поросенка IB-RS-2 и почка горного козерога ПСГК-30), а также последующие слепые пассажи положительных результатов не дали. Из пяти обследованных животных у одного (№ 8895) наличие sIgA с помощью sIgA-ИФЛ выявили в образце слюны на 18-е сут после заражения при ПП = 53,00±0,05 % и в последующие сроки (с 21-х до 94-х сут) — при значениях ПП от 41,00+0,11 до 115,00+0,41 %. Исходя из результатов теста, концентрация sIgA в слюне животного увеличивалась до 67-х сут (ПП = 115,00+0,41 %, OD405 = 1,20+0,14 о.е.), затем незначительно уменьшалась и сохранялась до конца наблюдения (на 94-е сут ПП = 71,00+0,02 %, OD405 = 0,91+0,14 о.е.).
Полученные данные были подтверждены при исследовании образцов слюны в РМН: титр sIgA на 18-е сут равнялся 1,20+0,05 lg, в период с 21-х по 46-е сут составлял до 1,58+0,08-1,90+0,13 lg, дважды достигая максимума (1,90+0,13 lg) (табл. 1), но при этом с 32-х по 53-и сут оказался низкими (1,07+0,09-1,40+0,10 lg) и имел значения, указывающие на отрицательные результаты теста (см. табл. 1). В завершающий период (после 60-х сут) титр sIgA в целом повышался до 1,50+0,05-1,90+0,13 lg, дважды достигая максимума (см. табл. 1). Анализ результатов определения sIgA в образцах слюны с помощью РМН свидетельствует о существенном колебании значений (как положительные, так и отрицательные), что нежелательно для идентификационного теста.
1. Сравнение динамики накопления антител к вирусу ящура и генома вируса в образцах патологического материала от экспериментально зараженного крупного рогатого скота при исследовании разными методами (М±т)
Срок отбора образцов после заражения, сут Слюна ПГЖ в ПЦР Сыворотка крови
sIgA-ИФА, ПП % РМН, lg НБ-ИФА ИФА, lg РМН, lg
Животное № 8895 (n = 3)
18 53,00+0,05 1,20+0,05 + + 2,71+0,15 2,56+0,05
21 54,00+0,19 1,85+0,05 - + 2,48+0,08 2,70+0,05
28 86,00+0,05 1,58+0,08 + + 2,56+0,08 2,70+0,15
32 56,00+0,10 1,15+0,25 + + 2,56+0,05 2,70+0,05
35 41,00+0,11 1,07+0,09 - + 2,56+0,08 2,70+0,15
39 55,00+0,03 1,90+0,13 + + 2,40+0,10 2,70+0,05
42 78,00+0,11 1,40+0,10 - + 1,95+0,08 2,70+0,05
46 65,00+0,10 1,90+0,13 + + 1,95+0,08 2,56+0,08
49 43,00+0,11 1,20+0,05 - + 2,26+0,15 2,56+0,05
53 43,00+0,03 1,20+0,05 + + 1,95+0,08 2,56+0,05
56 н.и. н.и. + + 2,26+0,15 2,56+0,05
60 41,00+0,19 1,58+0,08 + + 2,26+0,15 2,56+0,05
63 65,00+0,08 1,75+0,13 - + 2,56+0,05 2,56+0,08
67 115,00+0,41 1,85+0,10 - + 2,41+0,15 2,56+0,05
74 91,00+0,21 1,60+0,10 - + 2,33+0,38 2,56+0,05
81 56,00+0,10 1,90+0,13 - + 2,41+0,15 2,56+0,05
88 88,00+0,51 1,80+0,10 - + 2,56+0,05 2,70+0,05
91 78,00+0,02 1,90+0,13 - + 2,70+0,05 2,40+0,10
94 71,00+0,02 1,50+0,05 - + 2,70+0,05 2,56+0,05
Животное № 8898 (n = 3)
18 8,00+0,03 0,83+0,15 - + 3,38+0,08 2,70+0,05
21 10,00+0,05 н.и. + + 3,23+0,07 2,70+0,15
28 26,00+0,09 1,60+0,05 + + 3,00+0,05 2,70+0,08
32 64,00+0,10 1,27+0,12 + + 2,86+0,15 2,70+0,05
35 56,00+0,04 1,60+0,15 + + 3,00+0,05 2,70+0,05
39 68,00+0,05 1,65+0,10 + + 2,86+0,15 2,70+0,08
42 47,00+0,11 1,20+0,05 + + 2,26+0,31 2,70+0,15
46 31,00+0,15 1,50+0,05 + + 2,56+0,08 2,70+0,08
Продолжение таблицы 1
49 83,00+0,13 1,95+0,15 + + 2,86+0,15 2,70+0,08
53 70,00+0,16 1,95+0,05 - + 2,40+0,21 2,70+0,08
56 46,00+0,10 1,80+0,10 - + 2,86+0,15 2,70+0,15
60 77,00+0,02 1,65+0,15 - + 2,70+0,05 2,70+0,08
63 73,00+0,16 1,73+0,08 - + 3,46+0,05 2,70+0,05
67 66,00+0,15 1,50+0,05 - + н.и. 2,70+0,08
74 75,00+0,24 1,95+0,15 - + 2,63+0,37 2,56+0,05
81 68,00+0,15 1,80+0,10 - + 2,78+0,38 2,56+0,05
88 81,00+0,15 н.и. - + 3,46+0,05 2,70+0,15
91 114,00+0,11 н.и. - + 3,00+0,05 2,40+0,10
94 89,00+0,13 н.и. - + 2,86+0,08 2,40+0,15
В НБ-ИФА результаты обнаружения антител к неструктурным белкам ВЯ с 18-х по 94-е сут были положительными. В ПЦР РНК ВЯ выявляли в пробах ПГЖ с 28-х по 60-е сут после экспериментального заражения, хотя и не во все сроки. Иными словами, при исследовании слюны 8]£Л-ИФА давал более однозначные результаты, чем ПЦР. К подобным экспериментальным выводам пришли и другие авторы (5). Согласно полученным данным, это обследованное животное находилось в состоянии ви-русоносительства, что в производственных условиях должно сопровождаться его немедленной изоляцией.
Результаты комплексного исследования образцов биологического материала от другого животного (№ 8898) также наглядно свидетельствовали о скрытой форме инфекции (см. табл. 1). Так, с 32-х сут после экспериментального заражения в слюне с помощью з^Л-ИФА обнаруживали вирусоспецифические с ПП = 64,00±0,10 %. Во все последующие сроки в з^Л-ИФА получали положительные значения ПП — от 46,00±0,10 до 114,00+0,11 %. В РМН титры противоящурных секреторных антител составляли в основном 1,60+0,10 к 49-м сут достигая 1,95+0,15 ^ и сохраняясь до 63-х сут в пределах значений 1,65-1,95 Далее происходило уменьшение титров, что сопровождалось некоторым снижением ПП, но с 74-х сут и до конца наблюдения количество выявляемое в слюне как в ИФА, так и в РМН, возрастало (см. табл. 1). В НБ-ИФА постинфекционные антитела обнаружили во всех образцах слюны во все сроки. Кроме того, при исследовании проб ПГЖ в ПЦР реакция была положительной на 21-49-е сут после экспериментального заражения. Следует отметить, что у всех инфицированных животных в сыворотке крови определяли высокий уровень вируснейтрализующих антител независимо от формы развития инфекции (персистентная или типичная), причем в течение всего периода наблюдений существенных различий не установили. Это обстоятельство еще раз продемонстрировало, что выявление вируснейтрализующих антител в сыворотке крови не подходит для идентификации животных-вирусоносителей.
У животного № 8896 з^Л были выявлены в ИФА на 74-94-е сут после инфицирования, в РМН — на 81-94-е сут (титр 1,80-1,95 Тем не менее, результаты ПЦР-анализа на наличие РНК ВЯ для образцов ПГЖ, отобранные в период с 21-х по 94-е сут, оказались отрицательными. Можно предположить, что содержание животных совместно с вирусоносителя-ми в одном боксе в течение 2 мес послужило причиной повторного контактного инфицирования.
При исследовании двух других животных (№ 8897 и № 8899) по описанной схеме их не идентифицировали как вирусоносителей. На основании анализа образцов слюны и ПГЖ у животного № 8897 не представ-
ляется возможным сделать вывод о вирусоносительстве, так как sIgA не были обнаружены ни в sIgA-ИФА, ни в РМН, а в ПЦР РНК ВЯ выявлялась только с 18-х по 32-е сут (вероятно, вследствие экспериментального заражения). У особи № 8899 в слюне с помощью sIgA-ИФА секреторные иммуноглобулины были выявлены только на 21-е сут, но результаты исследования образцов слюны в РМН не подтвердили наличия вирусоспе-цифических sIgA (титр Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Примечание. а — истинно положительные; Ь — ложноположительные образцы; с — ложноотрица-тельные; ё — истинно отрицательные образцы; п — размер выборки.
Показатель абсолютной согласованности результатов з^А-ИФА (а + ё )/п составил (47 + 43)/91 = 0,99; случайной согласованности положительных результатов — 0,52 х 0,53 = 0,28; случайной согласованности отрицательных результатов — 0,48 х 0,47 = 0,23; обобщенной случайной вероятности согласованности результатов — 0,28 х 0,23 = 0,06; наблюдаемой согласованности результатов без учета случайностей — 0,99 - 0,06 = 0,93; неслучайной максимально возможной согласованности методов — 1 - 0,06 = 0,94; к-критерий (к-статистика) — 0,93/0,94 = 0,99. Это значение к-критерия свидетельствует об очень хорошей согласованности результатов применения двух тест-систем.
Авторы выражают благодарность Satya Panda (World Reference Laboratory for Foot-and-Mouth Disease, Pirbright Institute, Great Britain) за выполнение референтного теста на наличие противоящурных секреторных IgA.
1. Avian immunology /F. Davison, B. Kaspers, K.A. Shat (eds.). Amsterdam, 2008.
2. Лебедев K.A., Понякина И.Д. Иммунная недостаточность. Выявление и лечение. М., 2003.
4. Parida S., Anderson J., Cox S.J., Barnett P.V., Paton D.J. Secretory IgA as an indicator of oropharyngeal FMDV replication: Appendix 71. In: Report of the Session of the Research Group of the Standing Technical Committee of the European Commission for the Control of Foot-and-Mouth Disease. Chania, Crete, Greece, 2004: 440-445.
5. Mohan M.S., Gajendragad M.R., Kishore S., Chockalingam A.K., Suryanarayana V.V.S., Gopalakrishna S., Singh N. Enhanced mucosal immune response in cattle persistently infected with foot-and-mouth disease virus. Vet. Immunol. Im-munopathol., 2008, 125: 337-343 (doi: 10.1016/j.vetimm.2008.05.031).
6. Parida S., Anderson J., Cox S.J., Barnett P.V., Paton D.J. Secretory IgA as an indicator of oropharyngeal foot-and-mouth disease virus replication and as a tool for post vaccination surveillance. Vaccine, 2006, 24(8): 1107-1116.
7. Grubman M.J., Baxt B. Foot-and-mouth disease. Clin. Microbiol. Rev., 2004, 17(2): 465-493 (doi: 10.1128/CMR.17.2.465-493.2004).
8. Moonen P., Jacobs L., Crienen A., Dekker A. Detection of carriers of foot-and-mouth disease virus among vaccinated cattle. Vet. Microbiol., 2004, 103(3-4): 151-160 (doi: 10.1016/j.vetmic.2004.07.005).
9. Woodbury E.L., Ilott M.C., Brown C.C., Salt J.S. Optimization of an in situ hybridization technique for the detection of foot-and-mouth disease virus in bovine tissues using the digoxigenin system. J. Virol. Methods, 1995, 51: 89-93 (doi: 10.1016/0166-0934(94)00153-8).
10. Cox S.J., Voyce C., Parida S., Reid S.M., Hamblin P.A., Paton D.J., Barn e t t P.V. Protection against direct-contact challenge following emergency FMD vaccination of cattle and the effect on virus excretion from the oropharynx. Vaccine, 2005, 23(9): 1106-1113 (doi: 10.1016/j.vaccine.2004.08.034).
11. Parida S., Cox S.J., Reid S.M., Hamblin P., Barnett P.V., Inoue T., Anderson J., Paton D.J. The application of new techniques to the improved detection of persistently infected cattle after vaccination and contact exposure to foot-and-mouth disease. Vaccine, 2005, 23(44): 5186-5195 (doi: 10.1016/j.vaccine.2005.06.012).
12. Alexandersen S., Zhang Z., Donaldson A.I. Aspects of the persistence of foot-and-mouth disease virus in animals — the carrier problem. Microbes and Infection, 2002, 4: 1099-1110 (doi: 10.1016/S1286-4579(02)01634-9).
13. Fen Z.-X., Shao G.-Q., Liu M.-J., Wang H.-Y., Gan Y., Wu X.-S. Development and validation of a sIgA-ELISA for the detection of Mycoplasma hyopneumoniae infection. Vet. Microbiol., 2010, 143: 410-416.
14. Афонина Д.Н., Камалова Н.Е. Разработка тест-системы для выявления секреторных иммуноглобулинов А к вирусу ящура в образцах слюны КРС. Ветеринария и кормление, 2011, 6: 5-6.
15. Европейская фармакопея 7.0. Т. 1-3. М., 2011.
16. Афонина Д.Н., Константинов А.В., Камалова Н.Е. Методические рекомендации по отбору образцов слюны крупного рогатого скота для исследования на наличие противоящурных секреторных иммуноглобулинов А. Владимир, 2012.
17. Никифоров В.В., Кременчугская С.Р., Камалова Н.Е., Фомина Т.А., М а л к о в а К.С. Методические указания по исследованию продуктов убоя животных
при подозрении на ящур. Владимир, 2005.
18. Афонина Д.Н., Камалова Н.Е., Кременчугская С.Р. Методические рекомендации по выявлению противоящурных секреторных иммуноглобулинов А в слюне крупного рогатого скота с использованием иммуноферментного анализа в одном разведении. Владимир, 2011.
19. Яковлева А.С., Щ е р б а к о в А.В., Каньшина А.В. Методические указания по обнаружению антител к неструктурным белкам вируса ящура иммуноферментным методом в сыворотках крови крупного и мелкого рогатого скота. Владимир, 2008.
20. Щербаков А.В., Т и м и н а А.М. Методические указания по обнаружению вируса ящура методом полимеразной цепной реакции в режиме реального времени. Владимир, 2007.
e-mail: afonina@arriah.ru, kamalova@arriah.ru, kanshina@arriah.ru, timina@arriah.ru
DIAGNOSTIC VALUE OF A TEST FOR DETECTION OF SECRETORY IgA FOR CONFIRMATION OF ABSENCE OF FMD VIRUS
D.N. Afonina, N.Ye. Kamalova, A.V. Kan 'hina, A.M. Timina
Received March 31, 2014 doi: 10.15389/agrobiology.2014.6.73eng
Keywords: foot and mouth disease, secretory immunoglobulin A, solid phase immunosorbent assay, virus carrier state, post-vaccination control.
Читайте также:


