Хронический гепатит и его реактивация

Острая фаза гепатита С в большинстве случаев не проявляется ярко выраженными симптомами. Заболевание отличается многолетним течением. Из-за несвоевременно лечения часто приводит к циррозу печени, печеночной недостаточности и раку железы. Если гепатит С длится более полугода, он становится хроническим и делится на несколько последовательных фаз — репликативную, неактивную и реактивации. В большинстве случаев определить ту или иную степень развития гепатита С можно посредством лабораторных обследований.
Как протекает острый гепатит С
Острая фаза продолжается 6 месяцев, часто незаметно для инфицированного. Она также имеет название инаппарантной либо субклинической, а если дает внешние проявления — манифестной.
Из-за бессимптомного течения острой фазы инфицированные чувствуют себя полностью здоровыми, никаких жалоб не возникает, работоспособность не снижается, желтухи нет.
Вследствие отсутствия симптоматики больной не обращается к врачу. Выявить гепатит С в этом случае сложно, хотя уже на этом этапе можно заметить выраженное увеличение печени, а спустя пару месяцев после заражения в крови повышаются показатели АлАт, что говорит об окончании инкубационного периода. Первые антитела к вирусу гепатита С выявляются не сразу. Сроки варьируются от 5 до 50 недель после инфицирования, в среднем спустя 15-20 недель.
Манифестная стадия регистрируется лишь у 10-20% больных, в большинстве случаев вследствие посттрансфузионного заражения (после переливания крови). Продолжается в среднем 7-8 недель, но может колебаться от месяца до полугода. В этом случае зараженный гепатитом С жалуется на чрезмерную утомляемость, постоянную слабость, понижение физической и умственной активности, тяжесть под правым ребром. У 8% инфицированных появляются признаки желтухи: кожа и склеры глаз приобретают легкий желтый оттенок. На осмотре врач устанавливает выраженное увеличение размеров печени.
В процессе острой фазы гепатита С больной может выздороветь самостоятельно. Это случается благодаря сильному иммунитету. Однако чаще всего происходит хронизация заболевания с постоянным наличием инфекционного процесса.
Этапы хронической инфекции
Хронический гепатит С — это заболевание печени, которое продолжается больше полугода. Инкубационный срок длится примерно 20-150 суток, в среднем около 2 месяцев. Существует несколько стадий хронического гепатита — острая, скрытая (латентная), а также фаза реактивации, когда болезнь вспыхивает с новой силой. Последняя фаза сопровождается циррозом и раком печени.
Причина подобного течения гепатита С — практически полное отсутствие симптомов на протяжении долгого времени. Вследствие этого стандартное противовирусное лечение интерферонами может оказаться неэффективным.
Она подразумевает период размножения вируса в клетках печени. ВГС — это РНК-содержащий вирус. Чтобы вирусы размножались (происходила репликация), нужны гепатоциты либо иммунные клетки. В РНК вируса содержится более 9 тысяч нуклеотидов, 30% из которых могут мутировать. При попадании в клетки печени рибонуклеиновая кислота высвобождается, благодаря чему начинается размножение вируса.
В отличие от других видов гепатита, интенсивность репликации HCV не слишком высокая. Вследствие этого чаще всего хронический гепатит не проявляется ярко выраженными симптомами. Активность распространения вируса гепатита С в репликативной фазе зависит от генотипа заболевания. Ниже всего интенсивность репликации у гепатита 1b генотипа. Практически сразу он становится хроническим.
Инфицированный на протяжении долгого времени чувствует себя прекрасно, в то время как продолжается репликация вируса, что вызывает увеличение вирусной нагрузки. Даже если сначала иммунитет пытался бороться с патологическими клетками, вскоре они начинают мутировать, создавая квазивиды. Иммунная система просто не может их распознать.
Новые антитела создаются через некоторое время, но вирус снова мутирует, вследствие чего заболевание становится хроническим. В какой фазе находится инфекция, врачи узнают по маркерам гепатита С.
Латентная (неактивная) фаза может длиться достаточно долго (до 20 лет). Врачи называют это состояние хроническим носительством вируса. При анализе ПЦР выявляется РНК вируса в гепатоцитах, а в плазме крови они отсутствуют. При этом клинические проявления слабые или полностью отсутствуют. Латентная фаза чаще выявляется при генотипе 3а и реже при 1b генотипе.
В течение латентной фазы инфицированные люди считают себя полностью здоровыми, будучи при этом потенциальными переносчиками вируса. В качестве возможных жалоб выступают незначительные боли в области правого подреберья, которые иногда появляются вследствие чрезмерных физических нагрузок и неправильного питания. Во время обследования наблюдается незначительное увеличение печени и селезенки.
Поражение печени при скрытой фазе гепатита С, как правило, протекает с более легкими нарушениями и менее выраженным фиброзом, чем при хроническом течении заболевания. Однако в некоторых случаях может привести к циррозу.
Латентная инфекция может сохраняться после успешно проведенной противовирусной терапии. Это говорит о высоком риске рака печени.
Это повторная вспышка заболевания. В активной фазе гепатита С клетки печени перестают выполнять свои задачи, утрачивают защитную функцию, вследствие чего инфекционный процесс прогрессирует. При обследовании выявляется высокая активность РНК вируса гепатита. Данная фаза развивается в среднем в течение 14 лет после инфицирования, цирроз — через 18 лет, гепатоцеллюлярная карцинома — спустя 23-28 лет.
Начало стадии больные могут указать до дня. На фоне абсолютного здоровья резко появляются следующие симптомы:
- проблемы с аппетитом;
- тошнота, горький привкус во рту;
- боль под правым ребром;
- слабость, вялость;
- чрезмерная сонливость днем и ночью.
Желтуха на начальном этапе реактивной фазы, как правило, не наступает. Появляется она позже из-за выраженных расстройств функции печени. Гепатоциты погибают, на их месте появляется рубцовая ткань, что является началом цирроза, который впоследствии приводит к гепатоцеллюлярной карциноме. Обычно цирроз нарастает медленно, практически в 80% случаев симптомы стертые, проявляется примерно у 20-25% всех больных хроническим гепатитом.
В стадии реактивации возможны также осложнения со стороны других органов. Наблюдается развитие:
- сахарного диабета 2 типа;
- поражения почек;
- тиреоидита;
- кожной сыпи;
- суставных и мышечных болей.
Вследствие этого хронический гепатит рассматривается не только как патология печени, но также как воспалительный процесс, который затрагивает все системы и органы.
В процессе любой из фаз гепатита применяются эффективные лекарства прямого воздействия, направленные на уничтожение РНК вируса в организме: Софосбувир, Ледипасвир, Даклатасвир, Велпатасвир, а также более дешевые дженерики. Эффективность лечения этими лекарствами достигает 99% даже при циррозе печени.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Последние десятилетия ознаменовались огромным прогрессом как в диагностике, так и в создании новых препаратов для лечения хронического гепатита В (ХГВ), в частности аналогов нуклеозидов (АН). Однако остается много вопросов по их применению: как долго лечить, каков риск возникновения резистентности при длительной терапии, каковы критерии отмены АН без вероятности реактивации ХГВ, влияет ли терапия на предотвращение цирроза печени и гепатоцеллюлярной карциномы?
В статье представлен клинический случай ХГВ без дельта-агента, фаза 2 (HbeAg+), с высокой биохимической и вирусной нагрузкой, фиброзом 2 стадии. Больная получала в течение 10 лет аналог нуклеозида, активность печеночных ферментов на фоне его приема быстро нормализовалась и была стабильной. После самостоятельной отмены АН произошла реактивация ХГВ. При назначении тенофовира активность АЛТ нормализовалась, вирусная нагрузка уменьшилась на 2 log — до 1,45×10 4 МЕ/мл и держится в этих пределах.
Приведенный клинический случай показывает, что пациенты с ХГВ должны постоянно принимать АН, чтобы остановить прогрессирование и трансформацию заболевания в цирроз печени или гепатоцеллюлярную карциному. Остаются актуальными выявление маркеров, которые позволят определить возможность отмены АН, и разработка новых препаратов, воздействующих на ДНК вируса, чем сейчас и занимаются многие исследователи.
Ключевые слова: хронический гепатит В, лечение, аналоги нуклеозидов, реактивация HBV.
Для цитирования: Макашова В.В., Омарова Х.Г. Реактивация хронического гепатита В после отмены терапии. РМЖ. 2019;10:50-52.
Chronic hepatitis B reactivation after treatment discontinuation
V.V. Makashova 1,2 , Kh.G. Omarova 1
1 Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, Moscow
2 Infectious Clinical Hospital No. 2, Moscow
The last decades have witnessed dramatic progress both in the diagnosis and development of novel drugs for chronic hepatitis B, in particular, nucleoside analogues. However, many aspects are still challenging, i.e., treatment duration, the risk of resistance in long-term treatment, criteria for drug discontinuation without any risk of chronic hepatitis B reactivation, the effect on the prevention of liver cirrhosis and hepatocellular carcinoma etc.
The paper addresses case history of chronic hepatitis B without delta agent, phase 2 (HbeAg+), characterized by high biochemical marker levels, high viral load, and liver fibrosis stage 2. This woman has received nucleoside analogue for 10 years. Liver enzyme levels have returned to normal quickly and were stable. However, after discontinuing the treatment, hepatitis B reactivation has occurred. The patient was prescribed with tenofovir. ALT has re turned to normal levels, viral load has reduced by 2 logs (to 1.45×10 4 IU/ml) and was stable.
This case history demonstrates that patients should not discontinue the treatment with nucleoside analogues to prevent disease progression and its transformation to liver cirrhosis and hepatocellular carcinoma. Identification of markers to assess the possibility of nucleoside analogue discontinuation and the development of novel drugs targeting viral DNA are still important.
Keywords: chronic hepatitis B, treatment, nucleoside analogues, hepatitis B reactivation.
For citation: Makashova V.V., Omarova Kh.G. Chronic hepatitis B reactivation after treatment discontinuation. RMJ. 2019;10:50–52.
Статья посвящена проблеме реактивации хронического гепатита В после отмены терапии. Представлен клинический случай хронического гепатита В без дельта-агента, фаза 2, с высокой биохимической и вирусной нагрузкой, фиброзом 2 стадии
Вирусный гепатит В (ВГВ) представляет собой важную проблему здравоохранения во всем мире в связи с широкой распространенностью (350 млн носителей ВГВ) и высоким риском развития цирроза печени (ЦП) и гепатоцеллюлярной карциномы (ГЦК). В мире каждый год ВГВ заболевают около 50 млн человек, а умирают от него около 650 тыс. человек в год [1]. С 1999 по 2013 г. количество летальных исходов, связанных с ЦП и ГЦК в исходе хронического гепатита В (ХГВ), увеличилось на 33% [2]. В России приблизительно 3 млн носителей ВГВ и больных ХГВ [3].
Последние десятилетия ознаменовались огромным прогрессом как в диагностике, так и в создании новых препаратов для лечения ХГВ, в частности аналогов нуклеозидов (АН). Однако остается много вопросов по их применению: как долго лечить, каков риск возникновения резистентности при длительной терапии, каковы критерии отмены АН без вероятности реактивации ХГВ, влияет ли терапия на предотвращение ЦП и ГЦК — все это предстоит выяснить в ближайшее время.
В связи с этим представляется крайне важным рассмотреть клинический случай реактивации ХГВ у молодой женщины.
Пациентка К., 28 лет, обратилась в июле 2008 г. с жалобами на слабость, быструю утомляемость, сонливость в первой половине дня, снижение аппетита, периодическую тошноту, головные боли, нечастое повышение АД до 135/100 мм рт. ст.
Анамнез заболевания. В феврале — марте 2008 г. после сильного стресса стала беспокоить сильная слабость. Обратилась к врачу. Выявлено повышение печеночных ферментов в 2–3 раза, наличие HbsAg. При дополнительном обследовании выявлена ДНК HBV — 6,8×10 8 МЕ/мл.
Эпиданамнез. Удаляла зубы 1,5 года назад. У мужа однократно обнаруживали HbsAg, при повторном обследовании HbsAg не обнаружен.
Перенесенные заболевания. В детстве до 5 лет — корь, краснуха, ветряная оспа. Цистит с 21 года, пиелонефрит, кольпит после вторых родов, аутоиммунный тиреоидит.
Аллергоанамнез: не отягощен.
Наследственность: у бабушки по отцу — рак желудка, у матери — хронический пиелонефрит.
Объективно по результатам осмотра. Кожные покровы и видимые слизистые обычной окраски, чистые. Вторичных печеночных знаков нет. Печень пальпируется на 1,0–1,5 см ниже реберной дуги, селезенка не пальпируется. Рост 162 см, вес 53 кг.
Вредные привычки: не курит, алкоголь не употребляет.
Динамика основных показателей общего и биохимического анализов крови, данные ПЦР-диагностики, УЗИ органов брюшной полости и фиброэластометрии представлены в таблице 1.
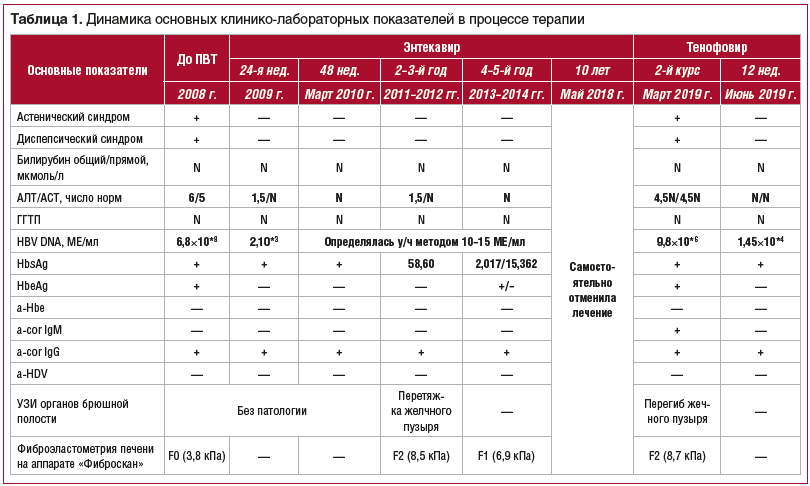
Пациентке было проведено обследование на гормоны щитовидной железы: Т4 свободный, ТТГ, АТ ТПО, АТ ТГ — все в пределах нормы. УЗИ щитовидной железы.
Заключение: Диффузные изменения тиреоидной ткани по типу аутоиммунного тиреоидита; фокальные изменения по типу коллоидных в левой доле (в центральной части левой доли визуализируется 2 фокальных образования округлой формы, гипоэхогенные, 2,3×4,5, без повышения кровотока).
Для решения вопроса о назначении противовирусной терапии (ПВТ), в частности интерферонотерапии, было проведено тестирование по госпитальной шкале тревоги и депрессии (HADS). Результат: 24 балла (в норме: до 11 баллов), что свидетельствовало о выраженном психоэмоциональном напряжении.
На основании вышеуказанных данных был поставлен диагноз: Хронический гепатит В (HbeAg позитивный), без дельта-агента, фаза 2 (высокая биохимическая и вирусная нагрузка). Сопутствующие диагнозы: аутоиммунный эутиреоидный тиреоидит; хронический пиелонефрит в стадии ремиссии; психовегетативный синдром.
В связи с последним сопутствующим диагнозом препараты интерферонов противопоказаны. Назначен аналог нуклеозида — энтекавир (0,5 мг/сут) длительно. С пациенткой была проведена подробная беседа о необходимости ежедневного приема препарата (без пропусков), своевременной сдачи анализов крови для контроля активности инфекционного процесса и коррекции терапии. Помимо ПВТ рекомендован прием следующих лекарственных средств: адеметионин в течение 1 мес., урсодезоксихолевая кислота 1 капс. (250 мг) × 2 р./день в течение 3 мес. Получено согласие на лечение и обследование.
Через 24 нед. приема энтекавира исчезли жалобы (см. табл. 1), активность АЛТ значительно снизилась — до 1,5 нормы, активность АСТ нормализовалась, уровень ДНК HBV уменьшился до 2,10* 3 МЕ/мл, HbeAg перестал определяться, но а-Hbe не появились, т. е. сероконверсии не произошло. На фоне ПВТ через 48 нед. (1 год) активность печеночных ферментов полностью нормализовалась, ДНК вируса гепатита В (ВГВ) определялась только ультрачувствительным методом (чувствительность 10–15 МЕ/мл). Однако сероконверсия HbeAg на а-Hbe не зафиксирована. Аналогичная клинико-лабораторная характеристика наблюдалась в течение 5 лет. Необходимо заметить, что периодически отмечалось повышение активности АЛТ до 1,5 нормы, титр HbsAg колебался от 58,960 до 2,017 МЕ/мл и вновь повышался до 15,362 МЕ/мл, фиброз печени, несмотря на противовирусную терапию в течение 2011–2013 гг., фиксировался на стадии F2, но к 5-му году лечения уменьшился до F1 (см. табл. 1).
В последующие 5 лет пациентка не наблюдалась (живет в другом городе). В марте 2019 г. по телефону с большой обеспокоенностью сообщила, что год назад (в мае 2018 г.) самостоятельно прекратила прием энтекавира, т. к. жалоб не было и они с мужем решили завести еще одного ребенка (двое детей у семейной пары уже есть). Дети и муж обследованы: маркеры ВГВ не обнаружены. Анализы не сдавала, а при сдаче в марте 2019 г. вновь обнаружено повышение активности АЛТ и АСТ в 4,5 раза, вирусная нагрузка — 9,8×10* 6 МЕ/мл, вновь появился HbeAg при отсутствии а-Hbe, фиброз печени — F2. Все эти данные свидетельствовали об активности патологического процесса: ХГВ, фаза 2. Назначен тенофовир 300 мг ежедневно постоянно. Повторно проведена беседа о необходимости постоянного приема. Объяснено, что в настоящее время гепатит излечить полностью невозможно, поэтому для подавления размножения ВГВ необходимо принимать противовирусный препарат. Через 12 нед. ПВТ активность ферментов нормализовалась (см. табл. 1), уровень ДНК ВГВ уменьшился на 2 логарифма, HbeAg перестал определяться, но без сероконверсии, a-cor, пробы на IgM стали отрицательными. Это свидетельствует о положительном результате лечения АН. Однако важно подчеркнуть, что эффективность терапии будет целиком зависеть от комплаентности пациентки.
Заключение
Лечение ХГВ остается сложной проблемой в связи с невозможностью полностью подавить вирусную репликацию, т. к. ДНК ВГВ внедрена в геном человека. Терапия интерфероном обладает огромным количеством побочных действий, многим больным она противопоказана, а эффективность ее очень мала (15–30%). Пациенты должны постоянно принимать АН, чтобы остановить прогрессирование и трансформацию заболевания в ЦП или ГЦК.
Поэтому в настоящее время основными целями, стоящими перед медицинским сообществом, являются: 1) выявление маркеров, которые позволят определить возможность отмены АН; 2) разработка и исследование новых препаратов, воздействующих на ДНК ВГВ. Исследования в этой области продолжаются.
Что такое Хронический вирусный гепатит В (ХВГВ) —
Вирусный гепатит В— одна из самых серьезных проблем здравоохранения во всем мира в связи с непрерывно увеличивающейся заболеваемостью, негативным влияниям на состояние здоровья и трудоспособность человека из-за частого развития неблагоприятных исходов (хронический гепатит, цирроз печени, гепатокарцинома) и смертностью как от острых, так и от хронических форм инфекции.
В патогенезе хронического гепатитарассматриваются репликация вируса гепатита В в печени, а также вне ее; гетерогенность генотипов и мутации генома вируса; иммуногенетическая основа хозяина; прямой цитотоксический эффект вируса и индуцированные им иммунные нарушения. Установлено наличие репликации HBV вне печени (в мононуклеарных клетках крови, клетках лимфатических узлов селезенки, костного мозга, почках, поджелудочной железе, надпочечниках, кишечнике, кожи и др.). Инфицирование лимфоцитов и моноцитов HBV нарушает их иммунную функцию, что играет важную роль в патогенезе поражения печени и других органов. В патогенезе поражения органов при HBV-инфекции в качестве главной детерминанты рассматривается взаимодействие факторов хозяина и вируса. От их взаимодействия зависит тот или иной ответ на ин-фект; возможность его персистенции, репликации, продукция антител, характер иммунного ответа. При HBV-индуцированном пора жении печени более важное значение имеют не факторы вируса а генетическая основа хозяина, составляющая не менее 50 % в детерминорованнии персистенции HBV-инфекции. В течении хронической jjgV-инфекции выделяют три фазы.
В первой фазе (иммунной толерантности) происходит активная репликация вируса с продукцией антигенов: HBcAg обнаруживается в значительной части гепатоцитов, HBsAg и HBeAg — в сыворотке крови. Наблюдается высокий уровень виремии (HBV ДНК). В печени отмечается морфологическая картина неактивного гепатита.
Механизмы развития низкоуровневой репликации HBV чрезвычайно многогранны. Так, суперинфекция вирусом гепатита D может оказывать ингибирующее влияние на репликацию HBV, что приводит к снижению уровня виремии HBV и клиренсу HBeAg. В случае суперинфекции HCV может наблюдаться клиренс не только HBeAg, но и HBsAg. Кроме того, алкоголь также может вмешиваться в механизмы репликации вируса. У лиц, злоупотребляющих алкоголем, часто единственным маркером хронической HBV-инфекции являются НВсАЬ. Аналогичное влияние на HBV характерно в ряде случаев и для вируса иммунодефицита человека (HIV). Наличие низкоуровневой репликации HBV может быть связано с мутациями в различных участках генома вируса, прежде всего в области перекреста С- и Х- генов, ответственных за его репликацию.
Патогенез повреждений печенипри латентной вирусной инфекции до сих пор остается неясным. В ряде исследований у больных с поражением печени неизвестной этиологии, с признаками умеренной и высокой степени активности воспалительного процесса и далеко зашедшего фиброза проводилась ПЦР на вирусы гепатита В и D. При этом, наряду с отсутствием серологических маркеров HBV-инфекции, в сыворотке крови выявлялась HBV ДНК, а при иммуногистохимическом исследовании в ткани печени отмечались антигены HBV. Это позволяет обсуждать роль латентной HBV-инфекции в развитии криптогенных поражений печени наряду с неизвестными гепатотропными вирусами.
HBsAg-специфическому Т-клеточному ответу отводится главная роль в разрешении острой HBV-инфекции. В элиминации вируса при хронической HBV-инфекции ведущее значение приобретает HBc/HBeAg-специфический Т-клеточный ответ. Главный дефект Т-клеток при хронической HBV-инфекции обусловлен недостаточной функцией CD4+-Tx, что ведет к нарушению образования ЦТЛ из клеток-предшественников. ЦТЛ активируются при взаимодействии своих Т-кле-точных рецепторов с молекулой HLA I класса и играют главную роль в элиминации вируса, что обусловлено их способностью вызывать гибель инфицированных клеток, экспрессирующих соответствующие пептиды, презентированные молекулами МНС I класса.
ХВГВ у большинства больных протекает малосимптомно, без желтухи. Необязательно заболевание развивается после перенесенной острой формы ВГВ. Субклиническое Течение заболевания может продолжаться в течение нескольких лет.
Клинические проявления заболеванияво многом зависят от репликативной активности возбудителя. О репликации вируса свидетельствует наличие HBeAg, выявление HBV DNA методом ПЦР. В ряде случаев судить о репликации вируса можно по высокому уровню концентраций HBsAg (более 100 нг/мл), наличию анти-HBcAb IgM. Отсутствие маркеров репликации при обнаружении HBsAg, HBcAb IgG, HBeAb свидетельствует о наличии интегративной фазы.
К внепеченочным симптомам при ХВГВ относят следующие патологические состояния:
- смешанная криоглобулинемия (слабость, артралгии, пурпура, периферическая полинейропатия, синдром Рейно, артериальная гипертензия);
- эндокринные нарушения (аутоиммунное поражение щитовидной железы, поджелудочной железы, сахарный диабет, аменорея);
- поражение кожи (акне, стрии, крапивница, гиперемия лица, кожная порфирия, красный плоский лишай, узловатая и мультиформная эритема);
- поражение мышц;
- поражение органов зрения;
- поражение желез;
- гематологические проявления (злокачественная лимфома, идиопатическая тромбоцитопения);
- гломерулонефрит.
Хронический интегративный гепатит В, как правило, имеет доброкачественное течение, протекает бессимптомно, при нормальных биохимических показателях крови. Заболевание диагностируется на основании идентификации специфических вирусных маркеров, морфологических изменений в печени, характеризующихся дистрофическими изменениями гепатоцитов, наличием минимальных проявлений воспалительной инфильтрации в портальных трактах и паренхиме с сохранением целостности пограничной пластинки, слабо выраженным перипортальным фиброзом.
Особенности диагностики. В диагностике имеет большое значение иммуносерологическое обследование, позволяющее не только определить наличие вирусного маркера, но и установить активность вируса, что является чрезвычайно важным для проведения этиотропного лечения. Степень активности процесса определяют по наличию или отсутствию в крови HBeAg. В случае обнаружения HBeAg в сыворотке крови на протяжении 6 мес и более от начала заболевания диагностируют ХВГВ с высокой репликативной активностью.
Если через 6 мес от начала заболевания произошла сероконверсия и в крови обнаруживаются НВеАЬ, диагностируют ХВГВ с низкой репликативной активностью (HBeAg-негативный ХВГВ).
Интегративная фаза ХВГВ характеризуется нормальной или незначительно повышенной степенью активности АлАТ, персистенциеи HBV-инфекции с интеграцией вируса в геном гепатоцита при отсутствии активного иммунного цитолиза.
Латентная HBV-инфекция может характеризоваться обнаружение HBV ДНК в сыворотке крови и/или ткани печени при отсутствии серологических маркеров, указывающих на персистирование вируса (прежде всего негативный результат выявления HBsAg) Раздают два варианта латентной HBV-инфекции. При первом — низкий уровень репликации HBV и, как следствие, пониженный синтез и экспрессия вирусных антигенов обусловлены адекватным отпетом иммунной системы; ингибирующим влиянием на HBV других вйрусов (HCV, HDV, HIV); мутациями в определенных участках генома вируса, ответственных за его репликативную активность. При втором варианте репликация вируса не подавлена, HBsAg синтезируется и экспрессируется, но не выявляется современными тест-системами вследствие мутаций, изменяющих структуру его основных детерминант.
Большое значение имеет определение концентрации вируса или степени репликации вируса, степени виремии HBV (генокопий ДНК). Выделяют очень низкую (менее 103), низкую (103-106), умеренную (106-108), высокую (более 108) виремию. Очень низкую виремию можно выявить только с помощью специально предназначенных фоРм полимеразной цепной реакции.
Особенности лечения хронического вирусного гепатита В.Лечение хронического гепатита В предусматривает уменьшение воспаления и степени фиброза в печени, подавление репликации HBV, достижение сероконверсии HBeAg в НВеАЬ, улучшение качества жизни больного. В репликативной фазе гепатита необходима противовирусная терапия, направленная на подавление активного размножения вируса, а при интегративном HBeAg-негативном ХВГВ терапевтические мероприятия должны быть направлены на предупреждение активации инфекционного процесса.
Для лечения хронического гепатита В используются три группы препаратов:
- интерферон, ПегИнтрон;
- аналоги нуклеозидов: ламивудин, адфовир, фамцикловир, энтекавир;
- иммуностимуляторы: тимозинa, вакцина HBV, интерлейкин-2, -12.
В настоящее время в клинической практике для лечения хронического вирусного гепатита В в фазе репликации чаще применяют препараты интерферона-Р, полученные рекомбинантным методом, интрон А, реаферон, роферон. Доказана и эффективность альфаферона, берофора, вэллферона, ферона, эгиферона и др. Перспективным направлением в лечении является применение ПегИнтрона в качестве монотерапии и в комбинации с аналогами нуклеозидов.
Интерферон-Р обладает противовирусным, иммуномодулирующим, антифибротическим и противоопухолевым действием и эффективно подавляет репликацию вируса гепатита В. Механизм действия нуклеозидных аналогов реализуется через блокирование построения цепи вирусной ДНК и, таким образом, прекращение репликации HBV.
о связи с тем, что ИФН тормозит размножение вируса в клетке, его значение целесообразно только при обнаружении маркеров репликации вируса HB V (HBeAg, HBV DNA в сыворотке крови или в нунк-татах печени).
Наиболее часто положительный и устойчивый ответ на лечение интерфероном наблюдается при наличии следующих клинических и вирусологических факторов:
- непродолжительное течение HBV-инфекции (до 2 лет);
- молодой возраст;
- начало заболевания в зрелом возрасте;
- женский пол;
- высокий уровень аминотрансфераз сыворотки крови (более чем в 5-6 раз превышающий норму);
- высокий уровень ЦИК;
- низкий уровень HBV ДНК в сыворотке крови;
- наличие в анамнезе желтушной формы острого вирусного гепатита В;
- отсутствие супер- и коинфекции вирусами гепатита D, С, F;
- отсутствие серьезных сопутствующих заболеваний внутренних органов;
- отсутствие признаков исхода в цирроз печени.
Существуют различные схемы лечения интерфероном хронического вирусного гепатита В. Чаще используется схема применения интерферона по 5 млн ME 5-7 раз в неделю или по 5 млн ME 3 раза в неделю, в зависимости от индивидуальной переносимости и чувствительности больного. Рядом авторов предлагаются высокие дозы ИФН — до 10 млн ME в сутки ежедневно или через день, а при микст-инфекции (HBV + HDV) до 12 мес. Длительность курса лечения составляет 4-6 мес. По мнению других специалистов, такие высокие дозы не оправданы и приводят к более выраженным побочным реакциям, подавляют продукцию эндогенного интерферона, угнетают антительный ответ на вирусный антиген, что способствует персистенции инфекционного процесса и накоплению противоинтерфероновых нейтрализующих антител. В целях профилактики развития резистентности к интерферону ударные дозы препарата целесообразно назначать в начале курса лечения, а затем быстро снижать дозу до оптимальной.
Дозы и схема лечения зависят от активности процесса, уровня сывороточной HBV DNA. Ответ на терапию интерфероном начинается с пикового подъема активности Ал AT в среднем через 8 нед и более от начала лечения (цитолитический криз), что предполагает наличие иммунного клиренса зараженных HBV-гепатоцитов. При условии положительного эффекта лечения, обычно после цитолитическог криза, из сыворотки крови исчезают HBV DNA и HBeAg, нормализуется активность аминотрансфераз. При отсутствии эффекта п еле перерыва можно продолжить лечение интерфероном-а в выше указанных дозах после предварительного лечения преднизолоном в терние 1 мес.
Критерии эффективности лечения:
По данным контролируемых исследований, 30-40 % больных ХВГВ дают полный ответ на лечение интерферонами. Наиболее высокий уровень сероконверсии HBeAg (33%) в случаях HBeAg-положительного ХГВ после 16 нед лечения интерфероном-а наблюдается, как правило, у больных с высокой активностью заболевания до начала лечения.
Предварительное лечение преднизолоном в дозе 30-40 мг/сут в течение 6-8 нед у больных ХГВ с субнормальной и/или колеблющейся в пределах 1,5-2 норм активностью АлАТ приводит к увеличению частоты развития сероконверсии HBeAg, что объясняют восстановлением функционирования иммунной системы после отмены кортикостероидов.
Однако надо помнить о том, что данное лечение сопряжено с риском развития резкой активации инфекции при цирротической стадии процесса, в связи с чем необходим тщательный отбор больных для данного варианта противовирусной терапии, включающего проведение биопсии печени для исключения ЦП.
Среди химиопрепаратов широко используются:
- противовирусный препарат аденин-арабинозит (видарабин), его назначают в дозе 7,5-15 мг в сутки в течение 3 нед. Первый трехдневный курс тормозит репликацию вируса гепатита В, повторный курс вызывает стойкий эффект со снижением активности ДНК-полимеразы у 73 % и исчезновение HBsAg у 40 % больных. Побочными эффектами аденин-арабинозита являются пирогенные реакции, нейромиопатия, возникающие при длительности лечения более 8 нед;
- рибавирин, аналог гуанозина, обладает широким спектром активности против РНК- и ДНК-вирусов, препарат ингибирует отдельные этапы их репликации. Используется в дозе 1000-1200 мг в 2 приема в течение 3-4 мес. Возможны побочные эффекты — абдоминальный дискомфорт, гемолитическая анемия. Монотерапия рйбавирином оказалась малоэффективной. Более целесообразно сочетанное лечение интроном и рйбавирином; . кроме указанных препаратов, используется тимазид по 600- 800 мг/сут.
Учитывая возможность репликации вируса гепатита В под влиянием глюкокортикоидов, в ряде случаев целесообразна комбинированная терапия преднизолоном и противовирусными средствами. Больным, находящимся в фазе интеграции, предварительно проводится недельный курс лечения преднизолоном (40 мг/сут) или метипредом (60 мг/сут) с последующим снижением доз до поддерживающих. Затем проводится курс лечения противовирусным препаратом по общепринятой схеме Указанная схема приводит к исчезновению ДНК-полимеразы и HBeAg из крови Снижается активность аминотрансфераз, содержание углобулинов, уменьшаются морфологические признаки активности процесса. Начальная доза преднизолона составляет 20-30 мг в сутки. Дозу препарата начинают снижать не раньше чем через 3-4 нед при наличии положительной клинической и биохимической динамики по 2,5 мг через 7-10 дней, при контроле состояния больного и уровня активности аминотрансфераз в крови, у-глобулинов, сывороточных маркеров вирусов гепатитов При нормализации биохимических показателей лечение продолжают индивидуально подобранными поддерживающими дозами (5-10 мг/сут) в течение 8-10 мес, после чего суточную дозу снижают каждый месяц на 2,5 мг. Иногда лечение продолжается до 2-3 лет.
К препаратам тимуса, помимо хорошо знакомых врачам тималина, тимогена, Т-активина, относятся такие средства, как имунофан (100 мкг/сут подкожно 2 раза в неделю в течение 8-12 нед), миелопид (3-6 мг подкожно, внутримышечно или внутривенно 1 раз в сутки с интервалом 2 сут; курс состоит из 3-5 инъекций), бионормолайзер — препарат растительного происхождения.
Читайте также:


