Есть ядро у вируса спида
В настоящее время проблема ВИЧ затрагивает многих людей. Общество старается защитить себя от заражения вирусом. Известно, что результатом развития заболевания, вызванного ВИЧ, является летальный исход. С детства людей учат простым правилам защиты, которые помогают уменьшить шанс заразиться вирусом. В статье мы выясним детальное строение вируса (ВИЧ), как он атакует и взаимодействует с клетками человеческого тела.
Что такое вирус иммунодефицита человека
ВИЧ (вирус иммунодефицита человека), провоцирует в здоровом организме медленное развитие инфекции. При попадании вируса в кровь он начинает постепенно уничтожать здоровые клетки иммунной системы. В процессе жизнедеятельности вируса, его количество в организме увеличивается, а число лимфоцитов неуклонно сокращается. От начала заражения до летального исхода врачи выделяют 5 стадий, которые проходит зараженный вирусом организм. Последняя стадия - это СПИД (синдром приобретенного иммунодефицита).
Заразиться вирусом возможно при непосредственном контакте с инфицированным человеком. Обычно это происходит при взаимодействии со слизистыми выделениями или путем повреждения кожного покрова. Опасны следующие биологические жидкости:
- кровь;
- семенная жидкость;
- выделения из влагалища;
- грудное молоко матери.
Когда произошел контакт с зараженным материалом, вирус попадает в организм и затаивается на некоторое время (инкубационный период). После чего начинает активно действовать, и проявляются первые симптомы заражения.
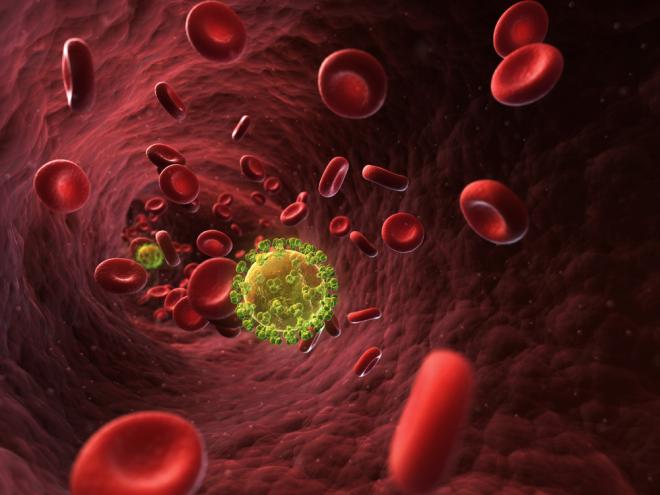
Вирус под микроскопом
При ближайшем рассмотрении патоген похож на сферу, по краям которой располагаются шипы. Размеры вируса достигают 150 нанометров, что больше многих других инфекционных агентов. Наружный слой сферы отвечает за контакт вируса с клетками организма. Состоит он из белков и вертикальных наростов.
С виду шипы напоминают грибы - у них имеется тонкая ножка со шляпкой. Благодаря наростам вирус может контактировать с другими клетками. На верхней части шляпки располагаются гликопротеины (GP120), а ножка состоит из трансмембранных гликопротеинов (GP41).
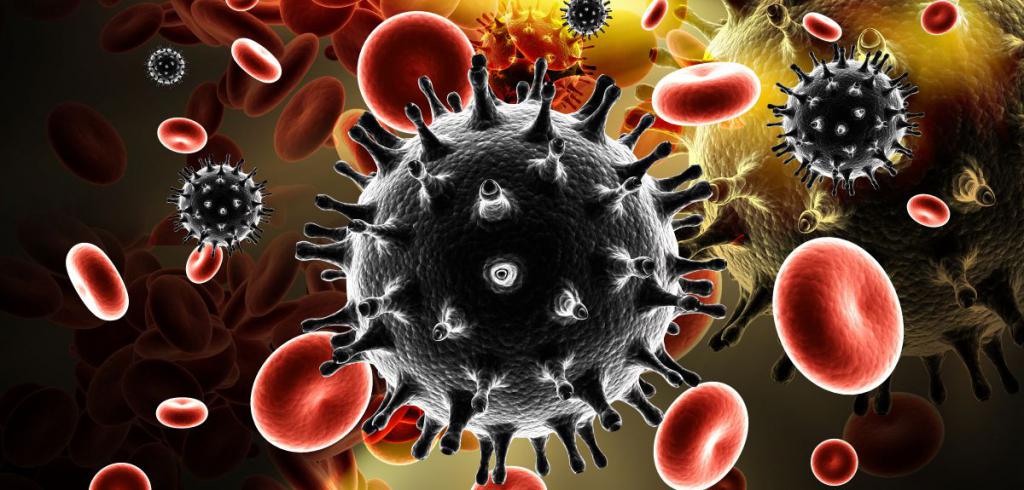
В основной (внутренней) части вируса располагается геном из 2 молекул, состоящих из 9 генов. Именно в них заложена наследственная память вируса, накопившаяся за время его существования. В ней заключается информация о строении, схеме заражения и принципе размножения вируса. Сам ген заключен в оболочку из матриксных и капсидных белков (P17 и P24). Посмотреть на фото строения вируса (ВИЧ) можно на протяжении всей статьи.
Ученые выявили 4 вируса иммунодефицита:
- ВИЧ-1 считается наиболее часто встречаемым видом. Основная территория распространения - Северная и Южная Америка, Евразия и Азия. Этот вид считается основным, вызывающим ВИЧ-инфекцию.
- ВИЧ-2 встречается реже, но является прямым родственником ВИЧ-1. Вызывает синдром приобретенного иммунодефицита человека. Распространение началось с западной части Африки.
- ВИЧ-3, ВИЧ-4 - наиболее редкая форма вируса.
Строение вируса
Заражение организма и уничтожение иммунных клеток - основные функции вируса. Строение ВИЧ имеет следующее:
- Нуклеокапсид – ядро вируса. В состав входят 2 молекулы и ферменты ревертаза, протеаза и интеграза. Все эти компоненты заключены в упаковку из капсидных белков (P7, P9, P24), а сверху располагается 2 000 молекул P17 (матриксный белок). Располагаются они между внешней оболочкой и капсидом.
- Мембрана – внешняя оболочка вируса. Состоит она из слоя фосфолипидов, мембранных клеток и гликопротеинов (именно они помогают выбрать нужные молекулы человеческого тела для последующей атаки).
Белки вируса
Состав вируса (ВИЧ) включает в себя следующие белки:
- Суперкапсид. Строения вируса (ВИЧ) обязательно включает эти компоненты в свой состав, поскольку они помогают выполнять якорную (с помощью суперкапсида вирус прикрепляется к клетке) и адресную (поиск мишеней) функции. Они относятся к сложным гликопротеидам.
- Структурные белки помогают формировать внешнюю оболочку вируса и его капсиды.
- Неструктурные белки отвечают за гены POL. Благодаря этому виду белка происходят репродуктивные функции вируса.
- Капсидные белки образуют нишу для нуклеиновой кислоты, а также помогают создать ферменты и присутствуют в геноме вируса.
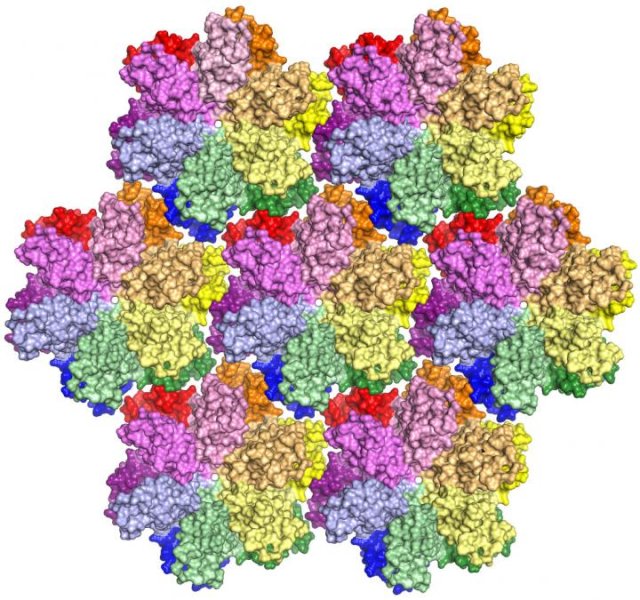
Какие клетки поражает ВИЧ
Когда вирус проникает в кровь человека, он атакует клетки, содержащие ген CD4 (моноциты, макрофаги, Т-лимфоциты и все родственные им клетки). Из-за строения вируса иммунодефицита человека (а именно, входящего в состав гликопротеина), он атакует клетки с этим геном. Локации, которые поражает вирус:
- все лимфоидные ткани;
- клетки микроглии (нервная система);
- клетки эпителия кишечника.
Процесс взаимодействия ВИЧ и клетки-мишени
Основными защитниками организма являются Т-лимфоциты, именно они направляются на борьбу с вирусом. Лимфоциты содержат ген CD4, на который реагирует вирус ВИЧ. Он присоединяется к Т-лимфоциту посредством указанного гена. Как уже упоминалось, происходит этот процесс благодаря расположенным на шипах вируса гликопротеинам (GP120). После чего патоген начинает активно проникать внутрь лимфоцита - сделать это помогают трансмембранные белки (GP41).
Вирус, оказавшийся внутри Т-лимфоцита, попадает в благоприятную среду для размножения. Через некоторое время после активной репликации инфекционному агенту становится тесно внутри оболочки, и она лопается. Этот процесс постоянно повторяется и все большее количество клеток иммунной системы погибает.

При взятии крови на анализ, у здорового пациента определяется CD4 в норме от 4 до 12 ед. А у человека с ВИЧ-инфекцией их количество снижается и составляет от 0 до 3 ед.
Благодаря своему строению вирус ВИЧ, попадая в здоровый организм, на определенное время замирает. Ему необходим период для адаптации - в основном этот срок длится около 7 дней. После чего окрепший вирус начинает действовать.
Из-за расположения вируса внутри клеток он удачно скрывается от любых лекарственных препаратов, а иммунная система прекращает на него правильно реагировать.
Стадии развития ВИЧ
Особое строение вируса ВИЧ предполагает его постепенное развитие в организме. Увеличение его численности позволяет производить активные атаки на организм. Выделяют несколько стадий развития ВИЧ (у каждого человека они протекают по-разному, в зависимости от состояния организма на момент заражения):
- Инкубационный период занимает от 2 недель до полугода. Длительность зависит от количества вирусов, проникших в организм. Если попало малое число, то им понадобится больше времени на увеличение численности. Стадия протекает без симптомов, но человек уже считается носителем вируса.
- Острая инфекция. На втором этапе количество вирусов вырастает, а число Т-лимфоцитов начинает снижаться. Появляются первые симптомы заболевания: увеличиваются лимфоузлы, повышается температура или появляется сыпь.
- Латентная стадия – самая длительная по времени стадия, занимает она около 6–7 лет. Наружных проявлений болезни практически нет. Процесс происходит внутри организма, вирусы активно занимаются уничтожением Т-лимфоцитов. Если принимать вспомогательные, поддерживающие препараты, период затишья можно продлить до 10 лет.
- Стадия вторичных заболеваний. Этот период начинается после уничтожения большей части иммунной системы. Любое простудное заболевание протекает с серьезными осложнениями и появлением дополнительных недугов.
- СПИД. На последней стадии в организме больного уничтожена вся иммунная система. Такие пациенты пребывают в стационаре под круглосуточным наблюдением. Неспособный бороться организм начинает себя полностью истощать, органы прекращают правильно работать, на коже появляются разрывы и гнойные раны. Благодаря лечению можно только облегчить состояние больного и отсрочить неминуемый исход.
Чтобы не заразиться вирусом, необходимо соблюдать правила личной безопасности и помнить, что патоген может попасть в организм человека через контакт с биологическими жидкостями.
Бороться с этим заболеванием и сдерживать его развитие ученым помогают знания о строение вируса (ВИЧ). Опишите врачу симптомы, возникшие после возможного заражения - это поможет подобрать необходимое лечение.
Просто о сложном


-->СТАТЬИ -->
| [07.07.2014] | [Вирусы] |
| Натуральная оспа (0) | |
| [18.07.2014] | [Вирусы] |
| Вирусы. Краткий обзор (0) | |
| [21.07.2014] | [Общие понятия] |
| Вирусология (0) | |
| [03.07.2014] | [Общие понятия] |
| Немного истории (0) | |
| [04.07.2014] | [Инфекции] |
| Цитомегаловирусная инфекция (0) | |
| [21.08.2014] | [Вирусы] |
| Вирус иммунодефицита человека (ВИЧ) (0) | |
| [22.08.2014] | [Вирусы] |
| Строение и жизненный цикл вируса иммунодефицита человека (ВИЧ) (1) | |
| [09.02.2016] | [Вирусы] |
| Лихорадка Зика (0) | |
Строение вируса иммунодефицита человека
 |
| Строение вируса иммунодефицита человека |
Вирионы ВИЧ имеют вид сферических частиц, диаметр которых составляет около 100—120 нанометров (это приблизительно в 60 раз меньше диаметра эритроцита).
В состав зрелых вирионов входит несколько тысяч белковых молекул различных типов.
Капсид зрелого вириона, состоящий из примерно 2000 молекул белка р24, имеет форму усечённого конуса.
Внутри капсида находится белково-нуклеиновый комплекс: две нити вирусной РНК, прочно связанные с белком нуклеокапсида p7, ферменты (обратная транскриптаза, протеаза, интеграза).
С капсидом также ассоциированы белки Nef и Vif (7—20 молекул Vif на вирион).
Внутри вириона (и, вероятнее всего, за пределами капсида) обнаружен белок Vpr8-11. Кроме того, с капсидом ВИЧ-1 (но не ВИЧ-2) связазны около 200 копий клеточного фермента пептидилпролилизомеразы, необходимого для сборки вириона.
Капсид окружён оболочкой, образованной примерно 2000 молекул матриксного белка p17. Матриксная оболочка в свою очередь окружена двуслойной липидной мембраной, являющейся наружной оболочкой вируса. Она образована молекулами фосфолипидов, захваченными вирусом во время его отпочковывания от клетки, в которой он сформировался.
С помощью белка gp120 вирус присоединяется к рецептору CD4 и корецептору, находящимся на поверхности Т-лимфоцитов человека. Стехиометрическое соотношение p24:gp120 в вирионе составляет 60—100:1.
Белки gp41 и в особенности gp120 интенсивно изучаются в качестве возможных мишеней для разработки лекарств и вакцины против ВИЧ .
При формировании наружной оболочки вируса также происходит захват некоторого количества мембранных белков клетки, в том числе человеческих лейкоцитарных антигенов (HLA) классов I и II и молекул адгезии.
Функции важных структурных белков ВИЧ-1
Сокращение
Описание
Функции
gp41 (TM, transmembrane)
Трансмембранный гликопротеин массой 41 кДа
gp120 (SU, surface)
Гликопротеин массой 120 кДа
Наружный белок вириона. Нековалентно связан с трансмембранным белком gp41. С одной молекулой gp41 связаны 3—5 молекул gp120. Способен связывать рецептор CD4. Играет важную роль в процессе проникновения вируса в клетку.
Белок массой 24 кДа
Образует капсид вируса
Матриксный белок массой 17 кДа
Около двух тысяч молекул этого белка образуют слой толщиной 5—7 нм, располагающийся между внешней оболочкой и капсидом вируса.
p7 (NC, nucleocapsid)
Нуклеокапсидный белок массой 7 кДа
Входит в состав ка псида вируса. Образует комплекс с вирусной РНК.
Геном и кодируемые белки
 |
| Геном ВИЧ-1 |
Геном ВИЧ-1
Генетический материал ВИЧ представлен двумя копиями положительно-смысловой (+)РНК. Геном ВИЧ-1 имеет длину 9000 нуклеотидов. Концы генома представлены длинными концевыми повторами (англ. long terminal repeat, LTR), которые управляют продукцией новых вирусов и могут активироваться и белками вируса, и белками инфицированной клетки. 9 генов ВИЧ-1 кодируют, по крайней мере, 15 белков.
Ген pol кодирует ферменты: обратную транскриптазу (RT), интегразу (IN) и протеазу (PR).
Ген gag кодирует полипротеин Gag/p55, расщепляемый вирусной протеазой до структурных белков p6, p7, p17,p24.
Ген env кодирует белок gp160, расщепляемый клеточной эндопротеазой фурином на структурные белки gp41 и gp120.
Другие шесть генов — tat, rev, nef, vif, vpr, vpu (vpx у ВИЧ-2) — кодируют белки, отвечающие за способность ВИЧ-1 инфицировать клетки и производить новые копии вируса. Репликация ВИЧ-1 in vitro возможна без генов nef, vif, vpr, vpu, однако их продукты необходимы для полноценной инфекции in vivo.
Gag: Полипротеин-предшественник Gag/p55 синтезируется с полноразмерной геномной РНК (которая в данном случае служит в качестве мРНК) в процессе стандартной кэп-зависимой трансляции, но возможна и IRES-зависимая трансляция. Предшественники функциональных белков располагаются в составе полипротеина Gag/p55 в следующем порядке: p17…p24…p2…p7…p1…p6 (р1 и р2 — соединительные пептиды; другие продукты расщепления Gag/p55 описаны выше).
Домен М, расположенный внутри области p17/МА, миристилируется (присоединяются остатки миристиновой кислоты) и направляет Gag/p55 к плазматической мембране. Домен I, находящийся внутри области p7/NC, отвечает за межмолекулярные взаимодействия отдельных мономеров Gag/p55. Домен L, также локализованный в области p7/NC, опосредует отпочковывание вирионов от плазматической мембраны; в этом процессе участвует также р6 область полипротеина Gag/p55.
Vpu: Двумя важными функциями белка Vpu являются:
1) разрушение клеточного рецептора CD4 в эндоплазматическом ретикулуме путём привлечения убиквитинлигазных комплексов и
Vpr: Белок Vpr необходим для репликации вируса в неделящихся клетках, в том числе макрофагах. Этот белок, наряду с другими клеточными и вирусными белками, активирует длинные концевые повторы генома ВИЧ. Белок Vpr играет важную роль в переносе провируса в ядро и вызывает задержку деления клетки в периоде G2.
Nef: Белок Nef выполняет несколько функций. Он подавляет экспрессию молекул CD4 и HLA классов I и II на поверхности инфицированных клеток, и тем самым позволяет вирусу ускользать от атаки цитотоксических T-лимфоцитов и от распознавания CD4+-лимфоцитами. Белок Nef может также угнетать активацию T-лимфоцитов, связывая различные белки-компоненты систем внутриклеточной передачи сигнала.
У инфицированных вирусом иммунодефицита макак-резусов активная репликация вируса и прогрессирование болезни возможны только при интактном гене nef. Делеции гена nef были обнаружены в штаммах ВИЧ, выделенных у группы австралийцев с длительным непрогрессирующим течением инфекции.
Однако у части из них со временем появились признаки прогрессирования инфекции, в том числе снижение числа CD4+-лимфоцитов. Таким образом, хотя делеции гена nef и могут замедлять репликацию вируса, это не гарантирует полной невозможности прогрессирования заболевания.
Tat и Rev: Регуляторные белки Tat (транс-активатор) и Rev накапливаются в ядре клетки и связывают определённые участки вирусной РНК. Белок Tat имеет молекулярную массу около 14-15 кДа, связывает вторичную структуру геномной РНК вблизи 5'-нетранслируемой области активирует обратную транскрипцию геномной РНК ВИЧ, синтез вирусных мРНК, необходим для репликации вируса почти во всех культурах клеток, регулирует выход вирионов из зараженных клеток, нуждается в клеточном кофакторе — циклине T1. Белок Rev регулирует экспрессию белков вириона, связывает мРНК гена env в области RRE (англ. Rev response element) интрона, разделающего экзоны генов Tat и Rev.
Белки Tat и Rev стимулируют транскрипцию провирусной ДНК и транспорт РНК из ядра в цитоплазму, а также необходимы для трансляции. Белок Rev обеспечивает также транспорт компонентов вируса из ядра и переключение синтеза регуляторных белков вируса на синтез структурных.
Жизненный цикл
На схеме показано слияние вирриона ВИЧ и плазматической мембраны Т-лимфоцита человека

Этап 1. Взаимодействие вирусного белка gp120 с клеточным рецептором CD4 (указано красной стрелкой)

Этап 2. Конформационные изменения вирусного белка gp120 обеспечивают связывание с клеточным рецептором CCR5 (указано красной стрелкой)

Этап 3. Концевые участки вирусного белка gp41 проникают в плазматическую мембрану клетки (указано красной стрелкой)

Этап 4. Вирусный белок gp41 подвергается значительным конформационным изменениям, складывается пополам (указано красной стрелкой) и образует спираль, что приводит к сближению и слиянию мембран вириона и клетки. Таким образом ВИЧ захватывает Т-лимфоцит с целью дальнейшей репродукции.
Проникновение в клетку и интеграция
Вирусная инфекция начинается, когда вирион ВИЧ сталкивается с человеческой клеткой, имеющей на своей мембране рецептор CD4. Вирусный гликопротеин gp120 прочно связывает рецептор CD4. В результате такого взаимодействия gp120 претерпевает конформационные изменения, которые позволяют ему также связать молекулу корецептора CXCR4 или CCR5 (экспрессируемых на поверхности Т-лимфоцитов, макрофагов, дендритных клеток и микроглии).
В зависимости от способности связывать эти корецепторы, ВИЧ классифицируют на R5-тропные (связывают только CCR5), X4-тропные (связывают только CXCR4) и R5X4-тропные (могут взаимодействовать с обоими корецепторами). Препараты, блокирующие корецепторы могут быть эффективны против ВИЧ.
После описанных событий мембрана клетки и мембрана вириона ВИЧ сливаются, и содержимое вириона проникает внутрь клетки. Белок gp41 очень важен для слияния мембран, поэтому его рассматривают в качестве мишени для разработки противовирусных препаратов. Внутри клетки вирусная РНК высвобождается из капсида, и происходит обратная транскрипция — синтез ДНК на основе матрицы одноцепочечной геномной РНК вируса, катализируемая обратной транскриптазой.
Большая часть лекарственных препаратов, одобренных для применения при ВИЧ-инфекции, направлена на нарушение работы обратной траскриптазы. Синтезированная ДНК транспортируется внутрь ядра клетки и встраивается в хромосому хозяина под действием интегразы. Несколько препаратов, ингибирующих интегразу, проходят ранние стадии клинических испытаний. Вирусная ДНК, встроившаяся в хромосому клетки, называется провирусом.
Человеческая РНК-полимераза в ядре клетки синтезирует информационную РНК (мРНК), а позднее и геномную РНК вируса. Синтезированные РНК транспортируются обратно в цитоплазму, где на матрице мРНК на рибосомах синтезируются вирусные ферменты, структурные и регуляторные белки.
Сборка и отпочковывание вирионов
Геномная РНК вируса, а также вирусные белки транспортируются к местам сборки вирионов. Сборка вирионов происходит на мембране, куда направляется миристилированный полипротеин Gag/p55. Вирионы первоначально формируются из полипротеинов-предшественников структурных белков и ферментов и на этой стадии не являются инфекционными.
В ходе созревания вирусной частицы вирусная протеаза расщепляет белки-предшественники до функциональных компонентов. Несколько одобренных противовирусных препаратов ингибируют работу протеазы и препятствуют формированию зрелых вирионов.
Новые вирусные частицы отпочковываются от поверхности клетки, захватывая часть её мембраны, и выходят в кровяное русло, а клетка хозяина, несущая рецептор CD4, погибает. Недавние исследования показали, что процесс отпочковывания вирионов может быть более сложным, чем считалось ранее. Так было обнаружено, что благодаря взаимодействию белка Gag с компонентами клетки вирионы накапливаются в особых внутриклеточных мультивезикулярных тельцах, которые обычно служат для экспорта белков. Таким образом вирусные частицы высвобождаются из клетки, эксплуатируя её собственную систему транспорта макромолекул.
Распространение по организму
В период острой фазы ВИЧ-инфекции отсутствие специфического иммунного ответа позволяет вирусу активно реплицироваться и достигать высоких концентраций в крови.
Вирус заселяет органы лимфатической системы, CD4 + -лимфоциты, CD8 + -лимфоциты и макрофаги, а также другие клетки: альвеолярные макрофаги лёгких,клетки Лангерганса, фолликулярные дендритные клетки лимфатических узлов, клетки олигодендроглии и астроциты мозга и эпителиальные клетки кишки.
В лимфоидной ткани ВИЧ размножается на протяжении всего заболевания, поражая макрофаги, активированные и покоящиеся CD4 + -лимфоциты и фолликулярные дендритные клетки. Количество клеток, содержащих провирусную ДНК, в лимфоидной ткани в 5—10 раз выше, чем среди клеток крови, а репликация ВИЧ в лимфоидной ткани на 1—2 порядка выше, чем в крови.
Резервуаром ВИЧ служат лимфатические узлы и конкретно дендритныe клетки, в которых вирус сохраняется длительное время после периода острой виремии.
Для активации CD8 + -лимфоцитов и образования антиген-специфических цитотоксических T-лимфоцитов необходима презентация пептидного антигена в комплексе с человеческим лейкоцитарным антигеном класса I.
Дендритные клетки, необходимыe для начала первичных антиген-специфичных реакций, захватывают антигены, перерабатывают и переносят их на свою поверхность, где эти антигены в комплексе с дополнительными стимулирующими молекулами активируют T-лимфоциты.
Заражённые клетки часто не выделяют дополнительных стимулирующих молекул и поэтому не способны вызвать активацию достаточного числа B и T-лимфоцитов, функция которых зависит от дендритных клеток.
После завершения обратной транскрипции в CD4 + -лимфоците вирусный геном представлен провирусной невстроенной ДНК. Для встраивания провирусной ДНК в геном клетки-хозяина и для образования новых вирусов необходима активация T-лимфоцитов.
Контакт CD4 + -лимфоцитов и антигенпредставляющих клеток в лимфоидной ткани, наличие вирусов на поверхности фолликулярных дендритных клеток и присутствие провоспалительных цитокинов (ИЛ-1, ИЛ-6 и ФНОα) способствуют размножению ВИЧ в инфицированных клетках. Именно поэтому лимфоидная ткань служит самой благоприятной средой для репликации ВИЧ.
На 2014 год ВИЧ-инфекция остаётся неизлечимым заболеванием, так как геном вируса интегрируется в хромосомы клеток и может реактивироваться даже после курса антиретровирусной терапии.
В настоящее время идёт поиск безопасных способов редактирования генома человека и исключения из него провирусной ДНК. В 2014 году был предложен метод удаления генома ВИЧ-1 из заражённых клеток при помощи системы CRISPR/Cas9. С помощью этого метода исследователям удалось вырезать фрагмент провирусной ДНК, заключённый между 5'- и 3'-концевыми LTR-областями из хромосом зарежённых клеток в культуре.
Кроме того, этот метод оказался также эффективным для профилактики заражения неинфицированных клеток. Описанный подход может привести к разработке способа полного избавления от ВИЧ-инфекции.
Вирус (лат. virus - яд) - неклеточная форма жизни, мельчайшие болезнетворные микроорганизмы, не видимые в микроскоп. Они значительно меньше бактерий: легко проходят через бактериальные фильтры.
Вирусы способны размножаться только внутри живых клеток, до проникновения в них вирусы не имеют признаков жизни: пассивно перемещаются во внешней среде, ожидая встречи с клеткой-мишенью.
В 1892 году Ивановский Д.И. в ходе изучения мозаичной болезни табака обнаружил, что болезнь вызывается мельчайшими субстанциями, которые проходят через бактериальный фильтр, то есть были меньше бактерий. Вирусы впервые увидели в электронный микроскоп в 1939 году (спустя 19 лет со смерти Ивановского), однако считается, что именно Ивановский положил начало вирусологии как науке.

Вирусы выделяют в отдельное, пятое царство. Несмотря на их кажущуюся безжизненность, от неживой материи их отличают следующие черты:
- Наличие наследственности и изменчивости
- Способность к репродукции (воспроизведению себе подобных)
Рекомендую обратить особое внимание на черты, которые отличают вирусы от живых организмов:
-
Неживое (инертное) состояние
Вне клетки хозяина находятся в неживом состоянии, ожидая внедрения. Вирусы - облигатные внутриклеточные паразиты.
У вирусов отсутствует обмен веществ с внешней средой (метаболизм).
Не имеют клеточной мембраны, ограничивающих их от внешней среды, и, соответственно, клеточного строения.
Не делятся, не размножаются половым путем
У вирусов отсутствует половое размножение и деление. Попав в живую клетку, вирус встраивает свою нуклеиновую кислоту (РНК/ДНК) в наследственный материал клетки-мишени. В результате клетка начинает синтезировать вирусные белки (новые вирусы): так увеличивается численность вирусов.
Вирусы не растут, не увеличиваются в размерах. Стратегия их жизни - безудержное размножение.
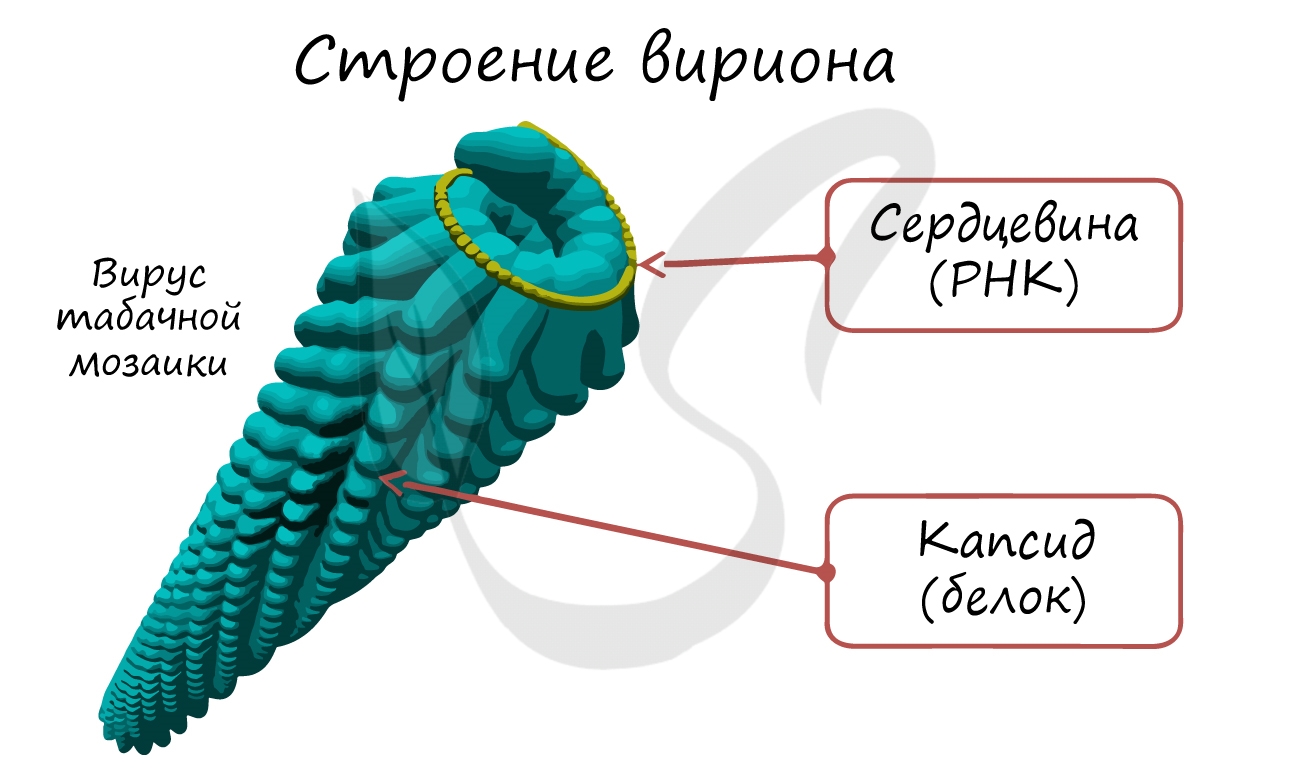
Если мы заглянем в клетку, инфицированную вирусом, то от вируса мы увидим только один элемент - его нуклеиновую кислоту (ДНК/РНК). Во внешней среде вирусы существуют в виде вирионов - полностью сформированных вирусных частиц, состоящих из белковой оболочки (капсида) и нуклеиновой кислоты внутри.
Носителем наследственной информации у вирусов может быть ДНК, РНК. В связи с этим все вирусы подразделяются на ДНК- и РНК-содержащие.
Найдя клетку, на поверхности которой есть подходящий рецептор, вирус взаимодействует с ним и прикрепляется к мембране клетки. Путем эндоцитоза (образование вакуоли) вирус проникает внутрь клетки, выходит из вакуоли в цитоплазму. Наследственный материал (ДНК/РНК) вируса реализуется по схеме: ДНК ↔ РНК → белок.
Проникнув внутрь клетки (инфицировав ее), вирус реализует собственный генетический материал (ДНК/РНК) путем синтеза вирусного белка на рибосомах клетки хозяина. Клетка даже и не подозревает, что вирус встроил в ее РНК/ДНК свой генетический код - она принимает его как свой собственный, а в результате синтезирует вирусные белки.
Образовавшиеся белки объединяются в вирусные частицы, которые могут выходить из клетки разными путями. Вирионы вирусов гепатита C выходят из клетки путем почкования (экзоцитозом), при таком варианте клетка долгое время остается живой и служит для продукции новых вирионов.
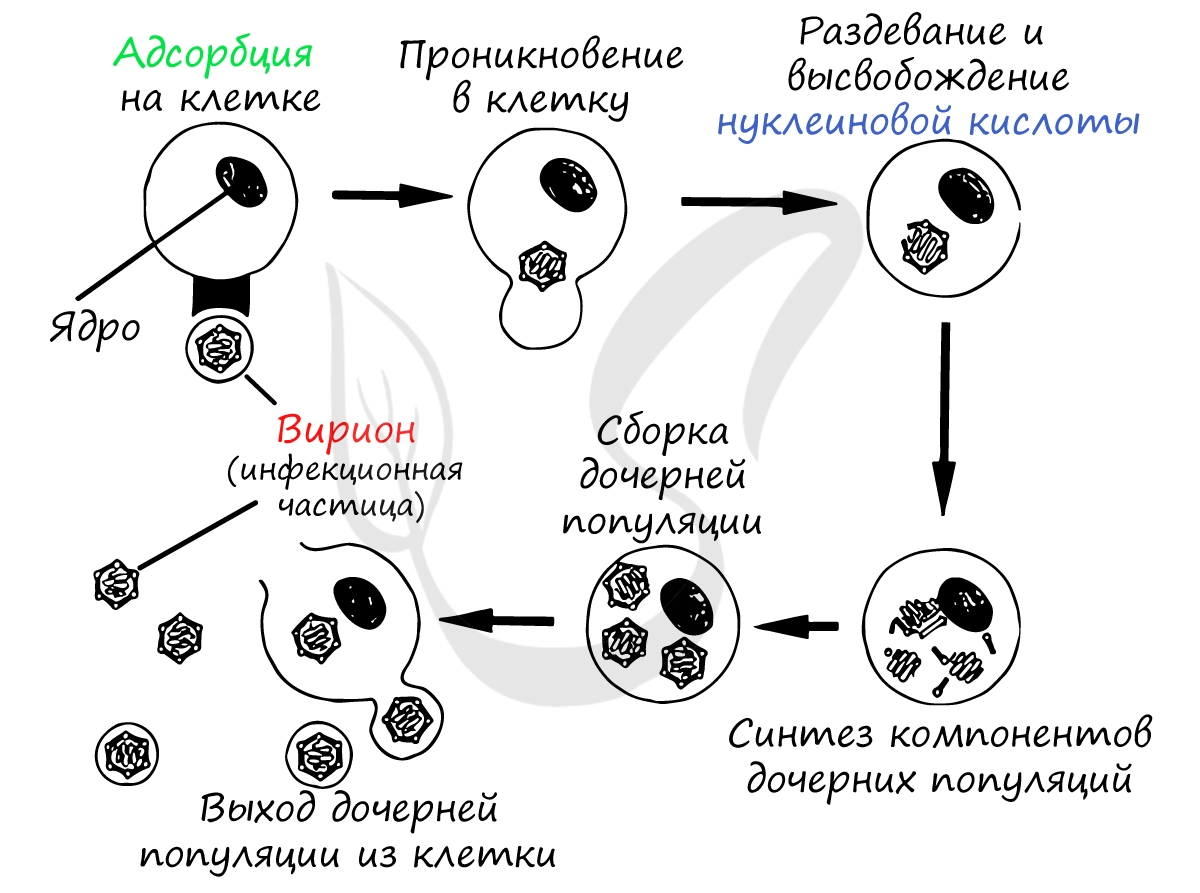
Известен и другой механизм выхода вирионов из клетки: взрывной, при котором оболочка клетки разрывается, и тысячи вирионов отправляются инфицировать новые клетки. Такой способ характерен для аденовирусов, ротавирусов.
Это уникальная группа вирусов, инфицирующая только бактерии. Бактериофаг имеет капсид, с содержащимся внутри наследственным материалом - ДНК (реже РНК), протеиновым хвостом. Бактериофаги открыты в 1915 году и с тех пор активно применяются в ходе генетических исследований.
Ниже вы можете видеть типичное строение бактериофага. Бактериофаг напоминает шприц, который протыкает стенку бактерии и впрыскивает внутрь нее свою нуклеиновую кислоту.
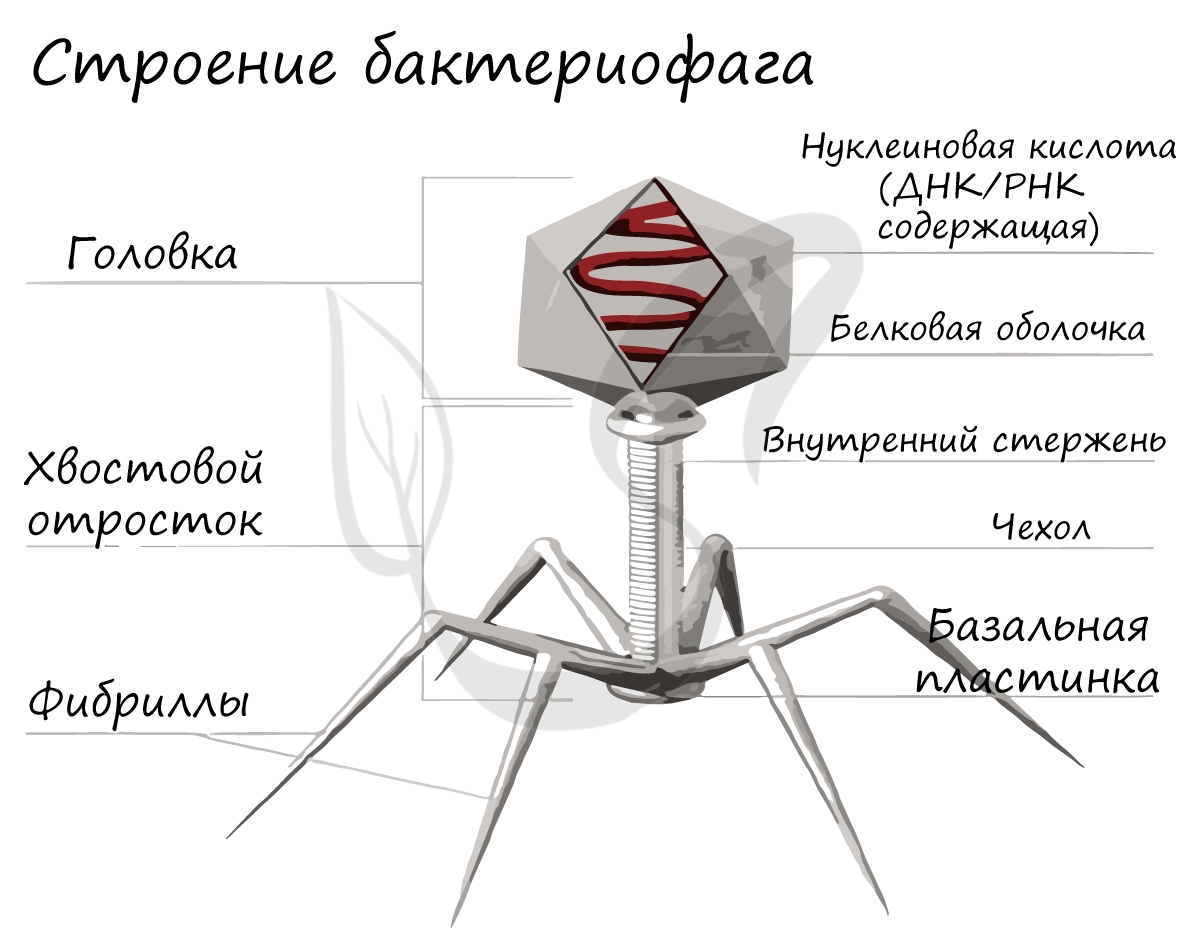
Бактериофаги успешно применяются в медицине для лечения многих заболеваний. Это высокоэффективные, дорогостоящие препараты, которые помогают, например, нормализовать микрофлору кишечника при бактериальных инфекциях.
Вирусы вызывают множество заболеваний человека и животных. Некоторые из них неизлечимы даже на современном этапе развития медицины, например бешенство. К вирусным инфекциям относятся грипп, корь, свинка, СПИД (вызванный ВИЧ), полиомиелит, желтая лихорадка, онковирусы.
Такая группа, как онковирусы, потенцируют развитие опухолей в организме. К ВИЧ и онкогенным вирусам не существует специфических антител, что затрудняет процесс создания вакцины. В то же время против ряда вирусных инфекций: корь, ветряная оспа созданы вакцины, создающие стойкий пожизненный иммунитет.
Клетки вырабатывают защитный белок - интерферон. Это вещество подавляет синтез новых вирусных частиц, приводит к повышению температуры тела (например, при гриппе).

Вирус иммунодефицита человека (ВИЧ) представляет для организма большую опасность. Он размножается в T-лимфоцитах - клетках крови, которые выполняют иммунную функцию. С гибелью T-лимфоцитов разрушается иммунная система, становится невозможным сопротивление организма бактериями, вирусам и грибам, что в отсутствии лечения приводит к вторичным инфекциям.
Риск заражения ВИЧ присутствует при гемотрансфузии (переливании крови), половом акте. Инфекция также может быть передана от ВИЧ инфицированной матери к плоду.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:
- Вирусы для персональных данных
- Сколько живет вирус сальмонеллы
- Люди это вирус а мы исцеление
- Ставит прививку от гриппа после простуды
- Как проникают в клетку вирусы животных и человека
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

