Бактерии и вирусы в биотехнологиях
КОНТРОЛЬНАЯ РАБОТА ПО БИОТЕХНОЛОГИИ Вариант № 8
студент группы 03031052
заочной формы обучения
Распопова марина Александровна
Белгород 2015 г.
Вариант №8
Вопрос №1: Вирусы и бактериофаги. Использование в биотехнологии.
Вирусы – это группа ультрамикроскопических облегантных (строгих) внутриклеточных паразитов, способных размножаться только в клетках живых организмов: многоклеточных и одноклеточных.
Среди микробов вирусы характеризуются наименьшей величиной – они измеряются в нанометрах (нм), и облигатным паразитизмом. Последний признак положен в основу классификации их на вирусы бактерий, или бактериофаги, вирусы растений и вирусы животных; имеются также и вирусы грибов.
Каждый вирион в очищенном виде представляет собой истинный кристалл, который построен из нуклеиновой кислоты и белка, не связанных друг с другом ковалентными связями. Понятие "вирион" относится к интактной вирусной частице (от лат. intactus – нетронутый, неповрежденный), способный к инфицированию или заражению.
Нуклеиновые кислоты – вещества наследственности вирусов. По типу нуклеиновой кислоты их подразделяют на РНК-содержащие вирусы и ДНК-содержащие вирусы. К первым относят все вирусы растений, ко вторым – большинство бактериофагов, ряд вирусов человека и животных (аденовирусы, вирусы герпеса, осповакцины и др.).
Белок структурируется вокруг вирусной нуклеиновой кислоты (генома) в виде оболочки и называется капсидом. Форма вириона определяется его капсидом. Вместе с нуклеиновой кислотой капсид образует нуклеокапсид.
Примерный перечень вирусов включает 17 семейств вирусов позвоночных и 7 семейств вирусов беспозвоночных животных, 10 семейств вирусов бактерий. Описаны 20 родов вирусов растений и 5 родов вирусов грибов. Классификационные схемы вирусов до конца еще не устоявшиеся, к тому же открывают новые для науки вирусы (пример с вирусами эбола, иммунодефицита человека). Представителями ДНК-содержащих вирусов являются вирусы контагиозного моллюска, оспы, герпеса, большинство фагов бактерий; РНК-содержащими являются вирусы растений, вирусы гриппа человека, бешенства, полиомиелита и др.
Вироиды. По молекулярной структуре вироиды представляют собой одноцепочечные, ковалентно замкнутые, кольцевые молекулы РНК, лишенные капсидов. Число нуклеотидов в таких РНК находится в пределах 240-400. По форме вироиды могут быть линейные и кольцевидные, они способны принимать шпилечную, квазидвухцепочечную конформацию (от лат. quasi – якобы, как-будто, почти, близко; conformatio – форма, расположение). Каждый тип вироида содержит уникальный, только ему присущий, особый вид низкомолекулярной РНК. Размеры вироидов находятся в пределах 15 нм. В чувствительных клетках растений-хозяев они сосредоточиваются в ядре, ассоциируясь с ядрышком в виде белково-нуклеинового комплекса, и реплицируются автономно целиком при помощи предшествующих или активированных ферментов хозяина. Вироиды не транслируются. Это подтверждается структурным сходством их между собой и отсутствием у ряда вироидов кодонов-инициаторов. В то же время репликация происходит благодаря транскрипции последовательностей вироидных РНК с РНК-матриц при участии РНК-полимераз.
Бактериофаги переводятся с греческого языка как "пожиратель бактерий". Они относятся к особым представителям царства вирусов, однако в отличие от других видов, бактериофаги умеют использовать бактериальные клетки для размножения.Бактериофаги очень мелкие, неклеточные организмы. Средняя величина одного экземпляра 0,1-0,2 миллимикрона, а проще говоря, миллионные доли миллиметра, что составляет 1/100 часть от клетки обычной бактерии размером около пяти микрон. Внешний вид бактериофагов тоже непривычный. Среди них есть роскошные кристаллы, с четкими гранями, расположенные на ножках, словно космические корабли. Их стенки состоят из белковых молекул, а внутри расположена бесценная генная информация - дезоксирибонуклеиновая кислота и рибонуклеиновая кислота, или же ДНК и РНК. Среда обитания, как и морфология, бактериофагов очень разнообразна. Их можно встретить везде, где обитают бактерии - в земле, воздухе, воде, в атмосферных осадках, на предметах, одежде и еде, на шерсти животных и коже, а также внутри нашего организма.Словом, там, где много микроорганизмов, можно встретить много бактериофагов. Самым излюбленным местом обитания фагов является вода и почва с органическими удобрениями и чернозем.
Использование вирусов и бактериофагов в биотехнологии.
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
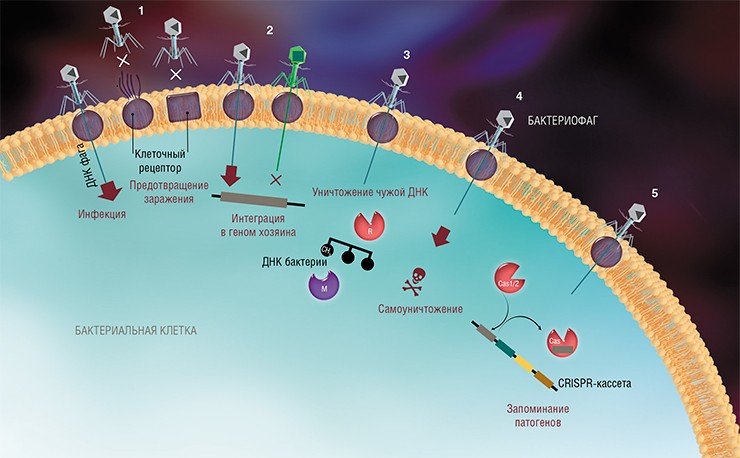
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
Врага нужно знать в лицо
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
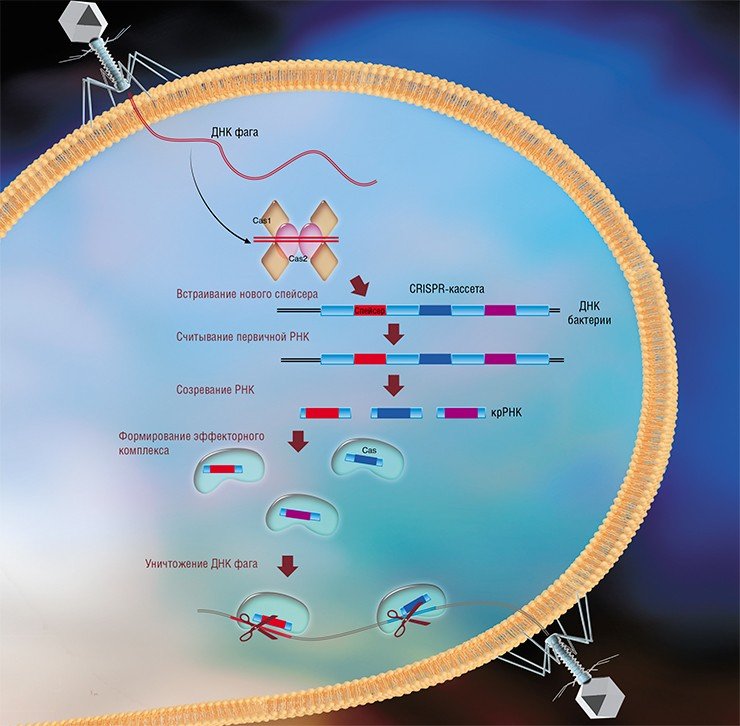
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
Гонка вооружений
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
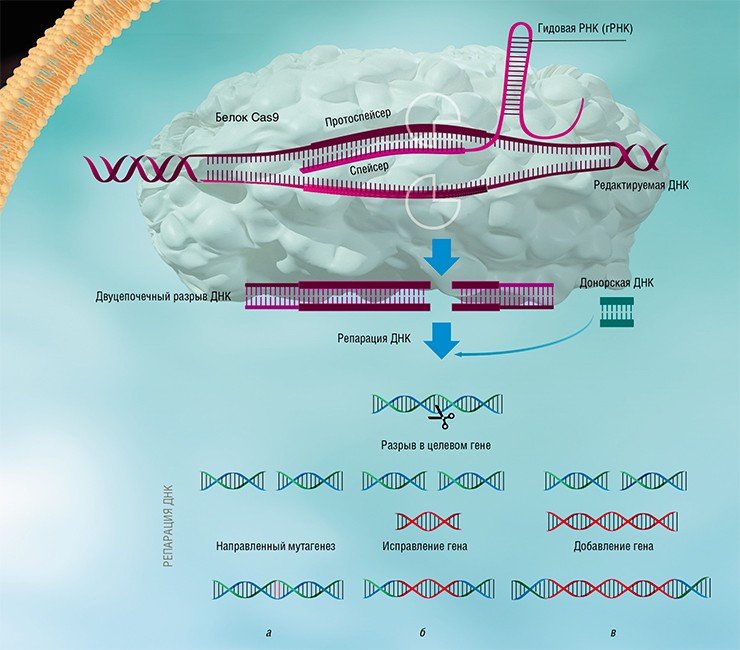
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)
Объекты, используемые в биотехнологии (они включают представителей, как прокариот, так и эукариот), чрезвычайно разнообразны по своей структурной организации и биологическим характеристикам. К объектам биотехнологии относятся:
— бактерии и цианобактерии;
— клетки растений и животных.
В группу низших растений входят и микроскопически малые организмы (одноклеточные и многоклеточные), и очень крупные по размерам. Но все они объединены такими общими признаками, как отсутствие расчленения тела на вегетативные органы и разнообразие способов размножения.
К низшим относят следующие отделы: Вирусы, Бактерии, группа отделов Водоросли (Сине-зеленые, Зеленые, Диатомовые, Бурые, Красные и др.), Миксомицеты, Грибы, Лишайники. По способу питания их подразделяют на две группы: автотрофы (водоросли и лишайники), способные к фотосинтезу, и гетеротрофы (вирусы, бактерии — за небольшим исключением, — миксомицеты, грибы), использующие для питания готовые органические вещества.
Низшие растения прошли длинный исторический путь развития, но многие их представители до сих пор сохранили черты примитивной организации. На определенном этапе развития они дали начало высшим растениям, венцом которых являются покрытосеменные.
Вирусы (от лат. virus — яд) — это мельчайшие организмы (не более 200-300 нм), невидимые в световой микроскоп, не имеющие клеточного строения, лишенные собственных систем энергообеспечения, отличающиеся паразитическим способом существования, т. е. являющиеся внутриклеточными паразитами. Детальное изучение вирусов стало возможным с развитием электронной микроскопии, биохимии, молекулярной биологии.
Механизм инфицирования. Условно процесс вирусного инфицирования в масштабах одной клетки можно разбить на следующие этапы.
Присоединение к клеточной мембране — так называемая адсорбция. Обычно, для того чтобы вирус адсорбировался на поверхности клетки, она должна иметь в составе своей плазматической мембраны специфический белок (часто гликопротеин) — рецептор, специфичный для данного вируса. Наличие рецептора нередко определяет круг хозяев данного вируса, а также его тканеспецифичность.
Проникновение в клетку. На этом этапе вирусу необходимо доставить внутрь клетки свою генетическую информацию. Некоторые вирусы привносят также собственные белки, необходимые для ее реализации. Различные вирусы для проникновения в клетку используют разные стратегии. Вирусы также различаются по локализации их репликации: часть вирусов размножается в цитоплазме клетки, а часть — в ее ядре.
Создание новых вирусных компонентов. Размножение вирусов в самом общем случае предусматривает три процесса:
— транскрипцию вирусного генома, т. е. синтез вирусной мРНК;
— трансляцию мРНК, т. е. синтез вирусных белков;
— репликацию вирусного генома.
У многих вирусов существуют системы контроля, обеспечивающие оптимальное расходование биоматериалов клетки-хозяина. Например, когда вирусной мРНК накоплено достаточно, транскрипция вирусного генома подавляется, а репликация, напротив, активируется.
Классификация вирусов. Систематику и таксономию вирусов кодифицирует и поддерживает Международный комитет по таксономии вирусов (International Committee on Taxonomy of Viruses, ICTV), поддерживающий также и таксономическую базу The Universal Virus Database ICTVdB.
Форма представления генетической информации лежит в основе современной классификации вирусов. В настоящее время их подразделяют на ДНК- и РНК-содержащие вирусы.
К вирусам относятся бактериофаги — паразиты микроорганизмов. Они состоят из двух частей: призматической головки и хвостового отростка. Если добавить к микробам бактериофаг, действующий именно на данный вид микробов, через несколько минут его можно обнаружить на поверхности микробной клетки, к которой он прикрепляется отростком. Затем бактериофаг выделяет фермент, растворяющий оболочку бактерии в месте прикрепления отростка. Сквозь это отверстие ДНК, находящаяся в головке, попадает в клетку. Капсид остается снаружи. Под влиянием ДНК фага обмен веществ бактерии перестраивается, белок синтезирующие системы бактерии образуют белки фага, происходит репликация фаговой ДНК. Через 15-30 мин оболочка клетки разрывается, и огромное количество фагов выходит в окружающую среду. Фаги заражают новые клетки, вызывая их лизис.
Значение вирусов. Вирусы вызывают ряд опасных заболеваний человека (оспу, гепатит, грипп, корь, полиомиелит, СПИД, рак и т. д.), растений (мозаичную болезнь табака, томата, огурца, карликовость, увядание земляники), животных (чуму свиней, ящур). Однако препараты соответствующих бактериофагов применяют для лечения бактериальных заболеваний — дизентерии и холеры.
Получение интерферона — особого клеточного белка, препятствующего размножению вирусов, — широко используют в медицине, особенно во время вспышек эпидемий гриппа. Это вещество универсального действия, активное по отношению ко многим вирусам, хотя чувствительность разных вирусов к нему неодинакова. Будучи продуктом самой клетки, интерферон полностью лишен токсического воздействия на нее. Сейчас применяют готовый интерферон, его можно синтезировать в клетках, культивируемых вне организма.
Строение бактерий. Подавляющее большинство бактерий (за исключением актиномицетов и нитчатых цианобактерий) одноклеточны. По форме клеток они могут быть шаровидными (кокки), палочковидными (бациллы, клостридии, псевдомонады), извитыми (вибрионы, спириллы, спирохеты), реже — звездчатыми, тетраэдрическими, кубическими, С- или О-образными. Обязательными клеточными структурами бактерий являются:
— цитоплазматическая мембрана (ЦПМ).
Прокариоты, в отличие от эукариот, не имеют в цитоплазме обособленного ядра. Вся необходимая для жизнедеятельности бактерий генетическая информация содержится и одной двухцепочечной ДНК (бактериальная хромосома), имеющей форму замкнутого кольца. Она в одной точке прикреплена к ЦПМ. ДНК в развернутом состоянии имеет длину более 1 мм. Бактериальная хромосома представлена обычно в единственном экземпляре, т. е. практически все прокариоты гаплоидны, хотя в отдельных случаях одна клетка может содержать несколько копий своей хромосомы. Деление хромосомы сопровождается делением клетки. Область клетки, в которой локализована хромосома, называется нуклеоидом; она не окружена ядерной мембраной. 1$ связи с этим новосинтезированная мРНК сразу доступна для связывания с рибосомами, т. е. процессы транскрипции и трансляции могут протекать одновременно. Ядрышка нет.
Помимо хромосомы, в клетках бактерий часто находятся плазмиды — замкнутые в кольцо небольшие молекулы ДНК, способные к независимой репликации. Они содержат дополнительные гены, необходимые лишь в специфических условиях. В них кодируются механизмы устойчивости к отдельным лекарственным препаратам, способности к переносу генов при конъюгации, синтеза веществ антибиотической природы, способности использовать некоторые сахара или обеспечивать деградацию ряда веществ. То есть плазмиды действуют как факторы адаптации. В некоторых случаях гены плазмиды могут интегрировать в хромосому бактерии.
Рибосомы прокариот отличаются от таковых у эукариот и имеют константу седиментации 70 S (у эукариот — 80 S).
У разных групп прокариот имеются локальные впячива- ния ЦПМ — мезосомы, выполняющие в клетке разнообразные функции и разделяющие ее на функционально различные части. Считается, что мезосомы принимают участие в делении бактерий. Когда на мембранах мезосом располагаются окислительно-восстановительные ферменты, они являются эквивалентами митохондрий клеток растений и животных. У фотосинтезирующих бактерий во впячивания мембран вмонтирован пигмент — бактериохлорофилл. С его помощью и осуществляется бактериальный фотосинтез.
С внешней стороны от ЦПМ находятся несколько слоев (клеточная стенка, капсула, слизистый чехол), называемых клеточной оболочкой, а также поверхностные структуры (жгутики, ворсинки, пили).
У бактерий существует два основных типа строения клеточной стенки, свойственных грамположительным и грамотрицательным видам. Клеточная стенка грамположительных бактерий представляет собой гомогенный слой толщиной 20-80 нм, построенный в основном из пептидогликана муреина с большим количеством тейхоевых кислот и небольшим количеством полисахаридов, белков и липидов. У грамотрицательных бактерий пептидогликановый слой неплотно прилегает к ЦПМ и имеет толщину лишь 2-3 нм. Он окружен наружной мембраной, имеющей, как правило, неровную, искривленную форму.
С внешней стороны от клеточной стенки может находиться капсула — аморфный слой гидратированных полисахаридов, сохраняющий связь со стенкой. Слизистые слои не имеют связи с клеткой и легко отделяются, чехлы же не аморфны, а имеют тонкую структуру.
Многие бактерии способны к активному движению с помощью жгутиков — выростов цитоплазмы.
Размножение бактерий. Бактерии не имеют полового процесса и размножаются лишь равновеликим бинарным поперечным делением или почкованием. Для одной группы одноклеточных цианобактерий описано множественное деление (ряд быстрых последовательных бинарных делений, приводящих к образованию от 4 до 1000 новых клеток под оболочкой материнской клетки).
У прокариот может происходить горизонтальный перенос генов. При конъюгации клетка-донор в ходе непосредственного контакта передает клетке-реципиенту часть своего генома (в некоторых случаях — весь геном). Участки ДНК донорной клетки могут обмениваться на гомологичные участки ДНК реципиента. Вероятность такого обмена значима только для бактерий одного вида.
Бактериальная клетка может поглощать и свободно находящуюся в среде ДНК, включая ее в свой геном. Данный процесс носит название трансформации. В природных условиях обмен генетической информацией протекает с помощью бактериофагов (трансдукция). При горизонтальном переносе новых генов не образуется, однако осуществляется создание разных генных сочетаний. Эти свойства бактерий очень важны для генетической инженерии.
Спорообразование у бактерий. Некоторые бактерии образуют споры. Их формирование характерно для особо устойчивых форм с замедленным метаболизмом и служит для сохранения в неблагоприятных условиях, а также для распространения. Споры могут сохраняться продолжительное время, не теряя жизнеспособности. Так, эндоспоры многих бактерий способны выдерживать 10-минутное кипячение при 100 °С, высушивание в течение тысячи лет и, по некоторым данным, сохраняются в жизнеспособном состоянии в почвах и горных породах миллионы лет.
Метаболизм бактерий. За исключением некоторых специфических моментов, биохимические пути, по которым осуществляется синтез белков, жиров, углеводов и нуклеотидов, у бактерий схожи с таковыми у других организмов. Однако по числу возможных биохимических путей и, соответственно, по степени зависимости от поступления органических веществ извне бактерии различаются. Часть бактерий может синтезировать все необходимые им органические молекулы из неорганических соединений (автотрофы), другие же требуют готовых органических соединений, которые они способны лишь трансформировать (гетеротрофы).
Значение бактерий. Бактерии-сапрофиты играют большую роль в круговороте веществ в природе, разрушая в экосистемах мертвый органический материал. Хорошо известна их роль во всех биогеохимических циклах на нашей планете. Бактерии принимают участие в круговоротах химических элементов (углерода, железа, серы, азота, фосфора и др.), в процессах почвообразования, определяют плодородие почв.
Биотехнологические функции, выполняемые бактериями, разнообразны. Их применяют при производстве различных веществ: уксуса (Gluconobacter suboxidans), молочнокислых напитков и продуктов (Lactobacillus, Leuconostoc), а также микробных инсектицидов (Bacillus thuringiensis) и гербицидов, белков (Methylomonas), витаминов (Clostridium — рибофлавин); при переработке отходов, получении бактериальных удобрений, растворителей и органических кислот, биогаза и фотоводорода. Широко используется такое свойство некоторых бактерий, как диазотрофность, т. е. способность к фиксации атмосферного азота.
Благодаря быстрому росту и размножению, а также простоте строения, бактерии активно применяют в научных исследованиях по молекулярной биологии, генетике и биохимии, в генно-инженерных работах при создании геномных клонотек и введении генов в растительные клетки (агробактерии). Информация о метаболических процессах бактерий позволила производить бактериальный синтез витаминов, гормонов, ферментов, антибиотиков и др.
Перспективными направлениями являются очистка с использованием бактерий почв и водоемов, загрязненных нефтепродуктами или ксенобиотиками, а также обогащение руд с помощью сероокисляющих бактерий.
Нельзя забывать о том, что отдельные виды бактерий вызывают опасные заболевания у человека (чуму, холеру, туберкулез, брюшной тиф, сибирскую язву, ботулизм и др.), животных и растений (бактериозы). Некоторые виды бактерий могут разрушать металл, стекло, резину, хлопок, древесину, масла, лаки, краски.
ВНИМАНИЕ! САЙТ ЛЕКЦИИ.ОРГ проводит недельный опрос. ПРИМИТЕ УЧАСТИЕ. ВСЕГО 1 МИНУТА.
Вирусы являются паразитами и могут размножаться только в клетках других организмов. Вне клеток вирусы представляют собой комплексы нуклеиновой кислоты (ДНК или РНК) с белком. Они не являются организмами в полном смысле слова, так как не имеют свойственных клеткам органелл, не обладают собственным обменом веществ и живут и размножаются в клетках животных, человека, растений, бактерий, используя для своей жизнедеятельности ресурсы и обменные процессы этих клеток.
Бактерии являются доядерными организмами (прокариотами), так как у них имеется примитивное ядро без оболочки, ядрышка, гистонов, а в цитоплазме отсутствуют высокоорганизованные органеллы <митохондрии, лизосомы, аппарат Гольджи и др.)
К растениям относятся водоросли, являющиеся водными организмами, и высшие растения, обитающие преимущественно на суше. Водоросли не имеют органов и тканей и состоят из недифференцированных (одинаковых) клеток. Высшие растения являются многоклеточными организмами, имеющими специализированные органы - корни, стебли, листья. Они состоят из тканей, образованных специализированными клетками. Растения служат поставщиками питательных веществ для других организмов.
Грибы сочетают в себе черты клеток растений и животных. Они имеют клеточное ядро и, как у растений, прочную клеточную стенку. Как клетки животных, они способны синтезировать полисахариды - хитин и гликоген и нуждаются в некоторых витаминах. Особенно интересны для биотехнологии микроскопические грибы - дрожжи, плесневые и другие микроорганизмы, применяемые в хлебопекарной, пивоваренной и молочной промышленности, а также для получения органических кислот, спиртов, антибиотиков, кормового белка, различных биологически активных веществ.
Животные состоят из двух основных групп: простейших (одноклеточных) и высших (многоклеточных). Их клетки, как и клетки растений, являются ядерными. Поскольку многие простейшие являются паразитами и возбудителями болезней высших животных и человека, культивирование их на искусственных средах затруднено. Они используются в основном в токсикологических исследованиях.
Основными технологическими принципами, используемыми в биотехнологии, являются:
а) брожение (ферментация);
б) биоконверсия (превращение одного вещества в другое);
в) культивирование бактерий, вирусов, растительных и животных клеток;
г) генетическая инженерия.
Простейшим способом получения биотехнологической продукции является использование животных и их органов и тканей. Ткани высших животных являются источниками белка, липидов, некоторых витаминов. Например, иммунные сывороточные препараты получают из крови иммунизированных животных (лошадей, кроликов); гормон инсулин - из поджелудочных желез крупного рогатого скота и свиней. Гормон роста получают из гипофиза умерших людей; для получения препаратов крови используют донорскую, плацентарную и абортную кровь.
Сырье животного происхождения является наиболее дорогим. В связи с этим в настоящее время все чаще используются культуры клеток животных или человека, выращиваемых на искусственных средах. Примером такой технологии является получение противовирусного препарата интерферона, применяющегося для профилактики и лечения гриппа и других вирусных инфекций. Наиболее перспективным способом производства биологически активных веществ является генная инженерия. В частности, так получают человеческий инсулин - гормон белковой природы.
Для получения многих лекарственных средств (сердечных, мочегонных, противовоспалительных и т.д.) используют растения. Несмотря на то, что традиционные методы извлечения физиологически активных и лекарственных соединений из растений (экстракция, перегонка, фильтрация) по-прежнему широко используются, все большее значение приобретают технологии получения биологически активных веществ из клеточных культур, а также производство продуктов из генетически модифицированных растений.
Из водорослей получают агар-агар и альгинаты - полисахариды, используемые в пищевой промышленности, а также для изготовления микробиологических сред.
Бактерии наиболее часто используются в биотехнологических процессах. Из биомассы бактерий получают различные органические вещества - аминокислоты, белки, в том числе ферменты. Бактерии являются удобным объектом для генетических исследований. Наиболее изученной и широко применяемой в генноинженерных исследованиях является кишечная палочка Escherichia coli (Е. coli), обитающая в толстом кишечнике человека.
Читайте также:


