Антиген к коровому антигену гепатита с
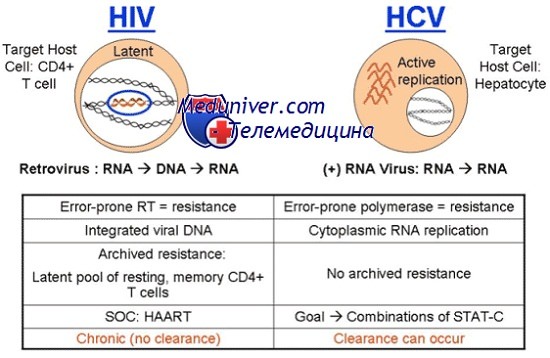
Сегодня известно минимум 10 структурных и неструктурных белков, кодируемых геномом HCV. К структурным белкам относят core, envelop 1 и envelop 2. Белок core является белком нуклеокапсида, тогда как envelop 1 и envelop 2 — гликопротеины внешней оболочки вируса. В структурной зоне кодируется также белок р7, функция которого не ясна, однако аналогия с другими представителями семейства Flaviviridae позволяет предположить, что его функция связана с высвобождением вириона из инфицированной клетки.
Этот белок отщепляется клеточной пептидазой от envelop 2, но не во всех случаях, что обусловливает существование envelop 2 в виде двух форм более и менее протяженной.
Неструктурная область генома HCV кодирует 6 белков — NS2, NS3, NS4A, NS4B, NS5A и NS5B. Белок NS2 является вирусной металлозависимой протеиназой. Белок NS4A действует как эффектор или кофактор для NSЗ-протеолитической активности в NS4A/NS4B, NS4B/NS5A, NS5A/NS5B сайтах нарезания полипротеина вируса.
В настоящее время фрагменты структурных и неструктурных белков, полученных генноинженерным путем (рекомбинантные белки) или с помощью химического синтеза, используют в качестве антигенов при конструировании иммуноферментных тест-систем. Первое поколение иммуноферментных тест-систем появилось на рынке в 1989 году и было основано на прямом ИФА. В качестве иммуносорбента были использованы фрагменты двух белков, NS3 и NS4, обозначаемых как 5-1-1 и С100-3.
Одновременно были разработаны и подтверждающие тесты на основе иммуноблота с рекомбинантными белками (RIBA). Чувствительность этих тест-систем первого поколения составляла только 64% для ИФА и 55% для иммуноблота. Тест-системы второго поколения появились на рынке в 1991 году. В качестве антигенов, сорбированных на твердой фазе, в этих тест-системах использовали капсидные белки (фрагмент с22-3) и антигены неструктурных регионов NS3 (фрагменты с200 и сЗЗс) и NS4, что позволило повысить чувствительность и специфичность исследований. Поскольку гуморальный иммунный ответ на капсидные антигены (структурные белки) нагинается быстрее, гем на неструктурные белки, период от инфицирования до выявляемой сероконверсии удалось уменьшить до двух месяцев.
Подтверждающие тест-системы на основе иммуноблота позволяли идентифицировать участвующие в реакции антигены. Результаты, полученные при помощи этих тест-систем, интерпретировали как положительные лишь при реакции антител, находящихся в исследуемом субстрате, по крайней мере, с двумя антигенами, тогда как при наличии реакции лишь с одним из антигенов результат считали неопределенным. Было установлено, что специфичность второго поколения тест-систем зависела от источника антигенов. В 1993 году на рынке появилось третье поколение тест-систем. В дополнение к вышеупомянутым антигенам в этих тест-системах используются также антигены, аминокислотная последовательность которых соответствует иммунодоминантным участкам NS5 белков.
В тест-системах первого, второго и третьего поколений в качестве антигенов использовались или рекомбинантные, или синтетические пептиды. В настоящее время можно выделить также тест-системы четвертого поколения, в которых в качестве иммуносорбента используют сочетания рекомбинантных и синтетических пептидов.
Опыт применения тест-систем различных поколений в мире очень большой. Было установлено, что если с помощью тест-систем первого или второго поколения у больных с острым вирусным гепатитом С антитела выявляли на 10-16, а в ряде случаев и 25-30 неделе от начала заболевания, то диагностикумы третьего поколения позволяли сократить этот срок до 2-3 недель. Согласно обобщенным данным чувствительность тест-систем первого, второго и третьего поколений составляет соответственно 70-80%, 92-95% и 97%.
В то же время, по данным С. Colin, 2001, чувствительность тест-систем третьего поколения составила 98,9% у пациентов с хроническими заболеваниями печени и 97,2% на специальных контрольных панелях сывороток. Достижение высокой чувствительности иммуноферментных тест-систем 3 и 4 поколения сопряжено с некоторыми проблемами в обеспечении специфичности исследований, что в ряде случаев может приводить к появлению ложноположительных результатов. В литературе имеются данные о возможных погрешностях в специфичности ELISA 3 тест-систем. Они являются общими для всех ELISA тест-систем, включая тест-системы для диагностики СПИДа.
Ложнопозитивные результаты могут быть следствием повышенного содержания в образцах гамма-глобулинов (сыворотки пациентов африканской расы, миеломная болезнь, ревматоидные факторы), заболеваний печени (цирроз, рак), аутоиммунных заболеваний (коллагенозы, аутоиммунные гепатиты), других вирусных инфекций (ВИЧ, гепатит В) и длительного хранения сывороток в меняющихся температурных условиях. Проведение какой-либо иммунизации также может сопровождаться повышением частоты ложнопозитивных реакций. Рекомендуемые в настоящее время меры по устранению этой проблемы следующие: а) повторная постановка образца в этой же ИФТС; б) повторная детекция anti-HCV в другой ИФТС; в) использование подтверждающих тестов на основе ИФА и иммуноблота.
Однако использование предлагаемых способов подтверждения результатов зачастую приводят к расхождениям в их итоговой трактовке, что показано исследованиями российских и зарубежных исследователей.
В настоящее время производители ИФТС для детекции anti-HCV достигают высокой чувствительности или за счет более полного выявления антител к NS3 или антител к антигенам core. Сравнительные исследования, выполненные на различных группах риска и специальных контрольных панелях показали, что тест-системы, лучше выявлявшие антитела к NS3, оказались несколько более чувствительными, чем тест-системы, лучше выявлявшие антитела к антигенам core. Их чувствительность составляла, соответственно 99,9% и 98,6%.
Острый вирусный гепатит - диффузное воспалительное поражение клеток печени, вызываемое специфическими гепатотропными вирусами.
Острый вирусный гепатит - это группа широкораспространенных болезней, вызываемых разными вирусами, но имеющих сходные клинические биохимические и морфологические признаки.
Этиология и характеристики вирусов
Причиной острого вирусного гепатита могут быть, по крайней мере, пять различных агентов. Инфекционные поражения печени, вызываемые вирусом Эпштейна-Барр, цитомегаловирусом и вирусом желтой лихорадки, считаются отдельными болезнями и обычно не подразумеваются при употреблении термина "острый вирусный гепатит".
Вирус гепатита A (HAV) - это одноцепочечный РНК-вирус подобный пикорнавирусам. Вирусный антиген (Ag) обнаруживается в плазме, каловых массах и печени только в острый период инфекции. IgM-антитела выявляются на ранних этапах болезни, но через несколько недель исчезают; им на смену приходят IgG, которые обычно сохраняются на протяжении всей жизни. Таким образом, IgM-антитела можно рассматривать как маркеры острой инфекции, тогда как IgG лишь указывают, что организм прежде подвергался воздействию вируса гепатита А и имеет иммунитет к повторному инфицированию. Вирус гепатита А неизменно исчезает после острой инфекции; в отличие от вирусов гепатитов В и С, неизвестны случаи его хронического носительства, он не играет никакой роли в развитии хронического активного гепатита или цирроза.
Вирус гепатита В (HBV) является наиболее изученным и сложным агентом. Инфекционная частица (частица Дейна) состоит из сердцевины (кора) и внешней оболочки (капсида). В состав вириона входит кольцевая двухцепочечная ДНК и ДНК-полимераза; репликация вирусных частиц происходит внутри ядер инфицированных гепатоцитов. Белки оболочки присутствуют в цитоплазме в значительных количествах; с помощью иммунологических методов их определяют в плазме как поверхностный антиген гепатита В (см. ниже).
По крайней мере четыре различные системы антиген-антитело тесно связаны с вирусом гепатита В:
- Поверхностный антиген вируса гепатита В (HBsAg, австралийский антиген) связан с белковой оболочкой вируса; обнаружение его в плазме крови позволяет диагностировать острый гепатит В и означает, что кровь больного стала потенциальным источником инфицирования. (Некоторые подтипы антигенов представляют эпидемиологический интерес, но их клиническое значение невелико.) Австралийский антиген выявляется во время инкубационного периода (обычно за 1-6 нед до развития клинических или биохимических признаков болезни) и исчезает при выздоровлении. Соответствующие антитела (анти-HBs) можно обнаружить значительно позже, лишь через недели или месяцы после клинического выздоровления; обычно они сохраняются в течение всей жизни и их присутствие в крови указывает на имевшее место инфицирование вирусом гепатита В в прошлом и наличие относительной защиты от него в будущем. У некоторых больных (до 10%) австралийский антиген продолжают обнаруживать после острой фазы инфекции, а соответствующие антитела не появляются; у таких больных обычно развивается хронический гепатит, или они становятся бессимптомными носителями вируса.
- Коровый антиген (HBcAg) ассоциируется с сердцевиной (кором) вириона. Он может быть обнаружен в инфицированных клетках печени, а в плазме выявляется лишь в том случае, если с помощью специальных методик разрушают вирусные частицы. Соответствующие антитела (анти-НВс), как правило, обнаруживают в начале периода манифестации; впоследствии их титр постепенно снижается. Наличие антител к HBcAg наряду с антителами к HBsAg указывает на предшествующее инфицирование HBV. Антитела к HBcAg регулярно обнаруживаются у носителей HBsAg, не способных к формированию антител к HBsAg. В хронических случаях анти-НВс-антитела представляют собой главным образом иммуноглобулины класса IgG, тогда как при острой инфекции доминируют анти-НВс-антитела класса IgM. Иногда последние выполняют роль маркера недавней инфекции HBV, заполняя "провал" между исчезновением HBsAg и появлением анти-НВв-антител.
- Антиген c (HBeAg), по-видимому, представляет собой пептид, входящий в состав вирусного кора. Он обнаруживается только в HBsAg-положительной плазме и связан каким-то образом с синтезом вирусной ДНК-полимеразы. Присутствие этого антигена свидетельствует об активной репликации вируса и, как правило, сочетается с более высокой инфицирующей способностью крови и повышенной вероятностью развития хронического поражения печени. Наоборот, присутствие соответствующих антител (анти-НВе) указывает на относительно более низкую инфицирующую способность и обычно предвещает благоприятный исход.
- Вирус гепатита D (HDV, дельта-фактор) является уникальным. Его РНК дефектна, вследствие чего данный вирус способен реплицироваться только в присутствии HBV. Гепатит D встречается либо как сочетанная инфекция при остром гепатите В, либо как суперинфекция при достоверном хроническом гепатите В. Инфицированные гепатоциты содержат дельта-частицы, покрытые HBsAg. Распространенность фактора широко варьирует географически при наличии эндемичных районов в нескольких странах. Относительно высок риск для наркоманов, но среди гомосексуалистов этот вирус (в отличие от HBV) еще не распространен. Клинически инфекция HDV, как правило, проявляется необычно тяжелым острым гепатитом В (до 50% случаев молниеносного гепатита В связаны с сочетанной инфекцией вирусом гепатита D), "обострением" у хронических носителей HBV (суперинфекция) или относительно агрессивным течением хронического гепатита В.
Термин "гепатит ни А ни В" (NAN В) был предложен для обозначения инфекций, не связанных с вирусами А- или В-типа. Недавно идентифицирован специфический одноцепочечный РНК-вирус, подобный флавивирусам (вирус гепатита С, HCV), являющийся причиной большинства посттрансфузионных и спорадических случаев гепатита NAN В. В некоторых случаях такие инфекции, по-видимому, обусловлены другими агентами, пока еще не идентифицированными.
Антитела к HCV часто появляются в плазме крови через несколько месяцев после острой инфекции. Затем титры медленно уменьшаются, если только инфекция не становится хронической (что имеет место почти в половине случаев). Вирус HCV удалось идентифицировать в плазме с помощью весьма сложных методик; соответствующий антиген также выделен из цитоплазмы инфицированных гепатоцитов.
Гепатит ни А ни В может встречаться в виде спорадических случаев и в форме эпидемий. В последнем случае причиной, по-видимому, служит вирус, в порядке рабочей гипотезы называемый вирусом гепатита Е (HEV); его природа еще неясна.
"Острый вирусный гепатит, причины развития заболевания" - статья из раздела Гепатология









Основные ссылки
Вы здесь
Чтобы просмотреть текст книги нажмите на нужную главу в оглавлении
Вирус гепатита B (HBV) принадлежит к новому семейству ДНК вирусов Hepadnaviridae. К его особенностям относятся поразительный гепатотропизм и уникальный способ репликации с использованием механизма обратной транскрипции. Собранный вирион или частица Дейна состоит из кольцевой молекулы ДНК, защищенной ядерным капсидом/коровым антигеном (HBcAg). Внешняя оболочка вируса образована поверхностным антигеном (HBsAg). HBsAg также обнаруживается в сыворотке в виде неинфекционных сферических частиц или нитей. Малые компоненты HBV- нуклеакапсиды, HBe антиген (HBeAg) также можно обнаружить в крови во время репликативной фазы вируса.
HBV является широко распространенным по всему миру вирусом. В Москве, как и в целом по России, в последние годы отмечается рост заболеваемости парентеральными вирусными гепатитами [158].
Основные пути заражения: горизонтальный - половое и парентеральное заражение, и вертикальный - перинатальная передача от инфицированной матери плоду. Клинические последствия от заражения гепатитом B варьируют от полностью неразличимых (70% случаев) до острых гепатитов. Большинство пациентов полностью выздоравливают в течение 6 месяцев с начала заболевания. У небольшой доли инфицированного населения ( 1:1000) IgM антител на HBcAg появляются во время острой фазы HBV инфекции, совпадая с появлением IgG и ростом аминотрансфераз. Так как уровень анти-HBc IgM быстро уменьшается, высокий титр этих антител является свидетельством острой фазы гепатита B. Поэтому тестирование на анти-HBc IgM является полезным инструментом при диагностике острой HBV инфекции, позволяющим различать острые и хронические гепатиты B.
Во время активной фазы болезни в организме появляются как IgM, так и IgG антитела к вирусному коровому антигену. В то время как анти-HBc IgM быстро исчезает, анти-HBc IgG сохраняются годы. Поэтому анти-HBc IgG являются удобным индикатором для подтверждения предшествующих контактов с HBV. Более того, анти-HBc IgG является единственным маркером, который можно обнаружить во время так называемого серологического окна острого гепатита B, периода, когда анти-HBs антитела, указывающие на элиминацию вируса, еще не обнаруживаются, а специфические IgM уже исчезли (Рис. 11).
Рисунок 11. Относительная концентрации маркеров гепатита B при острой инфекции в зависимости от времени инфицирования
Антитела к HBsAg (анти-HBs) являются основными нейтрализующими HBV антителами, которые защищают против повторного инфицирования и сохраняются в течение всей жизни. Поэтому обнаружение анти-HBs служит индикатором выздоровления от гепатита B или успеха вакцинации с использованием HBsAg частиц. Концентрация антител ? 10 IU/L указывает на иммунитет к HBV.
В 1999-2001 гг. ВОЗ провела сравнительные испытания быстрых простых тестов 10 производителей (Determine HBsAg, DoubleCheck HBs Antigen, ImmunoComb II HBs Ag 90’, Serodia-HBs.PA, GLD Rapid HBsAg, Hepacard, AQ One HBsAg Test, Uni-Cold HBsAg, Genedia HBsAg, Hep B Stark-Pack) для обнаружения поверхностного антигена вирусного гепатита B [160]. При этом оценивалась не только чувствительность и специфичность, но и результаты, полученные на сероконверсионных и низкотитражных панелях. В качестве образцов сравнения, референс-тестов, выступали ELISA тест-системы MonolisaAgHBs Plus и Hepanostika HBsAg. Результаты испытаний представлены на рисунке. Столбцы диаграммы характеризуют количество выявленных положительных образцов низкотитражной и сероконверсионных панелей. Как видно из диаграммы (Рис.12), тесты ИммуноКомб продемонстрировали результаты, близкие или превосходящие результаты ИФА референс-тестов на сероконверсионных и низкотитражных панелях.
Рисунок 12. Сравнительная характеристика тестов при диагностике образцов сероконверсионных и низкотитражных панелей
Количество образцов низкотитражной панели, идентифицированных тестом ИммуноКомб как содержащие HBsAg, совпадает с количеством образцов, выявленных референс-тестом Hepanostika и на один образец меньше, чем референс-тестом Monolisa. Количество образцов сероконверсионной панели, диагностированых тест-системами ИммуноКомб, превышает показатель референс-тестов. Все остальные тесты отставали от референс-тестов в определении положительных образцов этих панелей. Как видно из данных, представленных на рисунке 13 ИммуноКомб HBsAg 90’ диагностирует HBsAg в среднем на 1 сутки раньше, чем референс-тест Monolisa Ag HBs Plus. Все остальные тесты обнаруживают HBsAg, отставая от референс-теста, по крайней мере, на 2 суток.
Рисунок 13. Образцы сероконверсионной панели, определяемые каждым из тестов относительно референс-теста Monolisa Ag HBs Plus (0 соответсует первому образцу, определяемому референс-тестом)
Эффективность быстрых простых тестов по выявлению поверхностного антигена вируса Гепатита В не уступает аналогичным характеристикам ELISA тестов. ИммуноКомб диагностирует HBsAg на более ранних стадиях и в более низких концентрациях, чем другие участвующие в испытаниях тесты.
Данный диагностический препарат позволяет диагностировать антиген различных субтипов в концентрации 0,25 нг/мл и проводить индивидуальное и групповое тестирование.
В таблице 24 представлены результаты международных испытаний БПТ ИммуноКомб HBS AG 90' [13].
Таблица 24. Качество тестов ИммуноКомб HBS AG 90'

Антитела к NS и core гепатита С – специфические иммуноглобулины, которые вырабатываются к структурным и неструктурным белкам вируса. Антигены вируса и антитела к нему обнаруживаются в рамках серологического исследования, которое называется иммуноферментным анализом (ИФА). Его выполняют при подозрении на гепатит С, во время противовирусной терапии и после нее. Снижение уровня антител (anti-HCV) отдельных классов указывает на полное уничтожение возбудителя инфекции.
Структурные и неструктурные белки гепатовируса
HCV – вирус рода Hepacivirus из семейства Flaviviridae, провоцирующий инфекционное воспаление печени. Когда антиген (чужеродное вещество) проникает в организм, возникает иммунный ответ, который характеризуется выработкой антител. При заражении гепатитом С специфические иммуноглобулины синтезируются к разным частям вируса:
- Ядро – содержит структурный белок core. При инфицировании он встраивается в геном клеток печени. В результате они превращаются в фабрику по производству дочерних вирионов. В 1 зараженной клетке ежедневно синтезируется от 30 до 50 вирусов.
- Оболочка – нуклеотидные протеины типа Е1 и Е2. Участвуют во взаимодействии возбудителя с иммунными клетками крови. Они помогают вирусу гепатита С (ВГС) защищаться от Т-лимфоцитов, гранулоцитов, фагоцитов и других клеток, борющихся с антигенами.
- Фрагменты генома – неструктурные белки типа NS2, NS3, NS4, NS5. Выполняют регуляторные функции, участвуют в репликации, то есть образовании копий вируса.
Структурные и неструктурные белки ВГС – антигены, к которым иммунная система вырабатывает антитела. Поэтому анализ на anti-HCV назначается всем людям с подозрением на гепатит С.
В рамках иммуноферментного анализа определяют только три неструктурных белка – NS3, NS4 и NS5. В действительности их больше и каждый выполняет определенные функции. Одни участвуют в расщеплении ферментов и белков, а другие – в сборке скопированного генетического материала. Учеными обнаружено 11 неструктурных белков, но функции некоторых из них до сих пор неизвестны.
Как проводят анализ на антигены и антитела к вирусу гепатита
Анализ на антитела к ВГС (anti HCV) – молекулярно-биологическое исследование, направленное на выявление иммуноглобулинов к гепатиту С. В его основе лежит реакция антиген-антитело, при которой формируются устойчивые комплексы из белков возбудителя и плазмы крови.
Чтобы обнаружить anti-HCV, во время анализа используют специальные ферменты. Они выполняют функцию меток, позволяющих регистрировать соответствующие сигналы. Главное преимущество серологического анализа – высокая специфичность. Полученные результаты дают информацию о:
- типе возбудителя;
- стадии заболевания;
- форме гепатита (острый или хронический).
Для анализа берут венозную кровь из локтевой вены. Подготовка к исследованию не занимает много времени. Пациентам рекомендуют выполнять процедуру натощак в утренние часы, не курить за полчаса до сдачи крови.
Для чего назначается анализ на anti-HCV:
- первичная диагностика HCV-инфекции;
- дифференциальная диагностика гепатитов;
- выявление ранее перенесенного заболевания.
В случае раннего заражения (период до 4 недель) возрастает риск ложноотрицательного результата анализа. Поэтому даже при отсутствии в крови иммуноглобулинов дополнительно выполняется ПЦР на гепатит С. Если РНК возбудителя обнаруживается, диагноз подтверждают.
Анализ на anti-HCV выполняется при:
- обследовании лиц из группы риска (хирургов, прооперированных пациентов, реципиентов крови);
- признаках инфекционного поражения печени;
- повышенном содержании печеночных ферментов;
- планировании беременности;
- мониторинге эффективности антивирусной терапии.
Сразу после забора крови лаборант подписывает образец и отправляет его в лабораторию для анализа. На исследование уходит не более 2-3 рабочих дней.
Расшифровка результатов
Если в крови обнаруживают иммуноглобулины к ВГС, это еще не свидетельствует о заражении. По статистике, до 30% пациентов излечиваются самостоятельно. Все они даже не догадываются, что переболели опасным заболеванием, исходом которого нередко становится фиброз, цирроз и гепатоцеллюлярная карцинома.
Виды антител, которые выявляются при иммуноферментном анализе:
- Anti-HCV core IgM – иммуноглобулины, которые синтезируются к ядру возбудителя. Они начинают циркулировать в крови раньше других антител. При хронической форме гепатита их концентрация сильно уменьшается.
- Anti-HCV NS – антитела, синтезированные к неструктурным белкам ВГС. Если при анализе выявляются anti-NS3, это свидетельствует об острой форме гепатита. Белковые комплексы anti-NS4 и anti-NS5 обнаруживаются преимущественно при переходе гепатита в вялотекущую форму.
- Anti-HCV total – суммарные антитела, которые возникают к возбудителю. Если они выявляются во время анализа, это значит, что человек либо заражен гепатитом, либо перенес инфекцию.
Во время диагностики вирусной болезни учитываются результаты качественной ПЦР. При выявлении HCV RNA, то есть РНК возбудителя, диагноз подтверждается.
Пример иммуноферментного анализа с расшифровкой данных
| Данные анализа | Интерпретация данных |
| HCV IgG core 16.40 (положительно) | В плазме присутствуют высокие титры IgG (NS) и IgG (RNA). РНК предстоит выявить, так как велика вероятность заражения гепатитом |
| anti-HCV IgG NS3 14.20 (положительно) | |
| anti-HCV IgG NS4 16.40 (положительно) | |
| anti-HCV IgG NS5 0.34 (отрицательно) | |
| anti-HCV IgG NS3 0.08 (отрицательно) | Если core положительно, а NS –отрицательно, результат считается сомнительным. Для подтверждения диагноза прибегают к дополнительному анализу – реал-тайм ПЦР |
| anti-HCV IgG NS4 8.30 (положительно) | |
| anti-HCV IgG NS5 0.07 (отрицательно) | |
| anti-HCV IgG core 0.15 (отрицательно) |
Во время иммуноферментного анализа обязательно определяют позитивность пробы на структурный белок ВГС – КП (core-Ag). Коэффициент позитивности применяется для оценки уровня иммуноглобулинов в крови. В мировой практике он измеряется в МЕ/мл. Результаты анализа считаются положительными, если этот коэффициент превышает 1. Иными словами, чем выше КП, тем больше содержание иммуноглобулинов в образце.
Если данные иммуноферментного анализа указывают на инфицирование, выполняют ПЦ.
После подтверждения диагноза проводят дополнительные инструментально-лабораторные исследования, посредством которых определяются:
- структурные изменения – фиброз, цирроз печени, печеночно-клеточный рак;
- вирусная нагрузка – концентрация РНК возбудителя в 1 мл крови;
- активность воспаления – стадия гепатита С;
- генотип ВГС – тип и подтип возбудителя.
С учетом результатов анализов составляют схему противовирусной терапии. При курсовом приеме ингибиторов неструктурных белков ВГС – Софосбувира, Нарлапревира, Ледипасвира Омбитасвира, Даклатасвира – выздоровления достигают 96-100% пациентов. Поэтому если вы подозреваете гепатит, запишитесь на прием к врачу.
Среди всего населения планеты у 2 млрд человек в крови выявлен поверхностный антиген вируса гепатита В. Каждый год регистрируются десятки тысяч новых случаев заражения. Поэтому для профилактики распространения инфекции серологический скрининг назначают всем обратившимся за медицинской помощью и группе лиц, находящихся в зоне риска.
О чем я узнаю? Содержание статьи.
Что такое антигены вируса гепатита В?
Иммунитет здорового человека активизируется при появлении в организме чужеродных агентов. В ответ на антигенные свойства возбудителей болезней вырабатываются защитные антитела. Причиной инфицирования HBV-инфекцией становится проникновение в кровь инфицирующей дозы ДНК-вируса.
Вирусный штамм обладает чрезвычайно высокой вирулентностью, инфицирующая доза содержится в 0,0000001 мл сыворотки.
От начала инфицирования в серологических тестах можно обнаружить разные типы антигенов и соответствующих им антител, по которым судят о стадии инфекционного процесса. В составе вирусной частицы ВГВ различают 4 типа антегенов:
- поверхностный HBSAg находится среди молекул суперкапсида (внешней фосфолипидной мембраны вириона);
- сердцевинный HBCoreAg содержится в ядре (core);
- HBeAg совместно с геномом включен во внутреннюю ядерную часть (нуклеокапсид). Положительное значение в анализе свидетельствует об активной репликации вирусного ДНК.
- HBxAg до конца не изучен. В начале инфекции обнаружить нельзя, появляется при хронизации процесса. По мнению ученых влияет на развитие первичного рака печени — гепатоцеллюлярной карциномы.
Поверхностный антиген вируса гепатита В отвечает за проникновение возбудителя в гепатоциты. Это первый серологический маркер, который появляется в крови. Достигает максимального титра к четвертой недели и циркулирует в сыворотке до 6 месяцев.
Из-за постоянной генетической изменчивости HBSAg возбудителю свойственна неоднородность в разных регионах планеты. Мутации S-гена приводят к формированию генотипов инфекции, на сегодня их зарегистрировано восемь. В России до 93% случаев инфицирования числятся с генотипом D.
Мутационные штаммы являются причиной неэффективности вакцинации против ВГВ.
Тестирование сыворотки для выявления HBeAg проводится только в случае положительного поверхностного HBSAg для подтверждения диагноза. Наличие в крови антигена доказывает инфицированность человека. Подтверждается почти у 95% зараженных лиц в начале желтушного периода. При благоприятном течении болезни АГ исчезает при прогрессировании симптомов и к нему появляются АТ.
Обнаружить HBCAg при проведении ИФА нельзя, так как он локализуется внутри гепатоцитов. Подтвердить его можно только при биопсии печеночной ткани, что не оправдано из-за сложности инвазивной процедуры. Наиболее информативны антитела: anti-HBCAg IgM и IgG.
Среди четырех антигенов именно HBCAg обладает максимальной иммуногенностью, как чужеродный агент, он первым активизирует иммунитет на ответную реакцию.
Антитела к поверхностному антигену вируса гепатита В
В ответ на появление в крови поверхностного антигена, указывающего на положительный гепатит В, иммунная система начинает продуцировать anti-HBS двух видов:
Выявление АТ к поверхностному антигену помогает в составлении прогноза болезни:
- благоприятный прогностический признак отмечается при появлении anti-HBS на фоне клинических улучшений;
- неблагоприятный формируется при исчезновении anti-HBS в преджелтушном и желтушном периоде. В таких случаях быстро развивается паренхиматозная дистрофия.
Для формирования иммунитета к болезни вакцинацию проводят рекомбинантным HBSAg. В ответ на введение количество антител anti-HBS нарастает и колеблется на уровне 10 МЕ/мл в течение 10 лет.

Антигены вирусы гепатита В и взаимодействие с ними антител
Антитела к ядерному антигену вируса гепатита В
В серологических анализах на гепатит В особая диагностическая ценность принадлежит антителам к вирусу, так как самого HBCORAg в крови нет. Иммуноглобулины класса М (anti-HBCOR IgM) присутствуют в плазме до 18 месяцев.
Доноров тестируют на наличие anti-HBCOR (total). Для выбраковки донорского биоматериала достаточно присутствия суммарного количества иммуноглобулинов без учета их класса.
Маркер anti-HBCOR IgG у лиц переболевших HBV, носителей HBSAg и больных с хронизацией процесса присутствует в крови пожизненно. Поэтому для диагноста это более информативный показатель, чем anti-HBS.
Поверхностный антиген вируса гепатита В положительный: что это значит?
Тестирование на выявление HBSAg назначают отдельно или в комплексе с анализами на другие маркеры инфекции. Поверхностный антиген сохраняется в крови на протяжении начального периода заболевания. Наибольшее значение отмечается за 1—2 недели до окончания инкубационного периода.
Появление положительного результата свидетельствует о:
Всегда существует вероятность ложноположительных результатов к вирусу гепатита, при выявлении поверхностного АГ исказить ответ может:
- некачественная или нечувствительная тест-система;
- онкология;
- аутоиммунные заболевания и другие инфекции.
Что делать при обнаружении антител к антигенам вируса гепатита Б?
Точный диагноз HBV-инфекции по одному положительному ИФА не устанавливают. Врач-инфекционист дополнительно назначает:
- повторную серодиагностику;
- ПЦР для выявления генетического материала;
- биохимический анализ;
- УЗИ печени.
Носителям HBV-инфекции сдавать биоматериалы для донорства запрещено.
Своевременная диагностика факта инфицирования улучшает прогноз для больного, так как клинические формы многообразны: от бессимптомного течения до быстропрогрессирующего цирроза.
Массовые обследования людей на выявление поверхностного антигена HBV необходимы, так как только 15% случаев инфицирования заканчиваются выздоровлением.
При хронизации процесса современные препараты поддерживают качество жизни больного человека, но не исключается риск возникновения фиброзных изменений в печени, печеночной недостаточности и гепатокарциномы.
Читайте также:


