Морфологические исследования при туберкулезе
Цитологические и гистологические методы играют важную, а нередко и решающую роль в распознавании заболеваний органов дыхания. Большое значение имеет исследование клеточного состава мокроты. В нативных и специально окрашенных препаратах находят лейкоциты, эритроциты, клетки плоского и цилиндрического эпителия, альвеолярные макрофаги, пылевые, эпителиоидные, гигантские и опухолевые клетки, кристаллы холестерина и Шарко—Лейдена, неизмененные, обызвествленные коралловидные волокна, микобактерии туберкулеза, неспецифическую флору, друзы актиномицетов, аспергиллы, дрожжевые грибы, сферулы кокцидиоидногэ микоза и т. д.
Следует иметь в виду, что обызвествленные очаги в легких определяются иногда при хроническом абсцессе легкого и гистоплазмозе. Клетки метаплазированного эпителия бронхов со значительной атипией, весьма сходные с элементами злокачественного новообразования, встречаются при хронической пневмонии или бронхите.
Эпителиоидные и гигантские клетки Пирогова— Лангханса можно обнаружить не только при туберкулезе, но и при саркоидозе. Вот почему результаты цитологического анализа мокроты приобретают важное диагностическое значение, если они подтверждаются другими методами исследования.
Частота обнаружения тех или иных клеточных элементов в мокроте или в смывах из бронхов зависит от фазы и динамики процесса, локализации патологического образования в легких, например, при центральном или периферическом раке. Результативность цитологического диагноза, указывал в 1961 г. Umiker, обратно пропорциональна расстоянию опухоли от бифуркации трахеи. Этими факторами следует объяснить различную частоту выявления клеток опухоли при раке легких: в 70—87,6% по данным А. Я. Альтгаузена (1962), Н. Н. Шиллер-Волковой и соавт. (1964), в 24,6—38—45% по наблюдениям Р. Д. Блиновой (1972).
Тот же метод исследования оправдывает себя в диагностике периферических лимфаденитов. При туберкулезе характер обнаруживаемых тканевых изменений зависит от фазы процесса (Е. Д. Тимашева, 1953; М. Г. Абрамов, 1974). В I гиперпластической стадии определяется лишь гиперплазия лимфаденоидной ткани, во II стадии (гранулематозной) находят элементы туберкулезного бугорка, в III — массивный казеозный некроз, в IV — гной, в V (фиброзной) — соединительнотканные волокна, мелкие клеточные элементы.
При раке в пунктатах из лимфатических узлов обнаруживают клетки опухоли, при саркоидозе — эпителиоидные и гигантские клетки без признаков творожистого некроза, при лимфогранулематозе — клетки Березовского—Штернберга и большое число эозинофилов, при лимфолейкозе— картину мономорфной гиперплазии лимфоидной ткани и т. д.
Те или иные патологические изменения удается обнаружить при цитологическом исследовании пунктатов печени, селезенки, костного мозга. Пользуясь этим методом, Olderhauser и соавт. выявили туберкулезные бугорки в печени у 25,3 % больных диссеминированным туберкулезом и у 7,3% — при других его формах. Почти в 60% случаев при пункции печени находят гранулемы, характерные для саркоидоза, особенно при I его стадии (Scadding, 1967, и др.). Сочетая этот способ исследования с пери-тонеоскопией, Tachibana и соавт. (1971) выявили такие тканевые изменения в печени у 70%, a Liehr (1971) — у 90% больных саркоидозом.
Известное значение в дифференциальной диагностике приобретает цитологическое изучение материала, полученного при трансторакальной пункции легкого. Этот метод исследования, который впервые использовал Leyden .еще в 1883 г., в последнее время получил более широкое применение. В пунктате, помимо альвеолярного и бронхиального эпителия, можно обнаружить при туберкулезе эпителиоидные и гигантские клетки и элементы творожистого некроза, при саркоидозе — эпителиоидные и гигантские клетки, при раке и других злокачественных новообразованиях — клетки опухоли и т. д.
Sabow и соавт. при изучении пунктатов установили диагноз рака легкого у 117 больных, между тем как при бронхоскопии — у 81, а при цитологическом исследовании мокроты — лишь у 59 из них. По данным Р. Д. Блиновой (1972), диагноз рака удается верифицировать при пункции легкого у 91,9% больных, по наблюдениям И. С. Мечевой (1973), Н. А. Шмелева (1959) и др. — у 57—80%, а по материалам М. Г. Виннера и М. Л. Шулутко (1971) — у 50% больных. Менее результативна диагностическая пункция при аденоме, гамартохондроме и других доброкачественных образованиях легких. Однако Otto и Frick (1971) на обширном материале (1000 диагностических пункций легкого, произведенных на протяжении 1967—1971 гг. у больных со злокачественными и доброкачественными новообразованиями, туберкулезом, микозами, пневмокониозом, хроническим воспалительным процессом и т. д.) удалось подтвердить диагноз в среднем в 3/4 случаев.
Пункцию легкого целесообразно производить при периферической локализации процесса и достаточной величине патологического образования в легком. Не рекомендуется пользоваться этим методом при подозрении на асбсцесс или гангрену, кисту или эхинококкоз ввиду возможности инфицирования плевральной полости, а также при аневризме легочных сосудов. Его нельзя применять у больных с геморрагическим диатезом, при легочно-сердечной недостаточности у пожилых людей.

Морфологические изменения при туберкулезе
Морфологические изменения при туберкулезе многообразны и зависят от формы, фазы, локализации и распространенности процесса. У каждого больного туберкулезный процесс, как это видно при рентгенологическом исследовании, отражающем морфологию, своеобразен и почти неповторим. Однако имеются общие черты, характерные для туберкулезного заболевания в целом.
Это специфический воспалительный процесс, в сочетании с параспецифическими реакциями, несущий в себе элементы любого воспаления: альтерацию, экссудацию и пролиферацию. Возможно различное их сочетание в зоне туберкулезного процесса в зависимости от массивности и вирулентности инфекции, пути её распространения и реакции организма.
Характер морфологических изменений зависит от особенностей иммунореактивности, возникающей при воздействии токсических продуктов жизнедеятельности микобактерий на макроорганизм. Вначале в участке воспаления развивается реакция, не имеющая типичных для туберкулеза признаков. В ней в различной степени выражены альтеративные и экссудативные явления, нарушается микроциркуляция. Затем развиваются специфические изменения.
Типичным морфологическим элементом является развитие туберкулезного бугорка (гранулемы), в центре которого имеется участок творожистого (казеозного) некроза, окруженный эпителиоидными клетками с наличием гигантских многоядерных клеток Пирогова-Лангханса, вокруг которых имеется вал из лимфоидных клеток. Казеозный некроз – это плотные некротические массы, напоминающие высохший крошащийся творог после нескольких дней пребывания в холодильнике или на воздухе.
Эпителиоидные клетки образуются из мононуклеаров и макрофагов, которые накапливаются в зоне туберкулезного воспаления на начальном этапе воспалительной реакции. Гигантские клетки Пирогова-Лангханса могут образоваться из эпителиоидных клеток при их пролиферации (деление ядра при сохранении цитоплазмы), а также в результате слияния эпителиоидных клеток. Они способны к фагоцитозу и могут содержать МБТ, характеризуются высокой ферментативной активностью.
Цитоплазма гигантских клеток содержит большое количество ядер, множество митохондрий, лизосом и др. элементов. В зависимости от вирулентности инфекции и резистентности организма в туберкулезном бугорке может преобладать экссудативная, лимфоцитарная, казеозно-некротическая реакция. Бугорки могут быть типично эпителиоидно-гигантоклеточными. Такая гранулематозная реакция в целом – это защитная реакция, ограничивающая распространение МБТ.
Участки казеозного некроза обычно окружаются зоной экссудативного воспаления, называемого перифокальным (вокруг некротического фокуса или скопления бугорков). Обычно оно представляет собой пропитывание тканей серозным, серозно-фибринозным экссудатом, в котором содержатся клетки – лимфоидные, моноцитарные, гистиоцитарные и т. п. Экссудат может изливаться и в полости (плевральную, брюшную, перикарда) при поражении соответствующих оболочек. Тогда развивается туберкулезный плеврит, перикардит, перитонит, полисерозит.
При остром альтеративно-экссудативном процессе преобладают значительные участки творожистого (казеозного) некроза. Развитие обширных зон казеозного некроза характерно для остропрогрессирующих форм туберкулеза и особенно для казеозной пневмонии.
Свежий туберкулезный очаг (при очаговом туберкулезе), а также инфильтрат представляют собой сочетание участка творожистого некроза, перифокального воспаления и наличия туберкулезных гранулем. В казеозные массы проникают лейкоциты, выделяющие ферменты, которые расплавляют казеоз. Эти массы отторгаются, на их месте возникает дефект, который называется каверной в паренхиматозном органе (легкое, почка и др.) или язвой – в полом (бронх, кишка и др.).
Возможно при туберкулезе развитие гематогенной или лимфогенной диссеминации. При этом развиваются диффузные васкулиты, очаги с преимущественно продуктивной воспалительной реакцией. Заживление туберкулезных изменений связано с рассасыванием и пролиферативными процессами: рубцеванием, уплотнением очага, его инкапсулированием, гиалинизацией, в ряде случаев – кальцинацией, т.е. обызвествлением. В капсуле, окружающий туберкулезный очаг, могут находиться скопления лимфоцитов.
При заживлении в грануляционной ткани обнаруживаются фибробласты, формирующие коллагеновые волокна. В подобных очагах иногда обнаруживаются измененные формы МБТ, в частности, L-формы, что свидетельствует об их значении при возможной реактивации процесса. Полное их рассасывание наблюдается довольно редко. Чаще очаг подвергается фиброзной трансформации, т. е. прорастанию соединительной тканью с образованием рубцов, перифокальное воспаление при этом рассасывается. Возможно также врастание грануляций в некротические массы, т. е. их организация.
Встречается более массивное развитие соединительной ткани в органе, чаще в легком – может быть ограниченный фиброз; при сморщивании участков легкого – сегментов, долей или всего органа целиком – цирроз; возможен диффузный пневмосклероз с разрастанием соединительной ткани в интерстиции легкого, например, после диссеминированного или милиарного туберкулеза. При этом возникает смещение органов средостения, нарушение нормальной архитектоники сосудов, что ведет и к функциональным нарушениям. Все это – пролиферативные процессы. Следует помнить, что заживление при туберкулезе происходит медленно.
Под влиянием длительно существующей туберкулезной интоксикации в различных органах и тканях больного развиваются неспецифические дистрофические изменения, например, в печени, миокарде, а также амилоидоз почек и других органов.
Туберкулез отличается большим разнообразием клинико-морфологических проявлений. Главная роль в их изучении принадлежит отечественным патоморфологам: А.И.Струкову, А.И.Абрикосову, В.Г.Штефко, В.В.Серову, И.П.Соловьёвой и другим.
Выделяют три основных клинико-морфологических формы туберкулеза:
I. Первичный туберкулез
Первичный туберкулез характеризуется следующими особенностями: 1. Развитием заболевания в период инфицирования, то есть при первой встрече с инфекцией.
2. Сенсибилизацией и аллергией с развитием реакций гиперчувствительности немедленного типа;
3. Преобладанием изменений эксудативно-некротического характера;
4. Наклонностью к гематогенной и лимфогенной генерализации;
5. Параспецифическими реакциями в виде васкулитов, артритов, серозитов. Путь заражения, как правило, аэрогенный, редко алиментарный. Заболевание развивается в детском, подрастковом и молодом возрасте.
Патанатомия. Морфологическим выражением первичного туберкулеза является туберкулезный комплекс, который состоит из трех компонентов: первичного аффекта, туберкулезного воспаления отводящих лимфатических сосудов (лимфангита) и туберкулезного воспаления регионарных лимфатических узлов (лимфаденита).
Первичный аффект в легких возникает чаще в III, VIII, IX, X сегментах правого легкого. Размеры первичного аффекта различны: иногда только альвеолит, чаще ацинус или долька, реже вся доля и представлен очагом казеозной пневмонии. В плевре наблюдается серознофибринозный или фибринозный плеврит. В отводящих лимфатических сосудах наблюдается лимфостаз, а в периваскулярной ткани по ходу сосудов туберкулезные бугорки, которые образуют дорожку к корню легкого. Это носит название - туберкулезный лимфангит. Туберкулезный лимфаденит (см. Рис. 8) возникает в бронхопульмональных, бронхиальных и бифуркационных лимфатических узлах. Лимфатические узлы увеличиваются в несколько раз, в них быстро наступает тотальный или субтотальный казеозный некроз. При локализации входных ворот инфекции в кишечнике, в нем также развивается первичный туберкулезный комплекс из трех компонентов. Первичный очаг имеет вид язвы в слизистой оболочке кишки, которую дополняют лимфангит и регионарный (брыжеечный) казеозный лимфаденит. Если первичный аффект расположен в миндалине, развивается лимфангит и казеозный некроз лимфатических узлов шеи. Подобные проявления первичного туберкулеза наблюдаются в коже. Дальнейшее течение первичного туберкулеза предполагает три варианта:
1) Заживление очагов первичного комплекса (очаг Гона – см. Рис. 6 и7)
2) Прогрессирование с генерализацией процесса
· Рост первичного аффекта
· Смешанная форма прогрессирования
3) Хроническое течение
· Первичная легочная чахотка
Заживление первичного комплекса начинается в первичном легочном очаге со смены экссудативной тканевой реакции на продуктивную. Так вокруг очага казеозной пневмонии появляются фиброзная капсула и туберкулезные гранулемы. Казеозные массы уплотняются и обызвествляются (то есть происходит петрификация). Потом в них могут образоваться костные балки – оссификация. Подвергшийся инкапсуляции, петрификации и оссификации первичный очаг называют очагом Гона, по имени описавшего его чешского патолога. В связи с большим объемом поражения заживление в лимфатических узлах протекает медленнее, но также завершается петрификацией и оссификацией. Очаги Гона обнаруживаются на вскрытии у 25% людей в возрасте до 15 лет, от 20 до 30 лет – у 45%, после 40 лет – почти у всех. Это означает, что инфицирование туберкулезной микобактерией не всегда приводит к заболеванию с клиническими проявлениями. Чаще оно способствует становлению нестерильного иммунитета и предупреждению нового заражения. При туберкулезе кишечника после заживления первичной язвы образуется небольшой рубец, в лимфатических узлах появляются петрификаты и позже – оссификация. Прогрессирование первичного туберкулеза с генерализацией процесса имеет четыре варианта.
При первичном туберкулезе данный тип прогрессирования связан с попаданием самих возбудителей (микобактерий) в кровь из первичного очага или из казеозноизмененных лимфатических узлов. В результате диссеминации микобактерий в различных органах образуются очаги-отсевы размером от милиарных (просовидных) до крупных, величиной с горошину и более. В связи с этим различают милиарную и крупноочаговую формы гематогенной генерализации. Очаги отсева, спустя годы после затихания первичной инфекции, служат основой для гематогенного туберкулеза.
Лимфогенная форма прогрессирования первичного туберкулеза проявляется в увеличении объема поражения лимфатических узлов (бронхиальных, бифуркационных, околотрахеальных, шейных, мезентериальных и др.). Лимфатические узлы, в связи с прогрессированием казеозного некроза, увеличиваются, образуют конгломераты (пакеты), напоминающие опухоль, которые могут сдавить бронхи и сосуды. При разрушении стенки бронха развивается бронхиальный свищ.
Смешанная форма прогрессирования развивается в ослабленном организме. Её отличают рост первичного аффекта, выраженный казеозный бронхоаденит и многочисленные туберкулезные высыпания в легких и других органах.
Смерть больного при первичном туберкулезе может наступить от общей генерализации процесса, приводящей нередко к туберкулезному менингиту.
Хроническое течение первичного туберкулеза характеризуется чередованием обострений и ремиссий. Оно протекает на фоне сенсибилизация организма с развитием в тканях и органах параспецифических изменений (Струков А.И., 1948), к которым относятся: пролиферация лимфоцитов и макрофагов, гиперпластические изменения в кроветворной ткани; фибриноидные изменения соединительной ткани и стенок артериол; амилоидоз; воспаление суставов, напоминающее ревматизм (ревматизм Понсе). В ряде случаев хронически текущий первичный туберкулез сопровождается формированием первичной легочной каверны (первичная легочная чахотка). Эта каверна имеет три слоя: внутренний слой – некротические массы, средний – зона специфического продуктивного воспаленя (эпителиодные клетки, гигансткие клетки Пирогова-Лангханса, лимфоциты), наружный слой – грубоволокнистая соединительная ткань (см. Рис. 9).
II . Гематогенный туберкулез
Гематогенный туберкулез развивается через значительный срок после перенесенной первичной инфекции при обострении оставшихся очагов отсевов под влиянием неблагоприятных факторов, к которым относят:
1) Плохая экология
2) Снижения иммунитета организма, в связи с неполноценным питанием
3) Неудовлетворительные условия труда и быта
5) Алкоголь и т.д.
Необходим помнить, что, несмотря на клиническое или рентгенологическое выздоровление, с микробиологических позиций выздоровления от туберкулеза не происходит. Поэтому гематогенный туберкулез возникает после первичного туберкулеза. Источником обсеменения при гематогенном туберкулезе является не вполне заживший очаг после первичного туберкулеза в лимфатическом узле или других органах, костях, которые образовались в результате гематогенной генерализации при первичном туберкулезе. Особенностями гематогенного туберкулеза являются: преобладание продуктивной тканевой реакции (гранулемы); гематогенная генерализация, которая ведет к поражению различных органов и тканей.
Различают три разновидности гематогенного туберкулеза.
1) Генерализованный гематогенный туберкулез
2) Гематогенный туберкулез с преимущественным поражением легких
· Острый милиарный туберкулез
· Хронический милиарный туберкулез
· Хронический крупноочаговый туберкулез
3) Гематогенный туберкулез с преимущественными внелегочными поражениями
Генерализованный гематогенный туберкулез является наиболее тяжелой формой заболевания. Он сопровождается распространенным развитием во многих органах туберкулезных бугорков и очагов. В зависимости от их размеров (просовидные или до 1 см в диаметре) различают острый общий милиарный туберкулез и острый общий крупноочаговый туберкулез, который встречается у ослабленных больных. Если в очагах явно преобладает казеозный некроз, а пролиферативная и экссудативная реакции выражены слабо, процесс называется острейшим туберкулезным сепсисом.
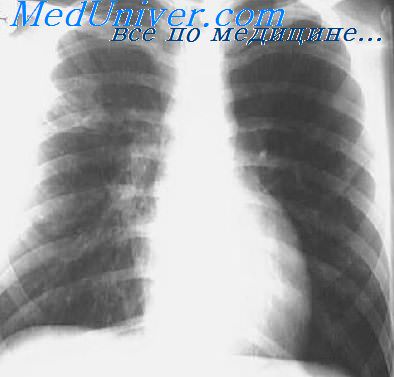
Гематогенный туберкулез с преимущественным поражением легких также может быть милиарным (см. Рис. 4) или крупноочаговым. При этом в других органах очаги-отсевы отсутствуют или единичны. Острый милиарный туберкулез характеризуется развитием густо рассеянных просовидных очагов во всех отделах обоих легких. Нередко он приводит к менингиту. Хронический милиарный туберкулез отличается рубцеванием бугорков и стойкой эмфиземой легких, что приводит к формированию легочного сердца. Хронический крупноочаговый туберкулез легких протекает с развитием сетчатого пневмосклероза, также осложняется эмфиземой и легочным сердцем.
Гематогенный туберкулез с преимущественными внелегочными поражениями развивается из очагов-отсевов, занесенных в какой-либо орган гематогенным путем при первичном туберкулезе. Туберкулез костей и суставов встречается чаще у детей и развивается после туберкулезного остеомиелита. Частой локализацией являются тела позвонков (туберкулезный спондилит – см. Рим. 10), тазобедренный (туберкулезный коксит) и коленный (туберкулезный гонит) суставы. Процесс может привести к разрушению кости, образованию секвестров, деформации суставов с формированием горба и т.д. Туберкулез мочеполовой системы подразумевает поражение почек, мочевого пузыря, простаты, придатка яичка, эндометрия, маточный труб, яичников. Туберкулез почек обычно бывает односторонним. Процесс начинается в сосочках пирамид с образования полостей – каверн, содержащих казеозные массы. Вокруг каверн развивается хроническое интерстициальное воспаление. При гематогенном туберкулезе поражаются другие органы: печень, эндокринные железы, центральная нервная система, а также серозные оболочки.
II . Вторичный туберкулез
Вторичный, реинфекционный, туберкулез развивается в организме взрослого человека, перенесшего ранее первичную инфекцию, которая не оградила от возможности повторного заболевания. Сейчас в возникновении вторичного туберкулеза отдают предпочтение теории эндогенного заражения, то есть из первичных очагов. Для вторичного туберкулеза характерны:
· избирательное поражение легких;
· контактное и интраканаликулярное распространение (по бронхам, желудочно-кишечному тракту);
· различные клинико-морфологические формы, которые являются фазами туберкулезного процесса.
При вторичном туберкулезе инфекция распространяется преимущественно интраканаликулярным или контактным путем, по бронхам, желудочно-кишечному тракту. Гематогенная генерализация возможна также и в терминальном периоде болезни.
Патоанатомия. Выделено 8 форм (фаз) вторичного туберкулеза:
· острый кавернозный туберкулез;
Острый очаговый туберкулез начинается со специфического воспаления внутридолькового бронха. В прилежащей легочной паренхиме развивается ацинозная или дольковая казеозная бронхопневмония. Вокруг очага воспаления формируется вал эпителиоидных, лимфоидных и гигантских клеток Пирогова-Лангханса. Такие очаги получили название очагов реинфекта Абрикосова. Они встречаются в количестве 1-2, располагаются в I и II сегментах правого, или реже левого легкого. В большинстве случаев процесс самостоятельно затихает, экссудативная тканевая реакция сменяется продуктивной тканевой реакцией, очаги казеозного некроза инкапсулируются и петрифицируются.
Фиброзно-очаговый туберкулез (см. Рис. 11) развивается после заживления очагов Абрикосова, на месте которых появляются крупные инкапсулированные и частично петрифицированные очаги, описанные немецкими учеными Л. Ашоффом и Х. Пулем (ашофф-пулевские очаги). Процесс остается односторонним, не выходит за пределы I и II сегментов. При этой форме сохраняется склонность к обострению туберкулеза.
Инфильтративный туберкулез является результатом прогрессирования острого очагового или обострения фиброзно-очагового туберкулеза. Его отличает явное преобладание перифокальных экссудативных изменений над казеозными. Очаги воспаления занимают дольку и даже сегмент и долю. Такой очаг называют очагом-инфильтратом Ассманна-Редекера (по имени ученых, впервые описавших его рентгенологическую картину). При благоприятном исходе перифокальное воспаление редуцируется, и процесс переходит в фиброзно-очаговую форму туберкулеза или туберкулему.
Туберкулема – округлый инкапсулированный очаг творожистого некроза диаметром более 1 см. Туберкулема расположена в I или II сегменте, чаще справа, достигает 5 см в диаметре. Может быть единичной или в виде конгломерата из нескольких очагов. При рентгенологическом обследовании её следует дифференцировать с опухолью (рак легкого или метастаз).
Казеозная пневмония чаще развивается в результате прогрессирования инфильтративного туберкулеза. Казеознопневмонические очаги занимают ацинус, дольку, сегмент или всю долю. Казеозная пневмония (см. Рис. 12) клинически протекает крайне тяжело, может завершать терминальный период любой формы туберкулеза. Часть легкого, вовлеченная в казеозную пневмонию, увеличена, уплотнена, на разрезе желто-серого цвета, с фибринозными наложениями на плевре.
Кавернозный туберкулез характеризуется образованием полости распада, а затем каверны на месте очага-инфильтрата или туберкулемы. Полость распада появляется при гнойном расплавлении казеозных масс, которые вместе с мокротой дренируются наружу через бронх. Это сопровождается выделением микобактерий в окружающую среду и создает условия для бронхогенного инфицирования легких. Обычно каверна локализуется в I или II сегменте, имеет овальную или округлую форму, диаметром 2-5 см. Стенка каверны изнутри покрыта казеозными массами, снаружи представлена уплотненной в результате воспаления легочной тканью.
Фиброзно-кавернозный туберкулез (см. Рис.9) представляет собой хроническую форму кавернозного туберкулеза. Стенка каверны утолщена, уплотнена, с неровной поверхностью, имеет три слоя: внутренний – пиогенный (некротический), богатый распадающимися лейкоцитами; средний – слой туберкулезной грануляционной ткани; наружный – соединительнотканный. Каверна имеет неправильную форму, может быть многокамерной и занимать несколько сегментов, выходя за пределы одной доли. Вокруг каверны определяются очаги ателектаза, пневмосклероза, эмфиземы, бронхоэктазы. При обострении заболевания появляются участки инфильтрации и казеоза. Поскольку процесс распространяется сверху вниз, более старые изменения наблюдаются в верхних отделах, а свежие – в нижних легких.
Цирротический туберкулез является следствием фибрознокавернозного туберкулеза, с массивным пневмосклерозом, рубцовыми изменениями, плевральными спайками, деформацией легких. Осложнения чаще развиваются при кавернозных формах вторичного туберкулеза. В их число входят:
· кровотечение из каверны;
· прорыв каверны в плевральную полость с развитием пневмоторакса и эмпиемы плевры;
· амилоидоз (при фиброзно-кавернозном туберкулезе);
· в посттуберкулезных рубцах возможно развитие рака легкого.
Причинами смерти больных легочным туберкулезом, кроме перечисленных осложнений, могут быть прогрессирование туберкулезного процесса и легочно-сердечная недостаточность.
Дата добавления: 2019-07-15 ; просмотров: 205 ;
Климова Е.Г. зав. фтизиотерапевтическим отделением
ТКБ № 7 Департамента Здравоохранения г. Москвы
Несмотря на обилие разнообразных методов исследования больных, своевременная диагностика туберкулёза органов дыхания остаётся непростой клинической проблемой. Ошибки при распознавании туберкулёза и иных, даже наиболее распространённых заболеваний органов дыхания однотипны и характерны. Их причины не столь очевидны, как принято считать. Дело не только в недостаточном образовании или отсутствии практических навыков у врачей: диагностика заболеваний лёгких представляет собой сложную клиническую проблему в силу веских объективных причин. Прежде всего, это клиническая универсальность сопровождающих болезни лёгких симптомов: клиническая картина самых различных по генезу заболеваний всегда складывается из сочетания респираторных и интоксикационных жалоб. При этом все заболевания лёгких весьма разнообразны по возможным вариантам течения и могут протекать как бурно, так и постепенно, торпидно, что во многом обусловлено особенностями организма больного, характером его реактивности. Затрудняют диагностику и сходные механизмы патогенеза дыхательных расстройств при большинстве заболеваний лёгких. Однако часто упускают из виду, что за каждым названием нозологической формы стоят вполне характерные морфологические проявления заболевания — тканевые реакции, определяющие генез клинических расстройств. Только при учёте взаимосвязи морфологической основы заболевания и имеющихся клинических проявлений возможна надёжная диагностика лёгочной патологии.
В связи с этим необходимо проведение стандартизировать диагностические исследования и тщательно контролировать полноценное выполнение диагностических процедур; разрабатывать принципы дифференциальной диагностики заболеваний лёгких, основанных на современных методиках исследования, доступных широкому кругу практических фтизиатрических и пульмонологических учреждений и опирающихся на единый клинико-морфологический подход к оценке выявляемых изменений.
Современный клинический диагноз представляет собой сложную систему понятий, на длительное время определяющую судьбу больного туберкулёзом. Диагноз туберкулёза выполняет регистрационно-статистическую, эпидемиологическую, клиническую и прогностическую функции. Это предопределяет комплексность обследования больного, поскольку даже самый информативный метод исследования не даёт ответа сразу на все требующие решения вопросы. В то же время существует последовательность в решении клинических задач, что обусловливает чёткую схему обследования больного.
Компоненты современного диагноза туберкулёза:
· локализация и протяжённость процесса,
· контагиозность больного (бактериовыделение),
· свойства возбудителя, в первую очередь лекарственная чувствительность.
МЕТОДЫ ДИАГНОСТИКИ ТУБЕРКУЛЁЗА ОРГАНОВ ДЫХАНИЯ
Современная медицина обладает широким набором методов диагностики туберкулёза. Это обусловлено самой природой туберкулёза — заболевания со сложным патогенезом, полиморфизмом проявлений, проходящего в своём развитии несколько стадий. Каждый из методов имеет ограничения организационного, медицинского, экономического и психологического характера, поэтому выделение только одного из них в качестве основного может нанести большой вред, поскольку в таком случае из поля зрения врача выпадает значительная часть больных, для которых этот метод заведомо неэффективен.
ВЫЯВЛЕНИЕ ХАРАКТЕРНЫХ ДЛЯ ТУБЕРКУЛЁЗА ИЗМЕНЕНИЙ В ОРГАНАХ И ТКАНЯХ
1. анамнез и физикальное обследование;
2. биохимические исследования;
3. функциональные исследования.
ПРЯМЫЕ МЕТОДЫ — ВИЗУАЛИЗАЦИЯ СТРУКТУРНЫХ ИЗМЕНЕНИЙ:
1. в тканях — морфологическая диагностика;
2. в органах — лучевая диагностика.
ВЫЯВЛЕНИЕ ВОЗБУДИТЕЛЯ ТУБЕРКУЛЁЗА
2. определение противотуберкулёзных антител;
3. исследование высвобождения γ-интерферона под воздействием специфических антигенов M. tuberculosis.
1. бактериоскопическая диагностика;
2. бактериологическая диагностика;
3. определение антигенов M. tuberculosis;
4. молекулярно-биологические методы.
Все методы диагностики туберкулёза можно разделить на две группы. К первой, общей для всех заболеваний, относят методы, основанные на определении тех или иных характерных для данного заболевания изменений в организме. Для туберкулёза прямыми методами этого типа являются морфологические и лучевые методики, косвенными — классические методы непосредственного обследования больного, различные лабораторные исследования (клинические, биохимические, некоторые иммунологические и проч.), методы функциональной диагностики.
Вторую группу, применяемую только при инфекционных заболеваниях, составляют методики, направленные на поиск и идентификацию возбудителя. Это могут быть либо прямые методы, такие как микроскопия диагностического материала, выделение культуры микроорганизмов, либо методы, позволяющие определить его присутствие в организме косвенно (например, по наличию специфических антител).
Очевидно, что диагностическое значение косвенных и прямых методов неравнозначно, однако область применения каждого из них вполне определена и отвечает тем или иным диагностическим задачам.
Необходимо подчеркнуть, что нужно различать методы диагностики, о которых мы говорим, и методики получения диагностического материала. Так, исследование получаемой при бронхоскопии лаважной жидкости можно проводить иммунологическими, биохимическими, цитологическими методами; исследование биоптата периферического лимфатического узла — гистологическим и микробиологическим методом и т.п.
АНАМНЕЗ И ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ
Знакомство с анамнезом и обследование больного позволяют охарактеризовать чахотку (phthisis) как длительное заболевание с преимущественным поражением органов дыхания и истощением, передающееся от больного людям, находящимся с ним в контакте. В основе клинической диагностики туберкулёза лежат синдром интоксикации и респираторный симптомокомплекс. Техническое совершенствование данного направления вряд ли возможно, но в настоящее время очевидна необходимость обучать врачей всех специальностей детальной клинической диагностике и проводить полноценное обследование больных различного профиля.
ОБЩИЕ КЛИНИЧЕСКИЕ, БИОХИМИЧЕСКИЕ И ИММУНОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ
Большинство лабораторных исследований не имеет самостоятельного значения в диагностике туберкулёза. Изменения, выявляемые в клинических анализах крови и мочи, биохимических исследованиях крови, указывают на степень выраженности воспалительного процесса, на состояние обменных процессов в организме больного, степень реактивности. Эти показатели очень важны для определения степени активности туберкулёза, для контроля эффективности лечения и для определения момента выздоровления, но при установлении диагноза туберкулёза имеют только вспомогательное значение, как и иммунологические исследования (оценка состояния лимфоцитов и их субпопуляций, альвеолярных и интерстициальных макрофагов и др.). Дополнительным критерием может служить оценка специфического клеточного или гуморального иммунитета. Трудности в применении этих методов связаны с высокой сенсибилизацией пациентов к микобактериям туберкулёза.
Исследование вентиляционной функции лёгких у больных туберкулёзом позволяет выявить нарушения вентиляции и газообменной функции лёгких. Среди них основное место занимают обструктивные, обструктивно-рестриктивные нарушения вентиляции, гипоксемия, лёгочная гипертензия. Эти изменения зависят от формы, распространённости и активности процесса, степени выраженности интоксикации, влияния рефлекторных и токсичных факторов и многих других составляющих заболевания. Именно поэтому самостоятельного диагностического значения данные исследования, несмотря на информативность при оценке эффективности лечения, не имеют.
Развитие патологической анатомии в XIX в. позволило охарактеризовать тканевые реакции и создать учение о туберкулёзном воспалении, которое стало прочной основой диагностики туберкулёза, однако в течение долгого времени точный нозологический диагноз устанавливали только посмертно. В настоящее время морфологические методы диагностики туберкулёза на основании изучения тканевого (цитологического или гистологического) материала традиционно считают одними из наиболее надёжных, а при туберкулезе внелёгочной локализации — зачастую единственными достоверными методами.
По мере расширения показаний к применению методов прижизненного получения тканевого диагностического материала было определено значение морфологического метода. Гистологическое и цитологическое исследования позволяют безошибочно дифференцировать туберкулёз от неспецифического воспаления и опухолевых процессов, однако зачастую не дают однозначного ответа при необходимости отличить туберкулёз от других гранулёматозных воспалительных изменений.
Морфологическая диагностика туберкулёза совершенствуется в следующих направлениях:
· использование объективных методов анализа изменений, происходящих в тканях (морфометрия);
· совмещение традиционного исследования с применением различных окрасок и иммуногистохимических исследований.
В России возможности морфологической диагностики в полной мере не используют поскольку техническая оснащённость большинства противотуберкулёзных учреждений недостаточна, отсутствуют квалифицированные специалисты и врачи предубеждённо относятся к широкому применению биопсии в диагностике туберкулёза. Нередко не только больные, но и фтизиатры двухмесячное пробное лечение по поводу возможного туберкулёза с непредсказуемым результатом предпочитают проведению эндоскопических и хирургических манипуляций, позволяющих быстро и достоверно установить диагноз.
Читайте также:


