Что такое лимфотропная терапия при туберкулезе
В конце ХХ века профессором Ю. М. Левиным был предложен новый подход к лечению, который получил название "лимфотропная терапия". Метод с успехом применяется и сегодня. Это способ лечения при котором инъекции лекарственных растворов вводятся в лимфоузлы и сосуды, сосредоточенные возле патологического очага. Методика отличается наибольшей эффективностью по сравнению с традиционными методами введения препаратов.
Суть метода терапии
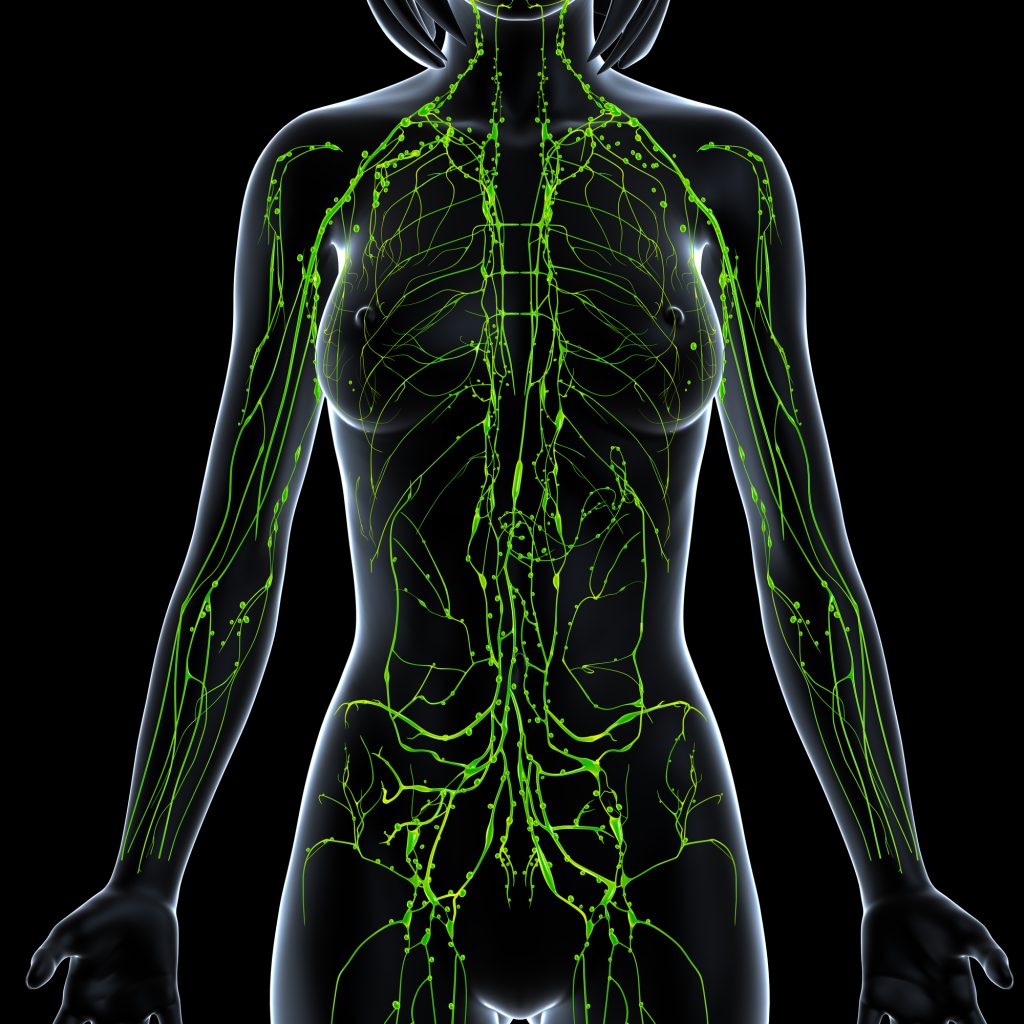
Лимфатическая система играет в организме роль биологического фильтра. Лимфоузлы расположены возле крупных кровеносных сосудов по всему организму. Введение в них лекарственных препаратов позволяет достичь максимальной концентрации вещества в пораженном органе.
При обычной внутримышечной, внутривенной или подкожной инъекции часть действующего вещества препарата после фильтрации оседает на мембранах клеток тканей кожи, капилляров. До очага поражения доходит небольшая часть препарата. К тому же, лекарство затрагивает другие органы и вызывает побочные эффекты. Введение лекарственного средства в лимфоузел позволяет избежать нежелательных явлений при максимальной эффективности терапии.
Преимущества лимфотропной терапии
Токсины патологических микроорганизмов, продукты разрушения тканей и клеток способствуют отеку пораженного места, инфильтрации периваскулярных пространств. Это затрудняет проникновение препарата и осложняет лечение.
По сравнению с традиционным, лимфотропное введение препаратов имеет ряд преимуществ:
- Необходимая концентрация лекарства сохраняется в пораженном органе на протяжении суток. Это позволяет корректировать количество лекарств в сторону уменьшения. Например, при туберкулезе лимфотропная терапия позволяет значительно снизить дозировку антибиотиков.
- За счет введения препарата-проводника увеличивается объем лимфы. Лимфатический дренаж способствует активации иммунной системы и способности организма к самоисцелению.
- При терапии антибиотиками нет необходимости принимать дополнительные средства для восстановления микрофлоры кишечника и функций печени.
- Низкая частота введения и высокая и быстрая результативность позволяют осуществлять терапию не в ущерб привычного для человека распорядка дня (в основном рабочего).
- Методика эффективна при большом круге патологических состояний.
Способы проведения терапии: хирургический
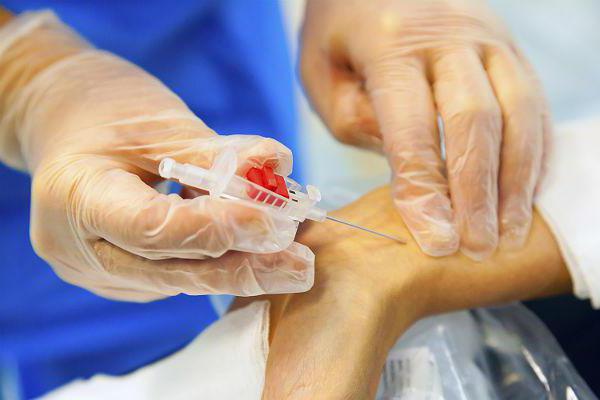
Эндолимфатическая терапия (хирургический способ) – введение лекарства в лимфоузел или лимфатический сосуд путем его пункции или катетеризации.
Для введения катетора чаще всего используют лимфатический сосуд, расположенный на руке или ноге. Для дозирования лекарства применяют инфузоматы (электронные инфузионные насосы), которые прикрепляются к катетеру. Устройства позволяют дозировать лекарство строго по времени. Применение такого способа лимфотропной терапии позволяет добиваться более длительных терапевтических концентраций.
Интранодулярный способ
Большим преимуществом интранодулярного способы является возможность введения лекарственного раствора в практически в любой периферический узел. В основном используются следующие зоны:
- подчелюстная;
- зона сосцевидного отростка;
- верхняя загрудинная;
- околопупковая;
- паховая.
Для применения способа не нужно дополнительного оснащения и подготовки персонала. Использование элементарной медицинской техники (шприцевого дозатора и иглы) делает способ простым и позволяет применять его на любых стадиях патологического состояния как взрослым, так и детям.
Показания

Лимфотропное ведение лекарственных средств позволяет добиться высоких терапевтических результатов при следующих заболеваниях:
- ЛОР-заболевания: хронический тонзиллит, отиты, гайморит, ангина.
- Стоматологические патологические состояния: пародонтит, остеомиелит, амилопластома.
- Патологии ЦНС и ПНС: ДЦП, рассеянный склероз, ишемия головного мозга.
- Офтальмологические болезни: ретинопатия, астигматизм, глаукома.
- Патологии органов дыхания: туберкулез, трахеит, бронхиальная астма, бронхит, пневмония.
- Заболевания органов пищеварительной системы: язвы, гепатиты, цирроз печени, панкреатит.
- Патологии мочевыделительной системы: пиелонефрит, цистит, уретрит.
- Болезни костно-мышечной системы: остеохондроз, межпозвоночная грыжа, артриты, артроз.
- Заболевания сосудистой системы: хроническая венозная недостаточность, посттромбофлебический синдром.
- Поражения кожного покрова: пиодермия, рожистое воспаление, фурункулезы.
В гинекологии лимфотропная терапия применяется для рассасывания спаек, лечения кист, при послеоперационной реабилитации.
Методика помогает улучшить иммунную систему, а также применяется в составе комплексного лечения при онкозаболеваниях.
Противопоказания
Любой метод, насколько бы хорош он не был, не может быть применим ко всем без исключения. Это обусловлено наличием противопоказаний:
- аллергией на вводимые препараты;
- нестерпимыми болевыми ощущениями при инъекциях;
- наличием индивидуальных особенностей организма.
Где проводят процедуру лимфотропного введения препаратов

Описываемая методика не применяется в обычных поликлиниках. Это связано с необходимостью дополнительного оснащения медучреждения. Осуществляется лимфотропная терапия в Москве и других крупных городах России в платных клиниках.
Начать лечение могут только после полного обследование, которое необходимо будет пройти в том же месте. Подобные клиники полностью оснащены необходимой аппаратурой и инструментами. Записать на прием могут в любое удобное для пациента время, но за все это придется заплатить.
Отзывы о лимфотропной терапии
Мнение пользователей больше описывают не сам процесс лечения, а клиники, где оно проходило. Сами пациенты изредка вникают в тонкости медицины, для них главное - это выздоровление.
Большинство отзывов связано с избавлением от мучительных ощущений. Одна из пациенток сообщает, что постоянно испытывала боль в яичнике, лимфотропная терапия избавила ее от страданий. Но самое приятное, что облегчение наступило уже после первой инъекции.
Большую благодарность выражают различным клиникам мамы детей с тяжелыми патологиями. Ребенку сложно выполнять медицинские манипуляции, к тому же, при серьезных заболеваниях их нужно делать очень много. Введение лекарства в лимфоузел значительно сокращает количество процедур. Единственный минус лимфотропной терапии заключается в том, что ее не проводят бесплатно.
Ведущее место в комплексе методов лечения туберкулёза занимает химиотерапия, как этиотропный метод, сущность которого заключается в уничтожении микобактерий туберкулёза, размножающихся в организме больного.
При проведении химиотерапии приходится сталкиваться с двумя основными трудностями, которые требуют определённого подхода к лечению. Во-первых, это устойчивость микобактерий туберкулёза к различным противотуберкулёзным препаратам, а во-вторых — побочное действие химиопрепаратов на организм больного.
Устойчивость микобактерий к химиопрепаратам приводит к неэффективности химиотерапии, а побочное действие — к перерывам в лечении, а иногда и к отмене тех или иных лекарственных средств.
В успешном решении проблемы лечения важное место принадлежит разработке способов повышения терапевтической активности антибиотиков, которая во многом зависит от их концентрации в воспалительном очаге, что определяется методом введения препаратов.
Патологические очаги более доступны для противотуберкулёзных препаратов, проникающих в них по лимфатическим путям [4]. Применение лимфотропной терапии описано в ряде работ, но ее значение в комплексной химиотерапии туберкулёза изучено ещё недостаточно [5].
Однако уже первые публикации и накопленный нами, хоть и небольшой, опыт свидетельствуют о перспективности этого метода.
Исследователи утверждают, что создание в лимфатической системе оптимальной концентрации лекарственных препаратов, регуляция барьерных, антитоксических функций лимфатической системы позволяют осуществлять детоксикацию на внеклеточном и клеточном уровнях, способствуют подведению лекарственных препаратов к патологическому очагу, отмечают высокий терапевтический эффект, снижение побочных действии лекарственных препаратов, создание высоких концентраций в лимфатической системе и постепенное поступление их в кровь [1, 3].
Преимуществом региональной лимфотропной терапии является приближение зоны введения лекарственных веществ к очагу воспаления, что обеспечивает проникновение препаратов в пораженные лёгкие по лимфатическим путям и создаёт благоприятные условия для достижения эффекта в лечении туберкулёза
Хороший эффект даёт применение данной методики у больных с различными поражениями печени (гепатиты, циррозы) и сопутствующими заболеваниями, которые снижают эффективность химиотерапии [2].
С целью ускорения сроков закрытия полостей распада и рассасывания очагово-инфильтративных изменений в лёгких, уменьшения частоты побочных реакций мы применили в комплексном лечении лимфотропную терапию по методике предложенной НИИ туберкулёза РАМН. В основе методики — подкожное введение 10% раствора изониазида (доза индивидуальная) после предварительного введения корректора микроциркуляции гепарина, оказывающего влияние через лимфатические сосуды, повышающего эффективность дренирующего потенциала последних [5].
В два одноразовых шприца набирается:
В 1-й шприц — 1,0 (5 тыс.) гепарина и 4,0 — 0,25% раствора новокаина; Во 2-й шприц — 10% раствор изониазида — 5,0 и 10,0 — 0,5% раствора новокаина. Используют три зоны введения:
- 1-я зона — претрахеальная (область яремной ямки);
- 2-я зона — подмышечная область на стороне туберкулёзного процесса;
- 3-я зона — зона вершины мечевидного отростка.
Зоны введения ежедневно чередуются. Одноразовая игла сгибается с помощью многослойной марлевой салфетки до формы крючка. В подкожножировую клетчатку сначала вводится содержимое первого шприца, затем, через эту же иглу, содержимое второго шприца. Длительность введений — 2-3 месяца, ежедневно, кроме выходных.
Для улучшения рассасывания место введения смазывалось гепариновой мазью.
Побочные реакции на фоне введения возникают редко, могут проявляться в виде длительной кровоточивости из места укола или уплотнения подкожножировой клетчатки. Помимо лимфотропного введения 10% изониазида, все больные получали комбинированную химиотерапию ещё 3-4 антибактериальными препаратами (стрептомицин или канамицин; рифампицин, этамбутол, пиразинамид), а также, по показаниям, патогенетическую терапию (тиосульфат натрия внутривенно, витамин E, преднизолон, иммунокорректоры, ингаляции противотуберкулёзными препаратами, физиопроцедуры.
Лимфотропную терапию начинали в различные сроки от момента поступления в стационар. Показанием к назначению лимфотропной терапии служили (в основном) выраженные экссудативные процессы в лёгких, торпидное течение процесса, появление побочных реакций на прием изониазида.
Эффективность лечения оценивалась по данным рентгенологического обследования. Методом региональной лимфотропной терапии нами пролечено 53 больных. Возраст больных — от 15 до 49 лет; женщин — 35, мужчин — 18.
По формам — инфильтративный туберкулёз — 44; ФКТ — 4; диссеминированный — 2; казеозная пневмония — 1; первичный туб. комплекс — 2.
У 51 больных были найдены MBT, полости распада определялись у 52 больных. 8 получали повторное лечение, остальные 45 — это впервые выявленные больные. Осложнения возникли только у трёх больных: у одной появилась кровоточивость из места введения, у двух других — ранее склерозирование подкожножировой клетчатки, в связи с чем лимфотропное введение изониазида было прекращено. Двое больных не долечены из-за отказа от стационарного лечения. Из 48 больных отмечено положительная динамика у 42 (87%) из них закрытие полостей распада через 2 месяца было у 10 (22%). Уменьшение размеров полостей распада в 2 раза через 2 месяца отмечено у 11 больных (23%). Значительное рассасывание очагово-инфильтративных изменений наступило у 20 больных (40%). Не получено эффекта у 6 больных, что можно объяснить поздним присоединением лимфотропного введения препаратов (более 3-4 месяцев от момента поступления в стационар).
Данные литературы и полученные нами результаты свидетельствуют в пользу назначения лимфотропной терапии сразу же после выявления специфического процесса, когда фиброзные изменения ещё отсутствуют.
- Применение лимфотропной терапии в комплексном лечении больных туберкулёзом лёгких повышает её эффективность, сокращает сроки стационарного лечения.
- Лимфотропная терапия легко переносится и не вызывает серьёзных локальных осложнений.
- Включение региональной лимфотропной терапии в комплекс лечебных мероприятий наиболее оправдано у больных впервые выявленными распространенными формами туберкулёза лёгких в ранние сроки от момента поступления.
При использовании материалов сайта ссылка на источник обязательна.
Проведен анализ влияния этиотропной и патогенетической терапии у 130 впервые выявленных больных инфильтративным туберкулезом легких на исход основного заболевания. Проанализирована частота и характер неблагоприятных побочных реакции на противотуберкулезны
The analysis of influence of etiotropny and pathogenetic therapy at 130 for the first time the revealed patients with infiltrative tuberculosis of lungs for the outcome of the main disease is carried out. Frequency and character adverse collateral reactions to antitubercular preparations is analysed.
Основное место в лечении больных туберкулезом занимает химиотерапия, проведение которой, к сожалению, чревато возникновением нежелательных лекарственных реакций (НЛР). Развитие побочных реакций на противотуберкулезные препараты (ПТП) создает угрозу для проведения полноценного курса химиотерапии [1]. Перерывы в приеме противотуберкулезных препаратов приводят к снижению эффективности лечения больных туберкулезом, формированию мультирезистентного туберкулеза и туберкулеза с широкой лекарственной устойчивостью [2, 3], а также к увеличению резервуара туберкулезной инфекции [1, 4]. В связи с этим часто возникает необходимость применения средств, которые способствуют нормализации реактивности организма, стимулируют процессы заживления, позволяют предупредить и устранить НЛР химиопрепаратов [5].
Целью настоящей работы было оценить влияние основных составляющих комплексной терапии и ее последствий на исход инфильтративного туберкулеза легких у впервые выявленных больных.
Сравнение по полу и возрасту в подгруппах, разделенных в зависимости от исхода основного заболевания, выявило следующие данные. В основной группе доля мужчин составила 65,0%, с наибольшим количеством лиц молодого возраста от 25 до 34 лет — 16,3% и от 35 до 44 лет — 15,0%, а доля женщин — 35,0%, из них почти третья часть была этой же возрастной категории — 26,3%. В группе сравнения лиц мужского пола было 54,0% (р > 0,05), с наибольшим количеством больных в старшей возрастной категории от 55 до 78 лет — 26,0%. Женщин в группе сравнения было 46,0% (р > 0,05), от 45 до 64 лет — 26,0% (р > 0,05). Вместе с тем в группе неэффективного лечения туберкулеза четверо мужчин были в возрасте до 24 лет, против отсутствия таких в группе сравнения (р 2 = 4,6; р = 0,03). Таким образом, сравниваемые группы были сопоставимы по полу.
Выполненная работа не ущемляла права, не подвергала опасности обследованных пациентов и осуществлялась с их информированного предварительного согласия на использование медицинской документации в научно-исследовательской работе, на основании приказа Минздрава РФ № 266 от 19.06.2003 г. Работа одобрена локальным этическим комитетом ОмГМА.
Полученные данные обработаны с помощью программного средства Microsoft Excel (функция Автофильтр). Для проверки статистических гипотез при сравнении числовых данных в независимых группах использовали хи-квадрат (χ2) Пирсона. Критический уровень значимости при проверке статистических гипотез в данном исследовании принимался равным χ 2 = 4,8, число степеней свободы df = 1, р 2 = 0,02; р = 0,8). Большинству пациентов лечение было начато по I режиму — 75,0% и 86,0% в группах соответственно; IV режим назначен 16,3% и 6,0% на основании выявленной устойчивости к рифампицину по результатам ускоренных молекулярно-генетических методов определения лекарственной устойчивости (GeneXpert). В некоторых случаях назначался IIБ режим химиотерапии при наличии контакта с известным больным бактериовыделителем у 8,8% и 8,0% (χ 2 = 0,02; р = 0,8). По III режиму пациенты вообще не лечились, что говорит об отсутствии ограниченных форм специфического процесса.
Изменение режима химиотерапии в связи с отсутствием эффекта от проводимого лечения происходило в обеих группах — у 7,5% в основной и у 2,0% в контрольной (χ 2 = 0,9; р = 0,3), в связи с новыми данными по лекарственной устойчивости у 18,8% и у 20,0% больных (χ 2 = 0,003; р = 0,9) в группах исследования соответственно. В связи с выявленными или подтвержденными сопутствующими заболеваниями изменение режима было сделано у 6,3% и 8,0% (χ 2 = 0,001; р = 0,9), а в связи с развитием некорригируемых НЛР на противотуберкулезные препараты — у 2,5% и 4,0% больных в группах соответственно (χ 2 = 0,002; р = 0,9).
После выявления множественной лекарственной устойчивости в 18,8% и 20,0% (p > 0,05) случаях, пациенты в группах сравнения были переведены на IV режим, а всего по данному режиму в основной группе лечилось 35,0%, в группе сравнения 26,0% (p > 0,05). По IIБ режиму химиотерапии продолжили лечиться 8,8% и 4,0% (p > 0,05) пациентов в группах при неэффективности лечения в течение 60–90 доз и отсутствии множественной лекарственной устойчивости или неполучении данных об устойчивости. Индивидуальный режим химиотерапии использовался при непереносимости ПТП и сопутствующей патологии, приводящей к непереносимости ПТП у 16,3% и 20,0% (p > 0,05) в группах сравнения соответственно. Однако в группе контроля лечение по I режиму было продолжено у 36,0%, а в основной группе только у 11,3% больных (χ 2 = 11,4; р = 0,001) (табл. 1).
Длительность интенсивной фазы лечения 90 доз в основной группе была у 37,5%, а в группе сравнения — у 58,0% пациентов (χ 2 = 5,2; р = 0,01), 120 доз — у 12,5% и 8,0% (χ 2 = 0,6; р = 0,5) в группах соответственно. Длительность интенсивной фазы 150 и 210 доз наблюдалась только в основной группе у 6,3% и 2,5% пациентов соответственно. Интенсивная фаза по IV режиму в количестве 180 доз была проведена у 41,3% и 34,0% (p > 0,05) в группах сравнения. Отрывы от лечения чаще встречались в основной группе — у 22,5% больных, в отличие от 6,0% пациентов в группе сравнения (χ 2 = 5,02; р = 0,02).
При оценке переносимости противотуберкулезных препаратов были получены следующие данные. Различного рода НЛР были зарегистрированы у 56,2% больных в основной группе и у 22,0% в группе сравнения (χ 2 = 11,6; р = 0,001). Аллергические реакции на ПТП в виде сыпи на коже и зуда развивались одинаково часто у пациентов обеих групп: в основной — в 8,8% случаев, в группе сравнения — в 8,0 (χ 2 = 0,03; р = 0,8). Желудочно-кишечные расстройства у больных туберкулезом проявлялись тошнотой либо после приема ПТП, либо в течение дня, ближе к вечеру, болью и тяжестью в эпигастральной области, изжогой и тяжестью в правом подреберье и развитием дисбактериоза кишечника. Данные расстройства возникали в основной группе у 35,0% больных, в группе сравнения — у 10,0% (χ 2 = 6,1; р = 0,008).
Кардиотоксическое действие ПТП проявлялось ощущением сердцебиения, признаками ишемии миокарда на ЭКГ в динамике, чувством жжения в области сердца и за грудиной, которые купировались после отмены препаратов. В основной группе токсическое действие на миокард было выявлено у 3,8%, в группе сравнения — у 4,0% пациентов (χ 2 = 0,1; р = 0,7).
Побочное нейротоксическое действие ПТП развивалось обычно в течение первых месяцев лечения и проявлялось головной болью, головокружением, чувством легкого опьянения, раздражительностью, бессонницей, парестезией, онемением конечностей, при правильной и своевременной терапии симптомы нейротоксического действия исчезали или значительно уменьшались по интенсивности. НЛР со стороны нервной системы были зарегистрированы у 26,3% больных, составивших основную группу, а в группе сравнения — у 14,0% (χ 2 = 2,05; р = 0,1). При этом сочетание нейротоксических реакций с желудочно-кишечными расстройствами чаще наблюдалось среди больных с неэффективно леченым туберкулезом легких — в 28,8% случаев, против 10,0% в группе сравнения (χ 2 = 5,3; р = 0,02).
Срок развития НЛР со стороны ЖКТ от начало приема ПТП у больных с неблагоприятным исходом инфильтративного туберкулеза составлял первые 4 недели лечения у 5,0% больных, а в группе сравнения — только у 2,0% (χ 2 = 0,1; р = 0,6). У 12,5% пациентов в группе сравнения данные реакции возникали спустя 1–2 месяца лечения, в основной группе — у 8,0% пациентов (χ 2 = 0,2; р = 0,6). НЛР на ПТП со стороны сердечно-сосудистой системы развивались через 2 месяца после начала лечения в стационаре в 3,8% и 4,0% случаев в группах сравнения соответственно (χ 2 = 0,1; р = 0,7).
Нейротоксические реакции на ПТП в группе больных с эффективно пролеченным инфильтративным туберкулезом развивались в первые два месяца химиотерапии в 14,0% случаев, при проведении корригирующей терапии симптомы реакций купировались. В группе пациентов с неэффективностью курса химиотерапии нейротоксические реакции в первые 2 месяца развились в 13,8% случаев (χ 2 = 0,04; р = 0,8), на 3–4 месяце химиотерапии — в 12,5% (χ 2 = 5,1; р = 0,02) и плохо поддавались коррекции.
Лимфотропная терапия в последнее время используется в комплексной химиотерапии туберкулеза. Преимуществом региональной лимфотропной терапии является приближение зоны введения лекарственных веществ к очагу воспаления, что обеспечивает проникновение препаратов в пораженные легкие по лимфатическим путям и создает благоприятные условия для достижения эффекта в лечении туберкулеза. В два одноразовых шприца набирается: 1,0 (5 тыс.) гепарина и 4,0–0,25% раствора новокаина; в другой шприц 10% раствор изониазида — 5,0 и 10,0–0,5% раствора Новокаина [7, 8]. Лимфотропная терапия в группе больных с неэффективно леченым туберкулезом легких проводилась в 10,0% случаев, против 22,0% в группе сравнения (χ 2 = 2,6; р = 0,1).
Лечение антиоксидантами, как препаратами, регулирующими процессы перекисного окисления липидов, в том числе в биологических мембранах [8], у больных в группах исследования проводилось редко — в 20,0% случаев в основной и в 24,0% в группе сравнения (χ 2 = 0,1; р = 0,7). Полиоксидоний, как иммуномодулирующее, детоксицирующее, антиоксидантное лекарственное средство, гораздо чаще использовался в группе с благоприятным исходом инфильтративного туберкулеза — в 20,0% случаев, против 2,5% в основной группе (χ 2 = 9,2; р = 0,002). Применение Ронколейкина наблюдалось еще реже: в основной группе у 6,3%, в группе сравнения у 4,0% и не повлияло на исход заболевания (χ 2 = 0,02; р = 0,8). Более чем у половины пациентов применение иммуномодуляторов не проводилось: в основной группе — у 91,3% и группе сравнения — у 76,0% (χ 2 = 4,5; р = 0,03), что вероятно связано с невозможностью противотуберкулезного диспансера обеспечить всех пациентов дорогостоящими препаратами из группы сопровождения и отсутствием платежеспособности самих больных.
Из гепатопротекторов у больных инфильтративным туберкулезом легких преимущественно использовался Карсил — в 83,8% и 84,0% случаев, редко Эссенциале форте Н в капсулированной форме — в 16,3% и 16,0% в основной группе и группе сравнения соответственно (χ 2 = 0,04; р = 0,8). Лечение кардиопротекторами проводилось у небольшого количества пациентов, исключительно в случае наличия жалоб — у 15,0% больных в основной группе и 16,0% в группе сравнения (χ 2 = 0,009; р = 0,9).
Витамины группы В в виде чередования инъекций тиамина бромида и пиридоксина получили все пациенты в обеих группах. Дезинтоксикационная терапия была проведена растворами кристаллоидов у 58,8% пациентов в основной группе и у 50,0% в группе сравнения (χ 2 = 0,6, р = 0,4). Энтеросорбенты чаще использовались в основной группе — в 47,5% случаев в связи с частым развитием желудочно-кишечных расстройств на фоне противотуберкулезной терапии, в группе сравнения — в 22,0% (χ 2 = 8,9; р = 0,001).
Физиотерапия проводилась в основной группе у 63,8% больных, против 24,0% в группе сравнения (χ 2 = 17,9; р = 0,000), с выполнением в основной группе ингаляций с изониазидом у 61,3% пациентов, а в группе сравнения — у 78,0% (χ 2 = 3,2; р = 0,07), электрофореза в основной группе — у 2,5%, в группе сравнения — у 12,0% (χ 2 = 3,3; р = 0,06).
Для выявления тесноты (силы) и направления корреляционной связи между двумя варьирующими признаками был произведен корреляционный анализ Спирмена, по результатам которого были получены следующие данные. Непереносимость химиотерапии, развитие НЛР на ПТП (р
А. В. Мордык* , 1 , доктор медицинских наук, профессор
Т. Л. Батищева**
Л. В. Пузырёва*, кандидат медицинских наук
Похожие темы научных работ по клинической медицине , автор научной работы — Цгоева Елена Анатольевна
ЭФФЕКТИВНОСТЬ ЛИМФОТРОПНЫХ МЕТОДОВ ЛЕЧЕНИЯ У БОЛЬНЫХ ОГРАНИЧЕННЫМИ ФОРМАМИ ТУБЕРКУЛЕЗА ЛЕГКИХ В УСЛОВИЯХ ПЕНИТЕНЦИАРНОЙ СИСТЕМЫ
Пермская государственная медицинская академия им. ак. Е. А. Вагнера, г. Пермь
Данные литературы показывают, что на общую ситуацию по туберкулезу оказывает высокий уровень заболеваемости туберкулезом в местах лишения свободы. По данным ФСИН, в 2006 году доля случаев заболевания туберкулезом, выявленных в учреждениях ФСИН, составляла 12,1% (14 283 больных). За семь лет, с 1999 по 2006 год, заболеваемость туберкулезом в пенитенциарной системе удалось снизить с 4347 до 1387 на 100 тыс. подозреваемых, обвиняемых и заключенных, что, тем не менее, выше аналогичного показателя заболеваемости среди общего населения в 16,8 раза. Риск заболеть туберкулезом в УИС во много раз выше, чем в общей популяции. Почти четверть всех впервые выявленных больных туберкулезом в России находилась в учреждениях уголовно-исполнительной системы [6]. Многие из них являются социально дезадаптированными лицами. В последующем асоциальное поведение таких больных значительно увеличивает риск развития хронических форм туберкулеза и повышает вероятность развития лекарственной устойчивости микобактерий туберкулеза к противотуберкулезным препаратам. Ограниченные формы туберкулеза, такие как очаговый, инфильтративный туберкулез, протекающие без распада легочной ткани и бактериовыделения, характеризуются
малосимптомным доброкачественным течением и благоприятным исходом. Однако у больных из мест лишения свободы, в отличие от остального населения, специфический воспалительный процесс склонен к осумкованию, фиброзированию, формированию больших остаточных изменений, прогрессирующему и рецидивирующему течению. Поэтому возникает необходимость разработки и применения высокоэффективных методов лечения, которым свойственны создание высокой концентрации химиопрепаратов в зоне специфического воспаления, воздействие на механизмы саногенеза, хорошая контролируемость, безопасность. Указанным требованиям отвечают лимфологические методы лечения [4]. С другой стороны, дефицит легочного сур-фактанта приводит к распространению специфического воспаления [2], а его достаточность обеспечивает не только анти-ателектатический, но и рассасывающий, антифибротический, иммуномодулирующий эффекты. Сурфактантпротективным действием при туберкулезе легких обладает препарат мукосольвинового ряда «Амброк-
Цель исследования — усовершенствование методов лимфотропного лечения, внедрение в работу туберкулезной больницы в системе исполнения наказаний и оценка их эффективности.
Материалы и методы
У пациентов 1-й группы в составе комплексной химиотерапии применялось лим-фотропное введение изониазида в дозировке 10 мг/кг в растворе из 15 мл 0,25%-ного раствора новокаина и 2,5 тыс. ЕД гепарина (ежедневно, начиная с момента установления диагноза, до 60 инъекций на курс) в около-грудинную, яремную, позадимечевидную зоны последовательно. Пациенты 2-й группы получали лимфотропное введение амброк-сола в дозе 7,5 мг (1 мл) в 9 мл 0,25%-ного раствора новокаина (2—3 раза в неделю, 5 инъекций на курс) и изониазида по выше-
Результаты и их обсуждение
Результаты исследования показали, что переносимость лимфотропной терапии хорошая. Осложнений не наблюдалось ни в одном случае. Поскольку лимфотропное введение препаратов является парентеральным, контроль за лечением осуществляется самой методикой. Включение пациентов в группы лимфотропной терапии повышало их комп-лаентность.
При выявлении туберкулеза жалобы наблюдались у 60% больных 1-й группы, у 72% пациентов 2-й группы и у 85% — 3-й. Интоксикационная симптоматика преобладала у 60% больных 1-й группы, у 66% — 2-й группы и у 75% — 3-й. Респираторные симптомы
были у 40% лиц 1-й, у 55% лиц 2-й и 65% лиц 3-й группы.
Через 2 месяца лечения жалобы сохранялись у 15, 22 и 65% пациентов соответственно. Интоксикационные симптомы наблюдались у 10, 11 и 55%, респираторные — у 5, 11 и 40% больных соответственно (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
До лечения 1,09+0,19 0,61+0,09 0,41+0,07
Через 2 месяца лечения 1,74+0,42 * 0,72+0,11 * 2,87+0,43
Примечание. * — различия достоверны при сравнении с 3-й группой (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Как уже было сказано в предыдущем ответе, если произошло первичное инфицирование, а организм слишком слабенький, чтобы оказывать сопротивление обнаглевшим МБТ, первичный туберкулёз. Он может развиться сразу после первичного инфицирования либо при прогрессировании латентной туберкулёзной инфекции. Чаще всего развивается в детском и подростковом возрасте. Выделяют 3 клинические формы первичного туберкулёза: туберкулезная интоксикация у детей (туберкулез без установленной локализации), первичный туберкулезный комплекс, туберкулез внутригрудных лимфатических узлов.
Но всё плохое когда-нибудь заканчивается (прям как учёба в меде) и у человека наступает клиническое излечение - большинство МБТ разрушены и элиминированы из организма, но кучка бравых солдатов трансформировалась в L-формы и засела в остаточных изменениях, которые формируются на месте первичных туберкулёзных очагов. За ними неусыпно следят макрофаги и лимфоциты и таким образом формируется нестерильный противотуберкулёзный иммунитет. Но если, упаси боже, произошло повторное заражение МБТ (экзогенная суперинфекция) или произошла реактивация остаточных посттуберкулёзных изменений первичного периода (эндогенная реактивация) и в результате этого нестерильный иммунитет ослаб, формируется вторичный туберкулёз. Его формы: острый очаговый, инфильтративный, туберкулема, казеозная пневмония, острый кавернозный, фиброзно-кавернозный, цирротический.
Отличия: нигде нет чёткого выделения отличий, но я предположу. Во-первых, первичный туберкулёз возникает при первичном инфицировании, в то время как вторичный возникает уже на фоне существующей инфекции. Во-вторых, течение первичного туберкулёза чаще доброкачественное и может закончиться клиническим или даже, если ты совсем везунчик, биологическим (это когда МБТ полностью вывелись из организма, даже без остаточных изменений) излечением. Но если ты заболел вторичным туберкулёзом, оставь надежду. Он будет постепенно прогрессировать с развитием всё более грубых изменений и единственное, что может тебя спасти - это противотуберкулёзные препараты, назначенные вовремя. Также, как вы уже наверное поняли, они отличаются клиническими формами. И последнее, первичный туберкулёз развивается в основном у детей, подростков и редко у молодых людей. Иногда первичным туберкулезом заболевают лица пожилого и старческого возраста, у них заболевание рассматривают как реактивацию зажившего в детстве туберкулезного процесса в лимфатических узлах (реинфицированный первичный туберкулез).
Гематогенный туберкулёз: возникает у больных, у которых первичная инфекция оставила изменения в виде очагов отсевов в различные органы.
Выделяют три вида гематогенного туберкулеза:
● генерализованный - представляет наиболее тяжелую форму заболевания с равномерным высыпанием в органах туберкулезных бугорков и очагов.
● туберкулез с преимущественным поражением легких - характеризуется преобладанием в легких высыпаний, в то время как в других органах они единичные или отсутствуют.
● гематогенный туберкулез с преимущественными внелегочными поражениями - развивается из очагов-отсевов, занесенных гематогенным путем в периоде первичной инфекции в тот или иной орган. Чаще поражаются кости скелета (костно-суставной туберкулез) и мочеполовая система (туберкулез почек, половых органов), кожа и другие органы, сами знаете, презентации делали.
Я хз, что от нас хотят в этом вопросе пролимфогенный туберкулёз. Ну в общем, к нему относится туберкулёз внутригрудных, периферических, мезентериальных л/у, туберкулёзный плеврит. По лимфогенным путям может произойти диссеминация МБТ. Из мезентериальных л/у туберкулёз может распространиться на кишечник.
Лимфотропная химиотерапия туберкулеза легких может быть использована при лечении инфильтративного, деструктивного и лекарственно-устойчивого туберкулеза легких.
Вроде как лимфотропная терапия изучена мало, но говорят, что она способствует подведению лекарственных препаратов к патологическому очагу, отмечают высокий терапевтический эффект, снижение побочных действии лекарственных препаратов, создание высоких концентраций в лимфатической системе и постепенное поступление их в кровь. При этом используются 2 шприца. В первом содержится 10 мл 0,5 % раствора новокаина и во втором — 20 мл с 10 % раствором изониазида в терапевтической дозе, разведенного полиглюкином. Первым шприцом обезболивают, вторым вводят лекарство Используют три зоны введения:
● 1-я зона — в заднемедиальную область бедра (вместо новокаина вводят лидазу)
● 2-я зона — в загрудинное пространство под рукоятку грудины
● 3-я зона — в загрудинное пространство под мечевидный отросток.
Читайте также:


