Антитела к эритроцитам малярия
Возбудителями тропической малярии являетсяPlasmodium falciparum, трехдневной малярии - Plasmodium vivax, четырехдневной малярии -Plasmodium malariaeи трехдневной или овале-малярии - Plasmodium ovale. Малярийные плазмодии претерпевают половой цикл развития в организме комара рода Anophelesи бесполый цикл (шизогония – рис.41) — в организме человека, поражая сначала клетки печени (тканевая шизогония), а затем эритроциты (эритроцитарная шизогония).
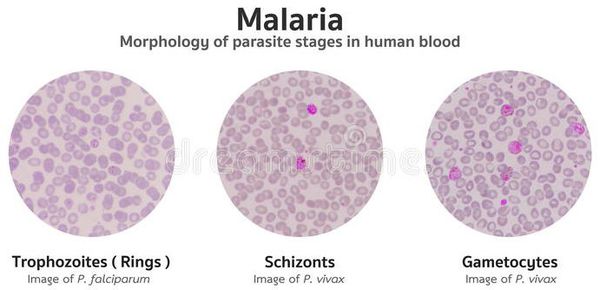
Микроскопический метод.Кровь на наличие плазмодиев малярии исследуют на стадии эритроцитарной шизогонии путем микроскопии обычных мазков и толстой капли, окрашенных по Романовскому-Гимзе. Плазмодии, цитоплазма которых окрашена в голубой цвет, а ядро в вишнево-красный, находят в эритроцитах.
Бесполые (эритроцитарные) формы паразитов имеют некоторые морфологические особенности. В частности, мерозоит представляет собой круглую или овальную форму с небольшим участком цитоплазмы около ядра; кольцевидный трофозоит - одноядерную форма сузким ободком цитоплазмы, окружающим небольшую вакуоль; амебовидный трофозоит - одноядерную форму с различным количеством и величиной псевдоподий; шизонт содержитдва или несколько ядер; морула характеризуется полным разделением ядра и цитоплазмы на мерозоиты.
Половые формы плазмодиев (гаметоциты или гамонты) не содержат вакуолей и псевдоподий. Мужские (микрогаметоциты) и женские (макрогаметоциты) формыотличаются по величине и структуре ядра, интенсивности окраски цитоплазмы и размерам.
При микроскопии тонкого мазка при малярии находят обычно кольцевидные трофозоиты. У P. vivax, P. malariae, P. оvale ониимеютразмеры от 2 до 4 мкм, занимают около 1/3 диаметра эритроцита. Ядра у трофозоитов P. vivax и P. malariaeкруглые, у P. ovale — неправильной формы, крупные; ободок цитоплазмы ровный, неширокий, суживается к ядру. Молодые кольцевидные трофозоиты P. falclparumмелкие (1,25-1,50 мкм), занимают примерно 1/6 часть диаметра эритроцита, имеют маленькое круглое ядро с тонким ободком цитоплазмы. Взрослые кольцевидные трофозоиты более крупные, занимают 1/3 диаметра эритроцита, ободок цитоплазмы толстый, резко суживающийся к ядру.
Амебовидные трофозоиты P. vivaxотличаются разнообразием форм, размеров, наличием одной или нескольких псевдоподий, вакуолей, круглого или овального ядра, пигмента в виде темно-коричневых цитоплазматических зерен различной величины и формы. Амебовидные трофозоиты P. malariaeокруглые и овальные (нередко ввиде ленты поперек эритроцита с продолговатым или вытянутым ядром), с короткими и широкими псевдоподиями, более темной цитоплазмой ипигментом, ядром неправильной формы.. Амебовидные трофозоиты P.falciparumв видекруглых или
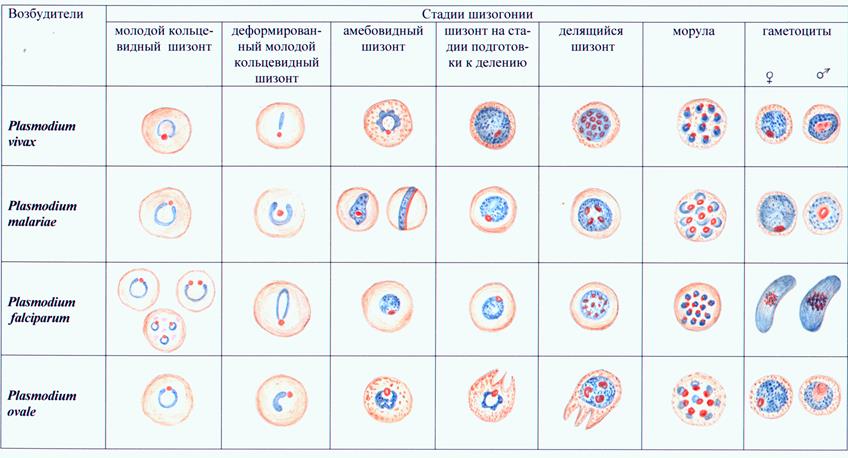
Рис. 41. Основные стадии эритроцитарной шизогонии малярийных плазмодиев
овальных форм лишены вакуоли, имеют ядро круглой или неправильной формы, пигмент черного цвета, расположенный компактно, однако они, как правило, в периферической крови не обнаруживаются. Молодые трофозоиты P. ovaleимеют кольцевидную форму, более взрослые сходны с P. malariae.
Размеры шизонтов у возбудителей малярии увеличиваются по нарастающей в ряду P.vivax, P. ovale, P.falciparum.
Морула P. vivaxсодержит обычно от 14 до 16 беспорядочно расположенных мерозоитов, между которыми лежат глыбки пигмента. В моруле P. malariaeоколо 8 крупных мерозоитов, расположенных в виде розетки; в моруле P.falciparum8-24 мелких мерозоитов, занимающих часть эритроцита; в моруле P. ovaleоколо 8 крупных мерозоитов с ядром неправильной формы. Гаметоциты Р. vivax(крупные), P. malariae (мелкие) и Р.ovaleокруглой или овальной формы;глыбки пигмента крупные, равномерно расположены в цитоплазме гаметоцитов. В женских гаметоцитах у края цитоплазмы обнаруживают компактное ядро темно-голубого цвета. Расположенное центрально ядро мужских гаметоцитов розовато-фиолетового цвета, крупное, рыхлое. Гаметоциты этих видов плазмодиев появляются и исчезают из периферической крови вместе с трофозоитами. Гаметоциты P.falciparumимеютхарактерную полулунную форму с ядром, расположенным в средней части цитоплазмы (у женских форм оно небольшое и компактное, у мужских - крупное и рыхлое). Пигмент окружает ядро в виде коротких палочек. Стадия развития гаметоцитов P.falciparumв эритроците существенно превышает длительность шизогонии. Эти гаметоциты выявляются в периферической крови на 8-10 день после появления кольцевидных трофозоитов, продолжая поступать в кровь через несколько недель после их исчезновения на фоне отсутствия клинических симптомов малярии..
Эритроциты, пораженные P. vivax и P. ovale, увеличиваются в диаметре до 10-12 мкм, хуже окрашиваются по Романовскому —Гимзе; эритроциты, пораженные P. ovale, могут приобретать неправильную форму, иметь бахромчатый край. Морфология эритроцитов, содержащих P. malariaeи P. falciparum, не меняется.
В эритроцитах, содержащих P. vivaxна различных стадиях развития, выявляются множественные мелкие азурофильные зерна (зернистость Шюффнера), при наличии в эритроцитах P. ovaleзерна редкие и крупные (зернистость Джеймса), при обнаружении в эритроцитах кольцевидных трофозоитов P.falciparumможно выявить небольшое количество крупных азурофильных зерен (зернистость Маурера), а в тех случаях, когда возбудителем является P. malariae, в эритроцитах выявляют мелкую зернистость Циманна.
Морфология возбудителей малярии в толстой капле.Кольцевидные трофозоиты P. vivax, P. ovale, P. malariae обычно имеют одинаковую величину, однако в толстой капле они часто дефор-
мируются, превращаясь в форму запятой или восклицательного знака; цитоплазма при этом концентрируется около ядра в виде округлого или треугольного комочка. Наряду с кольцевидными трофозоитами можно найти другие формы плазмодиев и определить вид возбудителя.
Для амебовидных трофозоитов P. vivaxв толстой капле характерна деформация их цитоплазмы в виде двух или нескольких комочков, располагающихся около ядра.
Трофозоиты P. malariaeв мазке выглядят как компактные овальные или округлые образования с большим количеством пигмента.
Женские гаметоциты (гамонты) P. vivax и P. malariaeв толстой капле не удается отличить от взрослых трофозоитов. Мужские гаметоциты имеют крупное ядро, окруженное узким ободком бледно-голубой цитоплазмы с рассеянными по ней зернами пигмента. Гаметоциты P. falciparumимеют характерную полулунную форму.
Серологический метод -определение антител к плазмодиям малярии с помощью РИА или ИФА с диагностическими целями проводится редко.
Не нашли то, что искали? Воспользуйтесь поиском:

Период беременности для каждой будущей мамы прекрасен и в то же время волнителен. Нося под сердцем свое дорогое дитя, каждая женщина переживает и желает легкой беременности и родов. Но резус-отрицательные мамочки могут столкнуться с некоторыми вопросами, касающихся их резус-отрицательной крови и здоровья своего малыша.
Антиэритроцитарные антитела — что это?

Резус-положительный и резус-отрицательный эритроциты
Антитела представляют собой белковые соединения плазмы крови, которые вырабатываются в ответ на наличие какого-то определенного антигена. Взаимодействуя, антитело и антиген образуют вместе иммунный комплекс, который запускает в иммунной системе организма определенные реакции. Если мы говорим об антиэритроцитарных антителах, то имеем в виду белковые соединения, которые вырабатываются в ответ на антигены на поверхности эритроцитов. Чаще всего в роли эритроцитарных антигенов выступает резус-фактор, который по своей сути является белком на мембране эритроцита. Отсюда можно сделать простой и понятный вывод, кто же такие резус-отрицательные и резус-положительные пациенты. Резус-положительные пациенты имеют на поверхности эритроцитов белок, у резус-отрицательных такой белок отсутствует.
Когда образуются антитела?

Гемотрансфузия может послужить причиной выработки антител
Если обратиться к иммунологии, то становится известным, что антитела образуются после того, как лимфоциты встретили попавшие в организм чужеродные антигены. Образование таких чужеродных антигенов возможно в следующих случаях:
- Переливание крови или гемотрансфузия. Попадая в организм пациента, нуждающегося в переливании крови (реципиента), эритроциты донора распознаются иммунной системой как чужеродные антигены (агенты). В ответ на них начинаются вырабатываться антиэритроцитарные антитела.
- Беременность. Во время беременности резус-положительные эритроциты плода могут проникать в кровоток резус-отрицательной матери через плаценту. Ее организм распознает этот белок на поверхности эритроцитов ребенка как чужеродный антиген и нарабатывает в ответ антирезусные антитела.
Виды антител
Механизм образования иммунных антиэритроцитарных антител
Различают два вида антиэритроцитарных антител — естественные и иммунные.
- Естественные (регулярные) антиэритроцитарные антитела образуются всегда и являются врожденными и образуются в ответ на антиэритроцитарные антигены из системы АВО.
- Иммунные (нерегулярные) антитела в отличие от первых нарабатываются тогда, когда в организм поступает чужеродный агент — указанные выше случаи с беременностью и переливанием крови. Другое название таких белковых соединений — аллоиммунные или изоиммунные. Эти антитела вступают в реакцию не со своими, а с чужими антигенами, поступающими в организм человека. Кроме указанных выше есть понятие и фиксированных антител или аутоантител. Из последнего слова понятно, что данные антитела вырабатываются к антигенам собственных эритроцитов под влиянием определенных факторов. Подобная ситуация может наблюдаться при гемолитической болезни новорожденных, аутоиммуной лекарственной анемии и др.
Всего на поверхности эритроцитов содержится около 100 антигенов, которые представляют 19 отдельных систем. Резус-фактор является самым иммуногенным. То есть в ответ на него реакция иммунной системы наиболее выражена.
Тест на определение антител

Суть реакции агглютинации
В основе теста на определение антител лежит реакция агглютинации. Она характеризуется образованием хлопьев или осадка, который представляет собой прореагировавшие антитела с антигенами. Для исследования производится забор венозной крови. Тест на определение антиэритроцитарных антител показан в следующих случаях:
- определение совместимости донора и реципиента перед проведением гемотрансфузии;
- выявление возможного резус-конфликта у матери и плода.
Подготовка теста не является особенной и состоит из следующих нехитрых рекомендаций, выполнить которые несложно. Вот на что необходимо обратить внимание:
- Сдавать кровь необходимо утром и натощак. Именно таким образом тест можно провести на фоне ограниченного приема жидкости. Последний прием пищи должен быть не позднее восьми часов до начала теста.
- Не рекомендуется накануне есть жареные или острые блюда, употреблять спиртные напитки.
- Накануне рекомендовано исключить любые физические нагрузки. Хотя бы полчаса перед проведением теста пациенты должны провести в покое. Это означает, что необходимо прийти немного раньше назначенного времени и посидеть.
- Исключить курение в последние 30 минут перед сдачей теста.
Проведение и интерпретация теста

Расшифровка теста агглютинации
Первый этап: в одну пробирку вносятся донорские эритроциты и сыворотка реципиента (пациента). Если антитела присутствуют, то они фиксируются на поверхности эритроцитов.
Второй этап: Прореагировавшие или непрореагировавшие эритроциты переносятся на стекло. Сюда же добавляется стандартная антиглобулиновая сыворотка с антителами к человеческому иммуноглобулину. Если антитела зафиксировались на эритроцитах, наблюдается положительная реакция агглютинации — осадок или хлопья. В противном случае реакция расценивается как отрицательная.
В зависимости от силы реакции агглютинации выделяют следующие результаты:
- сильноположительный или 4 плюса,
- положительный или 3 плюса,
- слабоположительный — 2 плюса,
- очень слабоположительный — 1 плюс,
- отрицательный — минус.
Есть ли в норме антиэритроцитаные антитела? Да, есть, но очень малых количествах, которые не поддаются определению с помощью обычных методов. Перед интерпретацией теста важно помнить, что положительным может оказаться тест, если инъекция антирезусного иимуноглобулина была сделана женщине в последние 6 месяцев. Кроме того, отрицательный результат у ребенка может наблюдаться и тогда, когда реакция положительная.
Малярийные комары

Восприимчивость к малярии практически всеобщая.
В эндемичных районах новорожденные, родившиеся от иммунных матерей, обладают пассивным иммунитетом до 2-3 месяцев. К шестимесячному возрасту защитные антитела в крови уже не обнаруживаются.
Имеются популяции населения, которые обладают полной или частичной врожденной невосприимчивостью к определенным видам возбудителей.
Африканские негры обладают врожденной, генетически обусловленной невосприимчивостью к P.vivax, которая до настоящего времени сохраняется у их потомков - американских негров. Причина невосприимчивости заключается в недостаточности у негроидов антигенов крови группы Даффи (Fy или Fy), которые являются паразитарными рецепторами, факторами прикрепления паразита к эритроцитам.
Выраженной устойчивостью к P.falciparum обладают носители гемоглобина S (HbS) и других патологических глобинов - С и В. По-видимому, малярийный паразит не способен усваивать аномальные гемоглобины. Установлено, что у неиммунных лиц с HbS при заражении P.falciparum тропическая малярия протекает с невысокой паразитемией и значительно легче, чем у больных с нормальным гемоглобином, а при наличии приобретенного иммунитета наблюдается полная невосприимчивость.
Имеется корреляция в распространении талассемии и малярии. Относительная устойчивость к малярии гетерозиготных носителей талассемии объясняется недостатком в эритроцитах необходимого паразиту железа.
У лиц с дефицитом глюкозо-6-фосфат-дегидрогеназы также имеется невосприимчивость к Р falciparum.
Приобретенный иммунитет при малярии включает клеточный и гуморальный ответы. Началом иммунных процессов, которые стимулируют выработку антител, является фагоцитирование малярийных паразитов макрофагами, в цитоплазме которого происходит процессинг поглощенного белка с выделением иммуногенных детерминант или э пито по в. Макрофаг через интерлейкин-1 (ИЛ-1) стимулирует Т-лимфоцит хелперного ряда, который помогает "загустить" иммунный ответ. Антигены предъявляются лимфоцитам Т-хелперам вместе с комплексом гистосовместимости (HLA), презентация способствует выроботке интерлейкина-2 (ИЛ-2), который и активизирует размножение и дифференцировку различных клонов В-клеток, синтезирующих специфические антитела. Антитела атакуют эпитоны антигенов, нарушая их функцию. Кроме того, ИЛ-2 стимулирует размножение и дифференцировку Т-цитотоксических лимфоцитов, которые атакуют инфицированные эритроциты в непосредственном клеточном контакте. Антигенными раздражителями в естественных условиях являются только эритроцитарные стадии плазмодиев. Антигенными детерминантами, которыми обладают не только поверхностные белки различных стадий развития паразита, но и его функциональные белки, в частности протеин-р41, обладающий в плазмодии альдолазной активностью. Он способствует выработке энергии, которая используется на репликацию и созревание плазмодия в эритроците. Спорозоиты, гаметоциты и тканевые стадии паразитов не вызывают активности иммунного ответа и, следовательно, образования к ним специфических антител.
Развивающийся иммунитет обуславливает синхронизацию размножения паразитов в эритроцитах с упорядочением лихорадочных пароксизмов, постепенное снижение паразитемии и в дальнейшем спонтанное прекращение приступов.
Образование специфических антител начинается с первых дней заболевания. Серологические реакции становятся положительными через 5-12 дней от начала заболевания. Наиболее высокие титры отмечаются через 4-6 недель. Затем наблюдается снижение титров антител, но серологические реакции остаются положительными в низких титрах еще в течение двух лет при тропической малярии, 6 лет - при трехдневной и 15 лет - при четырехдневной малярии.
У лиц, живущих в эндемичных районах, в результате постоянного ре инфицирования развивается высокий иммунитет, поэтому клинические проявления малярии выражены слабо, либо отсутствуют совсем. Но прекращение повторных заражений, в случае выезда из эндемичной зоны, приводит к постепенному угасанию иммунитета и при заражении малярией спустя несколько лет, повлечет за собой тяжелое течение заболевания.
Как и при других инфекциях, иммунитет при малярии строго в ид о- и штаммоспецифичен. Установлено, что быстрее вырабатывается иммунитет к P.vivax и P.malariae и медленнее - к P.falciparum. При обследовании населения деревень Центральной Африки получены следующие данные: в первые годы жизни дети заражаются всеми видами возбудителей малярии и тяжело болеют. К 9 годам у них из крови исчезает P.vivax, к 14 годам - P.malariae, и только после 16 лет вырабатывается некоторый иммунитет к тропической малярии. Иммунитет при овале-малярии развивается быстро, о чем свидетельствует быстрое спонтанное прекращение приступов при этой инфекции.
Известно, что размножение малярийных плазмодиев приводит к истощению иммунной системы инфицированного человека, что может частично объяснить развитие на фоне тропической малярии лимфомы Беркита, Показано, что инфицирование малярией приводит к иммунодефициту со снижением количества Т-хелперов, запускающих иммунный ответ, так как именно Т-хелперы элиминируются при малярийных приступах (Лалаянц И.Э., Милованова Л.С. 1988).
С 70-х годов проводятся исследования по созданию эффективных вакцин, однако к настоящему времени вакцин, пригодных для человека, нет. В то же время новейшие молекулярно-биологические исследования позволяют глубже проникнуть в биологию малярийного плазмодия и генез иммунного ответа, проследить динамику смены антигенов различных стадий развития плазмодия, их функциональную структуру. Можно надеяться, что в скором будущем будут созданы долгожданные действенные вакцины против малярии.
Причиной приступа лихорадки при малярии является массовое разрушение пораженных паразитом эритроцитов, выход в кровь мерозоитов, а также продуктов жизнедеятельности плазмодиев и распада эритроцитов в сочетании со своеобразной токсико-аллергической реакцией организма на эти вещества. В ретикулоэндотелии селезенки, печени, костном мозге и других органах откладывается темно-бурый пигмент - меланин, образующийся из гемоглобина (гемомеланин).
При его избытке происходит разрастание соединительной ткани, что приводит к индурации и циррозу органов, прежде всего печени и селезенки. При первых приступах малярии печень и селезенка увеличиваются за счет избыточного кровенаполнения этих органов. В связи с гемолизом сокращается продолжительность жизни эритроцитов; в крови появляются антиэритроцитарные антитела, становится положительной реакция Кумбса; снижается проницаемость оболочки эритроцита для ионов натрия, вследствие чего они легко разрушаются.
Существенно повышается фагоцитарная активность гистиоцитарной системы селезенки, поглощающей пораженные паразитом эритроциты. Это ведет к постоянному гемолизу эритроцитов и нарастанию в процессе болезни анемии, особенно при ее затяжных, рецидивирующих и хронических формах. Развивается синдром гиперспленизма, которому присущи анемия, лейкопения, тробмоцитопения; появляется кровоточивость.
У лиц с недостатком глюкозо-6-фосфатдегидрогеназы в эритроцитах анемия может быть усилена приемом противомалярийных препаратов, вызывающих гемолиз. У больных, длительно получавших хинин в связи с хронической инфекцией, образуются антитела к хинину, равно как и к другим препаратам, назначаемым в эндемичных по малярии местностях с профилактической и лечебной целями. Образующиеся антитела фиксируются на эритроцитах, приводят к усиленному гемолизу. Возникает острая почечная недостаточность с нередким летальным исходом.
При тропической малярии чаще, чем при других ее видах, возможно поражение ЦНС и развитие церебральной формы малярии, протекающей с комой. В основе мозговой комы при малярии лежит поражение мелких кровеносных сосудов и капилляров головного мозга с нарушением проницаемости сосудистой стенки и развитием тромбозов и кровоизлияний (М.В. Войно-Ясенецкий). В генезе расстройств кровообращения в головном мозге лежат не только нарушения сосудистой регуляции и тромбозы мелких сосудов, но и нарушения функции надпочечников, шейных симпатических ганглиев (Н.К. Боголепов).
При малярийной коме выражена картина кислородного голодания тканей, отека мозга, общей тяжелой интоксикации организма с нарушением функции многих органов и систем.
При хронической малярии могут быть тяжелые осложнения. Помимо малярийной комы, характеризующей злокачественное течение болезни, возможно развитие ИТШ (алгида), ОПН, ОДН и др. Это связано с быстрым нарастанием паразитемии, адгезией самих эритроцитов и адгезией их с эндотелием мелких кровеносных сосудов.
Цитоадгезия возникает благодаря наличию на поверхности эритроцитов лигандов -низкомолекулярных пептидов. Кроме того, в эндотелии сосудов мозга, легких, почек, плаценты содержится хондроитин сульфат А, который является цитоадгезивным рецептором для пораженных плазмодием малярии эритроцитов. СД36 способствует образованию на мембранах пораженных эритроцитов шиловидных выростов, заряженных положительно, а сама мембрана заряжена отрицательно, что обусловливает прилипание их к стенке сосудов. Такую же роль выполняет фактор некроза опухолей (TNF), который наряду с этим нарушает эритропоэз, оказывает пирогенное действие, вызывает гипогликемию и активирует оксид-синтетазу, в результате чего освобождается нитрит-оксид, нарушающий синаптическую передачу в ЦНС.
Изменяется система свертывания крови; следствием этих процессов является гиперкоагуляция, а затем гипокоагуляция. Массивный внутрисосудистый гемолиз ведет к гемоглобинурии и развитию ОПН. В патогенезе тяжелого течения тропической малярии у беременных женщин, у которых под влиянием избыточного кортизона и эстрогенов снижаются реакции клеточного иммунитета, отводится большая роль иммунопатологическим реакциям. При быстро нарастающей паразитемии увеличиваются возможности поражения плода, наступления преждевременных родов и мертворождения. При хронических формах малярии помимо гипохромной анемии развиваются серьезные нарушения различных видов обмена, общее истощение, а в ряде случаев и амилоидоз.
- Вернуться в оглавление раздела "Микробиология."
Что такое малярия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 12 лет.

Определение болезни. Причины заболевания
Малярия (febris intermittens, болотная лихорадка) — группа протозойных трансмиссивных заболеваний человека, вызываемых возбудителями рода Plasmodium, передающимися комарами рода Anopheles и поражающими элементы ретикулогистиоцитарной системы и эритроциты.
Клинически характеризуется синдромом общей инфекционной интоксикации в виде лихорадочных пароксизмов, увеличением печени и селезёнки, а также анемией. При отсутствии срочного высокоэффективного лечения возможны серьёзные осложнения и смерть.
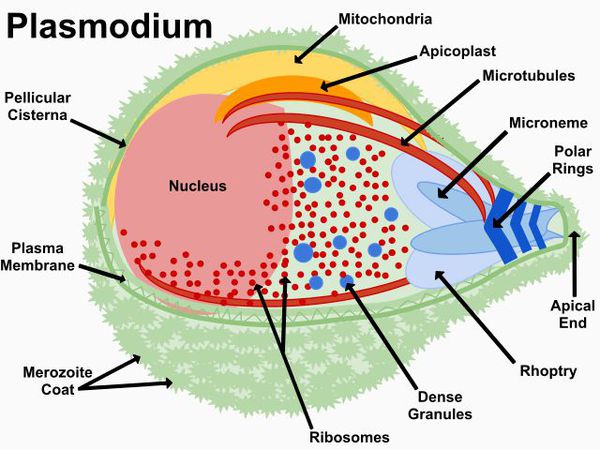
Тип — простейшие (Protozoa)
Класс — споровики (Sporozoa)
Отряд — гемоспоридий (Haemosporidia)
- P. malariae (четырёхдневная малярия);
- P. falciparum (тропическая малярия) — наиболее опасна;
- P. vivax (трёхдневная малярия);
- P. ovale (овале-малярия);
- P. knowlesi (зоонозная малярия Юго-Восточной Азии).
Продолжительность экзоэритроцитарной шизогонии (тканевого размножения):
- P. falciparum — 6 суток, P. Malariae — 15 суток (тахиспорозоиты — развитие после короткой инкубации);
- P. ovale — 9 суток, P. Vivax — 8 суток (брадиспорозоиты — развитие заболевания после длительной инкубации);
Продолжительность эритроцитарной шизогонии (размножения в эритроцитах, то есть в крови):
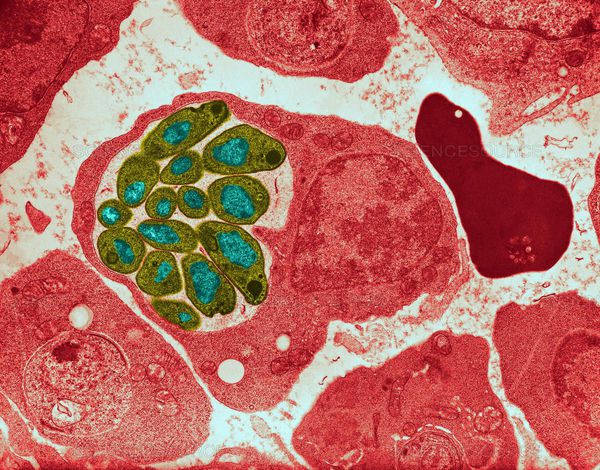
Малярия — распространённая паразитарная болезнь, характерная для стран с жарким климатом. Ежегодно заболевает более 500 млн человек, 450 тысяч из которых умирают (преимущественно в африканском регионе).
Источник инфекции — больной человек или паразитоноситель (исключение — зоонозная малярия knowlesi, источником которой могут являться длиннохвостые и свиные макаки).
Специфический переносчик — комар рода Anopheles (более 400 видов), который и является окончательным хозяином возбудителя инфекции. Человек же является лишь промежуточным хозяином. Комары активны в вечернее и ночное время. Большую роль играет наличие воды, поэтому наибольшее распространение инфекции наблюдается во влажных местах или в период дождей.
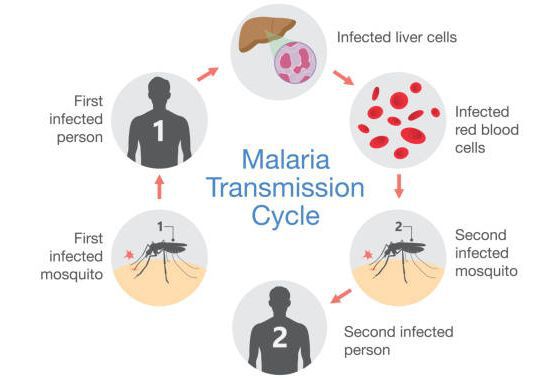
- трансмиссивный (инокуляция — укус);
- вертикальный (трансплацентарно от матери к плоду, при родах);
- парентеральный путь (переливание крови, пересадка органов).
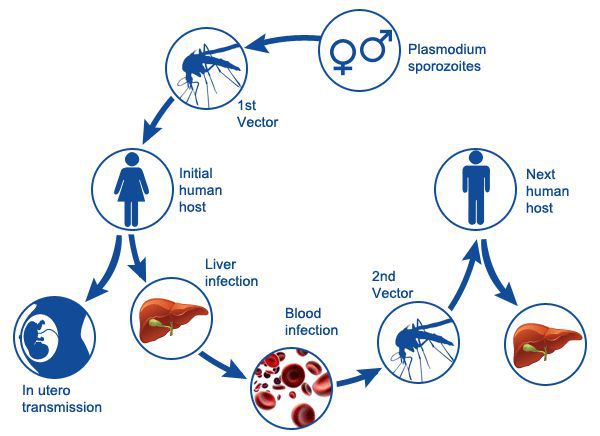
Распространение малярии возможно при наличии:
- источника инфекции;
- переносчика;
- благоприятных климатических условиях: температура воздуха окружающей среды должна быть постоянно не ниже 16°С и непрерывной в течение 30 дней — это условие является главенствующим в географическом ареале возможного распространения малярии (например в средней полосе РФ такие климатические условия практически невозможны).
Иммунитет видоспецифический, нестойкий. У жителей эндемичных регионов заболевание протекает чаще в лёгкой форме или форме паразитоносительства. [1] [2]
Симптомы малярии
Инкубационный период зависит от вида возбудителя:
- трёхдневная — 10-21 день (иногда 6-13 месяцев);
- четырёхдневная — 21-40 дней;
- тропическая — 8-16 дней (иногда месяц при внутривенном заражении, например, при переливании крови);
- овале-малярия — 2-16 дней (редко до 2 лет).
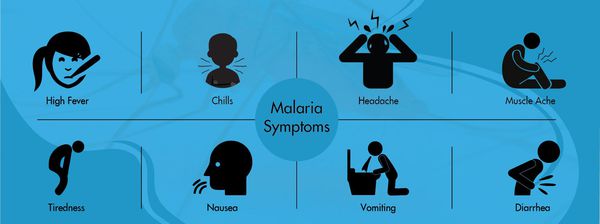
В среднем возможно около 10 малярийных приступов. К этому моменту в крови появляются антитела, которые вызывают частичную гибель плазмодиев, однако паразиты изменяют свою антигенную структуру и могут вызывать повторные заболевания. Если это брадиспорозоиты, то после последней серии приступов наступает длительная ремиссия, но весной следующего года процесс начинается снова. Отличительная особенность малярии Knowlesi — ежедневные приступы, тогда как при других формах малярии межприступный интервал может длиться несколько суток (у трёхдневной и овале-малярии повторный приступ возникают через день, у четырёхдневной — через два дня, у тропической — длительные приступы без чёткой периодичности).
При осмотре можно выявить различные степени угнетения сознания (исходя из тяжести заболевания). Положение больного так же соответствует степени тяжести болезни. Проявляется болезненность мышц и суставов, в период приступа есть некоторая вариабельность вида кожных покровов в зависимости от вида возбудителя:
- при трёхдневной малярии — бледность при ознобе и красная горячая кожа при жаре;
- при тропической малярии — бледная сухая кожа;
- при четырёхдневной болезни — постепенное развитие бледности.

Клинические критерии малярии:
- эпидпредпосылки (нахождение в странах жаркого климата последние два года);
- острое начало заболевания;
- характер лихорадки (перемежающаяся, приступы);
- гепатолиенальный синдром (из-за повышения кровенаполнения);
- анемия. [1][3][4]
Патогенез малярии
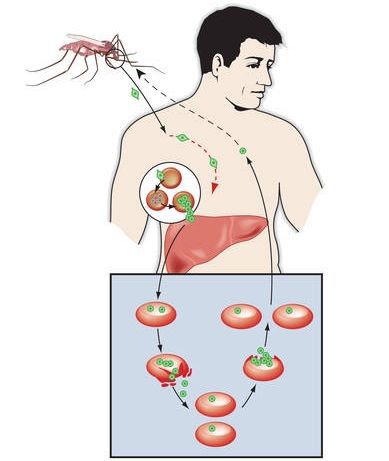
Комары различных видов рода Anopheles, выпивая кровь больного человека (за исключением зоонозной малярии), дают доступ крови больного в свой в желудок, куда попадают половые формы плазмодиев — мужские и женские гаметоциты. Прогресс спорогонии (полового развития) венчается формированием многих тысяч спорозоитов, которые, свою очередь, в значительных количествах накапливаются в слюнных железах комара. Таким образом, кровососущий комар становиться источником опасности для человека и сохраняет заразность до 1-1,5 месяцев. Инфицирование восприимчивого человека случается при укусе инфицированного (и заразного) комара.
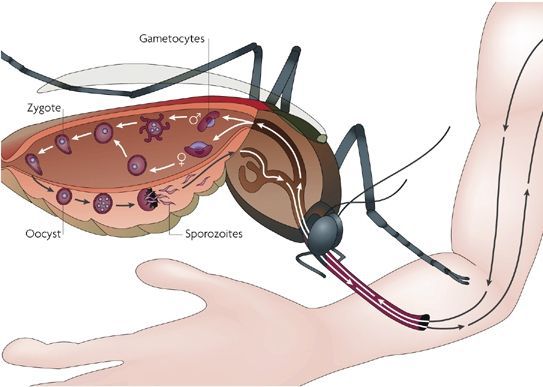
Далее спорозоиты посредством тока крови и лимфы (находятся в крови около 40 минут) проникают в печёночные клетки, где происходит их тканевая шизогония (бесполое размножение) и формируются мерозоиты. В этот период наблюдается клиническое благополучие. В дальнейшем при тропической и четырёхдневной малярии мерозоиты полностью покидают печень, а при трёхдневной и овале-малярии могут длительно квартировать в гепатоцитах.
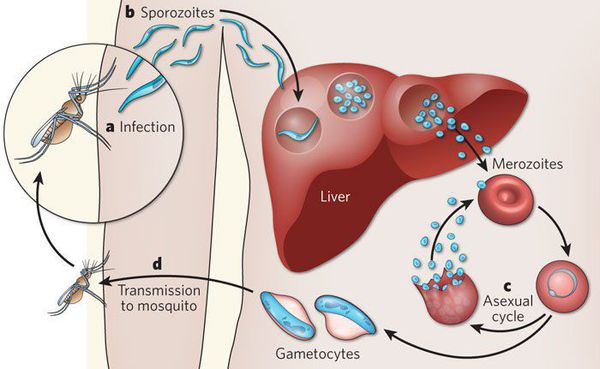
После периода латенции наступает эритроцитарная шизогония (рост и размножение в эритроцитах бесполых форм паразитов), оканчивающаяся массивным поступлением паразитов в кровь и развитием характерного малярийного пароксизма. В сосудистое русло попадают токсические продукты жизнедеятельности плазмодиев, различные пигменты, мерозоиты и части распада эритроцитов.
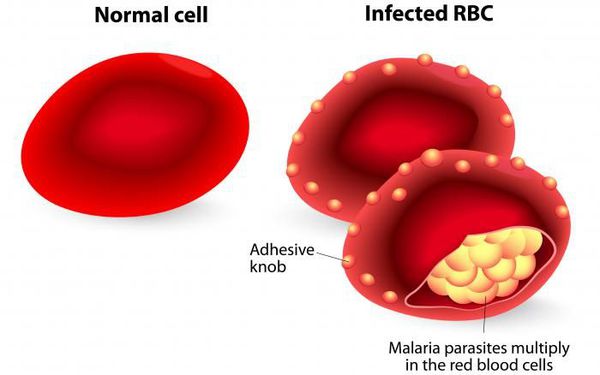
Учитывая тот факт, что в реализации приступа первостепенное значение имеет количество паразитов и аллергическая перестройка организма, следует считать, что малярийный приступ — это ответная реакция предварительно подготовленного (сенсибилизированного) организма на действие антигенов — пирогенных белков, высвобождающихся при разрушении заражённых эритроцитов. Неоднократно повторяющееся разрушение эритроцитов приводит к анемии и развитию аутоиммунных процессов (образование антител к самим эритроцитам). Увеличивается кровенаполнение печени, селезёнки и костного мозга, что усугубляет анемию. Происходит повышение концентрации гемомеланина, что приводит к гиперплазии эндотелия и фиброзным изменениям в сосудах. Приступы сопровождаются сужением периферических сосудов в период озноба, а в период жара — расширением. Это подталкивает организм к повышению синтеза кининов и, как следствие, к повышению проницаемости сосудистой стенки и вязкости крови, а также к ослаблению кровотока, что в свою очередь приводит к гиперкоагуляции и ДВС-синдрому.
Развитие гемоглобинурийной лихорадки (black water fever) связано с массивным внутрисосудистым гемолизом (разрушение эритроцитов с выделением гемоглобина) и дефицитом глюкозо-6-фосфат дегидрогеназы в эритроцитах (шоковая почка).
Малярийный энцефалит развивается при склеивании эритроцитов в капиллярах головного мозга и почек с образованием эритроцитарных тромбов, что в совокупности с общим процессом ведёт к повышению проницаемости стенок сосудов, выходу плазмы во внесосудистое русло и отёку мозга.
Малярия у беременных протекает очень тяжело, с частым развитием осложнений, характерен синдром злокачественной малярии. Летальность, по сравнению с небеременными, выше в 10 раз. При заболевании матери в первом триместре характерно значительное повышение риска абортов и гибели плода. Возможно внутриутробное заражение, ведущее к задержкам развития и клинико-лабораторным признакам малярии у новорождённого.
Дифференциальная диагностика:
- сепсис любой этиологии;
- грипп;
- лептоспироз;
- брюшной тиф;
- висцеральный лейшманиоз;
- бруцеллёз;
- геморрагические лихорадки;
- острый лейкоз. [1][4]
Классификация и стадии развития малярии
По степени тяжести:
Осложнения малярии
- Малярийная кома — развивается чаще при тропической малярии, характеризуется появлением на фоне заболевания гиперпиретической температуры (выше 41°С), невыносимой головной боли, повторной рвоты, нарушениями сознания разной степени выраженности. Прогноз неблагоприятный.
- Малярийный алгид (инфекционно-токсический шок).
- Гемоглобинурийная лихорадка — возникает при массивной паразитемии, применении некоторых противомалярийных препаратов на фоне дефицита глюкозо-6-фосфат дигидрогеназы. Характерно резкое повышение температуры тела, нарастание нарушения функции почек, моча тёмно-коричневого цвета, нарастание желтухи. При отмене препарата обычно наблюдается быстрое улучшение.
- Разрыв селезёнки — характерна резкая кинжальная боль в левых верхних отделах живота, нитевидный пульс, резкая слабость, снижение артериального давления. При отсутствии срочного оперативного вмешательства неизбежен летальный исход.
- ДВС-синдром, отёк лёгких, геморрагический синдром и другие. [1][2]
Диагностика малярии
Основа лабораторной диагностики малярии — микроскопия крови методом толстой капли (выявление малярийного плазмодия) и тонкого мазка (более точное установление вида плазмодия). При подозрении на малярию исследование следует повторять до трёх раз независимо от наличия лихорадки или апирексии.
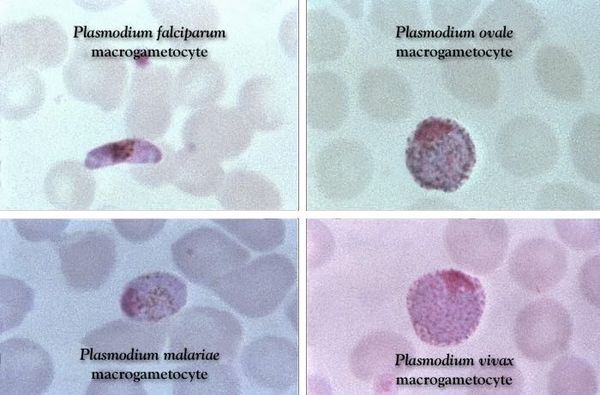
Проводятся следующие исследования:
- клинический анализ крови (анемия, тромбоцитопения, ретикулоцитоз, повышение СОЭ);
- ПЦР-диагностика;
- биохимический анализ крови (повышение общего блирубина, АЛТ, АСТ, ЛДГ);
- УЗИ органов брюшной полости (увеличение печени и в большей мере селезёнки). [1][3]
Лечение малярии
Место — инфекционное отделение больницы.
Необходимо применение противомалярийных препаратов исходя из наличия данных о возможности малярии (при недоступности метода этиологического подтверждения и высокой вероятности малярии обязательно назначение лечения), определение вида плазмодия.
Исходя из состояния больного и проявлений болезни назначается комплекс патогенетической и симптоматической терапии.
При малейших признаках малярии (температура, озноб после посещения южных стран) нужно незамедлительно посетить врача или вызвать скорую помощь. Заниматься самолечением — опасно для жизни. [1] [3]
Прогноз. Профилактика
При своевременно начатом лечении и отсутствии осложнений чаще всего наступает полное выздоровление. При запоздалом лечении (тем более у европейцев) и развитии осложнений прогноз неблагоприятен.
Основа профилактики — борьба с переносчиками инфекции. Она включает использование защитных противомоскитных сеток, пропитанных инсектицидами, применение инсектицидов в помещениях в виде распылителей репеллентов и химиопрофилактику малярии. Также достаточно эффективно осушение болот, низменностей и лишение комаров естественной природной среды. Путешественникам не следует находиться в темное время суток вне жилых защищённых помещений, особенно вне городов.
Имеет место применение ряда противомалярийных вакцин, например RTS,S/AS01 (Mosquirix™), однако её применение пока ограничено, так как оказываемый ею эффект обеспечивает лишь частичную защиту у детей (возможно применение у детей в особо опасных районах Африки). [1] [4]
Читайте также:


