Ученые встроили в геном кишечной палочки

Огурцы не виноваты
В поисках причины кишечной эпидемии, разразившейся в Германии, произошел существенный прогресс.
Как показали анализы, оперативно проведенные на испанских фермах, демонизированный немцами испанский огурец не несет на себе никакой экзотической бациллы и, скорей всего, в смерти немецких граждан не виновен.
Подробнее:
Вообще непонятно, почему именно овощи оказались в первых рядах подозреваемых.
национальный германский деликатес — обожаемые немцами колбаски из сырого мясного фарша.
Вторая подвижка — наконец-то назван по имени виновник суматохи.
В технологии ион-водородного секвенатора используется хорошо известный биохимический процесс: при встраивании нуклеотида с помощью.
За патогенные бактерии, выделенные в медицинском центре при Университете Гамбурга (именно этот город является центром эпидемии) из кала инфицированных, взялись китайские генетики. За три дня геном бактерий был расшифрован в лабораториях Пекинского института геномики с помощью ион-водородной детекции (см. врез) — метода, используемого в быстрых и относительно дешевых секвенаторах новейшего поколения.
Размер генома O104:H4 составляет примерно 5,2 Мб, это приблизительно 5 млн пар нуклеотидов. Сравнительный анализ показал, что 93% генов O104:H4 совпадают с генами другого штамма E.coli — EAEC 55989, вызвавшего эпидемию диареи в Центрально-Африканской Республике.
Также новый штамм содержит специфические последовательности генов, ответственные за развитие геморрагических колитов и гемолитических уремических синдромов (ГУС), наблюдаемых при заражении шига-токсичными кишечными палочками (то есть патогенными E.coli, продуцирующими токсин, сходный с токсином, выделяемым возбудителем дизентерии Shigella dysenteriae). Известно, что именно ГУС стал причиной смерти 17 человек в Германии.
Также найдены гены, отвечающие за невосприимчивость бактерий к антибиотикам, в частности аминогликозиду, макролидам и, что самое неприятное, бета-лактамным антибиотикам (пенициллинам, цефалоспоринам, карбапенемам), составляющим основу современной антибактериальной химиотерапии.
Все это крайне затрудняет (если делает возможным вообще) лечение разразившейся инфекции антибиотиками.
Таким образом, если отбросить теорию заговора мировой закулисы, изобретшей новое биологическое оружие массового поражения, а также ненаучные домыслы противников ГМО, считающих, что генетики могли искусственно спровоцировать патогенную мутацию E. coli (которые и так происходят ежесекундно естественным путем), новый штамм E. coli представляет собой очередной продукт стихийного творчества бактерий, умеющих повышать свое генетическое разнообразие методом прямого обмена опытом, то есть с помощью горизонтального переноса генов.
Ускорит ли расшифровка генома новой патогенной E. сoli сокращение масштабов эпидемии?
Напрямую вряд ли.
Подробнее:
Так что древним симбионтам бактерий, то есть нам с вами, чтобы не терять время в туалете, ничего не остается, кроме как следить за чистотой продуктов и мыть руки перед едой, а также серьезно подумать о переходе на вегетарианскую диету.
Кстати, повышенная резистентность патогенных E. coli, живущих в кишечнике у домашнего скота, к антибиотикам объясняется в том числе активным использованием антибиотиков в животноводстве.
— В чем ключевая разница между E.coli O104:H4 и другими серотипами группы O104, в частности O104:21, вызвавшего эпидемию геморрагического колита в Монтане (США) в 1994 году?
— Нет. Скорее всего, это говорит лишь, что у нового штамма большое количество одинаковых генов с другим штаммом, но автоматически это не означает, что новый штамм произошел от африканского.
— Что может провоцировать горизонтальный перенос генов?
— Это постоянный процесс, и горизонтальный перенос генов между бактериями происходит в вашем животе все время. В большинстве случаев никаких видимых эффектов он не продуцирует, играя чаще роль трансфера резистентности к антибиотикам и более редко — вирулентных факторов, что, похоже, и произошло в случае с кишечной эпидемией в Германии.
— Может ли локальная эпидемия E.coli O104:H4 в Германии спровоцировать глобальную эпидемию?
— Это не исключено. По всей вероятности, очень похожий штамм E. coli O157 возник локально в конце 70-х годов прошлого века, но распространился повсеместно благодаря домашнему скоту и сейчас провоцирует регулярные вспышки кишечных инфекций по всему миру.
— Можно ли разработать универсальную вакцину против патогенных E. coli?
— Можно, но не думаю, что мы имеем дело с таким сценарием в данном случае.
— Сколько времени потребуется, чтобы найти антибиотик, эффективный против штамма O104:H4?
--В большинстве случаев желательно вообще не лечить подобные инфекции антибиотиками.
— Неудивительно, что огурцы оказались не виноваты: их легко обрабатывать, и, в отличие от тех же листьев салата (возможной причины частых локальных кишечных эпидемий по обе стороны Атлантики), на их поверхности мало уголков, где могут накопиться патогенные бактерии.
— В таком случае как обезопасить себя от заражения через салаты?
— Убедитесь, что салат не рос в грунте, недавно удобренном навозом, и тщательно мойте его перед тем, как подавать на стол.
— Правильно ли утверждать, что эпидемии, подобные сегодняшней, происходят в мире регулярно, но мы их просто не замечаем, потому что во многих (особенно не таких развитых, как Германия) странах не налажен соответствующий мониторинг?
Как самый долгий биологический эксперимент породил новое существо
Изображение: Chris Bickel / Science Translational Medicine
Долговременный эксперимент по эволюции E.coli — попытка ученых в экспериментальных условиях наблюдать эволюционные процессы. Может возникнуть вопрос, почему для этих нужд ученые использовали именно кишечную палочку, а не собаку или лошадь? Одна из причин в том, что E.coli очень быстро размножается. Другая особенность, делающая бактерию удобной для исследований, — небольшой размер генома, который позволяет достаточно быстро определить, какие мутации возникают в генах со сменой поколений. Кроме того, E.coli можно без вреда для нее заморозить на длительное время.


12 популяций бактерий E.coli, участвующих в эксперименте
Фото: Michigan State University
Долговременный эксперимент по эволюции E.coli оказался удобной платформой для того, чтобы решить данную проблему. Ученые под руководством Ричарда Ленски проанализировали полные геномы 264 клонов из 12 популяций, в которых, в конечном итоге, сменилось 50 тысяч поколений. Предварительные результаты продемонстрировали, что приспособленность микроорганизмов, которая определяется как скорость роста популяции, увеличилась на 70 процентов по сравнению с той, что была у предкового штамма.

Бактерия Escherichia coli
Изображение: United States Department of Health and Human Services
Молекулярные биологи расшифровали геномы кишечных палочек, принадлежащих поколениям 500, 1000, 1500, 2000, 5000, 10 000, 15 000, 20 000, 30 000, 40 000, 50 000, с помощью метода секвенирования нового поколения. Всего было найдено более 14 тысяч мутаций, которые привели к потере 1,4 процента общего генома. При этом на половину популяций (Ara−1, Ara−2, Ara−3, Ara−4, Ara+3 и Ara+6) приходилось 96,5 процента точечных мутаций (мутаций, затрагивающих один нуклеотид). Это объясняется тем, что некоторые изменения в генах привели к нарушению процессов восстановления поврежденной ДНК, в результате чего скорость мутирования у этих штаммов значительно повысилась. Склонность к мутациям также придавали IS-элементы (Insertion Sequence) — короткие фрагменты ДНК, которые способны перемещаться и размножаться внутри генома, не выполняя никакую полезную функцию. Например, в популяции Ara+1 31,8 процента мутаций представляли собой вставки IS-элементов, а у популяции Ara−5 (поколение 30 000) доля этого же типа мутации достигала 38,7 процента.
Ученые отмечают, что склонность к генетическим изменениям лишь незначительно повышала приспособляемость организма, поскольку в то же время увеличивалось число не только полезных, но и вредных мутаций. В гипермутированных E.coli отличить полезные генетические изменения от моря остальных мутаций (нейтральных и негативных) становится очень затруднительно. Поэтому исследователи обратили свое внимание на популяции, где скорость генетических изменений осталась на предковом уровне. На основе данных они построили модель зависимости между временем и числом полезных мутаций, которая позволяла точно предсказать уровень приспособленности у микроорганизмов из поколения 50 000. Чтобы снизить влияние статистической неопределенности, биологи обратились к дополнительным доказательствам.

Биолог Ричард Ленски, руководитель долговременного эксперимента
Во-первых, так как нейтральные мутации не оказывают никакого влияния на приспособляемость, на них не действует естественный отбор, поэтому скорость их накопления должна быть сравнима с общей частотой мутаций. К таким генетическим изменениям, в частности, относят синонимичные замены, при которых изменение одного нуклеотида в гене на другой не приводит к замене аминокислоты в белке. Ученые рассчитали, во сколько раз несинонимичные мутации накапливаются быстрее, чем синонимичные. Результаты показали, что после 500-го поколения скорость была больше в 17,1 раза, а после 50 000-го — в 3,4 раза. Это говорит о том, что большинство несинонимичных мутаций были полезными и повышали приспособляемость организмов.
Исследователи также выяснили, что большинство мутаций, произошедших в ранних поколениях, были драйверными и оказывались полезными для кишечной палочки. С течением времени их доля снижалась, однако они не пропадали полностью.
Авторы статьи подчеркивают, что штаммы E. coli, участвующие в долговременном эксперименте, могут отличаться от многих природных популяций в важных аспектах, включая низкую частоту мутаций, отсутствие полового размножения и стабильные условия окружающей среды. Эффекты, которые могут накладывать неучтенные факторы на скорость накопления различных видов мутаций, должны быть учтены в будущих экспериментах.
- 684
- 0,6
- 0
- 4
Электронная микрофотография клетки Ca. Carsonella rudii. Шкала — 200 нм.
Определение минимального набора генов, необходимого для функционирования живого организма, долгое время привлекало внимание исследователей. Особенно интересны в этом отношении организмы с очень небольшим числом генов, а именно, свободноживущие и эндосимбиотические прокариоты, имеющие всего нескольких сотен генов (для сравнения, геном кишечной палочки Escherichia coli содержит около 4200 генов, а в геноме миксобактерии Sorangium cellulosum насчитывается более 11 тысяч генов). Чем отличается метаболизм клеток с такими маленькими геномами? Какие процессы привели к утрате огромного числа генов? Ответам на эти вопросы и посвящен наш обзор.
Геномы с необычно низким количеством генов (или редуцированные геномы) можно найти среди прокариот двух экологических групп: свободноживущих морских бактерий и бактерий-эндосимбионтов. Считается, что в случае свободноживущих микроорганизмов уменьшению числа генов способствует отбор, а у эндосимбиотических бактерий большую роль играют нейтральные процессы, а именно, утрата генов, которые просто-напросто стали ненужными в связи с образом жизни. Действительно, зачем таскать с собой при каждом делении множество генов замысловатых метаболических путей, когда почти все необходимое поставляется или организмом-хозяином, или другим организмом-симбионтом? Особенно любопытно, что среди очень маленьких геномов периодически попадаются такие, которые выбиваются из общего тренда эволюции бактериальных геномов — снижения GC-состава и сохранения порядка следования генов друг за другом (синтении). Кроме того, ученые уже много лет работают над получением бактерий с искусственно уменьшенными геномами и достигли определенных успехов.
В статье мы обсудим, как устроены самые маленькие геномы и как их обладатели приспособились к жизни с таким количеством генов, а также коснемся последних достижений по получению бактерий с искусственно уменьшенными геномами.
Свободноживущие прокариоты с малым числом генов
До появления и широкого распространения современных молекулярно-генетических методов считалось, что свободноживущие прокариоты имеют не менее 1300 генов. Однако в 2013 году с помощью метагеномики в образце воды из Средиземного моря описали актинобактерию Candidatus Actinomaria minuta, геном которой содержит всего лишь 800 генов. Как оказалось впоследствии, эта бактерия и сама по себе весьма миниатюрна: объем ее клеток составляет лишь 0,013 мкм 3 [2].
Среди свободноживущих архей обладателем мельчайшего генома считается Methanothermus fervidus: в его ДНК насчитывается 1311 белок-кодирующих генов и 50 генов, соответствующих некодирующим РНК [2] (рис. 1).
Рисунок 1. Methanothermus fervidus — архея с одним из самых маленьких геномов в своем домене. Фотография получена методом сканирующей электронной микроскопии.
Примерно столько же генов имеется у наиболее разнообразной группы морских гетеротрофных α-протеобактерий, известной как SAR11, и группы β-протеобактерий под названием OM43. Геномы фотосинтезирующих бактерий, как правило, содержат больше генов. Малое число генов имеется и у некоторых неморских прокариот: так, геном сапротрофной бактерии Acholeplasma laidlawii содержит 1380 белок-кодирующих генов, лактобацилла Weissela koreensis имеет 1335 генов, а архея Desulphurococcus mucosus, относящаяся к типу кренархеот и обладающая способностью к серному дыханию, — 1371 ген [2].
Что является движущей силой уменьшения числа генов у свободноживущих прокариот? На этот счет существует несколько гипотез.
Согласно гипотезе рационализации (streamlining hypothesis), естественный отбор поддерживает уменьшение генома свободноживущих прокариот, населяющих местообитания, бедные питательными веществами. Когда в геноме клетки происходит делеция, увеличивающая ее приспособленность, она быстро фиксируется в популяции: в условиях нехватки питательных веществ клеткам невыгодно волочить за собой большой геном, на поддержание которого тратится много энергии и других ресурсов.
Гипотезой рационализации можно объяснить и стремление к понижению GC-состава у свободноживущих микроорганизмов, населяющих бедные среды (в их ДНК суммарная доля гуанина и цитозина, как правило, не превышает 36%). Дело в том, что для репликации генома с низким GC-составом требуется меньше фосфора и азота. Кроме того, в скудных условиях клетке выгодно иметь большое соотношение площади поверхности к объему, чтобы более эффективно поглощать питательные вещества, а снижение объема клетки неизбежно ведет к уменьшению ее генома.
Стоит отметить, что уменьшить геном можно не только за счет утраты белок-кодирующих генов. Так, у бактерии Ca. Pelagibacter ubique с геномом в 1308 т.п.н. среднее расстояние между генами составляет лишь три нуклеотида, а псевдогенов, профагов или дуплицированных генов нет совсем [2].
Гипотезу рационализации удалось проверить в лабораторных условиях. Ученые получили штаммы Salmonella enterica, имеющие большие делеции, причем некоторые из них оказались более приспособленными к окружающим условиям, чем бактерии дикого типа [2].
При уменьшении размеров генома зачастую утрачиваются гены, белковые продукты которых задействованы в репарации, поэтому иногда у бактерий с редуцированными геномами (например, у ряда свободноживущих цианобактерий, а также симбиотических организмов) наблюдается повышенная скорость мутирования белок-кодирующих последовательностей. Это в некоторых условиях может быть на руку бактериям, например, при освоении новых местообитаний. Штаммы, отличающиеся повышенной частотой приобретения мутаций, иногда называют мутаторными [2].
Нас и здесь неплохо кормят: почему эндосимбиотические бактерии теряют множество генов
Уменьшение размеров генома происходит наиболее стремительно после того, как симбиоз становится облигатным, то есть бактерия оказывается неспособной существовать без своего хозяина. Так, эндосимбионт рисового долгоносика (Sitophilus oryzae), Candidatus Sodalis pierantonius, потерял 55% своих генов в течение всего лишь 28 тысяч лет — невероятно короткий срок по эволюционным меркам. Эта бактерия живет внутри специализированных клеток — бактериоцитов и имеет довольно внушительный геном, содержащий 2309 белок-кодирующих генов и 1771 псевдогенов. Еще более удивительно, что около 18% ее генома приходится на мобильные генетические элементы, на совести которых лежат многочисленные геномные перестройки Ca. Sodalis pierantonius и около 10% случаев инактивации генов. Однако стремительное уменьшение числа активных генов и размеров генома может происходить и без участия транспозонов. Например, бактерия Polynucleobacter necessaries, обитающая в клетках инфузории Euplotes aediculatus, утратила более 40% белок-кодирующих генов, хотя мобильных генетических элементов в ее геноме нет [2].
На завершающих этапах формирования эндосимбиотических отношений геном бактерии становится существенно стабильнее, и постоянство расположения генов на хромосоме (синтения) является одной из отличительных черт облигатных мутуалистических бактерий. Первоначально такую стабильность связывали с утратой эндосимбиотическими бактериями гена recA, продукт которого играет важнейшую роль в гомологичной рекомбинации. Однако впоследствии выяснилось, что у многих таких микробов со стабильными геномами ген recA все-таки есть. Верно и обратное: сокращение числа генов, кодирующих белки рекомбинации и репарации, не гарантирует стабильность генома. Эндосимбионт белокрылки Bemisia tabaci, Candidatus Portiera aleyrodidarum, отличается выраженным геномным полиморфизмом, который наблюдается даже среди бактерий, населяющих одно и то же насекомое, хотя активных генов рекомбинации и репарации у него чрезвычайно мало [2].
Известны две бактерии с крайне редуцированными геномами, которые, тем не менее, имеют необычно высокий для эндосимбионтов GC-состав. Речь идет о двух эндосимбионтах цикады Diceroprocta seminitica — Candidatus Hodgkinia cicadicola и Candidatus Sulcia muelleri. Геном ходжкинии достигает лишь 144 т.п.н. в длину, однако его GC-состав равен 58%. Причины, лежащие в основе повышения GC-состава, неясны. Часто этому могут способствовать ферменты, задействованные в конверсии генов, однако у ходжкинии таких белков нет. Польза от столь высокого GC-состава для эндосимбиотической бактерии также не очевидна [2].
У бактерии Candidatus Riesia pediculicola, обитающей в теле вшей Pediculus humanus corporis, есть другая особенность аппарата трансляции: набор ее тРНК сокращен до допустимого минимума. Эта бактерия утратила все ферменты, модифицирующие тРНК, за исключением тех, которые модифицируют антикодоновую шпильку. Именно эта часть молекулы тРНК принимает участие в распознавании комплементарного кодона в мРНК. Некоторые исследователи предположили, что такой скромный набор тРНК у Candidatus Riesia pediculicola похож на набор тРНК самых древних клеток. Действительно, фермент псевдоуридинсинтаза А, ответственный за появление псевдоуридинов в антикодоновой шпильке тРНК, имелся у последнего общего предка всех форм жизни. Однако пока неясно, насколько древними являются те немногие ферменты модификации тРНК, которыми обладает Candidatus Riesia pediculicola [2].
Стоит заметить, что эндосимбиотические бактерии не только теряют гены, но порой и приобретают. Когда в организме одного и того же хозяина обитает несколько бактерий-эндосимбионтов, между ними нередко происходит горизонтальный перенос генов, причем в некоторых случаях в обмене участвуют и гены самого хозяина. В качестве примера можно привести бактерию Ca. Carsonella rudii, которая является облигатным эндосимбионтом листоблошки Pachyphsylla venusta. Она обладает одним из мельчайших известных геномов: он состоит лишь из 160 т.п.н. и содержит 213 генов, среди которых нет ряда генов, необходимых для функционирования любой живой клетки. Однако карсонелла способна жить припеваючи и в отсутствие других эндосимбионтов в организме насекомого. Как показал детальный транскриптомный анализ, биосинтез ряда аминокислот карсонелла осуществляет совместно с бактериоцитом, в котором живет: некоторые реакции катализируют ферменты бактерии, другие — эукариотической клетки. Примечательно, что многие ферменты метаболизма аминокислот в бактериоцитах кодируются генами бактериального происхождения, вероятно, приобретенными от других эндосимбионтов (рис. 2) [2].
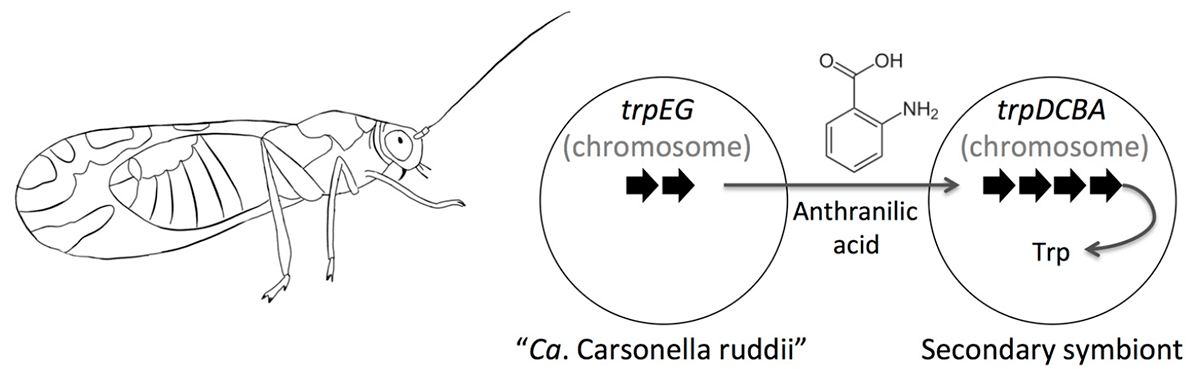
Рисунок 2. Схема синтеза триптофана в симбиотическом союзе листоблошки и Ca. Carsonella rudii. Ca. Carsonella rudii синтезирует антраниловую кислоту, которая превращается в триптофан под действием ферментов другого симбионта или ферментов, которые бактериоцит от него позаимствовал.
В обмен генами с эндосимбиотическими бактериями вступают не только насекомые, но и другие организмы. Например, нематода Brugia malayi более 10% своего генома обязана эндосимбиотической бактерии из рода Wolbachia. А некоторые бактерии приспособились к жизни внутри грибов [2].
Иногда сам хозяин становится зависимым от своих эндосимбионтов. Например, бактерии Buchnera aphidicola и Ca. Serratia symbiotica совместно снабжают своего хозяина, тлю Cinara cedri, триптофаном: часть ферментов его биосинтеза кодируется плазмидой B. aphidicola, а остальные — геномом Ca. Serratia symbiotica [2].
Наконец, эндосимбиотические бактерии иногда сами становятся хозяевами для других бактерий, образуя подобие матрешки. Обладательница одного из самых маленьких геномов Ca. Tremblaya princeps, живет в бактериоцитах войлочника Planococcus citri, но и сама является хозяином бактерии Ca. Moranella endobia. Эти бактерии сами по себе не имеют полного набора генов почти всех жизненно важных метаболических путей, однако взаимно дополняют друг друга, так что в их тандеме имеются все необходимые ферменты. Впрочем, как организован столь запутанный метаболический круг, неясно, поскольку непосредственного перемещения белков между цитоплазмами двух бактерий пока не удалось показать [2].
Синтетическая биология: сделаем мельчайший геном сами
В наше время исследователи располагают внушительным арсеналом методов редактирования геномов и синтеза протяженных последовательностей ДНК, что открывает перспективы создания новых форм жизни с геномами, собранными в лаборатории. Область биологии, занимающаяся созданием искусственных форм жизни и биологических систем, получила название синтетической биологии .
Подробнее о синтетической биологии и создании искусственной жизни читайте в наших статьях [3–5].
Пионером в области искусственных геномов стал известный ученый Крейг Вентер, изобретатель секвенирования методом дробовика и один из ведущих ученых, работавших над секвенированием генома человека. Его группа смогла в лабораторных условиях воссоздать геном бактерии Mycoplasma mycoides, который далее внесли в клетки другой микоплазмы, Mycoplasma capricolum, из которых предварительно удалили ее собственную ДНК. Сенсационные результаты получения нового вида бактерий, названного Mycoplasma laboratorium, были опубликованы в Science в 2010 году [6].
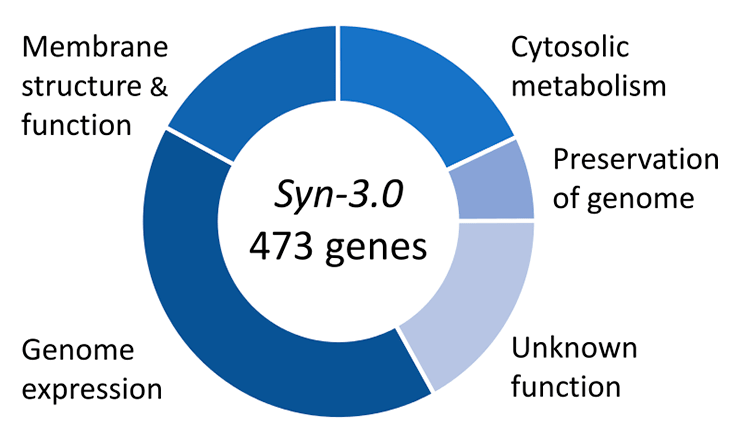
Рисунок 3. Функции генов в минимальном геноме, сконструированном в 2016 году на основе генома M. mycoides.
Стоит заметить, что предпринимались попытки уменьшить геном и других бактерий, правда, не для получения минимально возможного генома, а для других целей: например, клеток, эффективно производящих определенные вещества. Уменьшение генома проводили для кишечной палочки Escherichia coli, еще одной микоплазмы Mycoplasma genitalium, Bacillus subtilis, Corynebacterium glutamicum, Pseudomonas putida, Streptomyces avermitilis и Vibrio natriegens. В этих работах использовали искусственный химический синтез ДНК, а также различные варианты рекомбинации, например, опосредованные системами CRISPR/Cas9 или Cre-loxP (рекомбиназа Cre, распознающая локусы под названием loxP [11]). Ведутся активные работы по созданию оптимизированных геномов цианобактерий и других фотосинтетических бактерий с колоссальным потенциалом для получения биотоплива [7].
Основу генетического аппарата кишечной палочки составляет бактериальная хромосома, входящая в состав нуклеоида - ядерноподобной структуры. Нуклеоид по морфологии напоминает соцветие цветной капусты и занимает примерно 30% объема цитоплазмы. Бактериальная хромосома представляет собой кольцевую двуспиральную правозакрученную молекулу ДНК, которая свернута во вторичную спираль. Длина бактериальной хромосомы составляет примерно 4,7 млн. нуклеотидных пар (п.н.), или
1,6 мм. Вторичная структура хромосомы поддерживается с помощью гистоноподобных (основных) белков и РНК. Точка прикрепления бактериальной хромосомы к мезосоме (складке плазмалеммы) является точкой начала репликации ДНК (эта точка носит название OriC). Бактериальная хромосома удваивается перед делением клетки, и сестринские копии распределяются по дочерним клеткам с помощью мезосомы. Репликация ДНК идет в две стороны от точки OriC и завершается в точке TerC. Молекулы ДНК, способные себя воспроизводить путем репликации, называются репликоны. ген вирусный полипротеин
Одна бактериальная хромосома содержит до 1000 известных генов. Обычно это гены "домашнего хозяйства", то есть необходимые для поддержания жизнедеятельности клетки.
Все множество известных генов делится на 10 групп, контролирующих следующие процессы (в скобках указано количество изученных генов):
- 1. Транспорт различных соединений и ионов в клетку (92 гена).
- 2. Реакции, поставляющие энергию, включая катаболизм различных природных соединений (138 генов).
- 3. Реакции синтеза аминокислот, нуклеотидов, витаминов, компонентов цепей переноса электронов, жирных кислот, фосфолипидов и некоторых других соединений (221 гена).
- 4. Генерация АТФ при переносе электронов (15 генов).
- 5. Катаболизм макромолекул (22 гена).
- 6. Аппарат белкового синтеза (164 гена).
- 7. Синтез нуклеиновых кислот, включая гены, контролирующие рекомбинацию и репарацию (49 генов).
- 8. Синтез клеточной оболочки (42 гена).
- 9. Хемотаксис и подвижность (39 генов).
- 10. Прочие гены, в том числе с неизвестной функцией (110 генов).
В лаг-фазе в клетке имеется одна бактериальная хромосома, но в фазе экспоненциального роста ДНК реплицируется быстрее, чем происходит деление клетки; тогда число бактериальных хромосом на клетку увеличивается до 2. 4. 8. Такое состояние генетического аппарата называется полигаплоидностью.
При делении клетки сестринские копии бактериальной хромосомы распределяются по дочерним клеткам с помощью мезосомы.
Кроме бактериальной хромосомы в состав генетического аппарата прокариот входит множество мелких репликонов - плазмид - кольцевых молекул ДНК длиной в тысячи п.н. Плазмиды такого размера содержат несколько десятков генов. Обычно это "гены роскоши", обеспечивающие устойчивость к антибиотикам, тяжелым металлам, кодирующие специфические токсины, а также гены конъюгации и обмена генетическим материалом с другими особями. Известны также мелкие плазмиды длиной 2. 3 тпн, кодирующие не более 2 белков. У многих бактерий открыты мегаплазмиды длиной порядка миллиона пн, то есть немногим меньше бактериальной хромосомы. Плазмиды могут быть прикреплены к мезосомам, могут находиться в автономном состоянии и в интегрированном состоянии. В последнем случае плазмида включается в состав бактериальной хромосомы в определенных точках attB. Таким образом, одна и та же плазмида может включаться в состав хромосомы и может вырезаться из нее. Существуют плазмиды, представленные одной копией - они реплицируются синхронно с ДНК бактериальной хромосомы. Другие плазмиды могут быть представлены многими копиями, и их репликация происходит независимо от репликации бактериальной хромосомы. Репликация свободных плазмид часто протекает по принципу "катящегося кольца" - с одной кольцевой матрицы ДНК считывается "бесконечная" копия.
Репликация плазмид может быть синхронизирована с репликацией бактериальной хромосомы, но может быть и независимой. Соответственно, распределение плазмид по дочерним клеткам может быть точным или статистическим.
Молекулярно-генетические системы управления
(на примере лактозного оперона кишечной палочки)
Все гены организма можно разделить на две большие группы: конститутивные и индуцибельные.
Конститутивные гены постоянно включены: они функционируют на всех стадиях онтогенеза и во всех тканях. К конститутивным относятся гены, кодирующие тРНК, рРНК, ДНК-полимеразы, РНК-полимеразы, белки-гистоны, белки рибосом и т.д. Иначе говоря, это "гены домашнего хозяйства", или существенные гены без которых клетки не могут существовать.
Индуцибельные гены функционируют в разных тканях на определенных этапах онтогенеза, они могут включаться и выключаться, их активность может регулироваться по принципу "больше или меньше". Это тканеспецифичные гены, или "гены роскоши", которые часто являются несущественными. Включение индуцибельных генов называется индукцией, а выключение - репрессией. Регуляцию активности генов производят молекулярно-генетические системы управления.
Переключение генов лучше всего изучено у бактерий - одноклеточных организмов. Рассмотрим механизмы регуляции активности генов на примере лактозного оперона кишечной палочки.
Оперон - участок бактериальной хромосомы, включающий следующие участки ДНК: Р - промотор, О - оператор, Z, Y, А - структурные гены, Т - терминатор. (В состав других оперонов может входить до 10 структурных генов.)
Промотор служит для присоединения РНК-полимеразы к молекуле ДНК с помощью комплекса CAP-цАМФ (CAP - специфический белок; в свободной форме является неактивным активатором; цАМФ - циклоаденозинмонофосфат - циклическая форма аденозинмонофосфорной кислоты).
Оператор способен присоединять белок-репрессор (который кодируется соответствующим геном). Если репрессор присоединен к оператору, то РНК-полимераза не может двигаться вдоль молекулы ДНК и синтезировать иРНК.
Структурные гены кодируют три фермента, необходимые для расщепления лактозы (молочного сахара) на глюкозу и галактозу. Молочный сахар лактоза - менее ценный продукт питания, чем глюкоза, поэтому в присутствии глюкозы сбраживание лактозы является невыгодным для бактерии процессом. Однако при отсутствии глюкозы бактерия вынуждена переходить на питание лактозой, для чего синтезирует соответствующие ферменты Z, Y, А.
Терминатор служит для отсоединения РНК-полимеразы после окончания синтеза иРНК, соответствующей ферментам Z, Y, А, необходимым для усвоения лактозы.
Для регуляции работы оперона необходимы еще два гена: ген, кодирующий белок-репрессор, и ген, кодирующий белок СYА. Белок СYА катализирует образование цАМФ из АТФ. Если в клетке имеется глюкоза, то белок СYА вступает с ней в реакцию и переходит в неактивную форму. Таким образом, глюкоза блокирует синтез цАМФ и делает невозможным присоединение РНК-полимеразы к промотору. Итак, глюкоза является репрессором.
Если же в клетке имеется лактоза, то она взаимодействует с белком-репрессором и превращает его в неактивную форму. Белок-репрессор, связанный с лактозой, не может присоединиться к оператору и не преграждает путь РНК-полимеразе. Итак, лактоза является индуктором.
Предположим, что первоначально в клетке имеется только глюкоза. Тогда белок-репрессор присоединен к оператору, а РНК-полимераза не может присоединиться к промотору. Оперон не работает, структурные гены выключены.
При появлении в клетке лактозы и при наличии глюкозы белок-репрессор отщепляется от оператора и открывает путь РНК-полимеразе. Однако РНК-полимераза не может присоединиться к промотору, поскольку глюкоза блокирует синтез цАМФ. Оперон по-прежнему не работает, структурные гены выключены.
Если же в клетке имеется только лактоза, то белок-репрессор связывается с лактозой, отщепляется и открывает путь РНК-полимеразе. В отсутствии глюкозы белок СYА катализирует синтез цАМФ, и РНК-полимераза присоединяется к промотору. Структурные гены включаются, РНК-полимераза синтезирует иРНК, с которой транслируются ферменты, обеспечивающие сбраживание лактозы.
Таким образом, лактозный оперон находится под двойным контролем индуктора (лактозы) и репрессора (глюкозы).
Число генов в геноме инфузории оказалось таким же, как у человека.
Инфузории - самые сложные из одноклеточных организмов, и вообще - верх того, что смогла создать эволюция на одноклеточном уровне. Строение инфузорий во многом напоминает многоклеточных, несмотря что клетка всего одна. Например, у многоклеточных животных различают линию генеративных клеток, геном которых оберегается от всяческих изменений (ведь именно этот геном будет передан по наследству потомкам), и соматические клетки, геном которых может меняться по мере надобности (например, могут метилироваться или вовсе выбрасываться какие-то части генома, не нужные в данной ткани или органе, или могут происходить сложные целенаправленные перестройки, как в лимфоцитах). Генетические изменения соматических клеток в норме не передаются по наследству. У инфузорий тоже есть два генома - генеративный и вегетативный (соматический). Первый хранится в маленьком ядре (микронуклеусе), содержит много транспозонов и некодирующих участков, и в целом находится в нерабочем состоянии. Например, многие гены в нем разорваны на куски и перемешаны в такой клубок, что никаким сплайсингом не распутать. Но, тем не менее, это нормальный, хотя и сильно запущенный, большой эукариотический геном. Кстати, число генов у инфузорий и у человека примерно одинаково (порядка 30 тысяч). Геном микронуклеуса, естественно, не работает (он и не смог бы), и служит только для передачи генов потомству при половом размножении.
Вегетативный (соматический, рабочий) геном инфузории хранится в большом ядре (макронуклеусе) и по многим параметрам сильно отличается от других эукариотических геномов. У инфузории Oxytricha, которой посвящена обсуждаемая статья, он состоит из многих тысяч отдельных "нанохромосом". Это настоящие хромосомы, только очень маленькие, обычно содержащие всего один ген. Каждая нанохромосома, или МАК-хромосома, присутствует в макронуклеусе в очень большом количестве копий. Соответственно, и весь вегетативный геном многократно сдублирован, то есть макронуклеус является полиплоидным (микронуклеус - диплоидное ядро).
По размеру вегетативный геном окситрихи в целых 20 раз меньше генеративного (50 млн и 1 млрд пар оснований соответственно; для сравнения, у человека - 3 млрд, у бактерий - обычно до 10 млн). Такое радикальное сокращение достигается просто за счет выбрасывания из генеративного генома всего "лишнего".
Инфузории размножаются делением, при этом делятся оба ядра. Время от времени инфузории конъюгируют, чтобы обменяться наследственным материалом (конъюгация - особая разновидность полового процесса). Во время конъюгации микронуклеус претерпевает мейоз, то есть такое деление, в ходе которого число хромосом сокращается вдвое. Соединившиеся инфузории обмениваются "половинками" своих микронуклеусов. Эти половинки затем сливаются, и каждая инфузория получает один целый микронуклеус, в котором половина хромосом - ее собственная, а половина получена от партнера. Затем инфузории разъединяются и продолжают жить как жили, с той небольшой разницей, что с точки зрения генетики каждая из них теперь превратилась в свою собственную дочь.
Во время конъюгации или сразу после нее макронуклеус вместе со своим геномом разрушается, а затем восстанавливается заново. За основу берется генеративный геном микронуклеуса, но он при этом подвергается радикальной перестройке. 95% генеративного генома просто удаляется. "На выброс" идут практически все транспозоны и некодирующие последовательности. Остаются чистые гены, почти без примесей. Но реорганизация генома не сводится к удалению мусора. Происходит также "распутывание" - сборка работающих генов из разрозненных и перепутанных обрывков. Как мы помним, многие гены в генеративном геноме разорваны на мелкие кусочки и перемешаны. В промежутках между этими кусочками могут находиться длинные некодирующие вставки. Это не обычные интроны, которые удаляются при сплайсинге (интроны у инфузорий тоже есть, но они входят в состав сохраняемых фрагментов). Это особые, характерные только для инфузорий "лишние" куски генома, удаляемые при формировании вегетативного генома макронуклеуса.
Например, в генеративном геноме ген может иметь такую структуру: 2X7X5X4X8X1X3X6 (цифрами обозначены "рабочие" фрагменты гена, буквой X - "ненужные" вставки различной длины). В вегетативном геноме этот ген будет выглядеть так: 12345678.
Откуда клетка знает, в каком порядке нужно соединять обрывки? До сих пор ответа на этот вопрос не было.
Исследователи из Принстонского университета установили, что для "распутывания" генетической информации инфузории используют образцы (матрицы), представляющие собой молекулы РНК, считанные с нанохромосом макронуклеуса (МАК-хромосом) перед тем, как макронуклеус был разрушен.

РНК-матрица, считанная с МАК-хромосомы перед разрушением макронуклеуса, служит "ключом" для распутывания генетической информации, содержащейся в МИК-хромосоме. Черным цветом обозначены концевые участки хромосом - теломеры. Чтобы это выяснить, пришлось провести много сложных экспериментов.
Для проверки гипотезы о роли РНК-матриц в сборке МАК-хромосом исследователи воспользовались методом РНК-интерференции. Инфузорий кормили генно-модифицированными бактериями, производящими двухцепочечные молекулы РНК, совпадающие по последовательности нуклеотидов с фрагментом одной из МАК-хромосом. Эукариотические клетки относятся к двухцепочечным РНК с опаской, принимают их за вирусов и начинают уничтожать все РНК с такой последовательностью нуклеотидов, в том числе и обычные, одноцепочечные. На этом основана методика "выключения" генов. Идея состояла в том, что, поев бактерий, инфузория сама уничтожит одну из РНК-матриц, необходимых ей для сборки МАК-хромосом. Так и вышло. В результате после конъюгации получились инфузории, у которых соответствующий участок одной из МАК-хромосом оказался собран неправильно или вообще не собран - просто оставлен в том виде, в каком он был в МИК-хромосоме. При этом все остальные МАК-хромосомы были собраны правильно.
Стало быть, РНК-матрицы действительно участвуют в программируемой перестройке генома. Но что они собой представляют - являются ли они копиями целых нанохромосом или отдельных их участков?
Исследователи стали выделять и анализировать РНК из инфузорий на разных стадиях жизненного цикла. Выяснилось, что через несколько часов после конъюгации (как раз тогда, когда старый макронуклеус разрушается, а новый начинает формироваться) в клетках появляются длинные транскрипты (молекулы РНК), соответствующие целым МАК-хромосомам вместе с концевыми участками - теломерами. Через 30-50 часов после конъюгации эти транскрипты исчезают.
Таким образом, перед тем как уничтожить макронуклеус вместе с вегетативным геномом, клетка снимает "резервную копию" с каждой МАК-хромосомы. Эта копия, представляющая собой молекулу РНК, в дальнейшем используется как образец для сборки новых маленьких и аккуратных МАК-хромосом из того безобразия, которое записано в МИК-хромосомах.
Следующий вопрос состоял в том, насколько точно РНК-матрицы регулируют процесс сборки МАК-хромосом и можно ли управлять этим процессом, внедряя в клетку искусственные РНК-матрицы? Исследователи синтезировали несколько молекул РНК, похожих на "настоящие" РНК-матрицы, но с измененным порядком фрагментов. Например, если для МИК-гена со структурой 2X7X5X4X8X1X3X6 правильная РНК-матрица имеет вид 12345678, то в искусственной матрице какую-нибудь пару фрагментов меняли местами (например, так: 13245678).
Впрыскивание таких матриц в инфузорий после конъюгации приводило к формированию МАК-хромосом двух типов: одни воспроизводили правильный порядок фрагментов (ведь правильные матрицы из клеток не удалялись), другие - тот, который присутствовал в искусственных матрицах. Напомним, что каждая МАК-хромосома в макронуклеусе присутствует в огромном количестве копий. Таким образом, РНК-матрицы осуществляют весьма точное управление процессом сборки МАК-хромосом, и при помощи искусственных матриц можно направлять этот процесс в желаемую сторону.
Следующий важный вопрос: регулируют ли РНК-матрицы сборку только тех генов, которые в генеративном геноме перемешаны (то есть имеют неправильный порядок фрагментов) или же этот механизм универсален и применяется ко всем генам без исключения?
Исследователи изготовили и ввели в инфузорий РНК-матрицы с неправильным порядком фрагментов для тех генов, которые в генеративном геноме не перемешаны и потому в "распутывании" не нуждаются (из них нужно только вырезать "лишние" куски). В итоге соответствующие гены в МАК-хромосомах оказались неправильно собраны. Значит, механизм универсален.
Из этого, кстати, следует интересный эволюционный вывод. Поскольку у инфузорий уже развилась универсальная система "распутывания" измельченных и перепутанных генов, дальнейшая фрагментация МИК-генов и перестановки их частей уже не будут отсеиваться отбором. Ведь есть распутывающий механизм, ему всё равно, он всё исправит. Видимо, потому-то МИК-геномы инфузорий и пришли постепенно в состояние хаоса.
Предполагают, что система изначально могла развиться просто для удаления лишних кусков генома, а "распутывающая" функция ее возникла при этом автоматически, сама собой, как некий довесок - сначала ненужный, но потом ставший необходимым.
Таким образом, информация о последовательности, в которой нужно сшивать обрывки генов генеративного генома, передается потомству инфузорий "неклассическим" способом - в виде молекул РНК. А ведь это не такая уж маленькая часть наследственной информации!
Могут ли РНК-матрицы передавать потомству также и информацию о последовательности отдельных нуклеотидов? До сих пор речь у нас шла только о последовательности фрагментов генов, то есть о кусках длиной в десятки и сотни нуклеотидов. Каждый ген, как известно, может существовать в виде нескольких аллелей, различающихся единичными нуклеотидными заменами или вставками. Поэтому соответствие РНК-матрицы и собираемых на ее основе МАК-хромосом далеко не всегда является абсолютным. Отдельные нуклеотиды могут различаться, и это не мешает правильной сборке.
В принципе, не исключено, что какие-то нуклеотидные замены могут передаваться из РНК-матрицы в собираемую МАК-хромосому. Конечно, инфузориям нет смысла переносить в МАК-хромосому все различия такого рода. Ведь тогда МАК-хромосомы после конъюгации оставались бы полностью идентичными материнским, и конъюгация потеряла бы всякий смысл. Но, как выяснилось, некоторые нуклеотидные замены все-таки переносятся в МАК-хромосомы из РНК-матриц. Это, однако, происходит не по всей длине собираемого гена, а только в непосредственной близости от мест "сшивки" фрагментов. Это очень важный факт, однозначно свидетельствующий о том, что в сшивке кусочков ДНК у инфузорий принимает участие только что открытый (у дрожжей) механизм починки ДНК на основе РНК-матриц.
Могут ли подобные системы редактирования генома, основанные на использовании РНК-матриц, работать и у других организмов, а не только у инфузорий? Почему бы и нет? Нужно искать. Череда открытий последних лет однозначно показывает, что живая клетка по-прежнему таит в себе множество неизвестных нам молекулярных механизмов, в том числе и таких, которые используются для целенаправленного изменения собственного генома.
Читайте также:


