Хирургия эхинококкоза шевченко назыров
Представлены данные литературы по эхинококкозу печени. Подробно описаны различные классификации, современные методы инструментальной и лабораторной диагностики, а также эффективные способы лечения. Эхинококкоз печени, оставаясь достаточно распространенным заболеванием, требует своевременной диагностики. Консервативное и хирургическое лечение эхинококкоза дополняют друг друга и требуют индивидуального подхода. Для профилактики рецидива заболевания обязательным компонентом лечения должна быть химиотерапия альбендазолом.
Ключевые слова:
печень, эхинококкоз, классификация, диагностика, лечение, резекция, перицистэктомия, PAIR, альбендазол, liver, echinococcosis, classification, diagnosis, treatment, resection, pericystectomy, PAJR, albendazole
Литература:
1.Альперович Б.И. Оперативные вмешательства при эхинококкозе, их классификация. Анналы хирургической гепатологии. 1999; 4 (1): 104-106.
2.Альперович Б.И. Эхинококкоз печени. Лечение, профилактика и прогноз. Хирургия печени. М.: ГЭОТАР МЕД, 2010. C. 197-207.
3.Амиреев С.А., Бекшин Ж.М., Муминов Т.А., Лобзин Ю.В., Брико Н.И., Покровский В.И., Сергиев В.П. Стандартные определения случаев и алгоритмы мероприятий при инфекционных болезнях. Практическое руководство. 2-е изд., доп. Алматы, 2014. 638 с.
4.Бабабейли Э.Ю., Джифтчи Э., Бабабейли Н.Э. Мини инвазивные и малотравматичные методы лечения эхинококкоза печени. Хирургия. Бaку. 2012; 29 (1): 69-74.
5.Бабабейли Э.Ю., Джифтчи Э., Бабабейли Н.Э. Пункция и катетеризация эхинококковых кист. Хирургия. Бaку. 2012; 32 (4): 48-53.
6.Бабабейли Э.Ю. Сравнительная характеристика методов хирургического лечения больных с эхинококкозом. Вестник хирургии Казахстана. 2013; 3: 11-14.
7.Бронштейн А.М., Малышев Н.А., Жаров С.Н., Легоньков Ю.А., Лучшев В.И., Рахимова О.Ю. Эхинококкозы (гидатидозный и альвеолярный) - пограничная проблема медицинской паразитологии и хирургии (обзор и собственные наблюдения). Российский медицинский журнал. 2012; 3: 50-53.
8.Бронштейн А.М., Малышев Н.А. Руководство по гастроэнтерологии. Под ред. Ф.Ф. Комарова, С.И. Рапопорта. М.: МИА, 2010. С. 657-692.
9.Ветшев П.С., Мусаев Г.Х., Буслик С.В. Эхинококкоз: cовременное состояние проблемы. Украинский журнал хирургии. 2013; 22 (3): 196-201.
10.Гулов М.К., Калмыков Е.Л., Зардаков С.М., Мухаббатов Д.К., Садриев О.Н. Эхинококкоз печени: роль компьютерной томографии и морфологической диагностики состояния ткани печени. Российский медико-биологический вестник имени академика И.П. Павлова. 2016; 24 (4): 104-110. DOI: 10.23888/pavlovj20164104-111.
11.Домашенко О.Н., Шаталов А.Д., Паниева Д.С. Эхинококкоз печени: диагностика, лечебная тактика. Медицинские науки. Клиническая медицина. 2016; 39 (3): 35-39.
12.Дягилева Т.С. Альвеококкоз и эхинококкоз печени. Диагностика и хирургическое лечение. Якутск, 2002. С. 3-17.
13.Ибадильдин А.С., Кузьмин Д.Ю. Алгоритм диагностики и лечения осложненного эхинококкоза печени. Вестник хирургии Казахстана. 2012; 1: 32-33.
14.Сергиев В.П., Лобзина Ю.Л., Козлова С.С. Паразитарные болезни человека (протозоозы и гельминтозы). Руководство для врачей. СПб.: Фолиант, 2008. 592 с.
15.Сергиев В.П., Ющук Н.Д., Венгеров Ю.Я., Завойкин В.Д. Тропические болезни. Руководство для врачей. М.: БИНОМ, 2015. С. 535-548.
16.Сергиев В.П., Легоньков Ю.А., Полетаева О.Г. и др. Эхинококкоз цистный (однокамерный). Клиника, диагностика, лечение, профилактика. Информационно-методи ческое пособие. М., 2008. 33 с.
17.Brunetti E., Kern P., Vuitton D.A. Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans. Acta Tropica. 2010; 114 (1): 1-16. DOI: 10.1016/j.actatropica.2009.11.001.
18.Kjossev K.T., Losanoff J.E. Classification of hydatid liver cysts. J. Gastroenterol. Hepatol. 2005; 20 (3): 352-359. DOI.org/10.1111/j.1440-1746.2005.03742.x.
19.Касыев Н.Б., Айтназаров М.С., Нурбекова А.Н. Иммунохемилюминесценция в диагностике эхинококкоза. Вестник науки и образования. 2016; 7 (19): 96-98.
20.Краснов Е.А., Климова Н.В., Дарвин В.В., Цыкура В.А., Лысак М.М. Визуализационная диагностика различных форм эх инококкоза печени. Вестник СурГУ. Медицина. 2016; 2 (28): 39-47.
21.Поляков Н.В., Ромих В.В., Поляков В.Е. Однокамерный (гидатидный) эхинококкоз. Исследования и практика в медицине. 2015; 2 (1): 27-35.
22.Толстокоров А.С., Гергенретер Ю.С., Яицкий С.В. Эхинококкоз печени. Учебно-методические рекомендации. Саратов, 2011. С. 9-15.
23.Комилов Т.С., Мирходжаев И.А. Особенности диагностики и пути улучшения результатов хирургического лечения эхинококкоза печени. Анналы хирургической гепатологии. 2004; 9 (2): 104-107.
24.Скипенко О.Г., Паршин В.Д., Шатверян Г.А., Беджанян А.Л., Ратникова Н.П., Ганиев Ф.А., Завойкин В.Д., Боева И.А. Эхинококкоз печени: современные тенденции в хирургической тактике. Анналы хирургической гепатологии. 2011; 16 (4): 34-39.
25.Ничитайло М.Е., Буланов К.И., Черный В.В., Саенко В.Ф. Хирургическое лечение эхинококкоза печени. Анналы хирургической гепатологии. 2001; 6 (1): 40-46.
26.Четвериков С.Г., Закария Мохаммад Ахмад. Проблемные вопросы выбора метода лечения эхинококкоза печени. Вестник Украинской медико-стоматологической академии. 2013; 13 (1;41): 184-186.
27.Dogru D., Kiper N., Ozcelik U., Yalcin E., Gocmen A. Medical treatment of pulmonaryhydatid disease: for which child? Parasitology Internat. 2005; 54 (2): 135-138. DOI: 10.1016/j.parint.2005.02.003.
28.Arif S.H., Shams Ul.B., Wani N.A., Zargar S.A., Wani M.A., Tabassum R., Hussain Z., Baba A.A., Lone R.A. Albendazole as an adjuvant to the standard surgical management of hydatid cyst liver. Int. J. Surg. 2008; 6 (6): 448-451. DOI: 10.1016/j.ijsu.2008.08.003.
29.Bradley M., Horton J. Assessing the risk of benzimidazole therapy during pregnancy. Trans. RSoc. Trop. Med. Hyg. 2001; 95 (1): 72-73.
30.WHO-Informal Working Group on Echinococcosis. Guidelines for treatment of cystic and alveolar echinococcosis in humans. Bull. World Health Organ. 1996; 74 (3): 231-242.
31.New Dimensions in Hydatidology in the New Millennium: Proceedings of the 20th International congress of hydatidology. June 4-8, 2001, Kusadasi, Turkey. Acta Trop. 2003; 85 (2): 103-293.
32.Калиева Д.К. Эхинококкоз. Актуальные вопросы хирургического лечения. Наука и здравоохранение. 2014; 6: 4-7.
33.Filice C., Brunetti E., Bruno R., Crippa F.G. Percutaneous drainage of echinococcal cysts (PAIR: puncture, aspiration, injection, reaspiration): results of a worldwide survey for assessment of its safety and efficacy. Gut. 2000; 47 (1): 156-157. DOI: 10.1136/gut.47.1.156b.
34.Morris D.L., Taylor D.H. Echinococcus granulosus: Development of resistance to albendazole in an animal model. J. Helminthol. 1999; 64 (2): 171-174. DOI: 10.1017/S0022149X00012098.
35.Peter K. Clinical features and treatment of alveolar echinococcosis. Curr. Opin. Infect. Dis. 2010; 23 (5): 505-512. DOI: 10.1097/QCO.0b013e32833d7516.
36.Шевченко Ю.Л., Назыров Ф.Г. Хирургия эхинококкоза. М.: Династия, 2016. С. 129-151.
37.Давыдова И.В., Легоньков Ю.А., Бронштейн А.М., Межгихова Р.М. Гидатидозный эхинококкоз мышц: oписание случаев и обзор литературы. Медицинская паразитология. 2007; 4: 53-56.
38.Busić Z., Kolovrat M., Kopljar M., Servis D., Cavka V., Patrlj L., Busić N., Cavka M., Nikolić I. Laparoscopic surgery for large hydatide liver cyst after two previous laparotomies. Coll. Antropol. 2014; 38 (2): 577-581. DOI: 10.1080/00015458.2006.11679982.
39.Jiang Y., Peng X., Zhang S., Wu X., Yang H., Sun H. Echinococcus of the liver treated with laparoscopic subadventitial pericystectomy. Surg. Laparosc. Endosc. Percutan. Tech. 2013; 23 (2): 49-53. DOI: 10.1097/sle.0b013e3182680620.
40.Калиева Д.К. Методы санации остаточной полости при эхинококкэктомии. Медицина и экология. 2016; 3: 23-28.
41.Кубышкин В.А., Вишневский В.А., Кахаров М.А., Икрамов Р.З., Гаврилин А.В. Эволюция методов хирургического лечения эхинококкоза печени. Анналы хирургической гепатологии. 2002; 7 (1): 18-22.
42.Tagliocozzo S., Miccini M., Amore Bonapasta S., Gregori M., Tocchi A. Surgical ofhydatid disease of the liver: 25 years of experience. Am. J. Surg. 2011; 201 (6): 797-804. DOI: 10.1016/j.amjsurg.2010.02.011.
43.Akbulut S., Senol A., Sezgin A., Cakabay B., Dursun M., Satici O. Radical vs conservative surgery for hydatid liver cysts: experience from single center. World J. Gastroenterol. 2010; 16 (8): 953-959. DOI: 10.3748/wjg.v16.i8.953.
44.Шевченко Ю.Л., Харнас С.С., Самохвалов А.В., Лотов А.Н. Эволюция методов хирургического лечения эхинококкоза печени. Хирургия. Журнал им. Н.И. Пирогова. 2004; 7: 49-55.
45.Reuter S., Jensen B., Buttenschoen K., Kratzer W., Kern P. Benzimidazoles in the treatment of alveolar echinococcosis: a comparative study and review of the literature. J. Antimicrob. Chemother. 2000; 46 (3): 451-456.
46.Abu-Eshy S.A. Clinical characteristics, diagnosis and surgical management of hydatid cysts. WAJM. 2006; 25 (2): 144-152. DOI: 10.4314/wajm.v25i2.28266.
47.Atmatzidis K.S., Pavlidis T.E., Papaziogas B.T., Mirelis C., Papaziogas T.B. Recurrence and long-term outcome after open cystectomy with omentoplasty for Hepatic hydatid disease in an endemic area. Acta Chir. Belg. 2005; 105 (2): 198-202.
48.Yagci G., Ustunsoz B., Kaymakcioglu N., Bozlar U., Gorgulu S., Simsek A., Akdeniz A., Cetiner S., Tufan T. Results of surgical, laparoscopic, and percutaneous treatment for hydatid disease of the liver: 10 years experience with 355 patients. World J. Surg. 2005; 29 (12): 1670-1679. DOI: 10.1007/s00268-005-0058-1.
49.Gharbi H.A., Hassine W., Brauner M.W., Dupuch K. Ultrasound examination of the hydatic liver. Radiology. 1981; 139 (2): 459-463.
50.Вишневский В.А., Ефанов М.Г., Икрамов Р.З, Назаренко Н.А., Чжао А.В. Эхинококкоз печени. Хирургическое лечение. Доказательная гастроэнтерология. 2013; 2: 18-25.
Literature data for liver echinococcosis are reviewed. Various classifications, modern instrumental and laboratory diagnostic methods as well as effective treatment are analyzed. Liver echinococcosis requires timely diagnosis as a common disease. Conservative and surgical methods for echinococcosis complement each other and require individual approach. Chemotherapy with albendazole is mandatory to prevent recurrence.
Keywords:
печень, эхинококкоз, классификация, диагностика, лечение, резекция, перицистэктомия, PAIR, альбендазол, liver, echinococcosis, classification, diagnosis, treatment, resection, pericystectomy, PAJR, albendazole
Среди паразитарных заболеваний печени к объемным поражениям ее приводят эхинококкоз и альвеококкоз. Первый протекает с образованием кист печени, второй — опухоленодобных новообразований.
Эхинококкоз (гидатидный эхинококк) — хроническое заболевание, обусловленное поражением печени или других органов человека личинками ленточного гельминта. Наибольшее распространение эхинококкоз имеет в Австралии, Новой Зеландии, Южной Америке, Северной Африке и Монгольской Народной Республике, в СССР — на юге Украины и Казахстана, в Закавказье, Крыму. Молдавии. Якутии и Западной Сибири.
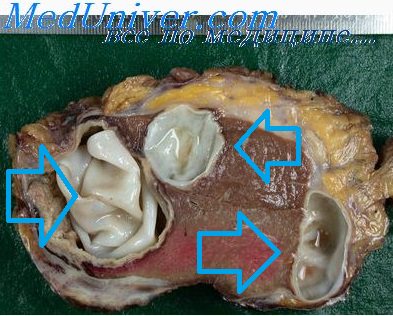
В патогенезе эхинококкоза большое значение имеет сенсибилизация организма человека продуктами обмена веществ паразита. Она приводит к аллергической перестройке, проявляющейся крапивницей, эозинофилией и пр. При рачрыые поверхностно лежащего эхинококкового пузыря возможен анафилактический шок с летальным исходом. Одновременно происходит обсеменение брюшной полости сколексами с образованием в последующем новых пузырей. Вторичная бактериальная нифекция приводит к нагноению пузыря. При гибели паразита происходит обызвествление его стенок. Эхинококковые кисты печени растут очень медленно, хотя иногда достигают огромных размеров и содержат 10 л и более жидкости. Чаще они бывают одиночными и локализуются в правой доле печени, по встречаются и множественные кисты. При тотальном поражении печень на разрезе напоминает медовые соты.
С клинической точки зрения в течении эхинококкоза печени целесообразно условно различать три стадии: I стадия — с момента заражения до первых клинических проявлений. Продолжительность ее различна, иногда несколько десятков лет. Состояние больных обычно не нарушается; II стадия — наблюдаются различные симптомы, связанные с увеличением размеров растущей кисты, оказывающей давление па окружающие органы. Больные отмечают тупые боли, чувство тяжести в правом подреберье, эпигастральной области или в нижнем отделе грудной клетки. Иногда присоединяются слабость, одышка, утомляемость, периодически появляются аллергические реакции в виде крапивницы, поноса, тошноты, рвоты. У ряда больных прощупывается опухолевидное образование в верхней половине живота или увеличение печени; III стадия — возникают симптомы, обусловленные различными осложнениями эхпиококкоза: разрывом поверхностно расположенной кисты или прорывом ее в одни из полых органов (желудок, кишки, бронх, желчный пузырь, виутрипеченочные протоки), плевральную или брюшную полость, наружу. Частым осложнением эхпиококкоза является нагноение кисты, которое может привести к тяжелому септическому состоянию.
В диагностике эхинококкоза печени большое значение имеет рентгенологическое исследование. С его помощью обнаруживают обызвествление кисты или контуры се стенок на фоне пневмоперитонеума, а также косвенные признаки кисты: высокое стояние или деформацию купола диафрагмы, смещение желудка или петель тонкой кишки. При селективной серийной ангиографии наблюдаются характерное дугообразное оттеснение сосудов печени и накопление контрастного вещества между кутнкулярной оболочкой кисты и фиброзной капсулой. Путем радиоизотопного сканирования печени выявляется округлый дефект накопления препарата. При лапароскопии удается видеть поверхностно расположенные паразитарные кисты печени.
Важное диагностическое значение имеют биологические тесты: внутрикожная проба Казони (со стерильной жидкостью эхинококковой кисты), реакция агглютинации с латексом (синтетическая полистирольная смола, используемая как адсорбент антигенов) и реакция непрямой гемагглютннаиии. Две последние пробы являются более точными и безопасными (при пробе Казони возможны тяжелые анафилактические реакции). Кроме того, они позволяют производить повторные исследования, что важно для выявления рецидива эхпиококкоза после операции. Эозинофилия (более 4%) должна приниматься во внимание, особенно при наличии признаков эхинококкоза. однако она может наблюдаться и при других заболеваниях. Большее значение имеет проба Анфилогова: увеличение количества эозинофилов после пальпации кисты (в случае гибели паразита этот симптом отсутствует).
Аннотация научной статьи по клинической медицине, автор научной работы — Шевченко Ю.Л., Назыров Ф.Г., Акбаров М.М., Сайдазимов Е.М., Сирожитдинов К.К.
MODERN ASPECTS OF SURGERY OF THE COMPLICATED LIVER ECHINOCOCCOSIS
Шевченко Ю.Л., Назыров Ф.Г., Акбаров М.М. и др. СОВРЕМЕННЫЕ АСПЕКТЫ ХИРУРГИИ ОСЛОЖНЕННОГО ЭХИНОКОККОЗА ПЕЧЕНИ
СОВРЕМЕННЫЕ АСПЕКТЫ ХИРУРГИИ ОСЛОЖНЕННОГО ЭХИНОКОККОЗА ПЕЧЕНИ
Шевченко Ю.Л.1, Назыров Ф.Г.2, Акбаров М.М.2, Сайдазимов Е.М.2, УДК: 616.36-951.21-06-089(312)
Сирожитдинов К.К.* 2 001: 10.2588VBPNMSC.2018.56.85.005
1 Национальный медико-хирургический Центр имени НИ. Пирогова, Москва
2 Республиканский специализированный научно-практический медицинский центр хирургии им. акад. В. Вахидова, Ташкент, Республика Узбекистан
Все больные были распределены на две группы для исследования: основная группа - 140 больных (оперированных с 2012 по 2016 гг.) и контрольная группа - 116 пациентов (оперированных с 2007 по 2011 гг.). Разделение больных основывалось на внедрении с 2012 года усовершенствованной лечебно-диагностической тактики.
Предложенный алгоритм выбора тактики лечения показал высокую эффективность в плане объективной дооперационной оценки, а также в повышении качества оказываемой хирургической помощи. Совершенствование тактико-технических аспектов хирургического лечения осложненного эхинококкоза печени на основании предложенного алгоритма позволило увеличить долю положительных результатов с 70,7% до 87,9%, снизить частоту специфических интра- и послеоперационных осложнений с 33,6% до 7,9%, летальности с 2,6% до 0,7% (P Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Материалы и методы исследования
Табл. 1. Распределение больных по группам и виду осложнения ЭП
Вид осложнения ЭП Основная группа Контрольная группа Всего
Прорыв в брюшную полость 44 17,2% 41 16,0% 85 33,2%
Прорыв в плевральную полость 6 2,3% 5 2,0% 11 4,3%
Прорыв в желчные протоки 16 6,3% 9 3,5% 25 9,8%
Итого 140 54,7% 116 45,3% 256 100,0%
Распределение больных по группам исследования и видам осложнений ЭП отображено в табл. 1.
Распределение больных на первичный и рецидивный ЭП показало, что в обеих группах отмечена приблизительно одинаковое соотношение. Так, в контрольной группе было 94 (81%) пациента с первичной формой заболевания и 22 (19%) с рецидивом. В основной группе эти показатели составили 112 (80%) и 28 (20%) соответственно.
При прорыве ЭП в брюшную полость открытая ЭЭ из печени и брюшной полости с дренированием ОП, санацией брюшной полости выполнена у 41 (93,2%) больного в основной группе и 27 (65,9%) в контрольной группе. Открытая ЭЭ из печени и брюшной полости с ушиванием ОП, санация произведена только у 3 (6,8%) больных в основной группе и 14 (34,1%) в контрольной группе.
При прорыве ЭП в плевральную полость в основной группе операции выполнены через лапаротомный и торакотомный доступы - 6 пациентов, тогда как в контрольной группе в большинстве случаев (4 из 5) операция выполнялась только через лапаротомный доступ.
При ЭП, осложненным прорывом в билиарные протоки открытая ЭЭ из печени с дренированием ОП, ХЭК, холедохотомия, экстракция хитина из холедоха, дренирование по Керу выполнена у 1 (6,3%) пациента в основной группе и 6 (66,7%) больных в контрольной группе. Аналогичное вмешательство, но с ушиванием ОП выполнено
Шевченко Ю.Л., Назыров Ф.Г., Акбаров М.М. и др. СОВРЕМЕННЫЕ АСПЕКТЫ ХИРУРГИИ ОСЛОЖНЕННОГО ЭХИНОКОККОЗА ПЕЧЕНИ
у 2 (12,5%) и 2 (22,2%) больных соответственно. Этапное вмешательство: ЭРХГ с ЭПСТ и экстракцией хитина из холедоха; открытая ЭЭ с дренированием ОП, ХЭК с дренированием холедоха по Холстеду произведено у 10 (62,5%) больных в основной группе и только в 1 (11,1%) случае в контрольной группе. Еще в 3 (18,8%) этапное вмешательство выполнено с использованием резекционных технологий в связи с интрапаренхиматозным расположением кисты в центральных сегментах печени.
Вторым по частоте встречаемости после нагноения эхинококковых кист и не менее тяжелым осложнением ЭП, является прорыв содержимого кисты в билиарные пути. Проведение УЗИ должно быть одним из первых методов инструментального исследования больных с осложненным течением паразитарной кисты. Тем ни менее, для более полной детализации синтопической и скелетотопической картины паразитарного поражения необходимо дополнительное использование МСКТ.
Для практически всех больных с МЖ срочное выполнение диагностических и дооперационных лечебных манипуляций, в числе которых эндоскопическая ретроградная холангиография, папиллосфинктеротомия и чрескожная чреспеченочная холангиостомия, диктуется необходимостью в связи с прогрессированием холестаза, гнойного холангита, печеночно-клеточной недостаточности. Следующим этапом выполнялся один из видов оперативного
вмешательства, который включал эхинококкэктомию из печени, если до операции обнаруживался не до конца опорожненный билиарный проток, то проводилась холе-дохотомия, санация, дренирование холедоха, ликвидации желчного свища, обработка остаточной полости.
По результатам проведенного анализа разработана схема лечебно-тактического алгоритма ведения больных с осложненным ЭП, основанная на полипозиционной оценке клинической ситуации и применении всего комплекса лечебной тактики. Целью построение данного алгоритма явилось обобщение имеющего опыта, но с учетом доминирующих позиций при лечении данной патологии на современном этапе. А именно, исполь-
Шевченко Ю.Л., Назыров Ф.Г., Акбаров М.М. и др.
СОВРЕМЕННЫЕ АСПЕКТЫ ХИРУРГИИ ОСЛОЖНЕННОГО ЭХИНОКОККОЗА ПЕЧЕНИ
зовать возможности эндоскопических вмешательств с учетом конкретных клинических ситуаций, которые на наш взгляд являются определяющими в вопросе выбора оптимальной хирургической тактики.
При поступлении больных с осложненным ЭП необходима полипозиционная оценка степени вовлечении в процесс зоны интереса (магистральные сосуды печени, брюшная и плевральная полость) с использованием всего комплекса лучевой диагностики, эндоскопических и эндоваскулярных технологий.
В этой связи, основными задачами лечебно-диагностической тактики при ЭП осложненным прорывом в билиарные протоки, являются:
• Оценка степени печеночной недостаточности и определение показаний для проведения ЭФГДС;
• Экстренная ЭФГДС с ЭПСТ;
• При выраженном внутрипеченочном холестазе и нестабильной гемодинамике, а так же при анатомических условиях невозможности проведения ЭПСТ, рекомендована ЧЧХС.
• Окончательным этапом у больных с данным осложнением является ЭЭ из печени, холедохотомия с дренирование холедоха.
При прорыве ЭП в брюшную полость, лечебная тактика определяется санацией брюшной полости и ограничивается ЭЭ из печени с дренированием остаточной полости.
При прорыве ЭП в плевральную полость принципиальным моментом является изолированный доступ: трансторакальный - к плевральной полости и лапаро-томный - к печени, а так же изолированное дренирование этих областей с разобщением билиопульмонального соустья.
Разработанный алгоритм лечебно-диагностических мероприятий при осложненном ЭП основанный на факторной оценке ситуации в группах риска и современных позиций выбора хирургической тактики при данной патологии, позволяет улучшить результаты лечения этой тяжелой категории больных. Предложенный алгоритм детализирует диагностические подходы и оптимизацию выбора тактики хирургического лечения (Рис. 3).
Выбор тактики лечения больных с осложненным ЭП остается одной из актуальных задач современной хирургии. Все этапы госпитального периода требуют индивидуального подхода как к верификации тяжести развившегося осложнения и его последствий со стороны других органов и систем, так и к выбору оптимального метода лечения. Предложенный алгоритм выбора тактики лечения показал высокую эффективность в плане объективной дооперационной оценки, а также в повышении качества оказываемой хирургической помощи.
Полное удаление хитиновых оболочек
Частичное удаление хитиновых оболочек
ЭЭ из печени, холедохототомия с ЭЭ, дренирование холедоха, ликвидация ЦБС
Рис. 3. Лечебно-тактический алгоритм при осложненном ЭП
выполнением щадящей операции позволили снизить общую долю послеоперационных осложнений с 19,5% (9) до 9,1% (4) и соответственно достоверно сократить период госпитализации с 14,1±0,6 до 12,1±0,6 суток (Р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
12. Назиров, Ф.Г., Акилов, Х.А., Девятов, А.В. Химиотерапевтическая профилактика рецидивных и резидуальных форм эхинококкоза брюшной полости // Хирургия Узбекистана. - 2GG1. - № 3. - С. 78. [Nazyrov, F.G., Akilov, X.A., Devyatov, A.V. Himioterapevticheskaya profilaktika recidivnix i rezidualnix form exin-okokkoza bryushnoy polosti// Xirurgiya Uzbekistana. 2GG1. 3 st, 78].
13. Саид, А.Х., Митьков, В.В. Ультразвуковая диагностика эхинококкоза печени. //УЗД. - 1999. - №4. - с. 5—10.[Said, A.X Mitkov, V.V. Ultrazvukovaya diagnostika exinokkokoza pecheni // UZD 1999. I 4 st/ 5-10].
15. Angheben, A., Mariconti, M., Degani, M. et al. Is there echinococcosis in West Africa? A refugee from Niger with a liver cyst. // Parasit Vectors. 2017 May 11; 10(1): 232.
16. Changing concepts in the management of liver hydatid disease / C. Dervenis et al. // J Gastrointest. Surg. 2005. - № 9 (6). - P. 869-77.
17. Mentha, G., Morel, P., Giostra, E. et al. Risk in major hepatectomy. A executive series of 113 extensive hepatectomies // Schweiz. Med. Wochenschr. - 1995. - Vol. 125, N 39. - P. 1820-1824.
18. Mohkam, K., Belkhir, L., Wallon, M. et al. Surgical management of liver hydatid disease: subadventitial cystectomy versus resection of the protruding dome. // World J Surg. 2014 Aug; 38(8): 2113-21.

Введение
В настоящее время в России и странах СНГ эхинококкоз печени (ЭП) является одной из наиболее распространенных составляющих современной хирургической гепатологии. В последние годы вопреки широкому внедрению высокоинформативных методов обследования и высокотехнологичных методов хирургического лечения больных с ЭП, их количество продолжает увеличиваться, более того, отмечается заметный рост частоты его осложненных форм и рецидивов заболевания [3,6]. По мнению многих хирургов решить эту проблему можно за счет выполнения радикальных операций в объеме резекции печени и перицистэктомии [2,3,7 и др.], однако доля этих операций у них составляет 27,33 %. Следует отметить, что проблема рецидива ЭП даже после выполнения радикальных вмешательств не может быть полностью решена. А.Н. Лотов с соавт. (2011) подчеркивают, что при выборе метода операции следует принимать во внимание паразитарную природу заболевания и реальную возможность повторного заражения [4]. Ф.Г. Назыров с соавт. (2011), анализируя результаты лечения 724 больных ЭП, пришел к выводу, что рецидив этого заболевания строго связан с областью первичной локализации паразитарной кисты лишь в 26,6 % наблюдений, что ставит под сомнение целесообразность радикальных операций, сопровождающихся достаточно большим количеством осложнений [1,5].
Главными критериями оценки эффективности хирургического лечения ЭП являются низкий уровень ранних послеоперационных осложнений, ликвидация остаточной полости, снижение количества рецидивов заболевания. Все эти проблемы успешно решаются путем совершенствования методик закрытой эхинококкэктомии.
Материалы и методы
В основу работы положен опыт хирургического лечения 87 больных ЭП с локализацией кист в 7-8 сегментах. У 9 больных кисты были небольших размеров до 5 см в диаметре, у 39 до 10 см, у 31 до 15 см и у 8 более 15 см.
Неосложненное течение заболевания диагностировано у 58 человек (66,7 %), у 29 (33,3 %) имело место осложненное течение в виде наличия цистобилиарных свищей (17), объизвествления кист (3), нагноения (8), у одного больного произошла перфорация кисты с прорывом ее содержимого в плевральную полость.
Сравнение результатов основных клинических и биохимических методов исследования крови у больного показал, что заметных различий их в лабораторных показателях нет. Однако по мере увеличения размеров кисты отчетливо прослеживается появление и нарастание признаков скрытой печеночной недостаточности. Так при размере кист более 15 см в диаметре у больных в 80 % наблюдений была отмечена гипо и диспротеинемия, в 40 % случаев - увеличение АСТ и АЛТ. При осложненном течении заболевания выявлено увеличение С-реактивного белка.
Ключевыми этапами при выполнении эхинококкэктомии (ЭЭ) являются надежное предотвращение рецидива заболевания и максимально возможная ликвидация остаточной полости. Достижение необходимого эффекта при выполнении этих этапов операции возможно лишь при обеспечении полноценной ревизии полости кисты и свободных манипуляций для ликвидации ЦБС и остаточной полости. Оптимальное решение этих задач в первую очередь зависит от адекватного хирургического доступа.
При локализации кист в 7-8 сегментах печени даже при мобилизации правой доли печени наибольшие сложности возникают при ликвидации ЦБС и остаточной полости. При больших размерах кист манипуляции, выполняемые из правостороннего подреберного доступа весьма затруднительны. Наш опыт показывает, что использование торакофренолапаротомии облегчает задачу хирурга и позволяет снизить количество ранних послеоперационных осложнений и улучшить отдаленные результаты.
Обсуждение результатов
Из 87 больных с локализацией кист на диафрагмальной поверхности печени у 38 закрытая и полузакрытая эхинококкэктомии были выполнены из трансторакального доступа. Противопоказанием для использования этого доступа считаем размеры кист до 5 см в диаметре (12 больных), гигантские кисты более 20 см в диаметре (4 больных), а также нагноение кисты (8 больных).
Известно, что к рецидиву ЭП приводят наличие недиагностированных мелких эхинококковых кист, сохранение в фиброзной капсуле внедренных зародышевых элементов и обсеменение ими брюшной полости во время операции.
Первым шагом профилактики рецидива заболевания является осуществление надежной антипаразитарной обработки полости кисты. С этой целью используется различные активные химические вещества, однако большинство из них обладают или низкой противопаразитарной активностью или высокой токсичностью. Наиболее выраженным губительным действием на зародышевые элементы гидатидного эхинококка обладают 90 %-100% глицерин и 3 % перекись водорода. Более того, оболочки живых кист непроницаемы для этих веществ, что исключает их токсическое воздействие на организм больного.
У 58 больных с неосложненным течением заболевания для антипаразитарной обработки фиброзной капсулы использовали 90-100 % глицерин, при осложненном ЭП у 29 больных применяли 3 % перекись водорода.
Следующим этапом операции, обеспечивающим благоприятное течение раннего послеоперационного периода, является выявление и ликвидация цистобилиарных свищей. Это осложнение было выявлено у 17 больных, следует отметить, что при локализации кист в 7-8 сегментах ни разу не встретились ЦБС с тяжелой желтушной формой течения, обусловленной прорывом содержимого кисты в крупные желчные протоки. При выявлении ЦБС с вовлечением сегментарных и более мелких протоков, ликвидацию их осуществляли плазменной коагуляцией устья свища и ушивания его атравматическим шовным материалом.
Ликвидацию остаточной полости при неосложненном течении заболевания у 49 больных выполняли путем иссечения свободной фиброзной капсулы и вворачивания оставшейся ее части в санированную полость, у 37 больных остаточные полости были ликвидированы методом капитонажа, при наличии ЦБС на 2-3 дня в остаточной полости оставляли микроирригатор.
Осложнения в раннем послеоперационном периоде развились у 14 больных (16,1 %), у 4 больных 4,6 % эхинококкэктомия была выполнена из торакотомного доступа, у 10 - 11,5 % лапаротомного (табл.1).
Характеристики послеоперационных осложнений
Читайте также:


