Принципы комплексного лечения синдрома эндогенной интоксикации
Интоксикация - патологическое состояние, возникающее в результате действия на организм токсических (ядовитых) веществ эндогенного или экзогенного происхождения. Соответственно и различают эндогенные и экзогенные интоксикации.
Эндогенные интоксикаций классифицируются в зависимости от:
· заболевания, послужившего источником их возникновения (травматическая, радиационная, инфекционная, гормональная).
· от расстройства физиологической системы, которое привело к накоплению в организме токсических продуктов (кишечная, почечная, печеночная).
Интоксикация обычно наступает в результате действия циркулирующих в крови токсических веществ; циркуляция в крови эндогенных ядов чаще обозначается как токсемия, а циркуляция токсинов - как токсинемия.
Часто используются термины, указывающие вещество, находящееся в крови, например - азотемия.
По механизму развития можно различать следующие виды:
Ретенционные - вследствие затрудненного выведения и задержки выделений, например, при нарушениях выделительной способности почек, при накоплении углекислоты и обеднении кислородом крови и тканей в связи с расстройством дыхания.
Резорбционные - вследствие образования ядовитых веществ в полостях тела при гниении и брожении с последующим всасыванием продуктов распада, например, при гнойных процессах в полости плевры, мочевого пузыря либо в кишечнике при непроходимости, кишок, кишечных, инфекциях, или при длительном запоре.
Обменные - вследствие нарушения обмена веществ и изменения состава тканей, крови и лимфы, в результате чего происходит избыточное накопление в организме ядовито действующих веществ:
1. фенольных соединений,
2. азотистых оснований типа бетаина,
3. аммонийных веществ,
4. кислых продуктов промежуточного углеводного обмена ( молочная и др.).
Сюда можно отнести азотемии при эндокринных заболеваниях (диабете, микседеме, базедовой и аддисоновой болезнях, паратиреоидной тетании), при авитаминозах, злокачественных новообразованиях, при заболевании печени, когда интоксикация может наступить вследствие потери печенью способности обезвреживать ядовитые продукты.
Инфекционные - вследствие накопления бактериальных токсинов и др. продуктов жизнедеятельности микробов, а также продуктов распада тканей при инфекционных заболеваниях.
Может иметь место сочетание нескольких факторов. Так при уремии задержка ядовитых продуктов вследствие недостаточности функции почек сочетается с нарушениями обмена веществ. При патологии беременности аутоинтоксикация возникает вследствие задержки ядовитых продуктов обмена в материнском организме и одновременно вследствие нарушения обмена веществ и совершающихся процессов распада в организме плода.
Особое место занимает кишечная аутоинтоксикация, которой И.И.Мечников придавал большое значение в патологии человека. В кишечнике и в норме проходят процессы брожения и гниения. Эксперимент этого является действие экстрактов содержимого кишечника.
При внутривенном введении их экспериментальному животному наблюдались судорога, центральные параличи, остановка дыхания и коллапс. В нормальных условиях всасывающиеся ядовитые вещества легко обезвреживаются печенью, но в патологических условиях пищеварения в кишечнике усиливаются процессы гниения и брожения, вследствие чего накапливаются ядовитые вещества. Всасываясь в увеличенном количестве, они могут оказывать токсическое действие. Среди этих ядовитых веществ следует отметить некоторые ароматические соединения (фенол, крезол, скатол, индол), образующиеся из аминокислот в результате превращения боковой цепи, а также продукты декарбоксилирования аминокислот - путресцин, кадаверин.
Кишечная аутоинтоксикация наиболее выражена в случаях, когда усиленные процессы гниения и брожения в кишечнике сочетаются с ослаблением барьерной функции кишечника, печени и выделительной деятельности почек.
При различных экстремальных воздействиях (механическая травма, обширный ожог, массивная кровопотеря) аутоинтоксикация может развиваться в результате поступления в кровь эндотоксииа Escherichia coli, вызывающего функциональные нарушения в системе кровообращения. Плазма, полученная от животных с необратимым постгеморрагическим шоком, вызывает некроз слизистой оболочки тонкого кишечника, пирогенную реакцию и лейкопению у здоровых животных. Существует концепция, объясняющая механизм эндотоксемии при экстремальных состояниях различного происхождения. Известно, что всем видам шока присуща недостаточность кровообращения внутренних органов с последующим развитием тканевой гипоксии, неизбежно приводящей к повышению активности клеток ретикулоэндотелиальной системы (РЭС). В результате РЭС утрачивает способность нейтрализовать эндотоксин, непрерывно поступающий из кишечника в кровь через воротную вену. Количество циркулирующего постоянно эндотоксина увеличивается, что отражается на функции кровообращения; возникает порочный круг при котором накопление эндоксииа усугубляет нарушение кровообращения и прежде всего микроциркуляцию.
Биофизические механизмы, аутоинтоксикации.
В основе биофизических механизмов аутоинтоксикации лежат нарушения физико-химических процессов в организме. Известно, что в клетке существуют как ферментативные, так и неферментативные системы, инициирующие процессы перикисного окисления липидов клеточных мембран. В результате этих физико-химических процессов образуются продукты окисления липидов- гидроперикиси, перикиси, альдегиды и кетоны ненасыщенных жирных кислот. Эти продукты обладают значительной реактивной способностью они взаимодействуют с аминокислотами белков, нуклеиновыми кислотами и другими молекулами клетки, что приводит к инактивации ферментов, разобщению окислительного фосфорилирования, возникновению хромосомных аберраций. Образование перекисей ненасыщенных жирных кислот в фосфолипидах мембран способствует изменению проницаемости этих мембран. Ряд экстремальных факторов стимулируют ПОЛ и в первую очередь к ним относятся отравление ядами, действие ионизирующей радиации, стрессовые воздействия.
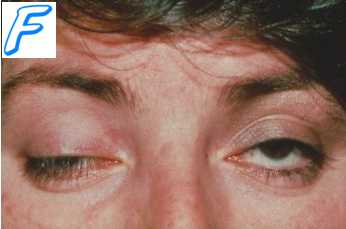
Клинические проявления аутоинтоксикации имеют свои особенности. Течение эндогенной интоксикации в значительной степени определяется характером основного заболевания. Так, например, для диффузного и токсического зоба характерны стойкая тахикардия, похудание, экзофтальм, симптомы токсического действия избыточного количества тиреоидных гормонов (тиреотоксикоз).
При хронической уремии отмечаются явления в местах выделения азотистых шлаков: в гортани, в глотке, желудочно-кишечном тракте, на коже обнаруживаются скопления кристаллов мочевины.
При хронической эндогенной интоксикации больные отмечают недомогание, раздражительность, разбитость, головную боль, головокружение, тошноту; наступает истощение, снижается резистентность организма. В ряде случаев аутоинтоксикация может протекать в форме тяжелого острого отравления (рвота, ступор, коматозное состояние). Такое течение характерно для острой почечной недостаточности, гепатаргии, острой ожоговой токсемии.
Возникновение аутоинтоксикации раньше представляли себе только как результат непосредственного воздействия эндотоксина на ткани и органы. Однако ядовитые продукты обмена, как и всякие другие биологически активные вещества, оказывают воздействия на органы и через центральную нервную систему. Возможно так же раздражение ими обширного поля рецепторных образований с последующим рефлекторным влиянием на разнообразные функции организма.
Таким образом, аутоинтоксикация (autos - сам + интоксикация) - самоотравление ядовитыми веществами, которые вырабатываются организмом как при некоторых нарушениях нормальной жизнедеятельности так и при различных заболеваниях. В основном вещества, вызывающие аутоинтоксикацию, представляют собой продукты обмена веществ или тканевого распада.
В нормальных условиях естественные метаболиты выделяются из организма (через почки с мочой, через толстую кишку с калом, через кожу с потом, через легкие с воздухом или различными секретами), либо подвергаются обезвреживанию в результате химического превращения в процессах промежуточного обмена веществ. Аутоинтоксикация возникает при патологических состояниях, когда защитные приспособления оказываются недостаточными, например, при нарушении функции выделительных органов или при расстройствах обмена веществ, а также при ненормальных процессах всасывания из различных полостей.
Основные принципы лечения:
1. При хирургической патологии - радикальное хирургическое вмешательство с удалением пораженного органа и эффективным дренированием. В некоторых случаях (например, при деструктивном холецистите, аппендиците), это удается сделать достаточно успешно, тем самым прерывается дальнейшее прогрессирование эндотоксикоза. В других случаях, например, при осложнении ЖКБ механической желтухой, радикальной операции может оказаться недостаточно, так как уже развились явления печеночной и печеночно-почечной недостаточности. Повышение эффективности лечения больных с механической желтухой может быть достигнуто с помощью патогенетически обоснованной коррекции нарушений гемостаза.
2. Устранение основного заболевания, которое послужило источником образования и накопления в организме эндогенных токсических веществ, например, при эндокринной недостаточности необходимо восполнение недостающего гормона, при уремии - восстановление функции почек, при инфекционной аутоинтоксикации - применение антибиотиков.
3. Устранение ядовитых веществ, например, при аутоинтоксикации углекислотой удаление ее избытка с помощью стимуляции дыхания, при аутоинтоксикации из полостей (кишок, матки, мочевого пузыря, плевральной, брюшной полостей) удаление содержимого промыванием или выведением его с помощью дренажа.
4. Обезвреживание ядовитых веществ прибавлением к промывающим жидкостям обеззараживающих средств либо введением их peros или внутривенно.
5. Усиление выделительной способности организма с помощью мочегонных, слабительных, патогенных средств.
6. Понижение концентрации ядовитых веществ введением в организм физиологических растворов, форсированный диурез, а при сильной аутоинтоксикации – плазмоферез, гемодиализ, гемосорбция.
Дезинтоксикационная терапия - лечебные меры, направленные на прекращение или снижение интенсивности действия на организм токсических веществ.
Имеющиеся в организме механизмы преодоления интоксикации антитоксическая функция печени и ретикулоцитарной системы, элиминация токсических веществ почками, органами желудочно-кишечного тракта и др.
При эндогенной интоксикации дезинтоксикационную терапию проводят в следующих направлениях.
1. Гемодилюция с целью снижения концентрации токсических веществ, циркулирующих в крови. С этой целью применяют обильное питье, па-рэнтералыюе введение изотонических растворов солей, глюкозы.
2. Улучшение кровоснабжения тканей и органов для ускорения вымывания токсических веществ. Этой цели служат внутривенное капельное введение реологически активных препаратов - низкомолекулярных декстранов (реополиглюкин, гемодез), обладающих также способностью связывать токсины и содействию выведения их с мочой.
3. Ускорение выведения токсических веществ с мочой, предпринимаемое, как правило, вслед за гемодилюцией и введения реологически активных препаратов и осуществляемое формированием диуреза с помощью значительных доз быстродействующих диуретических средств (фуросемид) при условии сохранения функции почек и при отсутствии артериальной гипертонии.
Методы внепочечного кровеочищения занимают особое место. К числу таких методов относятся плазмоферрез, перитонельный диализ, в/в лазерное, УФО облучение крови.
Проведение дезинтоксикационной терапии нуждается в систематическом клинико-лабораторном контроле, во избежание отрицательных для состояния больного ее последствий, которые могут быть обусловлены нарушением состава электролитов в организме и водного обмена. Основными осложнениями могут быть - гиперволемия и гипергидратация, ведущие к декомпенсации кровообращения с развитием анасарки, отека легких, головного мозга.
Более редкие побочные эффекты терапии - снижение толерантности миокарда к сердечным гликозидам, снижением эффективности антибиотиков и других препаратов, миграция конкрементов в желче- и мочевыводящих путях, аллергические реакции на вводимые препараты.
Водно-электролитные нарушения у хирургических больных и принципы инфузионной терапии. Показания, опасности и осложнения. Растворы для инфузионной терапии. Лечение осложнений инфузионной терапии.
Водно - солевой состав организмаВодно-солевой обмен (ВСО)- это совокупность процессов поступления воды и солей (электролитов) в организм, распределение их во внутренней среде и выведение. Системы регуляции ВСО обеспечивают постоянство суммарной концентрации растворенных частиц, ионного состава и КЩР, а также объема и качественного состава жидкостей организма.
Организм человека состоит в среднем на 65% из воды, которая находится в 3-х жидкостных фазах - внутриклеточной, внеклеточной и трансцеллюлярной. Наибольшее количество воды (40-45%) находится внутри клеток.
Внеклеточная жидкость включает (в процентах от массы тела) плазму крови (5%), межклеточную жидкость (16%) и лимфу (2%).
Трансцеллюлярная жидкость (1-3%) изолирована от сосудов слоем эпителия и по своему составу близка к внеклеточной. Это - спинномозговая и внутриглазная жидкости, а также жидкости брюшной полости, плевры, перикарда, суставных сумок и желудочно-кишечного тракта.
Вода свободно проходит через клеточные мембраны, выравнивая осмотическое давление внутриклеточной и внеклеточной жидкостей.
Измеряя осмолярность одного пространства (например, плазмы), мы оцениваем осмолярность всех жидкостных пространств организма.
Водный и электролитный балансы у человека рассчитываются по суточному потреблению и выделению воды и электролитов из организма.
Вода поступает в организм в виде питья - примерно 1,2 л и с пищей -примерно 1 л. Около 0,3 л воды образуется в процессе обмена веществ (из 100г жиров; 100 г углеводов и 100 г белков образуется 107, 55 и 41 мл воды соответственно).
Не нашли то, что искали? Воспользуйтесь поиском:
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Прогрессирование эндотоксикоза обусловлено накоплением в крови различных по происхождению, химической структуре и биологическому воздействию веществ, именуемых эндотоксинами. Эндотоксины способствуют развитию острой почечно-печеночной недостаточности, сердечно-сосудистой недостаточности, острого респираторного дистресс-синдрома, приводя в конечном итоге к появлению крайне тяжелого состояния - синдрома мультиорганной дисфункции.
Эндогенная интоксикация - клинический синдром, возникающий при различных по этиологии патологических состояниях, обусловленных накоплением в тканях и биологических жидкостях организма продуктов нарушенного обмена веществ, метаболитов, деструктивных клеточных и тканевых структур, разрушенных белковых молекул, pi сопровождающийся функциональными и морфологическими поражениями органов и систем организма.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Основным звеном патогенеза синдрома эндогенной интоксикации является токсемия. К сожалению, четкая дифференциация токсических веществ эндогенного происхождения практически невозможна. Однако в каждом конкретном случае можно выделить "первичные" и "вторичные" эндотоксины. Так, при ожогах, синдроме длительного раздавливания, облитерирующих сосудистых заболеваниях "первичными" являются продукты белковой деградации, "вторичными" - продукты естественного метаболизма, накопление которых в организме является следствием угнетения функций естественной детоксикации и экскреции.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
II стадия синдрома эндогенной интоксикации - стадия выраженной токсемии развивается после прорыва гастогематического барьера, когда в циркулирующую кровь попадают эндотоксины, образовавшиеся в первичном очаге интоксикации, с последующим распространением и накоплением в организме. В зависимости от состояния организма, его резистентности и исходного уровня детоксицирующих и иммунных систем выделяют компенсированную и декомпенсированную стадии выраженной токсемии.
III стадия синдрома эндогенной интоксикации - мультиорганной дисфункции (СМОД) наблюдается при дальнейшем прогрессировашш патологического процесса как следствие тяжелого повреждения эндотоксинами различных органов и систем с развитием их функциональной декомпенсацш!. Клинически эта стадия Проявляется нарушением сознания, гипоксией, выраженной сердечной Недостаточностью, олигурией, паралитической непроходимостью кишечника. В крови определяется высокая концентрация креатинина, мочевины, билирубина.
Главная 
Медицина 
Эндогенная интоксикация в хирургии
Вводят 15-20% раствор маннитола в дозе 1-1,5г. активного вещества на 1кг. Массы тела больного, а через 3-4 часа, когда темп диуреза начинает снижаться, добавляют по 20-40мг. лазикса каждые 3-4 часа.
3. Заключительный этап.
Поддержание диуреза. Восстановление ВЭБ, нормализация энергообеспечения за счет введения больших доз глюкозы, восполнение потребности в витаминах.
Чаще проводят вместе с перитонеальным промыванием полости брюшины после операции по поводу перитонита.
После окончания манипуляций на органах брюшной полости и санации их через отдельные проколы передней брюшной стенки в правом и левом подреберье вводят полихлорвиниловые трубки и укладывают их в правом и левом боковых каналах сверху вниз, включая полость малого таза. Малый таз дополнительно дренируют силиконовой трубкой. Перед зашиванием раны в брюшную полость вводят физиологический раствор, раствор 0,25% новокаина и гепарин. После перевода больного из операционной через 2 верхние трубки (нижняя перекрыта) 2-3 раза в сутки вводят диализирующий раствор в количестве 2-2,5л., проводят экспозицию его 40-60мин., после чего жидкость выпускают через нижний дренаж.
· Энтеросорбция (внутрикишечная детоксикация)
Метод активной детоксикации, основанный на связывании в просвете ЖКТ и выведении из него эндогенных и экзогенных веществ. Обеспечивается постоянное введение раствора с одновременной его аспирацией из просвета желудка и кишечника (лаваж) через назогастроинтестинальный зонд. Зонд чаще ставится интраоперационно. Осуществляется промывание кишечника солевыми сбалансированными растворами. Активную аспирацию кишечного содержимого проводят с разрежением 20-40 мм.рт.ст. После лаваж через тот же зонд пациенту вводят энтеросорбенты. В качестве энтеросорбентов (веществ, связывающих токсичные вещества в ЖКТ) применяют активированные угли и карбониты (полифепан, силикагели). Длительность пребывания зонда зависит от восстановления перистальтики кишечника и составляет 3-8 суток.
Восстановление нарушенного эндотоксинами метаболизма
- · Полноценное энтеральное и парентеральное питание
- · Инфузионно-трансфузионная терапия
- · Антигипоксанты, анаболические стероиды, витамины.
Искусственное удаление токсичных продуктов из организма
Методы искусственного удаления токсичных продуктов из организма имеют название методов экстракорпоральной детоксикации (эфферентные методы лечения - ЭМЛ). Они особенно ценны у больных с несостоятельностью системы выделения.
ЭМЛ - это трансфузиологические операции, направленные на изменение количественного и качественного состава крови в контуре кровообращения, который находится вне организма.
ЭМЛ осуществляются специально обученным врачом и реанимационной или операционной медсестрой. Они проводятся в операционной или реанимационной палате. Необходимо строгое соблюдение асептики. Больные должны быть обследованы. ЭМЛ регистрируют в операционном журнале и в истории болезни.
Эфферентные операции состоят из следующих этапов:
Премедикация. Назначают по показаниям больным при выраженных эмоциональных реакциях и при психомоторном возбуждении, а также при выраженном болевом синдроме. Она включает анальгетик, антигистаминный препарат и транквилизатор.
Обеспечение сосудистого доступа - периферические вены, катетеризация центральных вен, двухпросветный катетер, артериовенозный шунт.
Гемодилюция. Проводится при гиповолемии (снижении ОЦК) у больного с гемоконцентрацией, при содержании гемоглобина более 140 г/л. Проводится в/в инфузия в объеме 10-20 мл/кг. Применяются низкомолекулярные коллоиды и кристаллоиды, 5% глюкоза.
Стабилизация крови. Вводится гепарин в дозе от 50 до 350 ед/кг. При необходимости антикоагулянт вводят повторно в половинной дозе. Гепарин может вводиться в/в перед операцией, постоянно капельно во время операции
Основная часть операции.
Основные методы экстракорпоральной детоксикации
В основе лежит принцип диффузии и фильтрационного переноса через полупроницаемую мембрану низкомолекулярных токсических веществ и внутрисосудистой жидкости из циркулирующей в контуре крови в диализирующую жидкость.
Показания к гемодиализу:
- - острая почечная недостаточность любого генеза, в том числе при эндотоксикозе.
- - гиперкалиемия
- - гиперазотемия
- - острые отравления
- -хроническая почечная недостаточность.
- · Гемосорбция
Метод основан на выведении из крови больного токсичных субстанций эндогенной или экзогенной природы путем перфузии ее через сорбент. Большинство сорбентов имеют в основе активированный уголь. Для проведения гемосорбции используются специальные насосы и сорбционные колонки с сорбентом.
Показания к гемосорбции:
- - эндотоксикоз II-IIIст.
- - тяжелые формы инфекционных заболеваний (брюшной тиф, вирусный гепатит, дифтерия)
- - острые отравления
- - абстинентный синдром при наркомании и алкоголизме
- - некоторые психические заболевания (маниакальные и депрессивные состояния)
- - разрушение форменных элементов крови
- - обязательная гепаринизация ( при эндотоксикозе могут быть разные варианты патологии свертывания).
- · Лимфосорбция
Метод основан на дренировании грудного лимфатического протока с последующим пропуском лимфы через колонку с сорбентом. При этом сорбируются токсичные компоненты, а детоксицированная лимфа возвращается в сосудистое русло. Лимфосорбция позволяет удалять основную массу токсинов прежде, чем они попадут в кровь.
Показания к лимфосорбции:
- - острые деструктивные процессы в брюшной полости
- -острый панкреатит, панкреонекроз
- -острые отравления
- - большие потери лимфоцитов и тромбоцитов на сорбенте
- - частая невозможность дренирования грудного лимфатического протока (рассеянный тип строения).
- · Плазмаферез
В основе метода - разделение крови на плазму и форменные элементы, замена плазмы больного донорскими компонентами крови или кровезаменителями. Плазмаферез в объеме, приближающемся к общему объему плазмы называется плазмообменом.
Основные эффекты от плазмафереза:
иммунокоррекция (удаление из крови медиаторов воспаления)
улучшение реологии крови.
Показания к плазмаферезу:
- - гнойно-воспалительные процессы любой локализации с эндотоксикозом II-III ст.
- - тяжелые генерализованные формы инфекционных заболеваний
- - хронические аутоиммунные заболевания (бронх.астма, системные заболевания соединительной ткани, гематологические заболевания )
- - отравления гемолитическими ядами, синдром сдавления.
Если при плазмаферезе выведенная плазма не замещается компонентами крови или кровезаменителями, а сорбируется и возвращается обратно, эта операция называется плазмосорбцией. В результате улучшается эффект от плазмафереза. Плазмосорбция проводится при белковом дефиците, сохраняет все положительные качества плазмафереза и гемосорбции.
Плазмаферез делится на центрифужный (гравитационный) и мембранный (фильтрационный).
Аппаратный плазмаферез проводится на фракционаторах крови. Может удаляться до 2 объемов циркулирующей плазмы. Удаленная плазма может компенсироваться не только коллоидными и кристаллоидными растворами, но и замороженной плазмой и альбумином. Забранную плазму можно подвергнуть обработке и использовать при последующих операциях плазмафереза. Обработка плазмы в виде криопреципитации с последующей сорбцией, позволяет провести детоксикацию, удалить атерогенные факторы и ЦИК, сохранив полезные вещества, содержащиеся в плазме.
· Непрямое электрохимическое окисление крови
Метод заключается во введении в сосудистое русло больного раствора сильного окислителя - гипохлорита натрия (NaClO), получаемого экстракорпорально в электрохимических установках ЭДО-4 путем электролиза 0,9% раствора NaCl. В результате:
- - окисляются токсичные вещества
- - гипокоагуляция
- - подавление ферментативной активности крови
- - коррекция КОС
- - иммуностимуляция.
Гипохлорит натрия вводят в центральные вены (подключичная, бедренная) через катетер в концентрации 600мг/л в объеме 500мл. с темпом инфузии 40-60 капель в минуту. Обязательные условия: гематокрит менее 40%, ЦВД более 40 мм.вод.ст., общий белок в крови более 65 г/л., глюкоза крови более 6 ммоль/л. При наличии гемолиза НЭХО крови не проводится.
- - эндотоксикоз II-III ст.
- - острые отравления
- -гипогликемия
- - гипокоагуляция
- - возможно развитие гемолиза.
- · Ультрафиолетовое облучение крови
Метод основан на эффекте фотобиоактивации (изменение скорости метаболизма в результате воздействия энергии на разных уровнях). На уровне организма оказывает противовоспалительный, регенераторный, иммунокорригирующий, бактерицидный и бактериостатический, гипохолестеринемический, реологический эффекты.
- - эндотоксикоз во IIст.
- - вторичная иммунная недостаточностиь
- - артериальная гипоксемия
- - обратимые нарушения системы гемостаза (ДВС-синдром I-IIст.)
- - нарушение местных репаративных процессов.
При превышении дозы УФО развивается фотодеструкция и иммуносупрессия.
Хирургическое устранение источника интоксикации - основной метод детоксикационной терапии.
Развитие интенсивной терапии и реанимации, расширив пределы оживления, обнаружило ряд нерешенных проблем. ОдП ной из них следует считать проблему эндогенной интоксикации.
Современное представление об эндогенной интоксикации (ЭИ) связано, в первую очередь, с понятием полиорганной недоП статочности или множественной недостаточности органов, или синдромом 80Пютних, или МОБ Ииндромом.
Следует отметить, что среди составляющих синдрома поП лиорганных нарушений приоритетное значение традиционно отводилось и отводится нарушению кровообращения и дыхания, которые развиваются соответственно в 60 и 65% случаев. Тем не менее, достоверно установлено, что в исходе синдрома мультиорП тайных поражений существенную роль играют несостоятельность печени, почек, пищеварительного тракта, сопровождающие МОБ ? синдром соответственно в 60, 56 и 13% случаев. Таким образом, несостоятельность метаболического гомеостаза, развивающаяся вследствие печеночно Эючечной недостаточности, встречается столь же часто, сколь и сердечно Пгегочная недостаточность. ОдП нако клиническая картина нарушений метаболизма не проявля ? ется так ярко, как нарушения дыхания и кровообращения, осоП бенно на ранних этапах. Поэтому диагностика нарушенного меП таболизма, как правило, не поспевает за событиями развиваю ? щихся процессов, в том числе изЭа своего несовершенства, что зачастую приводит к констатации фактов при уже далеко зашедших или необратимых изменениях, определяющих неблагоприятный исход заболеваний.
Это делает проблему диагностики и лечения эндогенной интоксикации весьма актуальной и объясняет огромное число исследований в этой области. Поэтому основной целью изучения данной темы является умение установить наличие эндогенной интоксикации, определить ее характер и степень тяжести.
Эндогенную интоксикацию можно определить как нсспс цифический по большинству клинико [биохимических проявлений синдром несоответствия между образованием и выведением как продуктов нормального обмена, так и веществ нарушенного меП таболизма.
Приоритетное значение при этом приобрела концепция энП догенной интоксикации, рассматривающая последнюю как совой купность последствий нарушения макроциркуляции и микрогс молимфоциркуляции, реологии, газообмена и кислородного бюдП жета, иммунитета и противоинфекционной защиты, атакжеупП равления интеграцией этих процессов. Значение этой концепции важно потому, что эндогенная интоксикация рассматривается здесь с позиций общих закономерностей формирования полиорП тайных нарушений, неотъемлемой составной частью которых она является.
Наряду с этим, понятие эндогенной интоксикации базируй ется на концепции, представляющей детоксикацию не как сово ? купность функционирования отдельных органов (печени, почек, легких, пищеварительного тракта), а как систему, образуемую тремя взаимосвязанными составными частями: монооксигеназ? ной, иммунной, выделительной.
В характере иммунной и микросомальной реакции на токП сины прослеживаются черты сходства. И в первой, и во второй системе происходит индукция специфических белков, обеспечиП вающих связывание и метаболизм молекулы индуктора. Память о ксенобиотиках, метаболизируемых монооксигеназной системой, похожа на иммунную память: повторные введения низкомолекуП лярного ксенобиотика мощнее, чем в первый раз, активируют ферменты МОГ, подобно тому, как высота иммунного ответа возП растает при повторном введении антигена. Различные ксенобиоП тики при взаимодействии с оксидазами конкурируют за места свяП зывания аналогично конкуренции антигенов в процессах индукП ции синтеза антител.
Кроме того, многочисленные низкомолекулярные соединеП ния способны индуцировать иммунную реакцию, осуществляв ? мую в виде продукции иммуноглобулинов иммуноцитами в ответ на антигенную стимуляцию. Клетки печени, окисляющие ксеноП биотики, синтезируют альбумин Посновной белок плазматичесП кой детоксикации, напоминающий иммуноглобулины, но харакП теризующийся более низкой специфичностью.
Эти факты являются свидетельством того, что микросомаль? ное окисление и иммунитет представляют собой равнозначные составляющие системы детоксикации и обеспечивают соответствуй ющие звенья метаболического гомеостаза.
При этом нарушение взаимосвязи между монооксигеназ? ным и иммунным звеньями детоксикации приводит к несоответП ствию между скоростью накопления, биотрансформации ивывеП дения как патологических, так и физиологических метаболитов. Это, в свою очередь, обусловливает ретенцию в тканях и жидко ? стных секторах организма патологических продуктов клеточного распада, эндотоксинов, пирогенов, биологически активных веП ществ различных типов, нейромедиаторов, свободных радикалов и прочих продуктов нормального и патологического обмена.
Причинами этого могут быть два типа воздействия на клетП ки монооксигеназной и иммунной систем: прямое воздействие токсинов на структуры клетки и разобщение окислительного фосП форилирования, приводящее либо к гибели клетки, либо к снижеП нию ее функциональной активности. Следствием же является, с одной стороны, нарушение биохимического состава клеток и тканей, с другой ?нарушение антителопродукции, лимфоците? токсичности, синтеза медиаторов.
Следовательно, эндогенная интоксикация развивается или как следствие разбалансировки составляющих системы дстокси кации, или в результате несостоятельности одного или более ее компонентов. Это определяет сущность эндогенной интоксикаП ции, ее общие и отличительные черты в зависимости от основной причины, т.е. этиологии заболевания, а также степень ее тяжести соответственно числу органов и составных частей системы деП токсикации, вовлеченных в патологический процесс.
Показатели, отражающие состояние системы детоксикации условно можно разделить на следующие группы.
1 .Биохимические маркеры эндогенной интоксикации.
2. Иммунологические маркеры эндогенной интоксикации.
3. Пите тральные маркеры эндогенной интоксикации.
Читайте также:




