Антидоты при отравлениях барбитуратами
Употребление определенных веществ, способных изменять психическое состояние человека, практиковалось с древнейших времен. В разные эпохи у различных народов имелись свои предпочтения в выборе таких веществ, сегодня получивших название психоактивных (ПАВ)
Употребление определенных веществ, способных изменять психическое состояние человека, практиковалось с древнейших времен. В разные эпохи у различных народов имелись свои предпочтения в выборе таких веществ, сегодня получивших название психоактивных (ПАВ). Во всем мире, и наша страна не является исключением, употребление ПАВ (в ряде случаев при злоупотреблении разрешенными веществами — алкоголем, табаком, чаем, кофе и т. д.) остается острой и значимой проблемой.
Период эпизодического употребления ПАВ, по своей сути, представляет серию острых интоксикаций (отравлений), постепенно перетекающих в интоксикацию хроническую (табл. 1). Абсолютно предсказуемо, что в ряде случаев возможны тяжелые формы отравлений ПАВ, как правило — острых. Симптомы и тяжесть течения острых отравлений ПАВ напрямую зависят от вида, токсичности и дозы яда. Обычно при таких отравлениях требуются немедленная медицинская помощь и госпитализация в стационар токсикологического или реанимационного профиля.
В основе классификации всех острых отравлений (в том числе ПАВ) лежат нозологический, патогенетический и клинический принципы (рис. 1).
Нозологическая (этиологическая) классификация основана на названиях отдельных химических препаратов (кокаин), группы родственных веществ (опиаты) или целого вида химических соединений, одинаковых по происхождению (например, растительные или синтетические).
Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в РФ, приведен в таблице 2.
Таким образом, на современном этапе можно выделить 2 трактовки изучаемого явления: соматоневрологический, или общепатологический (терапевтический, неврологический, токсикологический), подход, согласно которому отравление рассматривается как интоксикация, наносящая вред всем органам и системам организма; психопатологический, или ментальный (психиатрический, наркологический), подход, когда то же явление рассматривается как опьянение.
Клиническая диагностика острых отравлений ПАВ основана на данных анамнеза и изучении клинической картины заболевания с применением лабораторных и инструментальных методов обследования больного. Последовательность оказания догоспитальной медицинской помощи пациентам с острыми отравлениями ПАВ схематично представлена на рисунках 2–4.
Чтобы быстрее обследовать больного и скорее приступить к лечебным мероприятиям, осмотр рекомендуется осуществлять в 3 этапа (рис. 4).
Отправной точкой для диагностики являются следующие симптомы доконтактной визуальной оценки состояния больного: размер зрачка, уровень изменения сознания, состояние кожных покровов и слизистых оболочек.
Исходя из ширины зрачка, отравления разделяют на условные группы: сужение зрачка — миоз; расширение — мидриаз; условная норма — без четкого изменения диаметра зрачка. Таким образом, предлагается начальный, отправной симптом.
Необходимо помнить, что в процессе развития отравления по мере углубления коматозного состояния и присоединения возможных осложнений перечисленные клинические критерии (в частности, диаметр зрачка) могут изменяться.
Например, возникшую в результате приема психоактивных веществ кому разделяют на осложненную и неосложненную. Неосложненная кома характеризуется непосредственным угнетающим влиянием токсического вещества на ткань мозга. Под осложненной комой чаще всего подразумевают присоединение токсического отека мозга, развивающегося по 2 механизмам: гидратация ткани мозга, за счет разности концентрации токсического вещества в нейронах и в окружающем пространстве; нарушение регионарного кровотока с образованием тромбов в микроциркуляторном русле в рамках ДВС-синдрома.
Таким образом, кома с отеком мозга может несколько изменять симптоматику, что объясняет некоторую вариабельность отдельных симптомов. Однако для обсуждения отдельных вариантов нужно хорошо представлять себе базовый симптомокомплекс.
После оценки состояния зрачка определяется уровень изменения сознания (угнетение или возбуждение). Особое внимание требуется уделить наличию судорог, как предвестников комы.
Для диагностики возможного эксикоза (что особо важно при отравлении стимуляторами ЦНС) и проведения дифференциального диагноза с патологией нетоксического характера надо оценить состояние слизистых оболочек и кожных покровов (сморщенная кожа, сухость слизистых оболочек ротовой полости и языка, сниженный тургор и т. д.).
Выявленная тетрада основных симптомов (оценка состояния зрачка, сознания, кожи и слизистых, а также наличие судороги) позволяет предварительно предположить отравление веществами, которые можно разделить на следующие группы: миоз с угнетением сознания (табл. 4) — опиаты, этанол; барбитураты и бензодиазепины; мидриаз с возбуждением (табл. 5) — кокаин, гашиш, амфетамин и его производные, ЛСД, грибы-галлюциногены; без четкого изменения диаметра зрачка и возбуждения (табл. 6) — фенциклидин.
При анализе клинической картины отравления психоактивными веществами важно выявить еще 8 симптомов (табл. 4–6).
На догоспитальном этапе лабораторная диагностика обычно ограничивается взятием биосред (надо указать время взятия биосред и данные пострадавшего) и полуколичественной оценкой уровня гликемии, глюкозурии, кетонурии. Вещественные доказательства (жидкости в бутылках, упаковки из-под лекарств, записки) необходимо собрать, так как они имеют не только медицинскую, но и юридическую ценность. При подозрении на острое отравление наркотическими веществами значительно облегчить диагностику могут иммунохроматографические экспресс-тесты на наличие ряда таких веществ в моче или слюне.
При проведении анализа следует надевать одноразовые резиновые или пластиковые перчатки, так как исследуемые образцы мочи могут содержать возбудителей инфекций.
Техника проведения анализа следующая. В чистую сухую емкость помещают исследуемый образец мочи таким образом, чтобы уровень ее не превышал 1-1,5 см. Затем вскрывают упаковку полоски (разорвать вдоль прорези), а извлеченную полоску погружают вертикально тем концом, на котором обозначены стрелки, в мочу до уровня ограничительной линии на 30–60 с. Извлеченную из мочи тест-полоску следует положить на ровную, чистую, сухую поверхность и по истечении 5 мин визуально оценить результат реакции.
Интерпретация исследования крайне проста, выявление 2 параллельных розовых полос свидетельствует об отрицательном анализе, выявление же только одной розовой полосы в контрольной зоне подтверждает положительный результат.
При отсутствии полос в течение 5 мин пробу следует повторить с помощью новой полоски.
Возможности экспресс-тестов отражены на упаковке. Каждая полоска позволяет определить в моче наличие одного ПАВ. Например, положительную реакцию при тестировании дают: при определении опиатов и/или их метаболитов — родственные морфину соединения: этилморфин, гидроморфон, мерперидин, морфин-3-глюкуронид, героин. При помощи данной методики можно выявлять оговариваемую концентрацию иных наркотических веществ, их метаболиты, а также структурно-родственные соединения таких средств, как метадон, барбитураты, бензодиазепины, каннабиноиды, РСР, амфетамины и др.
В тех случаях, когда не представляется возможным точно определить наименование вещества, вызвавшего острое отравление, диагноз ставят на основании ведущего клинического синдрома, представленного в таблице 7.
Последовательность лечебных мероприятий при острых отравлениях (в том числе ПАВ) схематично представлена на рисунке 5.
Промывание желудка через зонд наиболее эффективно в первый час отравления, поэтому если больного невозможно сразу же госпитализировать, эту процедуру производят на месте отравления.
Для предотвращения аспирации рвотных масс в дыхательные пути и предупреждения повреждения легких промывание желудка проводят после предварительной интубации трахеи трубкой с раздувной манжеткой. Больным, находящимся в бессознательном состоянии (например, при тяжелых отравлениях снотворными препаратами), промывания повторяют 2–3 раза в течение первых суток с момента отравления. Это необходимо, поскольку при коме резко замедляется всасывание токсического агента, и в желудочно-кишечном тракте обычно депонируется значительное количество невсосавшегося вещества. Кроме того, некоторые вещества (морфин, бензодиазепины) выделяются слизистыми оболочками желудка, а затем вновь всасываются. Наконец, находящиеся в складках слизистых оболочек желудка таблетированные лекарственные препараты могут не растворяться в течение длительного времени.
После промывания в качестве слабительного средства с целью ускорения выделения содержимого кишечника в желудок вводят 100–150 мл 30% раствора сульфата натрия или сульфата магния (при отравлениях водорастворимыми ядами) либо 100 мл вазелинового масла (при отравлениях жирорастворимыми ядами).
Адсорбцию находящихся в желудочно-кишечном тракте ТВ проводят активированным углем внутрь. Взвесью активированного угля (2–4 столовые ложки на 250–400 мл воды) промывают желудок, уголь вводят через зонд до и после промывания в виде кашицы (1 столовую ложку порошка или 5–10 таблеток — 50–100 мг активированного угля растворяют в 5–10 мл воды). Возможна очистительная клизма.
Если ТВ были введены в полость организма, их также промывают прохладной водой или сорбентами с помощью клизмы или спринцевания.
Для удаления из организма всосавшегося яда уже на догоспитальном этапе проводят детоксикацию организма. Основной метод детоксикации — форсирование диуреза, включающего 3 этапа: предварительную водную нагрузку; внутривенное введение мочегонных средств; заместительное введение растворов электролитов.
Параллельно определяют: почасовой диурез путем постановки мочевого катетера; концентрацию ТВ в крови и моче; содержание электролитов в крови; гематокрит (соотношение форменных элементов и плазмы крови).
Противоядия (антидоты) рекомендуется использовать как можно раньше, поскольку они непосредственно влияют на действие и метаболизм попавшего в организм ТВ, его депонирование или выведение и тем самым ослабляют действие яда.
Выделяют 4 группы специфических противоядий, из которых для купирования отравлений ПАВ обычно применяют лишь 2 первых: химические (токсикотропные); фармакологические (симптоматические); биохимические (токсикокинетические); антитоксические иммунопрепараты.
В основе действия фармакологических противоядий лежит фармакологический антагонизм веществ (например, аминостигмина и атропина или других холинолитиков, налоксона и опиатов, флумазенила и бензодиазепинов).
Таким образом, именно фармакологические антидоты составляют наиболее значимую группу медикаментозных препаратов для лечения острых отравлений ПАВ, из которых наибольшего внимания требуют налоксон, флумазенил, а также аминостигмин и ему подобные средства.
Налоксон (наркан, нарканти) — полный антагонист опиатных рецепторов. Выпускается в ампулах по 1 мл раствора — 0,04% (0,4 мг/мл), 0,1% (1 мг/мл), а также для новорожденных — 0,002% (0,02 мг/мл). Препарат вытесняет опиаты из специфичных рецепторов, быстро восстанавливает угнетенное дыхание и сознание и поэтому особо показан на догоспитальном этапе даже при невозможности интубации трахеи и искусственной вентиляции легких. Предпочтительнее (для достижения мгновенного эффекта) вводить налоксон внутривенно струйно, на изотоническом растворе хлорида натрия (однако возможно раздельное или комбинированное его введение — подкожное, внутримышечное или эндотрахеальное) в начальной дозе 0,4–0,8 мг. Затем дозу подбирают методом титрования, максимальная доза налоксона — 10 мг.
Продолжительность антагонистического действия налоксона составляет 30–45 мин, поэтому при ухудшении состояния может потребоваться его дополнительное введение. В ряде случаев после достижения терапевтического эффекта целесообразно закрепить результат внутримышечным или внутривенным капельным введением дополнительной дозы 0,4 мг.
При длительном пребывании больного в состоянии тяжелой гипоксии или возможной аспирации (признаки рвоты), а также введении налоксона можно получить нежелательный эффект в виде выраженного психомоторного возбуждения и отека легких через 30–60 мин. Поэтому в таких случаях введению налоксона должны предшествовать интубация трахеи (после премедикации атропином) и искусственная вентиляция легких.
Если введение налоксона обеспечивает улучшение или восстановление самостоятельного дыхания и повышение уровня сознания, это свидетельствует об отравлении ПАВ (героином, алкоголем, фенциклидином, есть литературные сведения об эффективности при отравлении барбитуратами и даже бензодиазепинами). Скорее всего, этот список неокончательный. Отсутствие эффекта от введения налоксона дает основание искать другую причину угнетения сознания и дыхания или сопутствующую патологию.
Флумазенил (анексат, мазикон, ромазикон) — антагонист бензодиазепиновых рецепторов — применяется у больных с тяжелым отравлением препаратами бензодиазепинового ряда. Антидот выпускается в виде 0,01% раствора (0,1 мг/мл) и вводится внутривенно струйно в дозе 0,3–0,5 мг на изотоническом растворе натрия хлорида; при отсутствии положительного эффекта (восстановление сознания) в течение нескольких минут введение можно повторить в той же дозе. Специфичность действия позволяет использовать анексат с дифференциально-диагностической целью. Максимальная разовая доза составляет 2 мг. Противопоказаниями для использования препарата являются сочетанные отравления бензодиазепиновыми производными и трициклическими антидепрессантами, а также случаи передозировки бензодиазепинов у больных эпилепсией.
При отравлениях, вызванных ПАВ с холинолитическим действием (к которым относятся нейролептики, трициклические антидепрессанты, антигистаминные), в качестве антидота применяют ряд антихолинэстеразных средств, предшественником которых является всем хорошо известный физостигмин (эзерин). К таким противоядиям относятся галантамин и аминостигмин.
Галантамина гидробромид (нивалин) является препаратом короткого действия, применяется в виде 0,5% раствора и вводится внутривенно по 4–8 мл.
Аминостигмин — антидот длительного действия — вводится внутримышечно по 1-2 мл в виде 0,1% раствора.
Первые 2 антидота (налоксон и флумазенил) используются в схеме лечения коматозных состояний (рис. 6).
Таким образом, применение фармакологических противоядий на догоспитальном этапе является важным и необходимым лечебно-диагностическим мероприятием, позволяющим повысить качество оказания неотложной помощи, сократить число выездов бригад СМП и госпитализаций.
По вопросам литературы обращайтесь в редакцию.
В. Г. Москвичев, кандидат медицинских наук
И. В. Духанина, кандидат медицинских наук
А. Л. Верткин, доктор медицинских наук, профессор
МГМСУ, ННПОСМП, Москва
К активным методам экстренной детоксикации организма при острых отравлениях принадлежит специфическая антидотная терапия. Цель ее — связывание яда, циркулирующего в организме, соответствующими веществами (антидотами). Кроме того, с целью значительного ограничения действия яда на соответствующие рецепторы используют лекарственные средства, которые проявляют антагонистическое, т.е. конкурентное для токсического агента, воздействие на эти рецепторы (фармакологические антагонисты). Антидоты при отравлениях и фармакологические антагонисты применяют только тогда, когда точно установлено, какое именно вещество вызвало острое отравление.
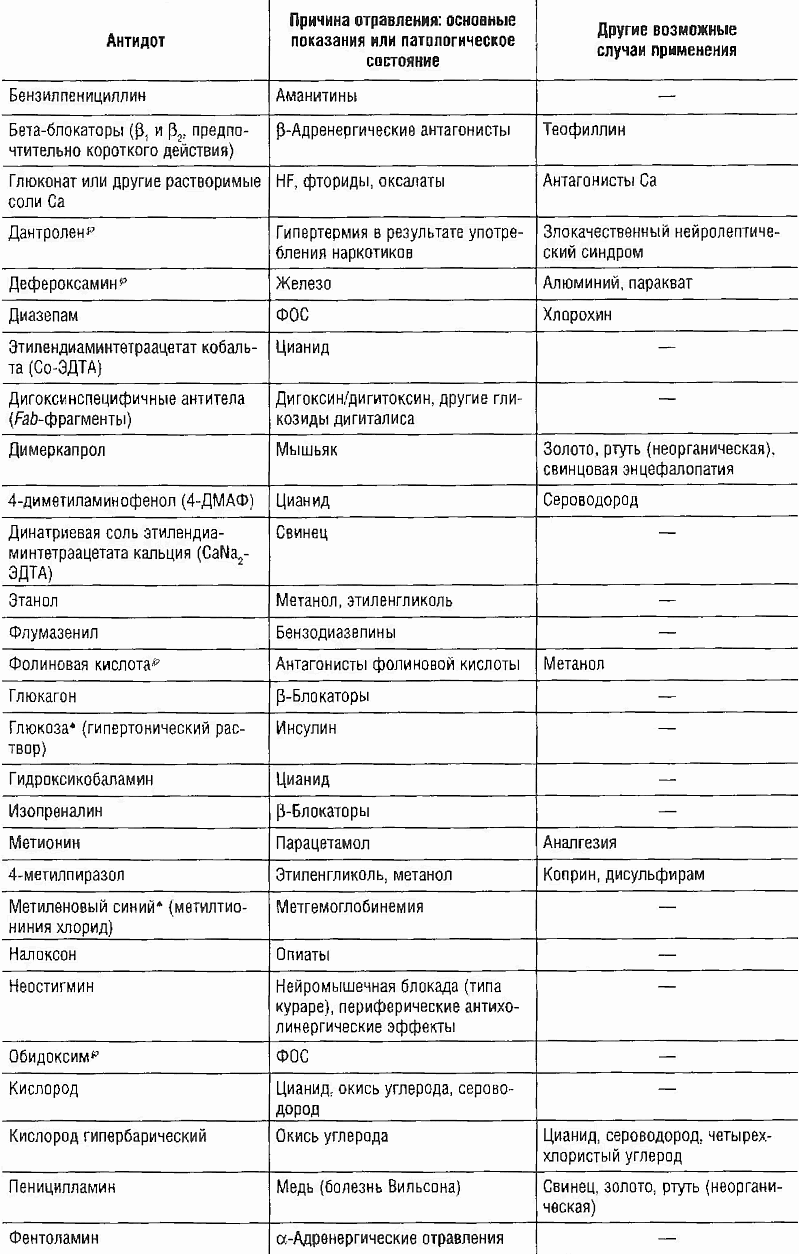
Существующее мнение о наличии противоядий для любого токсичного вещества не подтверждается действительностью. Относительно селективные эффективные антидоты существуют лишь для немногих классов токсичных веществ. Основные антидоты и антагонисты представлены в таблице.
Основные антидоты при отравлениях
Основные антидоты и фармакологические антагонисты, применяемые при острых отравлениях химическими агентами — таблица
| Антидот, фармакологический антагонист | Наименование токсического агента | Дозы и способы использования антидотов и фармакологических антагонистов |
| 1 | 2 | 3 |
| Тримефацин | Уран, бериллий | Внутривенно или ингаляционно в виде 5% раствора или 2,5% раствора в растворе кальция хлорида |
| Фероцин | Радиоизотопы цезия и рубидия, а также продукты деления урана | Внутрь по 1 г в виде водной суспензии (в 1/2 стакана воды) 2-3 раза в течение 10 дней |
| Унитиол | Соединения мышьяка, соли ртути, висмута и других тяжелых металлов, сердечные гликозиды, анаприлин, амитриптилин т.д. | Подкожно, внутримышечно или внутривенно по 5-10 мл 5% раствора (по 1 мл на 10 кг массы тела): в 1-й день — через каждые 6-8 ч, на 2-й день — через 8-12 ч , в последующие дни — по 1-2 инъекции в сутки в течение 6-7 дней и более |
| Цитохром С | Снотворные препараты, оксид углерода | Внутривенно капельно 20-40 мл 0,25% раствора в 250-500 мл изотонического раствора натрия хлорида или глюкозы (после биологической пробы — 0,1 мл 0,25% раствора внутрикожно) |

Наиболее эффективными антидотами при отравлениях металлами следует считать комплексоны (хелатные соединения). Из-за наличия в их структуре таких функциональных групп, как ОН,-SH и -NH, они могут отдавать электроны для связи с катионами металлов, т.е. образовывать координационно-ковалентные связи. В таком виде токсичные соединения выводятся из организма.
Эффективность хелатного соединения в значительной мере определяется количеством лиганд в его основе, способных связываться с металлом. Чем их больше, тем более стабильный и менее токсичен метало хелатный комплекс. Следует помнить, что комплексоны как антидоты имеют невысокую избирательность действия. Наряду с токсичными агентами они могут связывать необходимые для организма эндогенные ионы, например кальция и цинка.
Конечный результат такого взаимодействия определяется аффинитетом токсичных экзогенных и эссенциальных (эндогенных) металлов в хелатных соединений. Для того чтобы наступило значительное снижение уровня эндогенных металлов, их родство с комплексонами должен превышать аффинитет к эндогенным лиганд. В свою очередь, относительная скорость обмена металла между эндогенными лигандами и хелатных соединений должна превышать скорость элиминации комплексонов в комплексе с металлами. Если комплексоны выводится быстрее, чем комплекс металоэндогенных лиганд, его концентрация может не достичь того уровня, который необходим для эффективной конкуренции с эндогенными местами связывания.
Этот фактор особенно весомый в случае, когда вывод осуществляется через образование тройного комплекса, т.е. эндогенный лиганд-металоэкзогенный комплекс.
К комплексонам относятся:
- дефероксамин,
- тетацин-кальций,
- димеркапрол,
- пеницилламин,
- унитиол и др..
Дефероксамин (десферал) — комплексон, который активно связывает железо, в незначительной степени — эссенциальные микроэлементы. Может быть использован для ускорения выделения алюминия из организма при почечной недостаточности. Конкурируя за слабо связано железо в таких железосодержащих белках, как гемосидерин и ферритин дефероксамин не в состоянии конкурировать за то железо, которое содержится в биологических хелатных комплексах: микросомальных и митохондриальных цитохромах, гемопротеины т.п..
Фероксамин (комплекс железа с дефероксамином) представлен для демонстрации его функциональных групп. Здесь железо активно содержится в замкнутой системе. Димеркапрол, по сукцимер, захватывает металл (м) в стабильное гетероциклическое кольцо ковалентной связью.
Две молекулы пенициламина способны связывать одну молекулу меди или другого металла.
Продукты метаболизма дефероксамина выделяются почками, окрашивая мочу в темно-красный цвет. В процессе лечения дефероксамином могут возникнуть аллергические реакции (крапивница, кожная сыпь), коллапс (при быстром введении в вену), глухота, нарушение зрения, помутнение хрусталика. Встречается также коагулопатия, печеночная и почечная недостаточность, инфаркт кишечника.
Тетацин-кальций (кальций-динатриевая соль этилен-диаминтет-раоцтовой кислоты) — эффективный комплексон для многих двух-и трехвалентных тяжелых металлов и редкоземельных элементов, в частности для свинца, кадмия, кобальта, урана, иттрия, цезия и др.. Относительно плохо проникает через клеточные мембраны, поэтому более эффективно связывает внеклеточные ионы металла. Высокополярные ионные свойства тетацин-кальция препятствуют более или менее значительно энтеральному его всасыванию, поэтому он используется преимущественно для медленного внутримышечного или внутривенного введения.
В тетацин-кальции кальций замещается только ионами тех металлов и редкоземельных элементов, образующих более прочный комплекс (свинец, торий и др.), чем сам кальций. Барий и стронций, константа устойчивости комплекса которых ниже, чем кальция, не вступают в реакцию с тетацин-кальцием. Использование антидота тетацин-кальция для мобилизации ртути также неэффективно, видимо, из-за незначительного поступления этого комплексона в те ткани, где концентрируется ртуть, а также через менее успешную конкуренцию ее со связанным кальцием.
В больших дозах тетацин-кальций может вызвать повреждение почек, особенно их канальцев.
Пентацин — кальций-тринатриевая соль диетилентриамин-пентаоцтовой кислоты также эффективен как комплексон. В отличие от тетацин-кальция, он не влияет на выделение урана, полония, радия и радиоактивного стронция. При длительном введении элиминация металлов из организма снижается.
После введения пентацина возможно головокружение, головная боль, боли в груди и конечностях, поражение почек.
Димеркапрол (2,3-димеркаптопропанол, британский антилюизит, БАЛ). Выпускается в виде 10% раствора в арахисовом масле; вводится внутримышечно, инъекции болезненны. Своими SH-группами димеркапрол образует прочные хелатные комплексы с ионами ртути, мышьяка, свинца и золота, ускоряет их выведение из организма и восстановление функциональных белков, подавленных ядом. Эффективность этого антидота возрастает при минимальных сроках его применения после отравления. Он неэффективен, если лечение проводится через 24 ч и более.
Поэтому считают, что лечебные эффекты БАЛ обусловлены скорее предупреждением связывания металлов с компонентами клеток, крови и тканевой жидкости, а не удалением уже связанного яда.
Менее токсичными оказались некоторые производные димеркапрола, в частности сукцимер (димеркапрол сукцинат) и 2,3-димеркапропропан-1-сульфонат. Они более полярные, чем БАЛ; распределяются преимущественно во внеклеточной жидкости, поэтому в меньшей степени повреждают клеточные структуры крови и тканей.
Пеницилламин — Д-3 ,3-диметилцистеин гидрохлорид (купренил) — водорастворимый продукт метаболизма пенициллина. Д-изомер его относительно нетоксичен. Устойчив к метаболической деградации. Используется преимущественно при отравлении соединениями меди или для предупреждения их кумуляции, а также для лечения болезни Вильсона.
Как вспомогательное средство пеницилламин иногда применяют при лечении отравлений свинцом, золотом и мышьяком. Как и препараты золота, этот антидот тормозит прогрессирование деструкции костей и хрящей, поэтому используется в лечении ревматоидного артрита. Может быть причиной появления аллергических реакций, диспепсии, тромбоцитопении, лейкопении, анемии и т.д..
Натрия тиосульфат — серосодержащий антидот. В отличие от предыдущих препаратов, с металлами комплексных соединений не образует. Нейтрализует галоиды, цианиды, соединения мышьяка, ртути, свинца.
Как антидоты широкое распространение получили также окислители, адсорбенты. Слабые растворы кислот, обычно органических, ранее широко применяли для нейтрализации щелочей, а луга (натрия гидрокарбонат, магния оксид) — при отравлениях кислотами. Теперь преимущество предоставляется не нейтрализации кислот и щелочей, а их разведению.
Калия перманганат эффективен при отравлении морфином и другими алкалоидами, фосфором; танин — алкалоидами и тяжелыми металлами. Уголь активированный широко применяют при пероральном отравлении различными лекарственными средствами, а также алкалоидами, солями тяжелых металлов, бактериальными токсинами и т.д.. Он не адсорбирует железо, литий, калий и лишь в незначительной степени — алкоголь и цианиды. Совсем неэффективное при отравлении кислотами и щелочами, кислотой борной, тольбутамидом т.п..
Повторные приемы активированного угля через каждые 4 ч эффективны при отравлениях карбамазепином, дигитоксином, теофиллином и т.д..
В последние годы с целью ликвидации экзогенной (как и эндогенной) интоксикации начали использовать энтеросорбенты. Эти лекарственные препараты имеют свойство сорбировать (удерживать на своей поверхности) токсичные агенты, находящиеся в просвете желудочно-кишечного тракта. Сюда токсичные вещества могут попадать извне, выделяться путем диффузии из крови, находиться в составе пищеварительных соков и желчи или здесь образовываться. Энтеросорбенты, не являясь в полной мере антидотами, способствуют уменьшению уровня интоксикации, тем самым защищают организм от повреждения ядом.
Кроме того, энтеросорбенты улучшают пищеварение в желудке и кишечнике, так как способствуют более рациональной действия пищеварительных ферментов на элементы пищи, особенно белки. Они способствуют обезвреживанию ядовитых агентов в печени, улучшают окислительные процессы, процессы распада перекисных соединений и т.д.. Доказана их высокая эффективность при острой интоксикации микробными токсинами, атропином, сибазоном, грибами, бензином.
В медицинской практике используются как антидоты в основном углеродистые и полимерные сорбенты, в частности углеродные СКН (сферический карбонит насыщенный) и кремниевые — Полисорб, энтеросгель.
Клинический опыт показывает, что энтеросорбция эффективна при пищевых, медикаментозных, промышленных отравлениях. Энтеросорбенты эффективны также при заболеваниях, сопровождающихся эндотоксикозом, в частности органов пищеварения, сердечно-сосудистой, дыхательной и эндокринной систем, аллергических заболеваниях, токсикозах беременности.
В частности, при отравлении препаратами, оказывающими угнетающее влияние на ЦНС, используют стимуляторы ЦНС и аналептики:
- кофеин-бензоат натрия,
- эфедрина гидрохлорид,
- кордиамин,
- бемегрид,
- цититон и др..
В случае интоксикации ядами, возбуждающих ЦНС, как антагонисты используют препараты с подавляющим типом действия, в частности эфир для наркоза, нередко барбитураты, сибазон и т.д.. При отравлении холиномиметическими или Антихолинестеразными средствами применяют холинолитики (чаще атропина сульфат, скополамина гидробромид), а при отравлении атропином и ганглиолитикамы — антихолинэстеразные препараты (особенно прозерин).
- Антагонистом морфина и других наркотических болеутоляющих средств является налоксон;
- оксида углерода, сероводорода, сероуглерода и др. — кислород в ингаляции.
Налоксон назначается в начальной дозе 1-2 мг парентерально. Дозы увеличивают при интоксикации кодеином и фентанилом. Противопоказано использование физостигмина салицилата при отравлении трициклическими антидепрессантами.
К серьезным осложнениям может привести отравление барбитуратами, вплоть до летального исхода. Поэтому важно знать, что это за препараты, какие побочные действия они имеют.
Во второй половине 19 века немецкий ученый Адольф фон Байер открыл барбитуровую кислоту, что положило начало дальнейшему созданию и использованию барбитуратов. Эти вещества, являющиеся производными барбитуровой кислоты, угнетают центральную нервную систему. Эффект от их использования может варьироваться от успокоительного до стадии наркоза, в зависимости от того, какая доза была введена.

- Продолжительное действие. Эти препараты используются при лечении эпилепсии, они имеют замедленное воздействие.
- Средней и короткой продолжительности. Их действие начинается через 15-20 минут после приема и длится около 6 часов.
- Ультракороткое. Они способны вызвать медикаментозный сон, применяются как кратковременный наркоз перед введением основного.
К барбитуратам относятся препараты, которые оказывают депрессивное воздействие на ЦНС, они входят в состав корвалола, валокордина и других лекарств. В список популярных препаратов-барбитуратов входят: Люминал, Барбитал, Барбитурат Натрия, Нембутал, Тальбутал, Секобарбитал, Алюрат, Пентотал, Тиопентал, Суритал.
Механизм действия барбитуратов
При проникновении в организм происходит активация барбитуратных рецепторов, что усиливает эффект гамма-аминомасляной кислоты. Эта кислота оказывает тормозное действие при передаче электрохимического импульса от нервной клетки к мышечной ткани. Так, препараты барбитуровой кислоты оказывают успокоительный, болеутоляющий, снотворный, противосудорожный эффект. При попадании барбитуратов в кровь они связываются с белками плазмы и накапливаются. Выводятся из организма медленно.

Являются ли барбитураты наркотиком
Барбитураты по действию приравнивают наркотическим веществам, так как их применение может вызывать привыкание. Стоит серьезно относиться к приему таких лекарств. Под воздействием этих препаратов человек испытывает чувство эйфории. Помимо угнетения ЦНС может возникнуть и противоположное действие – агрессия, гиперактивность, раздражительность.
Длительный прием может привести к психическому сдвигу, человек постоянно находится в состоянии угнетения. Так как у разума нет выходов для самореализации, появляются мысли о самоубийстве.
Отмечалось, что у людей принимающих барбитураты-наркотики возникает чувство уверенности в себе, спокойствие, общительность. Чтобы продлить действие этих эффектов, приходится снова принимать препарат. Со временем, чтобы получить результат, дозировку приходится увеличивать. Таким образом и возникает зависимость. Если резко прекратить употребление барбитуратов возникает эффект ломки, бессонница, абстинентный синдром, могут возникнуть приступы эпилепсии, возможна смерть.

Разрешены ли препараты барбитурата?
До второй половины 20 века отдавали предпочтение депрессантам в лечении бессонницы, и активно использовали их в качестве снотворных и успокоительного. Однако из-за их способности вызывать привыкание применение сокращалось и в связи с этим в 70-е годы барбитураты убрали из свободной продажи.
Сейчас в исключительных случаях врачи применяют некоторые препараты в качестве болеутоляющего, успокаивающего средства. Также ветеринары применяют их для безболезненного усыпления животных. Приобрести препараты барбитуровой кислоты сейчас в официальных аптеках без рецепта невозможно. Если есть необходимость, их выдает лечащий врач в ограниченном количестве.
Симптомы при отравлении
Если в крови высокая концентрация отравляющего вещества блокируются дыхательные ферменты мозга, возникает кислородное голодание, клетки мозга гибнут. Обмен веществ нарушается, возникает кома, затем отек мозга, остановка дыхания.

Степени отравления можно классифицировать следующим образом:
- Засыпание. На этой стадии человек сонлив, апатичен, слаб.
- Поверхностная кома. Пациент теряет сознание, зрачки сужаются, глотательный рефлекс и реакция на боль присутствуют, рефлексы сухожилий ослаблены.
- Глубокая кома. У пациента мышечный тонус значительно снижен, зрачки расширяются, реакции на боль нет, возникает токсикогенный коллапс, поверхностное редкое дыхание, возможна его остановка. Нередко больных подключают к ИВЛ. Кома может длиться от нескольких часов до суток и более.
- Посткоматозный период. При выходе из комы наблюдается двигательное возбуждение, после этого несколько дней может длиться депрессия, астения.
Основное отравляющее действие барбитуратов в снижении активности головного мозга. Вначале у человека возникает сонливость, чувство расслабленности, успокоение. Данное состояние не опасно для жизни.

Опасность передозировки
Без рекомендаций врача принимать эти седативные препараты нельзя. Передозировка барбитуратами имеет серьезные последствия. Симптомы отравления барбитуратами, которые указывают производители, это липкая кожа, поверхностное дыхание, слабый и учащенный пульс, кома, смерть. Во время барбитуратного сна возможна остановка дыхания, и существует опасность захлебнуться рвотой в результате возникающих рвотных позывов.
Экстренная помощь при отравлении барбитуратами
Вначале при интоксикации нужно срочно вызвать врача. Выведение барбитуратов из организма проводят в несколько этапов: промывают желудок, проводят энтеросорбцию (принимают активированный уголь), затем повторно промывают желудок, делают клизмы. Универсального противоядия не существует. Лечение поводят симптоматическое. Для того чтобы узнать, каким препаратом пациент отравлен, делают анализ мочи.
Самолечением заниматься при серьезном отравлении нельзя. Необходимо обратиться к врачу, гастроэнтерологу или токсикологу. При коме проводят ультрафиолетовое очищение крови, гемодиализ, гемосорбцию.

Выведение токсинов через мочеполовую систему и инфузионную терапию проводят на любой стадии. Так как одного специфического антидота не существует, из лекарств применяют гидрокарбонат натрия, глюкозу, аскорбиновую кислоту, инсулин. Для уменьшения гипоксии вводят такие препараты как винпоцетин, пирацетам, мексидол.
При дыхательной недостаточности вводят кофеин. В качестве антидота вводят антагонисты снотворных средств. В зависимости от того, каким препаратом произошло отравление, подбираются антидоты. При отравлении диазепамом антидот – налоксон, при отравлении фенобарбиталом, циклобарбиталом антидот – бемегрид.
При отеке тканей головного мозга делают переливание плазмы, назначают мочегонные средства, чтобы отравляющие вещества вывести почками. Для уменьшения гипоксии и улучшения обмена веществ назначают витамины. В качестве профилактики пролежней часто меняют положение больного, тело протирают камфорным маслом.
Последствия отравления

Очень важно вовремя очистить организм. Однако даже после адекватного лечения могут возникнуть осложнения токсического отравления:
- пневмония,
- тахикардия,
- атония желудочно-кишечного тракта,
- нарушение диуреза,
- острая почечная недостаточность, снижается функциональность мочевыделительной системы,
- в ряде случаев от яда, поступившего в организм, начинается распад мышечных волокон, возникает предрасположенность к пролежням.
Отравление может возникнуть вследствие разных факторов, в лучшем случае итогом является длительное лечение и восстановление, но не всегда все заканчивается хорошо.
При неаккуратном соблюдении дозировок прием снотворного может стать последним. Чтобы избежать трагических последствий, необходимо тщательно соблюдать все предписания врача при приеме таких сильных препаратов.
Видео
Посмотрите очень познавательное и информативное видео о вредном воздействии барбитуратов.
Читайте также:


