Герпетический энцефалит у детей клинические рекомендации
В статье рассматриваются некоторые аспекты этиопатогенеза герпесвирусных заболеваний у детей, современные подходы к лекарственной терапии и профилактике рецидивов.
This article discusses some aspects of the pathogenesis of herpes-associated diseases in children, modern approaches to drug therapy and relapse prevention.
В последние годы среди основных возбудителей вирусных инфекций у детей особое место занимают герпес-вирусы, что связано с их повсеместным распространением, широким разнообразием, полиорганностью поражения, многообразием клинических проявлений, а также высокой частотой хронического течения. Герпес-ассоциированные заболевания входят в число наиболее распространенных и плохо контролируемых инфекций человека. Это связано с тем, что герпес-вирусы могут длительно бессимптомно циркулировать в организме человека с нормальной иммунной системой, а при иммуносупрессии способствовать развитию тяжелых заболеваний, вплоть до угрожающих жизни генерализованных инфекций. Так, по данным Всемирной организации здравоохранения (World Health Organization, WHO), смертность от герпетической инфекции составляет около 16% и находится на втором месте после гепатита среди вирусных заболеваний [1].
.jpg)
Герпес-вирусы (от греч. ?ρπειν (herpein) — ползать) — семейство ДНК-вирусов, объединены в семейство Herpesviridae, которое включает в себя 8 классифицируемых видов вирусов человека: вирусы простого герпеса — вирус простого герпеса (ВПГ-1) и вирус генитального герпеса (ВПГ-2), вирус варицелла зостер, вирус Эпштейна–Барр, цитомегаловирус, вирус герпеса человека 6-го, 7-го, 8-го типов, а также около 80 неклассифицируемых вирусов герпеса человека и животных. К подсемейству α-герпес-вирусов относятся ВПГ-1, ВПГ-2 и вирус варицелла зостер, которые характеризуются быстрой репликацией в различных типах клеток и обладают цитопатическим действием на культуры инфицированных клеток. Бета-герпес-вирусы (цитомегаловирус, вирусы герпеса 6-го и 7-го типов) также поражают различные виды клеток, приводят к увеличению их размеров (цитомегалия), могут способствовать развитию иммуносупрессивных состояний. К подсемейству γ-герпес-вирусов относятся вирус Эпштейна–Барр и вирус герпеса 8-го типа — вирус, ассоциированный с саркомой Капоши (KSHV). Их характеризует тропность к лимфоидным клеткам (Т- и В-лимфоцитам), в которых они могут длительно персистировать. В некоторых случаях способны вызывать развитие лимфомы, саркомы [2].
Вирионы герпес-вирусов термолабильны — они инактивируются в течение 30 мин при температуре 50–52 °C, в течение 20 ч — при температуре 37,5 °C, но хорошо переносят лиофилизацию. На металлических поверхностях (монеты, дверные ручки, водопроводные краны) герпес-вирусы выживают в течение 2 ч, на пластике и дереве — до 3 ч, на влажных медицинских материалах (вата и марля) — до их высыхания при комнатной температуре (до 6 ч). Уникальность герпес-вирусов заключается в том, что они способны непрерывно или циклично размножаться в инфицированных клетках тропных тканей (персистенция), а также пожизненно сохраняться в морфологически и иммунохимически видоизмененной форме в нервных клетках регионарных нервных ганглиев (латенция) и реактивироваться под влиянием различных экзо- и эндогенных провоцирующих факторов. Однако способность к персистенции и латенции у различных штаммов неодинаковая: наиболее активны в этом отношении вирусы простого герпеса, наименее — вирус Эпштейна–Барр.
По данным многочисленных исследований, к 18 годам более 90% жителей городов инфицируются одним или несколькими штаммами вирусов. Основной путь инфицирования — воздушно-капельный, при прямом контакте или через предметы обихода (общие посуда, полотенца, носовые платки и пр.). Отмечается также оральный, генитальный, трансфузионный, трансплантационный и трансплацентарный пути передачи инфекции. ВПГ 1-го и 2-го типов, цитомегаловирус входят в число возбудителей TORCH-инфекций, способствуют развитию серьезных заболеваний новорожденных и детей младшего возраста. Вирусы простого герпеса, цитомегаловирус, вирус Эпштейна–Барр рассматриваются как индикаторы СПИДа в связи с их частым обнаружением при данном заболевании [3, 4]. С герпес-вирусами связывают развитие синдрома хронической усталости (Chronic fatigue syndrome — CFS) [5].
Клинически герпес-инфекция у детей может протекать в виде ветряной оспы (вирус варицелла зостер), инфекционного мононуклеоза (вирус Эпштейна–Барр), внезапной экзантемы (вирус герпеса человека 6-го и 7-го типов), афтозного стоматита (ВПГ 1-го или 2-го типа), мононуклеозоподобного синдрома (цитомегаловирус). У подростков и взрослых людей часто инфекция протекает бессимптомно, что объясняется как биологическими свойствами штаммов, так и индивидуальными особенностями иммунного ответа. Часто при снижении иммунореактивности организма герпес-вирусы выступают в качестве вирусов-оппортунистов, приводя к более тяжелому течению основного заболевания, развитию осложнений. Велика роль герпесвирусных инфекций, особенно цитомегаловирусной, в формировании младенческой смертности. Наибольшую угрозу для жизни и здоровья детей представляют герпетические нейроинфекции — летальность при них достигает 20%, а инвалидизация — 50%. Тяжело протекают офтальмогерпес (развитие катаракты или глаукомы — до 50%), генитальный герпес, генерализованная форма Эпштейна–Барр-вирусной инфекции (инфекционного мононуклеоза) [1, 6].
Герпесвирусная инфекция относится к трудноконтролируемым заболеваниям. Несмотря на разнообразие лекарственных препаратов, использующихся для лечения данной патологии, средств, обеспечивающих полное излечение, не существует. Это обусловлено генотипическими особенностями возбудителя, формированием резистентности герпес-вирусов и молекулярной мимикрией.
Открытые с помощью методов молекулярной биологии механизмов репликации герпес-вирусов, а также изучение взаимодействия вируса с клеткой позволили создать целый ряд эффективных химиотерапевтических средств, обладающих противогерпетической активностью. Однако, эффективно купируя острые проявления инфекции, они не предотвращают рецидивирования, не всегда снижают частоту рецидивов.
Учитывая, что при герпес-ассоциированных инфекциях, как и при других хронических заболеваниях с длительной персистенцией вируса, развиваются иммунодефицитные состояния, для повышения эффективности лечения в схемы терапии наряду с противовирусными препаратами приходится включать препараты, способствующие коррекции иммунного статуса больного. Все это диктует необходимость правильно подбирать лекарственное средство, его дозу и длительность приема, при необходимости использовать комбинацию различных препаратов, избегая при этом полипрагмазии. Определенную сложность терапии в детском возрасте вызывают возрастные ограничения для ряда лекарственных средств, наличие нежелательных лекарстввенных реакций (НЛР) и противопоказаний.
В настоящее время для лечения герпесвирусных заболеваний и профилактики рецидивов используют следующие группы препаратов (табл.).
При лечении герпес-инфекций следует придерживаться комплексного подхода. Длительность и интенсивность терапии определяются возрастом больного, клинической формой заболевания, тяжестью его течения, а также наличием осложнений и сопутствующей патологии. Лечебно-профилактические мероприятия следует разделять на несколько этапов.
- Острый период болезни (рецидив) — охранительный режим, лечебное питание, противовирусные препараты, интерфероны и их индукторы. По показаниям назначаются иммуноглобулины, антибактериальные препараты местного и системного действия, глюкокортикоиды, нейро- и ангиопротекторы, гепатопротекторы, кардиотропные препараты, ингибиторы протеаз. Симптоматическая терапия может включать жаропонижающие, отхаркивающие и муколитические препараты.
- Ремиссия, стихание основных клинических проявлений (иммуномодуляторы, адаптогены растительного происхождения, пре- и пробиотики, витамино-минеральные комплексы).
- Профилактика рецидивов (специфическая профилактика — вакцинация, санация хронических очагов инфекции, восстановление иммунного статуса и пр.).
Следует отметить, что сочетанное применение противовирусных препаратов и иммунобиологических средств имеет ряд преимуществ. Во-первых, комплексная терапия обеспечивает синергидный эффект. Во-вторых, позволяет снизить дозу противовирусного химиопрепарата, уменьшая вероятность развития НЛР, сокращая его токсическое воздействие на организм и снижая вероятность возникновения устойчивых штаммов герпес-вирусов. Кроме того, это значительно сокращает продолжительность острого периода болезни и сроки лечения.
Одним из препаратов, показавшим свою эффективность при лечении герпес-ассоциированных заболеваний у детей, является инозин пранобекс. Инозин пранобекс — это синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием. Препарат восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию иммуноглобулина G, интерферонов, интерлейкинов (ИЛ-1 и ИЛ-2), снижает образование провоспалительных цитокинов (ИЛ-4 и ИЛ-10), потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов. Механизм противовирусного действия препарата связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации, усилении подавленного вирусами синтеза мРНК лимфоцитов, что сопровождается угнетением биосинтеза вирусной РНК и трансляции вирусных белков.
Инозин пранобекс малотоксичен, хорошо переносится, в России рекомендован в виде таблеток детям с 3-летнего возраста (масса тела более 15 кг). За рубежом он доступен и в форме сиропа и не имеет возрастных ограничений. Препарат назначается по 50–100 мг/кг/сут внутрь в 3–4 приема в течение всего острого периода болезни (5–10 дней в зависимости от длительности вирусемии и выраженности синдрома интоксикации). В качестве поддерживающей терапии для восстановления иммунологических показателей возможно назначение препарата по иммуномодулирующей схеме (50 мг 2 раза в день в течение 14–28 дней). Доказана высокая эффективность курсовой терапии инозином пранобексом (50 мг/кг массы тела в сутки в 3–4 приема внутрь, три курса лечения по 10 дней с интервалом 10 дней) [7], комбинированной курсовой терапии с использованием инозина пранобекса и рекомбинантного интерферона α-2β (3 курса по 10 дней с интервалом 14 дней) у детей с микст-вирусными инфекциями [8].
Применение инозина пранобекса как препарата с иммунотропным и противовирусным действием на различных этапах лечебно-профилактических мероприятий позволяет избежать полипрагмазии, тем самым снизить медикаментозную нагрузку на организм и уменьшить риск нежелательных эффектов.
Литература
- Кускова Т. К., Белова Е. Г. Семейство герпес-вирусов на современном этапе // Лечащий Врач. 2004, № 5, с. 64–69.
- Hjalgrim H., Askling J., Rostgaard K. et al. Characteristics of Hodgkin’s lymphoma after infectious mononucleosis // N. Engl. J. Med. 2003; 349: 1324–1332.
- Никольский И. С., Юрченко В. Д., Никольская К. И. Характеристика активной хронической Эпштейна–Барр вирусной инфекции: клинико-иммунологический синдром // Современные инфекции. 2003, № 3, с. 60–62.
- Katz B. Z., Shiraishi Y., Mears C. J., Binns H. J., Taylor R. Chronic fatigue syndrome after infectious mononucleosis in adolescents // Pediatrics. 2009, Jul; 124 (1): 189–193.
- Lerner A. M., Begar S. N., Deeter R. G. IgM serum antibodies to Epstein-Barr virus are uniquely present in a subset of patients with the chronic fatigue syndrome // In Vivo. 2004, Mar-Apr; 18 (2): 101–106.
- Maakaroun N. R., Moanna A., Jacob J. T., Albrecht H. Viral infections associated with haemophagocytic syndrome // Rev. Med. Virol. 2010, Mar; 20 (2): 93–105.
- Симованьян Э. Н., Денисенко В. Б., Григорян А. В. Эффективность применения инозина пранобекс у часто болеющих детей с хронической Эпштейна-Барр вирусной инфекцией: результаты рандомизированного исследования // Вопросы современной педиатрии. 2011, Т. 10, № 2, С. 16–21.
- Нестерова И. В., Ковалева С. В., Чудилова Г. А., Ломтатидзе Л. В., Клещенко Е. И., Шинкарева О. Н. Динамика изменений фенотипа и функциональной активности нейтрофильных гранулоцитов у иммунокомпрометированных детей с повторными ОРВИ, ассоциированными с герпесвирусными инфекциями, на фоне комбинированной интерфероно- и иммунотерапии // Цитокины и воспаление. 2014, Т. 13, № 1, с. 113.
Т. А. Бокова, доктор медицинских наук, профессор
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
[youtube.player]Заболевание, причиной появления которого служит вирус простого герпеса (ВПГ) называется герпетическая инфекция. Оно может быть у каждого человека и даже у маленького ребенка. В этой статье мы подробно рассмотрим симптомы, клинические рекомендации и этапы лечения болезни.
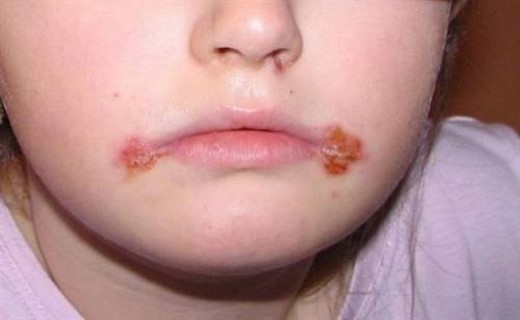
Симптомы заболевания
Приобретенная форма в 90% случаев протекает бессимптомно. При манифестном течении выделяют следующие периоды:
- инкубационный - 2 - 14 дней (в среднем 4 - 5 дней),
- начальный (продромальный),
- разгара (развития болезни),
- угасания (клинического выздоровления).
В зависимости от локализации патологического процесса различают: герпетические поражения кожи, слизистых оболочек, глаз, нервной системы, половых и внутренних органов (патологический процесс может быть изолированным и сочетанным). Наиболее часто встречаются такие симптомы герпетической инфекции, как поражения кожи и слизистых оболочек.
Клинические рекомендации о герпетической инфекции
При типичной форме кожного герпеса в начальном периоде у больного отмечаются такие симптомы: синдром интоксикации, повышается температура тела, в местах будущих высыпаний - жжение и зуд. В периоде разгара появляется характерная сыпь при герпетической инфекции: пятно, превращающееся в везикулу, наполненную серозной жидкостью. Пузырьки обычно располагаются группами на фоне гиперемии и отечности кожи, локализуясь в области каймы губ и крыльев носа, реже - на щеках, лбу, ушах, ягодицах, задней и внутренней поверхности бедер, предплечьях, кистях. Через несколько дней содержимое пузырьков мутнеет. После вскрытия везикул образуются мокнущие эрозии, которые вскоре покрываются бурыми корочками и эпителизируются. Корочки отторгаются, оставляя пигментацию. Воспалительный процесс разрешается в течение 10-14 дней.
Классификация
Типы герпетических инфекций:
А. Приобретенная герпетическая форма:
Б. Врожденная герпетическая форма:
Типы герпетических инфекций по локализации поражения:
- кожи;
- слизистых оболочек;
- глаз;
- половых органов;
- нервной системы;
- внутренних органов.
Типы инфекций по распространенности:
- локализованная;
- распространенная;
- генерализованная.
Типы герпетических инфекций:
- абортивная;
- отечная;
- зостериформная;
- геморрагическая;
- язвенно-некротическая;
- герпетиформная экзема Капоши.
Типы по тяжести:
- выраженность синдрома интоксикации;
- выраженность местных изменений.
Типы по течению:
А. По длительности:
- с осложнениями;
- с рецидивами;
- с наслоением вторичной;
- с обострением хронических заболеваний.
Лечение
Чтобы вылечить заболевание ребенку показан постельный режим, особенно при тяжелых и генерализованных формах заболевания. Диета молочно-растительная, механически щадящая при поражениях желудочно-кишечного тракта и полости рта.
В случаях локализованных кожных форм, протекающих легко, с необширными поражениями и редкими рецидивами (1 раз в 6 мес. и реже), можно ограничиться симптоматическими препаратами, которые обладают дезинфицирующим, подсушивающим, эпителизирующим действием (1 - 2% спиртовые растворы бриллиантового зеленого, метиленового синего, 3% перекиси водорода). У больных с частыми рецидивами (1 раз в 3 мес. и более) проводят этапное лечение: купирование острого процесса в период рецидива и проведение противорецидивной терапии в период ремиссии.
Чтобы провести лечение, в качестве этиотропной терапии используют препараты, блокирующие репликацию вирусов за счет нарушения синтеза их нуклеиновых кислот (ацикловир, теброфен, бонафтон, рио-доксол, идоксуридин, видарабин). При локализованных формах с редкими рецидивами назначают противогерпетические лекарства местно в виде капель, кремов, мазей. При частых рецидивах их применяют внутрь и парентерально. Лечение герпетической инфекции у детей необходимо назначать как можно раньше, до появления пузырьков, и продолжать до эпителизации эрозий. Доза и курс лечения зависят от длительности болезни, локализации и распространенности поражения, частоты рецидивов.
Направлена на нормализацию функций иммунной системы, в том числе интерфероновой защиты. Чтобы провести лечение назначают интерфероны: человеческий лейкоцитарный (в виде аппликаций), при тяжелых генерализованных формах с поражением ЦНС - рекомбинантные (реаферон, берофор, роферон, виферон, велферон).
Используют индукторы интерферона (интерфероногены): циклоферон, полудан, неовир.
В схеме лечения применяют иммуномодуляторы: тимоген, тактивин, тималин, дибазол, метилурацил, нуклеинат Na, витамины С, А, Е; растительные адаптогены - элеутерококк, женьшень, китайский лимонник.
При лечении офтальмогерпеса, герпетического энцефалита и герпетического стоматита (у детей с первичной формой заболевания) особенно эффективен специфический иммуноглобулин.
Нестероидные противовоспалительные средства (индометацин, вольтарен, мефенаминовая кислота), которыми проводят лечение герпетической инфекции у детей, применяют при выраженном отеке, чувстве жжения, зуде.
Всем больным проводят симптоматическую терапию. Антибиотики назначают при генерализованных формах и наслоении бактериальной флоры.
В период ремиссии проводят противорецидивную терапию: обработку противовирусными мазями (кремами) ранее пораженных участков, назначение противовирусных препаратов или индукторов интерферона, неспецифических иммуномодуляторов, растительных адаптогенов, витаминов А, С, Е. Взрослым больным в период стойкой ремиссии возможно проведение вакцинотерапии герпетической поливакциной.
Диспансерное наблюдение рекомендуется только для детей с иммунодефицитными состояниями. Осмотр осуществляет врач поликлиники 1 раз в 3 - 6 мес. в зависимости от степени выраженности иммуносупрессии.
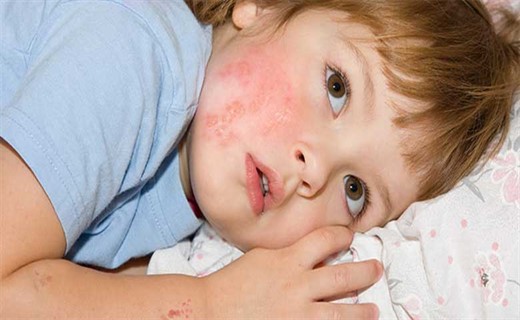
Лекарственные препараты
Противогерпетические (теброфен, риодоксол, идоксуридин, видарабин, ацикловир, валацикловир, фамацикловир) и противоцитомегаловирусные (ганцикловир, фосфоноформат) препараты блокируют репликацию, то есть нарушают синтез нуклеиновых кислот вируса.
Противогерпетические лекарства имеют следующий спектр действия:
- Herpes simplex (типа 1 и 2), Varicella zoster, аденовирусы.
- Риодоксол – оказывает дополнительно противогрибковое действие (микроспория, трихофития, кандидоз).
- Ацикловир, фамацикловир и валацикловир – дополнительно влияют на вирус Эпштейн-Барра, человеческий вирус герпеса 6-го типа, и слабо – на цитомегаловирус.
- Ганцикловир и фосфоноформат влияют – на цитомегаловирус.
- Фосфоноформат – на вирус иммунодефицита человека.
Фармакокинетика противогерпетических препаратов
Противогерпетические препараты теброфен и риодоксол – применяют местно, в виде мази. Идоксуридин – практически используют только местно:
- при заболевании глаз – раствор препарата капают в конъюнктивальный мешок через 1 ч днем и через 2 ч ночью;
- при постгерпетической невралгии. От внутривенного введения идоксуридина сейчас отказались из-за очень высокой токсичности.
Видарабин применяют местно, а при диссеминированной герпетической инфекции (энцефалит) вводят внутривенно капельно. Но препарат плохо растворяется, поэтому его инфузия в большом количестве жидкости длится около 12 ч, что нежелательно для больного с энцефалитом, отеком мозга.
Проникновение видарабина через гематоэнцефалический барьер составляет примерно 30% от концентрации препарата в плазме крови. В печени происходит превращение препарата в арабинозин гипоксантин, этот метаболит сохраняет активность и быстр 0 распределяется в тканях. Элиминация происходит с мочой (50%) и калом (50%).

Ацикловир, валацикловир, фамацикловир и ганцикловир – внутрь во время еды, а также вводят внутримышечно (только ацикловир) и внутривенно (только ацикловир, ганацикловир и фамацикловир).
Биоусвоение из желудочно-кишечного тракта равно 15 - 20% (для валацикловира – 54 %), тем не менее этого достаточно для оказания эффекта. У препаратов лечения высокая активность, и они обладают способностью избирательно накапливаться в клетках, инфицированных вирусом, но не в тканях. Их концентрация в инфицированных клетках может быть в 30 - 120 раз больше, чем в плазме крови. Это важное обстоятельство объясняет значительно большую широту терапевтического действия данных препаратов по сравнению с другими и меньшую опасность возникновения осложнений.
Связывание с белками плазмы крови всего 9-30%, поэтому препараты хорошо проникают в различные ткани и жидкости (включая и ликвор). В организме человека валацикловир (1-валиновый эфир ацикловира) быстро и почти полностью превращается в ацикловир и валин под действием фермента валацикловиргидролазы. 10-15% ацикловира и ганцикловира подвергается биотрансформации в печени.
Большая часть препаратов (80 – 90 %) в неизмененном виде и в виде метаболита 9-карбоксиметоксиметилгуанина выводится почками. Период полуэлиминации примерно 3,3 ч, однако при почечной недостаточности он может увеличиваться до 20 ч, поэтому необходимо корректировать их дозированияе. Так, при Cl кр 1 /3; при Cl кр 1 /2; и при Cl кр 
Осложнения
В остром периоде осложнения имеют в основном, неспецифический характер и обусловлены наслоением вторичной бактериальной флоры. При тяжелых поражениях герпетической этиологии возможно развитие специфических осложнений и формирование резидуальных явлений (очаговая неврологическая симптоматика, минимальная мозговая дисфункция церебро-астенический синдром, слепоте рубцовое сужение пищевода, слоновость половых органов, карцинома шейки матки, привычное невынашивание беременности).
Врожденная герпетическая инфекция
Внутриутробное инфицирование плода может происходить в том случае, если у матери во время беременности наблюдается первичное инфицирование или рецидив, сопровождающийся вирусемией. Возможно заражение восходящим путем при генитальном герпесе. Герпетическая инфекция у матери является фактором риска невынышиваемости беременности и перинатальной патологии ребенка. При заболеваний матери в:
- I триместре беременности возможны выкидыши,
- во II триместре - мертворождение и пороки развития (микроцефалия, слепота, атрезии различных отделов желудочно-кишечного тракта и др.),
- в III триместре - врожденная инфекция новорожденного.
Симптомы герпетической инфекции у детей не всегда проявляются поражением кожи и слизистых оболочек. Часто заболевание протекает как манифестное заражение; преобладают генерализованные формы с признаками менингоэнцефалита, гепатита, пневмонии, поражения желудочно-кишечного тракта. У детей, не получавших этиотропной терапии, летальность составляет 65%.
Особенности герпетической инфекции у детей раннего возраста
Заражение новорожденных происходит от больной матери интранатально или непосредственно после рождения, а также от персонала родильного дома. Заболевание чаще развивается на 5 - 10-й дни жизни, протекает с высокой лихорадкой (до 39 - 40° С), резко выраженной интоксикацией (рвотой, бледностью кожи, акроцианозом, одышкой, беспокойством или заторможенностью). Первично поражается слизистая оболочка полости рта, в горле, затем появляются герпетические высыпания на коже. У детей с предшествующим поражением кожи (экзема, нейродермит) возможно развитие герпетиформной экземы Капоши. Иногда наблюдаются такие симптомы: судороги, редко - потеря сознания, геморрагические высыпания, диарейный синдром. Течение болезни имеет генерализованный характер с вовлечением в патологический процесс ЦНС и внутренних органов. Летальность высокая, смерть часто наступает при явлениях инфекционно-токсического шока.
Профилактика
Большое значение в профилактике герпетической инфекции имеет санитарно-просветительная работа по формированию гигиенических навыков, закаливание, а также устранение факторов, способствующих активации герпетической инфекции (стрессовые ситуации, избыточная инсоляция, физические перегрузки, очаги хронического заражения). Особое внимание необходимо уделять детям, страдающим экземой и мокнущими формами атопического дерматита. Роженицам, имеющим герпетические высыпания на гениталиях, рекомендуют проведение кесарева сечения. Новорожденным в случае контакта с больными герпетической инфекцией следует назначать специфический противогерпетический иммуноглобулин.
Доктор Комаровский о герпетической инфекции
[youtube.player]Герпетическая вирусная инфекция встречается в скрытом виде у большинства взрослого населения во всем мире. Считается, что уровень инфицированности в развитых странах достигает 95% среди людей взрослого возраста и 70% среди детей. Наиболее часто вирусы простого герпеса вызывают локализованные высыпания на слизистой оболочке губ или половых органов.
При наличии у пациента иммунодефицитного состояния или других факторов риска, возможно возникновение герпетического серозного энцефалита, характеризующегося лихорадкой, появлением головной боли, ригидностью мышц и другими неврологическими симптомами. Инфекционное поражение головного мозга требует немедленной госпитализации больного для проведения комплексной диагностики и терапии. При позднем начале лечения болезнь может стать причиной инвалидизации или привести к летальному исходу.
Общая информация
Вирусные энцефалиты представляют серьезную угрозу для заболевшего человека в связи с возникновением стойкого неврологического дефицита и риска развития отека мозга. Последние исследования данной группы болезней показывает, что у 40-45% больных с вирусным поражением центральной нервной системы, в качестве основного возбудителя выступает вирус простого герпеса 1 типа (ВПГ-1 типа).
Герпетический энцефалит может встречаться у людей любого возраста. Однако выделяют два основных пика заболеваемости – от полугода до 20 лет и после 50 лет. До активного использования Ацикловира и его производных, показатель смертности достигал 70%. На сегодня летальный исход наблюдается у одного больного из десяти.
Клинические проявления
Симптомы герпетического энцефалита развиваются в соответствии с определенными периодами течения патологии:
- инкубационный период, характеризуется полным отсутствием каких-либо признаков заболевания (говоря о том, сколько дней длится инкубационный период при герпетической инфекции, врачи выделяют срок от 2 до 14 дней, необходимых возбудителю для начала активного размножения);
- продромальный период, как правило, не выражен, в связи с острым или молниеносным началом болезни (у пожилых больных возможно появление синдрома интоксикации за несколько дней до возникновения симптомов энцефалита);
- стадия специфических проявлений, во время которой возникают характерные клинические признаки герпетического энцефалита в виде неврологических нарушений;
- период реконвалесценции или выздоровления, характеризующийся восстановлением структуры и функции головного мозга.
Основной период герпетического энцефалита – стадия разгара, связанная с поражением структур центральной нервной системы. У взрослых людей, также, как и у детей, преимущественно отмечается следующая клиническая картина инфекции:
- симптомы возникают остро или молниеносно, в среднем, появление признаков энцефалита занимает один день;
- повышение температуры тела до 38 о С и более, а также головные боли – ведущие клинические проявления герпетического поражения головного мозга;
- у больных наблюдаются количественные нарушения сознания в виде ступора и сопора, характеризующиеся заторможенностью и отсутствием взаимодействия с окружающими людьми;
- пациент дезориентирован во времени, в пространстве и собственной личности, может вести себя неадекватно обстановке;
- судорожные проявления различной степени выраженности;
- очаговые неврологические симптомы, определяющиеся преимущественным поражением конкретного участка головного мозга: нарушения зрения, чувствительности, двигательной сферы и пр.
Помимо характерных признаков энцефалита, у ряда пациентов возникают проявления менингита: ригидность затылочных мышц и симптом Кернига. Последний характеризуется невозможностью разогнуть ногу в колене при ее предварительном сгибании в коленном и тазобедренном суставе.

Течение серозного энцефалита у пожилых людей имеет ряд особенностей:
- клиническая картина развивается подостро – в течение нескольких суток;
- наиболее выражены нарушения памяти и расстройства в когнитивных функциях, пациент становится рассеянным, не способным концентрироваться на задачах;
- спутанность сознания постепенно прогрессирует на фоне нарушений поведения;
- в связи с частым поражением лобной доли, у больных отмечается снижение самоконтроля, спонтанности в движениях и возможности анализировать обстановку;
- близкие люди и доктор отмечают нарушения речи, которые усиливаются в отсутствии терапии.
Разнообразие клинических симптомов может представлять проблему для быстрой диагностики герпетического энцефалита. При обращении в лечебное учреждение с симптомами инфекции, лечащий врач проводит комплексное обследование, позволяющее выставить точный диагноз.
Диагностические мероприятия
Согласно современным клиническим рекомендациям, диагностика герпетического энцефалита у новорожденных, детей и взрослых пациентов основывается на следующих двух методах:
- ПЦР-исследовании ликвора, полученного путем люмбальной пункции.
- Нейровизуализации, основанной на проведении магнитно-резонансной или компьютерной томографии.
Анализ ПЦР на возбудителей ВПГ 1 и 2 типа рекомендуют дополнять проведением магнитно-резонансной томографии. Метод позволяет врачу определить локализацию воспалительного очага в ЦНС, а также выраженность изменений в головном мозге. При недоступности или невозможности проведения МРТ, возможно использование компьютерной томографии или электроэнцефалографии (ЭЭГ). Однако два данных метода обладают более низкой чувствительностью и специфичностью в отношении энцефалита.
Помимо двух указанных методов, в клинической практике используются следующие подходы:
- Сбор жалоб, а также истории развития болезни. Лечащий врач при внимательном расспросе может установить факт недавнего обострения герпеса, проявившегося в виде характерных высыпаний на слизистой оболочке губ.
- При клиническом анализе крови отмечается лимфоцитоз (увеличение количества лимфоцитов, ответственных за противовирусный ответ) и ускорение скорости оседания эритроцитов (СОЭ).
- В биохимическом исследовании выявляется повышение концентрации фибриногена и С-реактивного белка, что свидетельствует о развитии воспалительного процесса.
Проведение вирусологических и серологических исследований (иммуноферментный анализ, реакция преципитации) не рекомендуется в связи с длительностью выполнения анализов и низкой информативностью результатов для лечащего врача.
Важно отметить, что интерпретировать полученные данные должен всегда только доктор. Попытки самостоятельной постановки диагноза и последующего самолечения приводят к развитию осложнений и ухудшению прогноза при герпетическом энцефалите.
Принципы проведения терапии
В связи с тем, что основной причиной развития герпетического энцефалита является вирус простого герпеса, на первое место в лечении выходят противогерпетические средства – Ацикловир и его аналоги.
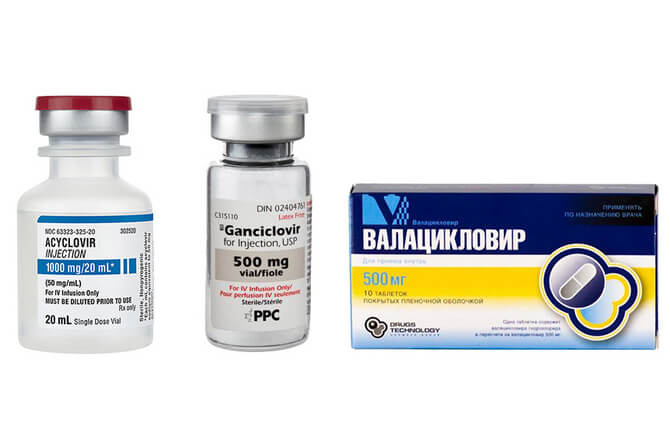
Противовирусные препараты используемые в терапии герпетического энцефалита
Ацикловир назначается всем больным с симптомами энцефалита и подтвержденным диагнозом по ПЦР-исследованию ликвора. Стандартная схема лечения – 14 дней приема Ацикловира по 10 мг на кг массы тела трижды в сутки. Если у человека имеются признаки иммунодефицита или больному от 3 месяцев до 12 лет, то терапия должна продолжаться 21 день с сохранением указанной дозировки препаратов.
По окончанию первого цикла приема Ацикловира проводится контрольная люмбальная пункция и ПЦР-анализ ликвора. Если результаты отрицательные, то противогерпетические препараты отменяют. Если в ликворе выявлен генетический материал возбудителя, – терапия продолжается еще одну неделю.
При наличии нечувствительности герпес-вирусов к Ацикловиру, используется Ганцикловир (5 мг на кг массы тела каждые 12 часов) или Фоскарнет (90 мг на кг массы тела каждые 12 часов или по 60 мг на кг массы тела каждые 8 часов). Кроме того, современные исследования демонстрируют высокую эффективность использования Валацикловира в дозе 1 гр каждые 8 часов. При подобной схеме лечения в ликворе наблюдается быстрое повышение концентрации ацикловира (действующее вещество препарата) до терапевтического уровня. Важным преимуществом Валацикловира, является его прием в виде таблеток, в отличие от внутривенного введения Ацикловира.
Помимо противовирусного лечения герпетического энцефалита у каждого больного проводится симптоматическая терапия, направленная на устранение основных признаков заболевания.
При развитии отека мозга, пациенту показано внутривенное введение Маннитола, являющегося диуретиком. Препарат обеспечивает снижение объема ликвора и снижает риски развития тяжелых последствий смещения головного мозга. Дополнительный терапевтический эффект наблюдается при использовании глюкокортикостероидов (Дексаметазона и др.).
У 40% пациентов с герпетическим энцефалитом наблюдается судорожный синдром, который требует отдельного лечения. Высокой эффективностью в терапии судорог обладает Диазепам, Лоразепам и их аналоги. При сохранении судорожных явлений, пациента переводят на Пропофол или Фенобарбитал.
Медикаментозные препараты, используемые для лечения серозного энцефалита, обладают определенными показаниями и противопоказаниями к своему использованию. В связи с этим, а также с тяжестью заболевания, все методы терапии должен назначать только лечащий врач после госпитализации и обследования пациента.
Возможные осложнения
Неправильная диагностика и лечение герпетического энцефалита – причина развития неблагоприятных последствий. У пациентов часто отмечаются следующие состояния:
- менингит с развитием характерных менингиальных признаков: ригидность затылочных мышц, рвота, сильные головные боли и т.д.;
- хронические головные боли и головокружения;
- нарушения работы органов чувств: зрения, слуха, а также изменения речи различной степени тяжести;
- двигательные нарушения в виде парезов и параличей;
- когнитивные расстройства, проявляющиеся снижением памяти, внимания, способности концентрироваться на деятельности;
- нарушения функций мочевыделительной системы, вплоть до недержания мочи;
- снижение интеллекта;
- галлюцинации, эмоциональная лабильность и другие изменения личности.
Возникновение любых осложнений серозного воспаления головного мозга связано с органическим повреждением структур ЦНС или переходом воспалительной реакции в хроническое течение. Больные с признаками неблагоприятных последствий нуждаются в дополнительном обследовании и назначении реабилитационных мероприятий. В среднем, легкая неврологическая симптоматика проходит через 2-4 недели после выздоровления. В случае тяжелых нарушений работы головного мозга, процесс его восстановления может затянуться до нескольких лет.
Тяжелым осложнением инфекции считается переход заболевания в хроническую форму, характеризующуюся рецидивами воспаления в отдельных структурах головного мозга. Больные при этом предъявляют жалобы на постоянные головные боли, а также нарушения отдельных неврологических функций. Лечение в этом случае направлено на подавление развитие вируса и предупреждение рецидивов инфекции за счет использования противогерпетических препаратов, в первую очередь, Ацикловира.
Развитие герпетического энцефалита у детей и взрослых может стать причиной тяжелой инвалидности или гибели пациента. Своевременное обращение за медицинской помощью при первых признаках инфекции – залог правильного лечения и предупреждения последствий заболевания. Ни в коем случае не стоит заниматься самостоятельной терапией или применять методы народной медицины, так как они не имеют доказанной эффективности и безопасности.
[youtube.player]Читайте также:


