Седьмая пандемия холеры вызвана циркуляцией вибриона
ГОУ Педагогическая академия последипломного образования, Москва, Россия;
Национальный НИИ общественного здоровья РАМН, Москва, Россия.
Пандемии холеры в мире
и её профилактика в Российской Федерации
Г лобализация мировой экономики в последние десятилетия XX века — начале XXI столетия способствовала бурному развитию транспортных связей, международной торговли, трудовой миграции и туризма, в результате чего увеличилась быстрота распространения различных инфекционных заболеваний между континентами и риск их проникно вения в районы, где ранее эти болезни были практически искоренены (в частности, малярия, лейшманиозы, различные трансмиссивные лихорадки, холера и другие). Помимо этого, всё чаще стали возникать вспышки особо опасных инфекций, ранее не регистрируемые на данных территориях. Примером могут служить марбургская ге моррагическая лихорадка, лихорадка Эбола, ВИЧ-инфекция . Всё это осложняет эпидемиологическую ситуацию и требует соответствующих мер со стороны Всемирной организации здравоохранения (ВОЗ) и её государств-членов.
В настоящее время особенностью холеры является доминирующая удельная доля детей в структуре заболевания (до 70 %) и резко возрастающие экономические потери при ликвидации эпидемических вспышек [3]. В условиях глобализации в 1990-2000 гг. в России произошло резкое изменение социальных условий жизни, рост международной и внутренней миграции, ухудшение инфраструктуры населённых пунктов, сброс недостаточно очищенных и необеззараженных хозяйственно-бытовых сточных вод, недостаточная готовность медицинских учреждений к своевременному проведению противоэпидемических мероприятий, что обусловило распространение социально опасных инфекций, включая холеру. В неблагоприятно складывающейся эпидемиологической ситуации крупные города часто представляют всю гамму предпосылок для возникновения первоначальных мест эпидемии холеры и основных этапов на пути её продвижения [3, 7].
Расхождения в оценке сроков окончания пандемий вероятно связаны с тем, что редко когда спад заболеваемости холерой был отчётливо выражен. Общепринято, что первая пандемия классической холеры была зарегистрирована в 1817 г. и завершилась к 1823 г., вторая — с 1826 г. по 1837 г., третья — с 1844 г. по 1861 г., четвёртая — с 1863 г. по 1875 г., пятая — с 1883 г. по 1896 г., шестая — с 1900 г. по 1926 г. Для каждой из указанных пандемий было характерно широкое распространение холеры во многих странах мира с последующим постепенным угасанием эпидемии и локализацией заболевания в эндемичных очагах — дельтах рек Ганга и Брахмапутры (Индия).
На территорию России в XIX веке холера проникала восемь раз (1823 г., 1829 г., 1830 г., 1837 г., 1847 г., 1852 г., 1865 г. и 1892 г.). По официальным данным Медицинского департамента холерой заболело 4,8 млн. человек, из которых почти 2 млн. умерло. В XX веке в период шестой пандемии эпидемические пики регистрировали в 1910, 1915, 1918 и 1921 годах. С 1902 по 1916 г оды холерные очаги поразили 40 губерний, в результате чего заболело 358 тыс. и умерло 157 тыс. человек . Во время Гражданской войны (1918-1921 гг.) заболеваемость холерой резко возросла на Кавказе, в Сибири, и особенно среди голодающих Поволжья. В целом в указанный период в Европейской части России, в Сибири и на Кавказе холерой было охвачено 37 губерний. В 1920-1922 гг. в Ростове-на-Дону больные выявлялись практически круглогодично, что явилось основанием полагать об эндемичности очагов холеры в данном районе [2, 14]. По официальным данным в России после 1926 г. холеру не наблюдали и болезнь считалась ликвидированной. Этот год считается годом окончания шестой пандемии холеры в мире.
Важно отметить, что после открытия Робертом Кохом в 1884 г. холерного вибриона, в последующем было установлено, что в природе встречается большое число вибрионов, обладающих гемолитическими свойствами, в то время как классические холерные вибрионы гемолитических свойств не имеют. Исходя из этого, Kraus (1903) предложил использовать гемолитический тест для дифференциации непатогенных и патогенных холерных вибрионов. Этот критерий казался вполне обоснованным до 1906 г., когда Gotschlich выделил гемолитические штаммы холерных вибрионов от трупов паломников на карантинном пункте Эль Тор (Египет). Поскольку в этот период холерной эпидемии не было, то и патогенность гемолитического вибриона не считали полностью доказанной.
Однако в 1937 г. в Индонезии возник эндемичный очаг инфекции с синдромом холеры. Это заболевание было названо парахолерой в связи с тем, что возбудителем явился вибрион Эль-Тор, ранее считавшийся непатогенным. В 1939 г. de Moor описал эндемическую холеру на острове Целебес, причиной которой был Эль-Тор — гемолитический биотип V. c holerae. И хотя заболевание не имело тенденции к распространению, иногда оно выходило за пределы о. Целебес. Так, эпидемические вспышки были зарегистрированы на о. Сулавеси, в г. Джакарте (о. Ява) и г. Сингапуре (п-ов Малакка). Со временем вибрион Эль-Тор потерял свои гемолитические свойства и отличался от классического вибриона лишь устойчивостью к IV фагу Mukerjee и к полимиксину, а также способностью вызывать агглютинацию куриных эритроцитов [20, 21].
В первые годы седьмой пандемии стало ясно, что по эпидемиологическим особенностям холера Эль-Тор отличалась от классической формы заболевания. Во-первых, это относится к условиям распространения инфекции как в каждой отдельно взятой стране, так и при перемещении из одной страны в другую. Холера Эль-Тор характеризовалась тем, что инфекция не проявляла себя в странах, расположенных рядом с очагами болезни на пограничных с ними территориях, и, в то же время, вспышки её возникали в непредвиденных местах. Во-вторых, в отличие от классического варианта, холера Эль-Тор нередко проявлялась в виде трудно диагностируемых форм и носительства. При этом было установлено, что вспышки инфекции протекали без алгидных заболеваний и зачастую проходили полностью незамеченными.
Сравнительный анализ свидетельствует, что возбудитель Эль-Тор отличается от классической холеры именно своей большей устойчивостью к воздействию факторов внешней среды. Продолжительное выживание холерных вибрионов ctx + и ctx - было обусловлено формированием симбиотических связей вибрионов с компонентами водной экосистемы, их экологической толерантностью к абиотическим (температура, концентрация солей, рН и другие) и биотическим факторам (различные биоценозы). Сохранение жизнеспособности холерных вибрионов Эль-Тор обеспечивала их экологическая пластичность и способность к адаптации в условиях окружающей среды, в том числе образованию L-форм и форм некультивируемых холерных вибрионов.
Особенностями возбудителя Эль-Тор объясняется, что в этиологическом отношении седьмая пандемия холеры на ранних этапах характеризовалась как смешанная, т.е. была вызвана как классическим вибрионом, так и вибрионом Эль-Тор. Весьма важно, что вибрион Эль-Тор может долго сохраняться в организме переболевших и вибриононосителей. Имеются сведения, что у ряда переболевших холерой Эль-Тор вибриононосительство наблюдалось в течение 3-4 месяцев и был описан случай вибриононосительства в течение 6 лет у переболевшей холерой женщины. Исследователи сравнивали распространение холеры Эль-Тор с айсбергом, большая часть которого находится под водой. При этом, отношение числа тяжёлых форм холеры к количеству скрытых источников инфекции, колебалось в широких пределах: 1:1, 1:10, 1:25 и даже 1:100, в связи с чем не всегда удавалось проследить эпидемическую связь между отдельными вспышками заболевания.
В настоящее время основные эпидемиологические аспекты холеры определяются пандемическим распространением возбудителя V. c holerae eltor, хотя в эндемичных очагах Бангладеш в 1981 г., 1983 г., 1988 г. и 1992 г. продолжали регистрировать вспышки классической холеры. В 1990-х годах крупные эпидемии, вызванные V. c holerae 0139 (Бенгал) были зарегистрированы в странах Южной и Юго-Восточной Азии. В дальнейшем отмечали случаи завоза холеры Бенгал (без последующего распространения) в Северную Америку, Европу (в т.ч. — Россию) и Азию в связи, с чем прогнозировали начало восьмой пандемии холеры, хотя эксперты ВОЗ высказывали точку зрения, что глобальная угроза распространения холеры маловероятна.
В связи с этим необходимо отметить, что в последнее время неоднократно высказывались сомнения в антропонозной природе холеры. Сегодня некоторые учёные придерживаются мнения, что нетоксигенные штаммы холерных вибрионов являются естественными обитателями сточных солоноватых вод и эстуариев и составляют компонент автохтонной микрофлоры в зоне умеренного климата [1, 3, 6]. Механизмы автохтонного, независимого от человека, существования V . cholerae в природных водоёмах обусловлены их устойчивостью к абиотическим факторам водной среды и случаями постоянного взаимодействия с другими сочленами водных сообществ. Это обстоятельство позволяет отнести холеру к водным сапронозам. Получены доказательства перехода V . cholerae в некультивируемое состояние и L -формы, обеспечивающие сохранение возбудителя во внешней среде [13]. Вероятно, в этом кроется причина возникновения сезонных эпидемий без заноса извне.
Одним из главных признаков холеры Эль-Тор является формирование стойких вторичных очагов на территориях, по климатическим условиям значительно отличающимся от районов с эндемическими очагами данной инфекции. Следует отметить, что, в Ростовской области (1995), Дагестане (1996) и Саратовской области (1995, 1996) в пробах воды поверхностных водоёмов встречались единичные токсигенные штаммы холеры. Отсутствие эпидемических осложнений при выделении этих штаммов возбудителя свидетельствовало о невыявленных больных или вибриононосителях. Регистрация случаев заболеваний и вибриононосительства в течение семи и более лет подряд на фоне преимущественного выделения вибрионов Эль-Тор из поверхностных водоёмов в Астраханской области позволила ряду исследователей предположить возможность временного укоренения инфекции на данной территории [3, 5, 9].
В итоге, основными причинами, обусловливающими мировое распространение холеры и её детерминирующее отличие в различных регионах, считают способность данной инфекции к пандемичному, поступательному распространению, а также способность формировать эндемичные очаги во взаимосвязи с социально-экономическим развитием отдельных стран и предпринимаемыми мерами по профилактике и борьбе с холерой на таких территориях.
В этом состояла особенность седьмой пандемии. Основными путями распространения холерного вибриона были водный и пищевой, вследствие употребления морских продуктов, а также овощей, выращенных при поливе сточными водами. Во время вспышек холеры значительный удельный вес составлял контактный путь передачи. Рядом исследователей было сделано предположение о проникновении в Южную Америку холерного вибриона в балластном слое воды на днищах китайских грузовых судов [18].
В последующем разгадка происхождения эпидемических штаммов холеры была сделана на основе генетических и молекулярно-биологических методик. В результате было установлено, что штаммы холерных вибрионов, выделенные в странах Южной Америки, идентичны штаммам, вызывающим эпидемии в Африке, Азии и Тихоокеанском регионе. Летальность от холеры в мире в 1990-1998 гг. варьировала от 1,8 до 4,7 % с максимальными показателями в Азии — 5,7 %, Африке — 9,1 %, Америке — 2,1 % и Европе — 1,7 %. В Южной Европе высокий уровень летальности отмечали в Румынии — 4,0 % (1991 г.) и 6,7 % (1993 г.); в Албании — 4,0 % (1994 г.) [4].
Холера в Российской Федерации (РФ) и странах Содружества Независимых Государств (СНГ) имела завозной характер. За период наблюдения было зафиксировано более 100 завозов из Индии, Пакистана, Руанды, Шри-Ланка, Ливана, Турции, Ганы, Румынии. В России наибольшую частоту завозов из других стран выявляли в Центральном регион е — 51 %, северном Кавказе — 24,8 %, Волго-Вятском регион е — 8 %, Западной Сибири — 7 %, Поволжье — 5 %. Основной причиной завоза холеры на территорию РФ и стран СНГ являлась увеличившаяся в 1990-е годы международная миграция [5]. Так, в 1994-1995 гг. в Сибири отмечались вспышки холеры, возбудитель которой проник из Индии и Турции, первоначально в города Омск, Барнаул и Новосибирск, а в 1997 г. — из Республики Казахстан — в Иркутск и Ачинск.
Единичные случаи холеры встречались в г. Кисловодске (1992 г.), г. Ессентуки (1993 г.), г. Астрахани (1996 г.), г. Махачкале (1996 г.), г. Челябинске (2000 г.). Впервые в 1999 г. холера была зарегистрирована в Приморском крае и на Сахалине, где темп её прироста составил +56,5 %. Наиболее высокие показатели холеры отмечались на Северном Кавказе из-за вспышек в г. Ставрополе (1990 г.) и эпидемии в Дагестане (1994 г.), где заболеваемость составляла соответственно 14,4 и 0,5 на 100 тыс. населения. В Центральном регионе РФ, Среднем и Нижнем Поволжье, Западной Сибири интенсивные показатели варьировали в пределах от 0,05 до 0,1 на 100 тыс. человек [5, 9, 10].
Научным обоснованием для дифференцированного проведения профилактических мероприятий (с учётом оценочных данных на наличие у холерных вибрионов ctx-гена, степени потенциальной опасности пути передачи и возникновения вспышек) в 1990 г. стало разделение России на административно- территориальные группы, в результате чего было выделено три основных типа территорий — I-й тип, II-й тип (подтипы А и Б) и III-й тип (подтипы А, Б и В), что позволило оптимально регламентировать сроки и объём бактериологических обследований и способствовало уменьшению финансовых затрат.
Среди противоэпидемических мероприятий по локализации и ликвидации очагов холеры основную роль играют мероприятия, направленные на установление и нейтрализацию источника инфекции и активное выявление заболевших путём подворных обходов. Провизорная госпитализация и изоляция контактировавших с заболевшим (пациентом) имеет решающее значение в общей системе профилактических мероприятий. Важным звеном в ходе ликвидации холерных вспышек являются специализированные противоэпидемические бригады (СПЭБ). Использование базы данных позволяет оперативно осуществлять слежение за уровнем и динамикой инфицированности и лечения, определять территорию риска, действующие пути и факторы передачи холеры, что, в свою очередь, обеспечивает принятие адекватных противоэпидемических мер.
1. Бароян О.В., Бургасов П.Н., Гайлонская И.Н., Мединский Г.М. Экология холерных вибрионов. //Вестник АМН СССР. 1975. № 2. С 45-53.
2. Ефременко А.А., Ревенок Н.Д. Из истории холерных эпидемий (Херсонщина, 1920-1922 годы). //Журнал микробиологии, эпидемиологии и иммунобиологии. 1974. № 3. С. 148-151.
5. Ломов Ю.М., Онищенко Г.Г., Москвитина Э.А. и др. Эпидемиологическая обстановка по холере в 90-е годы в мире, странах СНГ и России. //Эпидемиология и инфекционные болезни. 1999. № 3. С. 17-21.
6. Мишанькин Б.Н., Романова Л.В., Ломов Ю.М. и др. Vibrio cholerae О139, выделенные от людей и из воды открытых водоёмов: сравнительное генотипирование. //Журнал микробиологии, эпидемиологии и иммунобиологии. 2000. № 3. С. 3-7.
7. Онищенко Г.Г. Современные проблемы особо опасных инфекций в России и мире. //Здравоохранение Российской Федерации. 2005. № 4. С . 21–26.
8. Онищенко Г.Г. Эпидемиологическая обстановка в России в 1991-1996 гг. по заболеваемости социально обусловленными инфекционными заболеваниями. //Журнал микробиологии, эпидемиологии и иммунобиологии. 1998. № 1. С. 24-35.
9. Онищенко Г.Г., Ломов Ю.М., Москвитина Э.А. Холера в Республике Дагестан. //Журнал микробиологии, эпидемиологии и иммунобиологии. 1995. № 2 (приложение).
11. Ряпис Л.А., Беляков В.Д. Современные достижения в молекулярной эпидемиологии холеры. //Журнал микробиологии, эпидемиологии и иммунобиологии. 1995. № 1. С. 109-111.
12. Смирнова Н.И., Кокушкин А.М. Эпидемически значимые штаммы холерного вибриона: генетические особенности и возникновение. //Эпидемиология и инфекционные болезни. 2000. № 3. С. 25-29.
13. Смоликова Л.М., Милютин В.Н., Лопатина Н.В. и др. Обнаружение L-форм холерных вибрионов в воде открытого водоёма. //Журнал микробиологии, эпидемиологии и иммунобиологии. 1977. № 9. С . 118-122.
16. Cook W.L., Wachsmuth K., Feeley J., Huq I. The question of classical cholera. //Lancet. 1983. Vol. 1, № 8329. PP. 879-880.
17. Faruque S.M., Albert M.J., Siddique A.K. et al. Emergence of a new clon of toxigenic V. cholerae 01 biotype El Tor displacing V. cholerae 0139 Bengal in Bangladesh. //J. Clin. Microbiol. 1993. Vol. 31. № 9. PP. 2513-2516.
18. Glass R.I., Idbel M., Brandling-Bennet A.D. //Science. 1992. Vol. 256. PP. 1524-1525.
20. Mosley W.H., Alvero M.G., Joseph P.R. et al. Studies of cholera El Tor in the Philippines. Transmission of infection among neighbourhood and community contacts of cholera patients. //Bull. WHO. 1965. Vol. 35. № 5. PP. 651-660.
21. Mosley W.H., Khan M. Cholera epidemiology — some environmental aspects. //Progr. Water Technol . 1979. Vol . 11. № 1-2. PP . 308-316.
22. Mukerjee S, Rudra B.S., Guha Roy U.K. Observation on cholera endemicity in Calcutta: survival of V. cholerae in the water sources. //Ann. Biochem. Exp. med. 1961. Vol. 21. № 2. PP. 31-40.
23. Mukerjee S. Approaches to the problem of cholera control. //Indian J. Med. Res. 1970. Vol. 52. № 4. PP. 331-354.
Седьмая пандемия существенно отличается от шести предыдущих укоренением холеры на длительный период далеко за пределами своего исторического очага. Для стран со стойкими эндемичными зонами холеры характерны: высокая плотность населения; теснейшая связь с загрязненной водой рек, лагун, озер, протоков, староречий, прудов; преимущественно щелочная или нейтральная реакция воды поверхностных водоемов; постоянно высокая температура воды, насыщенность ее органическими веществами и солями; наименьший доход на душу населения; нехватка продовольствия, приводящая к белковому голоданию и авитаминозам; неудовлетворительные санитарные условия жизни; недостаток медицинских кадров, медикаментов, дезинфекционных средств, коечного фонда; низкий санитарно-культурный уровень. Такое своеобразное сочетание природных и социальных факторов жизни населения является определяющим условием формирования эндемичных очагов. В этих очагах возбудитель холеры, пребывая различные промежутки времени в объектах окружающей среды и размножаясь в них, может беспрепятственно пассироваться через организм человека и тем самым постоянно сохранять высокую степень вирулентности. Развивающиеся страны Азии и Африки испытывают значительные трудности при проведении противоэпидемических и профилактических мероприятий, поэтому борьба с холерой требует эффективного международного сотрудничества.
Возбудителями холеры признаны микроорганизмы семейства Vibrionaceae, рода Vibrio, вида choleorae, серогруппы 01, биоваров cholerae и eltor. Другие представители V. cholerae, принадлежащие к не 01 серологическим группам (НАГ-вибрионы) по специфичности 0-антигена подразделены на 90 самостоятельных сероваров, часть из которых способна вызвать острые кишечные заболевания.
Холерные вибрионы обладают широким набором ферментов, синтезирующих большинство необходимых для них веществ. Они утилизируют D-глюкозу, являющуюся основным источником углерода и энергии, а в качестве источника азота используют соли аммония. Как типичные представители рода Vibrio продуцируют индофенолоксидазу, декарбоксилируют лизин и орнитин, не содержат дигидролазы аргинина, принадлежат к 1-й биохимической группе Хейберга.
Среди холерных вибрионов обоих биоваров различают 3 серологических варианта - Огава, Инаба и Гикошима: последний занимает промежуточное положение и на вспышках холеры встречается редко. Пандемия холеры Эль-Тор почти во всех странах началась с серовара Огава, который затем в некоторых из них оставался ведущим, в других сменился на серовар Инаба. Изменение антигенной структуры популяции возбудителя холеры может происходить под действием специфических антител и различных условий окружающей среды. Из эпидемиологической практики известно, что при быстро протекающих заносных вспышках циркулирует определенный серовар, а в эндемичных очагах и при укоренении холеры на несколько лет вполне вероятен переход в другой серовар. Возможность смены серовара возбудителя в естественных условиях обитания следует принимать во внимание при установлении эпидемиологической связи между очагами и выяснении путей распространения возбудителя инфекции.

Наиболее достоверными дифференциальными признаками V. cholerae и V. eltor считают чувствительность к холерным фагам С и Эль-Тор 30 ед/мл полимиксина и способность агглютинировать эритроциты.
В микробиологической практике встречаются промежуточные варианты, обладающие признаками холерных вибрионов обоих биоваров. Вероятно, оба биовара длительное время существовали вместе, что способствовало постепенному приобретению вибрионом Эль-Тор некоторых признаков, свойственных классическому вибриону.
Степень чувствительности вибриона Эль-Тор к диагностическим фагам зависит от длительности циркуляции возбудителя в очаге холеры. Холерные вибрионы, выделяемые из различных объектов окружающей среды, нередко проявляют устойчивость к диагностическим фагам. На вспышках холеры Эль-Тор были выявлены единичные штаммы, лизировавшиеся классическим фагом. Установлена вариабельность характерного признака биовара Эль-Тор - резистентности к полимиксину. Среди холерных вибрионов, выделенных в Бангладеш, было обнаружено несколько штаммов, агглютинировавших куриные эритроциты и в то же время обладавших всеми признаками классического биовара. На Филиппинах и в других странах изолированы такие культуры, которые не вызывали гемагглютинации, но сохраняли типичными все остальные свойства вибриона Эль-Тор. Необходимо комплексное использование тестов внутривидовой дифференциации для суждения о принадлежности холерных вибрионов к определенному биовару.
Во всех сомнительных случаях определение вирулентности проводится по результатам исследования холерогенности на новорожденных крольчатах. Возможность использования техники молекулярных зондов позволит выявлять структурный ген холерного вибриона, кодирующий образование энтеротоксина, и оперативно определять потенциальную опасность штаммов, циркулирующих в объектах окружающей среды в условиях эпидемического благополучия. Оценка степени вирулентности V. eltor необходима для решения вопроса о проведении дифференцированных противохолерных мероприятий.
Вариабельность гемолитической активности V. eltor приобретает особую значимость в связи с использованием теста Грейга при комплексном методе определения вирулентности. В начале седьмой пандемии большинство штаммов обладало гемолитическими свойствами. После 1964 г. в Азии, Африке и Европе в основном циркулируют негемолитические варианты V. eltor. Колебания гемолитической активности у субкультур одного и того же штамма, свидетельствующие о неоднородности его популяции, характерны для слабовирулентных и авирулентных V. eltor. Вирулентные штаммы не вызывают гемолиз эритроцитов и популяция их, как правило, однородна по данному признаку. V. eltor, изолированные во время вспышек, в 99,3% лизировались монофагами ХДФ-3, ХДФ-4 и ХДФ-5, а штаммы, циркулирующие в поверхностных водоемах при отсутствии заболеваний среди людей, оказывались резистентными или слабо чувствительными к указанным фагам. Степень вирулентности холерный вибрионов подвержена значительным колебаниям и зависит от условий существования их в организме человека и в объектах окружающей среды.
Отечественная схема фаготипирования позволяет определять 8 фаготипов V. cholerae и 11 фаготипов V. eltor. Применение метода фаготипирования на вспышках холеры способствует выявлению источников возбудителя инфекции и путей его распространения внутри очага и за его пределами.

Иллюстрация 1866 года. Источник
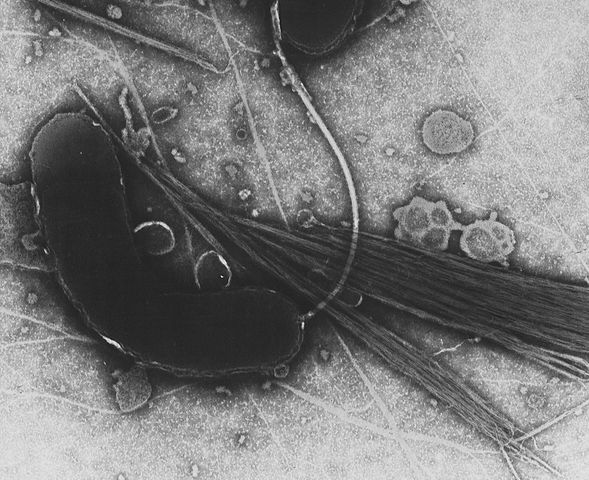
Холера вызывается подвижными бактериями — холерным вибрионом, Vibrio cholerae. Вибрионы размножаются в планктоне в солёной и пресной воде. Механизм заражения холерой — фекально-оральный. Возбудитель выводится из организма с фекалиями, мочой или рвотой, а проникает в новый организм через рот — с грязной водой или через не немытые руки. К эпидемиям приводит смешение сточных вод с питьевой водой и отсутствие обеззараживания.
Бактерии выделяют экзотоксин, который в организме человека приводит к выходу ионов и воды из кишечника, что приводит к диарее и обезвоживанию. Некоторые разновидности бактерии вызывают холеру, другие — холероподобную дизентерию.
Болезнь приводит к гиповолемическому шоку — это состояние, обусловленное быстрым уменьшением объёма крови из-за потери воды, и к смерти.
Учёные выделяют семь пандемий холеры:
- Первая пандемия, 1816—1824 гг.
- Вторая пандемия, 1829—1851 гг.
- Третья пандемия, 1852—1860 гг.
- Четвертая пандемия, 1863—1875 гг.
- Пятая пандемия, 1881—1896 гг.
- Шестая пандемия, 1899—1923 гг.
- Седьмая пандемия, 1961—1975 гг.
Возможной причиной первой эпидемии холеры была аномальная погода, вызвавшая мутацию холерного вибриона. В апреле 1815 года произошло извержение вулкана Тамбора на территории нынешней Индонезии, катастрофа в 7 баллов унесла жизни десяти тысяч жителей острова. Затем погибли до 50 000 человек от последствия, включая голод.
Остановить пандемию смог тот же фактор, что послужил её началом: аномальный холод 1823-1824 года. Всего первая пандемия продлилась восемь лет, с 1816 по 1824 года.
Спокойствие было недолгим. Всего через пять лет, в 1829 году, на берегах Ганга вспыхнула вторая пандемия. Она продлилась уже 20 лет — до 1851 года. Колониальная торговля, усовершенствованная транспортная инфраструктура, передвижения армий помогали болезни распространяться по миру. Холера дошла до Европы, США и Японии. И, конечно, она пришла в Россию. Пик в нашей стране пришёлся 1830-1831 годы. По России прокатились холерные бунты. Крестьяне, рабочие и солдаты отказывались терпеть карантин и высокие цены на продукты и потому убивали офицеров, купцов и врачей.
В России в период второй эпидемии холеры заболели 466 457 человек, из которых умерли 197 069 человек. Распространению способствовало возвращение из Азии русской армии после войн с персами и турками.

Император Николай I своим присутствием усмиряет холерный бунт в Санкт-Петербурге в 1831 году. Литография из французского периодического издания Album Cosmopolite. Датирована 1839 годом. Источник
Третью пандемию относят к периоду с 1852 по 1860 год. На этот раз только в России умерли более миллиона человек.
Лондонский врач Джон Сноу в 1854 году установил, что болезнь передаётся через загрязнённую воду. Общество на эту новость не обратило особого внимания. Сноу пришлось доказывать свою точку зрения властям. Сначала он убедил снять ручку водозаборной колонки на Брод-Стрит, где был очаг эпидемии. Затем он составил карту случаев холеры, которая показала связь между местами заболевания и его источниками. Наибольшее число умерших было зафиксировано на окрестности именно этой водозаборной колонки. Было одно исключение: никто не умер в монастыре. Ответ был прост — монахи пили исключительно пиво собственного производства. Через пять лет была принята новая схема канализационной системы.

Объявление в Лондоне, распространяемое в 1854 году, предписывало употреблять только кипячёную воду
Седьмая, последняя на сегодня пандемия холеры, началась в 1961 году. Она была вызвана более стойким в окружающей среде холерным вибрионом, получившим название Эль-Тор — по названию карантинной станции, на которой мутировавший вибрион обнаружил в 1905 году.
К 1970 году холера Эль-Тор охватила 39 стран. К 1975 она наблюдалась в 30 странах мира. На данный момент опасность завоза холеры из некоторых стран не ушла.
Высочайшую скорость распространения инфекции показывает тот факт, что в 1977 году вспышка холеры на Ближнем Востоке всего за месяц распространилась на одиннадцать сопредельных стран, включая Сирию, Иордан, Ливан и Иран.

Обложка журнала начала XX века
В 2016 году холера не так страшна, как сто и двести лет назад. Гораздо большему количеству людей доступна чистая вода, канализация редко выводится в те же водоёмы, из которых люди пьют. Очистные сооружения и водопровод находятся на абсолютно другом уровне, с несколькими степенями очистки.
Хотя в некоторых странах вспышки холеры происходят до сих пор. Один из последних на данный момент случаев эпидемии холеры начался (и продолжается) на Гаити в 2010 году. Всего были заражены более 800 000 человек. В пиковые периоды за день заболевали до 200 человек. В стране живут 9,8 миллиона человек, то есть холера затронула почти 10% населения. Считают, что начало эпидемии положили непальские миротворцы, которые занесли холеру в одну из главных рек страны.
8 ноября 2016 года в стране объявили о массовой вакцинации. В течение нескольких недель планируют вакцинировать 800 000 человек.
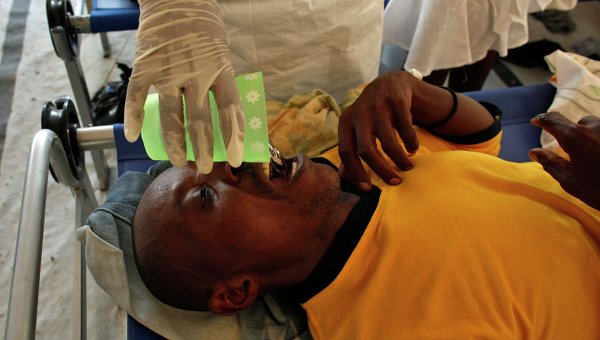
Холера на Гаити. Фото: РИА Новости
В октябре 2016 года сообщалось, что в Адене, втором по величине городе Йемена, зафиксировали двести случаев заболевания холерой, при этом девять человек умерли. Болезнь распространилась через питьевую воду. Проблема усугубляется голодом и войной. По последним данным, во всём Йемене холеру подозревают у 4 116 человек.
В США эта лихорадка распространена и сейчас, ежегодно регистрируется до 650 случаев болезни. О распространении говорит тот факт что в период с 1981 по 1996 годы лихорадка встречалась в каждом штате США, кроме Гавайи, Вермонт, Мэн и Аляска. Даже сегодня, когда медицина находится на гораздо более высоком уровне, смертность составляет 5-8%. До изобретения антибиотиков количество летальных исходов доходило до 30%.
Бактерии проникают в организм через начёсы или другие повреждения кожи.
После того, как вошь укусила человека, болезнь может не наступить. Но как только человек начинает чесаться, он втирает выделения кишечника вши, в которых содержатся риккетсии. Через 10-14 дней, после инкубационного периода, начинается озноб, лихорадка, головная боль. Через несколько дней появляется розовая сыпь. У больных наблюдается дезориентация, нарушения речи, температура до 40 °C. Смертность во время эпидемии может составить до 50%.
В 1942 году Алексей Васильевич Пшеничнов, советский учёный в области микробиологии и эпидемиологии, внёс огромный вклад методологию профилактики и лечения сыпного тифа и разработал вакцину против него. Сложность в создании вакцины была в том, что риккетсии нельзя культивировать обычными методами — бактериям необходимы живые клетки животного или человека. Советский учёный разработал оригинальный метод заражения кровососущих насекомых. Благодаря быстрому запуску в нескольких институтах производства этой вакцины во время Великой Отечественной войны СССР удалось избежать эпидемии.
Тиф иногда поражал армии эффективнее, чем живой противник. Вторая крупная эпидемия этой болезни датируется 1505-1530 годами. Итальянский врач Фракастор наблюдал за ней во французских войсках, осаждавших Неаполь. Тогда отмечали высокую смертность и заболеваемость до 50%.
В Отечественной войне 1812 года Наполеон потерял треть войска от сыпного тифа. Армия Кутузова потеряла от этой болезни до 50% солдат. Следующая эпидемия в России была в 1917-1921 годах, на этот раз погибли около трёх миллионов человек.
Сейчас для лечения сыпного тифа используют антибиотики тетрациклиновой группы и левомицетин. Для профилактики заболевания используются две вакцины: Vi-полисахаридная вакцина и вакцина Ту21а, разработанная в 1970-х.
Брюшной тиф характеризуется лихорадкой, интоксикацией, высыпаниями на коже и поражением лимфатической системы нижнего отдела тонкой кишки. Его вызывает бактерия Salmonella typhi. Бактерии передаются алиментарным, или фекально-оральным, способом. За 2000 год брюшным тифом во всём мире переболели 21,6 миллиона человек. Смертность составила 1%. Один из эффективных способов профилактики брюшного тифа — мытьё рук и посуды. А также внимательное отношение к питьевой воде.
У больных наблюдается сыпь — розеолы, брахикардия и гипотония, запор, увеличение объёмов печени и селезёнки и, что характерно для всех видов тифа, заторможенность, бред и галлюцинации. Больных госпитализируют, дают левомицетин и бисептол. В самых тяжёлых случаях используют ампициллин и гентамицин. При этом необходимо обильное питьё, возможно добавление глюкозно-солевых растворов. Все больные принимают стимуляторы выработки лейкоцитов и ангиопротекторы.
После укуса клеща или вши, переносчика бактерии, у человека начинается первый приступ, который характеризуется ознобом, сменяемым жаром и головной болью с тошнотой. У больного поднимается температура, кожа высыхает, пульс учащается. Увеличивается печень и селезёнка, может развиться желтуха. Также отмечают признаки поражения сердца, бронхит и пневмонию.
От двух до шести дней продолжается приступ, который повторяется через 4-8 суток. Если для болезни после укуса вши характерны один-два приступа, то клещевой возвратный тиф вызывает четыре и более приступов, хотя они легче по клиническим проявлениям. Осложнения после болезни — миокардит, поражения глаз, абсцессы селезёнка, инфаркты, пневмония, временные параличи.
Для лечения используют антибиотики — пенициллин, левомицетин, хлортетрациклин, а также мышьяковистые препараты — новарсенол.
Летальный исход при возвратном тифе случается редко, за исключением случае в Центральной Африке. Как и остальные виды тифа, заболевание зависит от социально-экономических факторов — в частности, от питания. Эпидемии среди групп населения, которым недоступна квалифицированная медицинская помощь, могут приводить к смертности до 80%.
Во время Первой мировой в Судане от возвратного тифа погибли 100 000 человек, это 10% населения страны.
Чуму и оспу человечество сумело загнать в пробирку благодаря высокому уровню современной медицины, но даже эти болезни иногда прорываются к людям. А угроза холеры и тифа существует даже в развитых странах, что уж говорить о развивающихся, в которых в любой момент может вспыхнуть очередная эпидемия.
Причиной заражения в Махачкале была водопроводная вода. Директор местного водоканала арестован, ещё двадцать три человека — под следствием. Сейчас того же опасаются жители Ростова.
Читайте также:


