Национальная лаборатория диагностики полиомиелита
от 26 декабря 1997 г. N 386
Перечень
региональных центров и Национального центра по лабораторной диагностике полиомиелита и административных территорий, закрепленных за ними
27 августа 1998 г.
Приказом Министерства здравоохранения РФ от 27 августа 1998 г. N 257 во изменение пункта 1 настоящего Перечня функции регионального центра возложены на Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера
I. Объединенный: Центр госсанэпиднадзора в г. Санкт-Петербурге и Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера (Материалы от больных с острыми вялыми параличами направляются в Центр госсанэпиднадзора в г. Санкт-Петербурге):
Республика Карелия, Республика Коми, Архангельская область, Ненецкий автономный округ, Вологодская область, Мурманская область, Ленинградская область, Новгородская область, Псковская область, Калининградская область, Костромская область, Смоленская область, Ярославская область, Республика Мордовия, г. Санкт-Петербург.
II. Центр госсанэпиднадзора в Ставропольском крае:
Республика Северная Осетия (Алания), Чеченская Республика, Ингушская Республика, Карачаево-Черкесская Республика, Республика Адыгея, Кабардино-Балкарская Республика, Республика Дагестан, Краснодарский край, Ростовская область, Астраханская область, Волгоградская область, Республика Калмыкия, Ставропольский край, Ульяновская область.
III. Центр госсанэпиднадзора в Хабаровском крае:
Республика Саха (Якутия), Приморский край, Камчатская область, Корякский автономный округ, Магаданская область, Сахалинская область, Амурская область, Еврейская автономная область, Усть-Ордынский Бурятский автономный округ, Агинский Бурятский автономный округ, Чукотский автономный округ, Республика Бурятия, Иркутская область, Читинская область, Хабаровский край.
IV. Центр госсанэпиднадзора в Омской области:
Республика Алтай, Республика Тува, Республика Хакасия, Кемеровская область, Тюменская область, Алтайский край, Новосибирская область, Томская область, Красноярский край, Эвенкийский автономный округ, Ханты-Мансийский автономный округ, Ямало-Ненецкий автономный округ, Оренбургская область, Омская область.
V. Центр госсанэпиднадзора в Свердловской области:
Республика Башкортостан, Удмуртская Республика, Курганская область, Кировская область, Пермская область, Коми-Пермяцкий автономный округ, Челябинская область, Республика Татарстан, Пензенская область, Самарская область, Саратовская область, Чувашская Республика, Республика Марий-Эл, Нижегородская область, Свердловская область.
Национальный центр на базе НИИПиВЭ им. М.П. Чумакова РАМН:
Москва, Московская область, Брянская область, Владимирская область, Ивановская область, Калужская область, Тверская область, Орловская область, Рязанская область, Тульская область, Белгородская область, Воронежская область, Курская область, Липецкая область, Тамбовская область, Таймырский автономный округ.
Примечание: Вирусологические лаборатории, которые не вошли в перечень лабораторий, определенных как региональные, проводят исследования 1/2 пробы материала (фекалий) от больных острыми вялыми параличами и 1/2 пробы материала направляют в региональную лабораторию, выделенные вирусы направляются в Национальный центр по лабораторной диагностике полиомиелита.
Лабораторные исследования сточных вод по выделению вирусов полиомиелита осуществляются на базе вирусологических лабораторий центров госсанэпиднадзора в субъектах Российской Федерации в установленном порядке. Выделенные вирусы полиомиелита направляются в Национальный центр по лабораторной диагностике полиомиелита.
Откройте актуальную версию документа прямо сейчас или получите полный доступ к системе ГАРАНТ на 3 дня бесплатно!
Если вы являетесь пользователем интернет-версии системы ГАРАНТ, вы можете открыть этот документ прямо сейчас или запросить по Горячей линии в системе.
Полиомиелит – это серьезное заболевание, вызванное вирусной инфекцией. Недуг тяжелый, протекает преимущественно с поражением ЦНС. Он приводит к самым разным последствиям, а потому важно вовремя его обнаружить и начать лечение.
Диагностика полиомиелита подразумевает проведение ряда исследований. О них следует рассказать подробнее, а также уделить немного внимания причинам, симптомам и возможным последствиям данного недуга.
Вкратце о заболевании
Прежде чем обсудить принципы диагностики полиомиелита, необходимо изучить специфику данного недуга. Это – энтеровирусная инфекция, которую вызывают полиовирусы. Они поражают мотонейроны передних рогов спинного мозга. Данное воздействие приводит к серьезным паралитическим осложнениям с последующей инвалидизацией больного.
Как правило, недуг поражает детей, возраст которых составляет менее 4 лет. На них приходится 60-80% случаев.
Последняя эпидемия пришлась на середину прошлого столетия. В конце 80-х ВОЗ приняла резолюцию, целью которой стала ликвидация данного заболевания во всем мире.
На сегодняшний день в странах, где проводят профилактическую вакцинацию против полиомиелита, недуг встречается в виде спорадических единичных случаев. Это Индия, Афганистан, Сирия, Нигерия, Пакистан. Наша страна, а также Северная Америка и государства Западной Европы свободны от полиомиелита.
Причины
Данное заболевание вызывают антигенные типы полиовируса, которые относятся к роду энтеровирусов. Всего их три. Но наибольшую опасность несет вирус первого типа – на него приходится 85% случаев. Он очень живучий, может сохраняться до 6 месяцев в испражнениях и до 100 суток в воде.
Он переносит даже замораживание и высушивание, на него не воздействуют антибиотики и пищеварительные соки. Погибнуть вирус может лишь в результате следующих воздействий:
- Нагревание и последующее кипячение.
- Обработка дезинфицирующими средствами.
- Ультрафиолетовое облучение.
Источником вируса может быть не только зараженный человек. Его способен распространить бессимптомный носитель. Сам он может не болеть полиомиелитом. Однако своей носоглоточной слизью и испражнениями распространять будет. Передается вирус фекально-оральным, воздушно-капельным и контактным путями.
Попадая в организм, он внедряется в клетки, вследствие чего нарушается синтез белка и нуклеиновых кислот. Результатом становятся деструктивные и дистрофические изменения. Возможна полная гибель нейрона. Следствие разрушения 1/3-1/4 нервных клеток – развитие полных параличей и парезов.

Симптомы
Прежде чем перейти к обсуждению диагностики и принципов лечения полиомиелита у детей и взрослых, надо перечислить симптомы, которые указывают на развитие столь специфического недуга.
Инкубационный период длится 8-12 дней. Если развивается инаппарантная форма, то клинически недуг никак не проявляется. Его обнаруживают лишь в результате лабораторных исследований.
Недуг висцеральной формы проявляется интоксикацией, лихорадкой, диареей, болями в животе, умеренными катаральными явлениями. Заболевание заканчивается примерно через 3-7 дней после того, как симптомы дают о себе знать. Никаких остаточных неврологических проявлений не наблюдается.
Самым тяжелым является заболевание паралитической формы. Наблюдается диспепсия, трахеит, фарингит, ринит, боли в конечностях и позвоночнике, 2-волновая лихорадка, судороги, спутанность сознания. На 3-6 день наступает паралитическая фаза. К концу второй недели поражаются жизненно важные центры продолговатого мозга, возможен паралич диафрагмы и дыхательных мышц.
Диагностика
Рассмотрев причины, симптомы и виды полиомиелита, нужно уделить внимание и этой теме. Этот серьезный редкий недуг обычно начинает подозревать детский невролог или педиатр. Основаниями для предположений является анамнез, диагностически значимые симптомы и эпидемиологические данные.
Есть определенные трудности. Не все доктора сразу назначают анализ на полиомиелит, так как не всегда подозревается именно данный недуг. Часто ошибочно устанавливают диагноз серозного менингита, острой кишечной инфекции, ОРВИ, гриппа.
Точно определить заболевание способны помочь лабораторные тесты, о которых подробно будет рассказано далее. Сейчас же нужно обсудить другие методы.
Важно дифференцировать вирус, а потому проводится полимеразная цепная реакция. Еще часто назначают люмбальную пункцию. При ее проведении спинномозговая жидкость вытекает под большим давлением. В ходе исследования удается выявить ее бесцветность, прозрачность, а также увеличенное содержание глюкозы и белка. После проведения электромиографии удается подтвердить поражение на уровне передних рогов спинного мозга.
Рассказывая про методы диагностики полиомиелита, также следует оговориться, что недуг необходимо вовремя дифференцировать с ботулизмом, миелитом, синдромом Гийена-Барре, серозным менингитом, клещевым энцефалитом и полиомиелитоподобными заболеваниями.

Вирусологический метод
Он применим в диагностике полиомиелита в обязательном порядке. Очень важно выделить вирус и идентифицировать его. В качестве биоматериала необходим кал больного. Чуть реже берут ликвор, кровь и носоглоточный смыв.
Материал сначала фильтруют, а затем подвергают обработке антибиотиком. Затем вносят его в культуру клеток Нер-2 и RD (из человеческой рабдомиосаркомы). Приблизительно через 5-7 суток возникает цитопатическое действие вирусов (ЦПД), проявляющееся в форме мелкозернистой деструкции клеток.
Идентификацию вируса проводят в реакции нейтрализации. Это значит, что в культуры тканей заносят вирус, соединенный с поливалентной противополиомиелитной сывороткой трех типов. Это первый этап. Следующий шаг – ведение вируса с отдельными типовыми сыворотками, являющимися моновалентными. Каков результат? Если сыворотка и тип вируса идентичны, то ЦПД не наблюдается.
Серологический метод
Его также задействуют для диагностики полиомиелита. Он помогает определить, нарастает ли в крови переболевших пациентов титр антител.
Для этого в культуре ткани применяют реакцию нейтрализации с парными сыворотками, которые были получены в период острой стадии заболевания, а также в момент реконвалесценции.
Ставят иммуноферментный анализ (ИФА), а также реакцию связывания комплемента (РСК). В случае положительного результата удается определить 4-кратное нарастание титра антител во 2-й сыворотке, если сравнивать с 1-й.
Что это такое – ИФА-анализ? Активно развивающееся направление химической энзимологии. Это метод с уникальной специфичностью иммунохимической реакции. Проще говоря, антитела связываются лишь с конкретными антигенами. ИФА широко внедрился в разные медицинские области, поскольку используемые реагенты стабильны, методы регистрации просты, а цена проведения довольно мала.

Формы заболевания
Рассуждая о диагностике полиомиелита у детей и взрослых, необходимо оговориться, что пресловутая дифференциация всегда проводится на основе симптоматики. И у каждой формы заболевания она индивидуальна. Можно выделить такой перечень:
- Менингеальная форма. Проявления: выраженный болевой синдром, натянутые корешки спинномозговых нервов и нервных стволов, их болезненность при пальпации.
- Спинальная форма. Проявления: щадящая, не паретическая походка, сохранность мышечного тонуса, дискомфорт в суставах при пассивных движениях, повышение глубоких рефлексов, воспалительные изменения в крови. Данный недуг часто путают с полирадикулоневритом, дифтерийной полинейропатией, спинальной амиотрофией Верднига-Гоффманна.
- Полиомиелитическая форма. Патологический процесс диагностируется в шейных сегментах. Проявления: параличи мышц плечевого пояса и шеи, вялые парезы, лимфоцитарный плеоцитоз (незначительный, 40-60 клеток), увеличенный уровень белка (примерно 0,66-1,0 г/л). Изучая исследуемый материал при лабораторной диагностике полиомиелита, врачи учитывают эпидемиологический анамнез. Это может быть употребление сырого молока, укус клеща и т. д.
- Дифтерийная форма. Проявления: симметричность поражений, медленное нарастание парезов на протяжении нескольких недель, обнаружение нарушений биоэлектрической активности в процессе проведения электронейромиографии. Диагностируется спустя 1,5-2 месяца после дифтерии.
- Полирадикулоневрит. Проявления: медленное развитие и дальнейшее нарастание симметричных парезов, расстройство чувствительности по корешковому и полиневритическому типам, повышенное количество в спинно-мозговой жидкости белка.
- Понтийная форма. Проявления: снижение вкусовой восприимчивости на соленое и сладкое, слезотечение на пораженной стороне, ощущаемая при пальпации боль тригеминальных точек, нарушения в чувствительности лица и спонтанные боли.
- Бульбарная форма. Проявления: судорожный синдром и глубокие расстройства сознания. Важно дифференцировать ее со стволовыми энцефалитами.
В рамках темы, касающейся дифференциальной и микробиологической диагностики полиомиелита, надо оговориться, что поражения нервной системы, которые клинически не отличаются от рассматриваемого недуга, часто вызывают энтеровирусы группы Коксаки-ЕСНО. В таких случаях задействуют весь комплекс серологических и вирусологических диагностических методов и уже упомянутый ранее метод ПЦР.

Специфическая профилактика
Выше было рассказано об особенностях недуга, основном методе лабораторной диагностике и о том, что такое ИФА-анализ. Это все важно, но теперь стоит также поведать про специфическую профилактику, осуществляемую убитыми и живыми вакцинами.
Метод интересный. В убитой вакцине содержатся вирусы полиомиелита З-го, 2-го и 1-го типов. Их выращивают в почечной ткани обезьян. Убитая вакцина провоцирует гуморальный иммунитет – образование IgM и IgG. Но в то же время не препятствует происходящей в клетках слизистой оболочки кишечника репродукции вирусов.
Живая вакцина типов 3, 2 и 1 образуется из аттенуированных штаммов, которых культивируют также в почечных клетках, но только других животных – зеленых африканских мартышек.
Кроме пресловутых IgM и IgG-антител, ею индуцируются секреторные IgA. Данный процесс происходит в слизистой оболочке ЖКТ (тонкого кишечника, если быть точнее). И именно они являются антителами к полиомиелиту, препятствующими циркуляции диких штаммов.
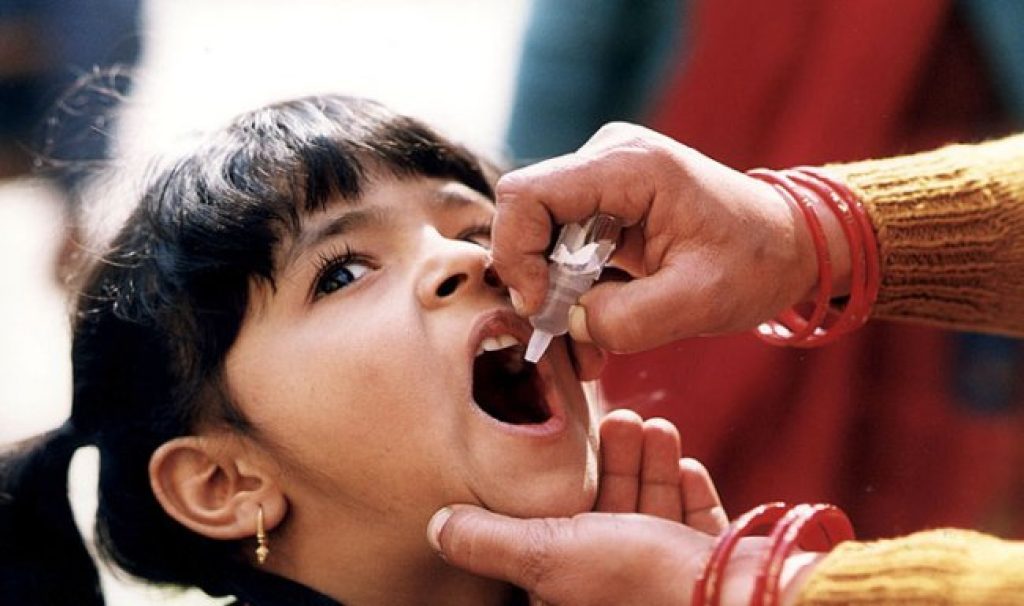
Прием вакцины
В подавляющем большинстве больниц стран СНГ распространена оральная вакцина. Прививка делается просто: препарат, о котором рассказывалось выше, закапывают в ротовую полость.
Выполняют это после того, как ребенку исполнится 3 месяца. Далее потребуется сделать еще две вакцинации. Интервал между ними – 1,5 месяца. Выходит, к врачу младенца нужно будет отнести, когда ему будет 4 и 6 соответственно. Ревакцинацию проводят в 18 и 20 месяцев, а потом лишь в 14 лет.
Нужно быть предупрежденным о том, что после введения в организм ослабленных вирусов, способен развиться так называемый вакцинноассоциированный полиомиелит. Вероятность очень мала, но имеется. Чаще всего недуг развивается у младенцев после их первой вакцинации. Какова причина? Обычно – сниженный иммунитет или спонтанная мутация вируса в условиях организма ребенка.
И, кстати, так как после прививки грудничок становится потенциальным носителем вируса, от него могут заразиться не вакцинированные люди, а еще те, у кого иммунитет подавлен.
Лечение
Немного внимания надо уделить и клиническим рекомендациям. Полиомиелит манифестных форм всегда лечится стационарно. Больному показана изоляция, покой, высококалорийная диета и постельный режим.
Очень важно придать конечностям правильное с точки зрения физиологии положение. Необходим массаж грудной клетки и профилактика пролежней. Если у больного наблюдается дисфагия, то питание организуют через назогастральный зонд. В случае нарушения самостоятельного дыхания показана искусственная вентиляция легких.
К сожалению, специфическое лечение не разработано. Вакцины, особенности которых были рассмотрены выше, предотвращают развитие заболевания, не давая ему развиться (выработка иммунитета). Но они не лечат полиомиелит. А потому проводят патогенетическую и симптоматическую терапию.
Прописывают прием аскорбиновой кислоты, витаминов группы В, дегидратирующих и обезболивающих препаратов, дыхательных аналептиков, неостигмина и т. д.
В восстановительный период время уделяется реабилитационным мероприятиям. А именно:
- Лечебная физкультура.
- УВЧ.
- Лечение в санаториях.
- Ортопедический массаж.
- Общие лечебные ванны.
- Парафинолечение.
Лечение и профилактика детей всегда проводится при непосредственном участии детского ортопеда. Если выявляется риск развития контрактур, то назначают наложение лонгет, гипсовых повязок, ортопедических шин, а также ношение специальной обуви.
Всегда есть вероятность возникновения остаточных явлений. Их лечение обычно включает сухожильно-мышечную пластику, теномиотомию, артрориз, тенодез, резекцию и дальнейшую остеотомию костей, коррекцию сколиоза хирургическим методом и т. д.

Осложнения и прогнозы
Нельзя не рассказать о том, чем опасен полиомиелит. Данное заболевание часто приводит к инвалидности. Если парализованные конечности и начинают двигаться, то они остаются деформированными – они укорачиваются, а мышцы атрофируются.
Патологический процесс может затронуть дыхательную систему, а это чревато дыхательными расстройствами, из-за которых человек может даже умереть (задохнуться).
Легкие формы недуга обычно проходят бесследно. А за счет целенаправленной многолетней вакцинопрофилактики в структуре преобладают лишь абортивная и инаппарантная формы инфекции. Они лечатся успешно. Паралитические формы поражают лишь людей, не прививавшихся от полиомиелита. А это – обязательная профилактика.
Если вдруг возникает подозрение, что ребенок заразился полиомиелитом, то его немедленно изолируют, а в помещениях, где он находился, проводят дезинфекцию. Лица, с которыми он контактировал, помещаются под наблюдение, а также подвергаются иммунизации ОПВ вне очереди.
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека направляет для информации и использования в работе рекомендации совещания лабораторной сети Российской Федерации по диагностике полиомиелита, состоявшегося 10-12 сентября 2007г. в г. Сочи с участием специалистов Всемирной организации здравоохранения.
Приложение: на 5-ти листах в 1 экз.
Рекомендации
совещания лабораторной сети Российской Федерации
по диагностике полиомиелита
г. Сочи, 10—12 сентября 2007г.
В работе совещания приняли участия вирусологи региональных центров эпидемиологического надзора за полиомиелитом и острыми вялыми параличами (ОВП) (гг. Москва, Санкт-Петербург, Ставрополь, Хабаровск, Омск, Екатеринбург), сотрудники Национальной лаборатории по диагностике полиомиелита (Институт полиомиелита и вирусных энцефалитов им. М. П. Чумакова РАМН), Института физико-химической биологии им. А. Н. Белозерского МГУ им. М. В. Ломоносова, специалисты Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Федерального Центра гигиены и эпидемиологии Роспотребнадзора, управления Роспотребнадзора по Краснодарскому краю, Европейского Регионального Бюро ВОЗ.
Представлены доклады о процессе выполнения глобальной программы ликвидации полиомиелита, ситуации в Европейском регионе, о деятельности Европейской лабораторной сети в 2006—2007 гг., новые данные о вакциннородственных полиовирусах, выявленных в Чехии и Израиле, о статусе и дальнейших направлениях развития программы контейнмента в Европейском регионе и Российской Федерации, материалы о современном состоянии надзора за полиомиелитом и ОВП в Российской Федерации, о деятельности лабораторной сети Российской Федерации по диагностике полиомиелита. Обсуждались вопросы о состоянии эпидемиологического надзора за неполиоэнтеровирусами (НПЭВ) – современное состояние, проблемы, пути решения, внедрения метода ПЦР для диагностики полио/НПЭВ инфекции в вирусологических лабораториях Центров гигиены и эпидемиологии.
Большое внимание было уделено вопросам биологической безопасности при работе с вирусом полиомиелита и материалами, инфицированными или потенциально инфицированными диким полиовирусом. Представлены новые международные требования к иммунизации против полиомиелита при пересечении границ государств, к пересылке материалов, а так же доклад о проблемах вирусных гепатитов.
В большинстве регионов страны внедряется регистрация и надзор за энтеровирусными инфекциями, однако объем и качество надзора нуждается в систематизации и унификации.
Вместе с тем, в деятельности лабораторной сети по диагностике полиомиелита имеется ряд недостатков.
Не во всех случаях обеспечивается полное и адекватное вирусологическое и иммунологическое обследование больных вакциноассоциированным паралитическим полиомиелитом, реконвалесцентов этого заболевания.
В ряде случаев необоснованно увеличивается количество обследуемых контактных лиц в эпидемических очагах ПОЛИО /ОВП.
В ряде регионов не выполнены рекомендации предыдущих совещаний лабораторной сети Российской Федерации по диагностике полиомиелита в части проведения процедуры внутреннего контроля качества вирусологических исследований путем ежеквартального титрования референс-штаммов вируса полиомиелита на культуре клеток.
Внедрение контроля на присутствие микоплазмы в клеточных культурах выявило наличие контаминации в некоторых лабораториях, однако это не послужило показанием для пересмотра процедуры поддержания и состояния клеточных культур, их обновления.
Исследования сточных вод на энтеровирусы в ряде субъектов Российской Федерации проводится не на должном профессиональном уровне.
При осложнении эпидемиологической ситуации по энтеровирусным инфекциям, возникновении вспышек этого заболевания не во всех случаях штаммы выделенных энтеровирусов направляются в Национальную лабораторию по диагностике полиомиелита для их идентификации.
Остается проблемой в ряде лабораторий обеспечение режима биологической безопасности работы.
4. Просить Институт полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН:
4.1. продолжить работу по совершенствованию диагностических препаратов для определения и идентификации полио и других (неполио) энтеровирусов;
4.2. активизировать работу по созданию и производству поливалентных сывороток для диагностики энтеровирусных инфекций;
4.5. увеличить объем подготовки врачей-вирусологов учреждений Роспотребнадзора по вопросам диагностики полиомиелита и других (неполио) энтеровирусных инфекций;
4.6. обеспечить изготовление необходимых диагностических препаратов для внедрения системы внешнего контроля качества исследований на полио, другие (неполио) энтеровирусы в вирусологических лабораториях учреждений Роспотребнадзора.
5. Просить ЕРБ ВОЗ:
5.1. принять участие в разработке пилотного проекта усовершенствованного надзора за энтеровирусными инфекциями для последующей реализации на 2-3-х территориях Российской Федерации.
5.2. рассмотреть вопрос о бесперебойном снабжении FTA-карт, необходимых для проведения тестирования в вирусологических лабораториях учреждений Роспотребнадзора
(c) Управление Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по Ямало-Ненецкому автономному округу, 2006-2020 г.
Адрес: 629000, г. Салехард, ул. Титова, д. 10
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека направляет для информации и использования в работе рекомендации совещания лабораторной сети Российской Федерации по диагностике полиомиелита, состоявшегося 25-26 июня 2006г. в г. Калининграде с участием специалистов Всемирной организации здравоохранения.
Приложение:
Рекомендации совещания лабораторной сети Российской Федерации
по диагностике полиомиелита
Были заслушаны доклады о текущем состоянии процесса ликвидации полиомиелита в мире и ситуации в Европейском регионе, о деятельности Европейской лабораторной сети, о реализации программы безопасного лабораторного хранения диких полиовирусов (контейнмента) в Европейском регионе и приоритетных задачах на будущее, о перспективах развития лабораторного проекта ВОЗ по сокращению срока вирусологических исследований на полиомиелит . Представлены материалы о современном состоянии эпидемиологического надзора за полиомиелитом и ОВП в Российской Федерации, о деятельности лабораторной сети Российской Федерации. Были заслушаны доклады руководителей вирусологических лабораторий региональных центров эпидемиологического надзора за полиомиелитом и ОВП, о результатах дополнительного надзора за вирусом полиомиелита, научный доклад, посвященный эволюции вакцинных штаммов .
Значительное время было уделено сообщениям об опыте лабораторного обеспечения эпидемиологического надзора за другими вирусными инфекциями (корь, ротавирусная инфекция, вирусные гепатиты, арбовирусные инфекции, гемморрагические лихорадки). Представлены результаты пилотного проекта по программе ликвидации кори. Выступления участников совещания подтвердили успешную интеграцию программ ВОЗ по лабораторному обеспечению эпидемиологического надзора за различными инфекциями и значительные потенциальные возможности лабораторий сети по диагностике полиомиелита по вовлечению в диагностические исследования других вирусных инфекций.
Участники совещания заслушали и обсудили материалы о мерах по предупреждению распространения гриппа птиц в Российской Федерации. Большое внимание было уделено вопросам биологической безопасности, новым медико-санитарным правилам ВОЗ и аспектам лабораторной работы с высокопатогенными штаммами вируса гриппа.
Совещание подтвердило высокий уровень работы лабораторной сети Российской Федерации по диагностике полиомиелита в 2005—2006 гг. Основные показатели качества деятельности лабораторий отвечают критериям ВОЗ, оценка выполнения профессионального теста составила 100% для всех лабораторий сети.
Однако, совещание отмечает, что в ряде случаев имеет место неудовлетворительное качество и несвоевременная доставка проб фекалий от больных ОВП в региональные центры эпидемиологического надзора за полиомиелитом и ОВП, Национальный центр по лабораторной диагностике полиомиелита. Недостаточна эффективность вирусологических исследований проб сточных вод, не организована процедура внутреннего контроля качества вирусологических исследований.
Участники совещания выражают озабоченность тем, что в настоящее время, после сертификации ликвидации полиомиелита в Европе, включая Российскую Федерацию, страна оказывается перед возрастающей опасностью завоза дикого вируса полиомиелита в результате недавнего восстановления передачи инфекции в Африке и ряде стран Восточно-Средиземноморского региона.
В тоже время в ряде субъектов Российской Федерации отмечается снижение внимания и ответственности руководителей органов и учреждений Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека к мероприятиям по профилактике полиомиелита. Такое положение представляет угрозу для успехов, достигнутых в результате большой организационной и практической работы по ликвидации полиомиелита в стране.
3. Просить институт полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН:
– продолжить практику проведения курсов повышения квалификации врачей вирусологов по актуальным вопросам диагностики, полиомиелита и других неполиомиелитных энтеровирусных инфекций, безопасного лабораторного хранения диких полиовирусов;
– обеспечить производство диагностических препаратов нового поколения для детекции и идентификации полиовирусов и других неполиомиелитных энтеровирусов.
Часовой пояс: UTC + 3 часа [ Летнее время ]
National Polio Laboratory Checklist
Национальная лаборатория по диагностике полиомиелита
Контрольный вопросник для ежегодной аккредитации ВОЗ
Надзор за острыми вялыми параличами (ОВП) среди детей в возрасте до 15 лет c ежегодным
показателем регистрации параличей неполиомиелитного происхождения на уровне не менее 1 на
100,000 является стандартом для сертификации ликвидации полиомиелита для всех стран.
Конечной целью является создание системы классификации полиомиелита, основанной на вирусологической оценке всех случаев ОВП. Вирусологическая оценка проводится путем тестирования двух адекватных образцов стула, собранных с интервалом в 24-48 часов от каждого пациента с ОВП в течение 14 дней после наступления паралича. При необходимости может потребоваться осуществление дополнительного вирусологического надзора, включающего тестирование образцов, собранных при проведении специальных исследований от здоровых детей, лиц, контактировавших с больными с ОВП, из объектов окружающей среды. Для соблюдения принципа сертификации лабораторные результаты принимаются только от полиомиелитных лабораторий, аккредитованных ВОЗ.
Аккредитация обеспечивает документальное подтверждение, что лаборатория имеет возможности и способна выявлять и идентифицировать дикие и вакцинно-родственные полиовирусы (ВPПВ), которые могут присутствовать в клинических образцах и образцах сточных вод, а также своевременно направлять отчеты о результатах лабораторных исследований. Аккредитация дает возможности проведения дополнительного обучения, оказания поддержки в случае необходимости, оценки достигнутого прогресса, а также обеспечивает связь с Глобальной лабораторной сетью ВОЗ.
Аккредитация национальных лабораторий по полиомиелиту проводится региональным офисом ВОЗ ежегодно и основывается на оценке показателей работы лаборатории в течение 12 месяцев, предшествующих дате проведения оценки. Аккредитация выдается на последующий календарный год.
Шесть критериев аккредитации:
1. Результаты лабораторного исследования образцов от больных ОВП предоставляются не менее чем для 80% образцов в течение 28 дней (традиционный алгоритм) или 14 дней (новый алгоритм) со дня их поступления в лабораторию.
Этот критерий должен выполняться для всех отрицательных образцов после 2 пассажей в течение 14 дней (традиционный алгоритм) или в течение 10 дней (новый алгоритм). И так же вирусы, продемонстрировавшие цитопатический эффект (ЦПЭ), должны быть идентифицированы с помощью серотипирования до истечения 28 дневного срока (традиционный алгоритм) или направлены на внутритиповую дифференциацию до истечения 14 дневного срока (новый алгоритм).
3. Правильность выявления и идентификация полиовируса среди других вирусных изолятов составляет не менее 90%.
Правильность определяется по совпадению результатов серотипирования полиовирусов (при использовании традиционного алгоритма), направленных лабораторией, выделившей вирусы, в лабораторию, выполняющую внутритиповую дифференциацию (ВТД), в течение 12месячного периода, предшествующего аккредитации.
Возможно, произошла перекрестная контаминация линий клеток или у сотрудников лаборатории были проблемы с дифференцировкой между неспецифической дегенерацией клеток и цитопатическим эффектом.
4. Не менее 80% полиовирусов или изолятов, подозрительных на полиовирус, от случаев ОВП направлены в РРЛ для ВТД в течение 7 дней после получения результата.
Очень важно, чтобы программа ликвидации полиомиелита получала информацию обо всех изолятах дикого и вакцинно-родственного полиовируса как можно скорее. Все изоляты полиовируса от случаев ОВП, контактных и других подозрительных на полиомиелит случаев должны без промедления направляться в лабораторию, выполняющую ВТД. Полиовирусы, выделенные от не ОВП случаев или во время проведения дополнительных мероприятий по надзору (например, из окружающей среды), должны также пройти ВТД. Их следует также направлять в референс-лабораторию как можно скорее (в идеале, а течение 7 дней после обнаружения).
5. Оценка результатов последнего проведенного ВОЗ профессионального тестирования составляет не менее 80%.
Для получения полной аккредитации результаты профессионального тестирования (ПТ) должны быть представлены в течение 28 дней (традиционный алгоритм) или 14 дней (новый алгоритм) со дня получения панели ПТ.
6. Оценка работы лаборатории по результатам ежегодного аккредитационного визита составляет не менее 80%.
Для лабораторий, получающих высокую оценку в течение 3 или более лет подряд, при отсутствии изменений в руководящем составе лаборатории в течение этого периода глобальным лабораторным координатором может быть принято решение отложить визит в лабораторию и провести ее аккредитацию на основании результатов заполненного лабораторией проверочного листа.
Ежегодный показатель выявления неполиомиелитных энтеровирусов (НПЭВ):
Уровень изоляции НПЭВ не является критерием для аккредитации, поскольку вариабельность результатов определяется сезоном года, плотностью и гигиеническим уровнем населения. Тем не менее, этот показатель может быть полезным индикатором работы лаборатории и должен обсуждаться с рецензентом. Ежегодный показатель изоляции НПЭВ в большинстве тропических стран обычно превышает 10%.
Определить сферы деятельности, требующие улучшения.
• Разработать и внедрить план работы.
• Отслеживать прогресс, достигнутый в работе лаборатории.
• Предоставить возможность выполнения повторного тестирования, если потребуется.
• Предоставить возможность выполнения дополнительного ПТ в случае необходимости.
• Продолжить работу по достижению полной аккредитации.
• Лаборатория, не справившаяся с выполнением ПТ, в течение 6 месяцев после проведения оценки считается не аккредитованной, и в сотрудничестве с ВОЗ должна быть достигнута договоренность с аккредитованной лабораторией о дублирующем тестировании всех образцов.
Проверочный лист составлен в первую очередь для лабораторий тех стран, в которых проводится надзор за ОВП. Подходящие компоненты критериев 2-6 могут быть использованы и для лабораторий, работающих в других областях общественного здравоохранения.
Проверочный лист состоит из четырех частей. Часть I обобщает результаты обзора и данные, на которых основывается аккредитация. Часть II содержит таблицы для подсчета и записи показателей работы лаборатории по критериям 1- 5 за предшествующие 12 месяцев. (Выбор последних 12 месяцев, а не последнего календарного года в качестве основы для расчетов дает возможность оценить работу лаборатории в любое время года в течение календарного года). В части III дается описание лаборатории, что позволяет определить ее потребности. Часть IV представляет собой проверочный лист для оценки используемых лабораторией операционных процедур и методик согласно критерию 6.
Данный проверочный лист не охватывает всех видов деятельности лаборатории или всех возможных ситуаций. Он предназначен для использования в качестве руководства.
Предполагается, что опытный рецензент проведет детальный расспрос и даст рекомендации, которые помогут лаборатории достичь высоких показателей в своей работе.
January 2008 National Polio Laboratory Checklist Национальная лаборатория по диагностике полиомиелита Контрольный вопросник для ежегодной аккредитации ВОЗ Лаборатории уведомляются заранее о проведении аккредитации и предоставляют копию заполненной формы с целью оказания помощи при сборе информации.
Дата проверки: Аккредитация на календарный год:
Лаборатория:
Адрес:
Тел.: Факс: E-mail:
Руководитель учреждения:
Руководитель лаборатории:
Ответственный исполнитель:
Кем проведена аккредитация
Название Национального органа аккредитации и текущий статус аккредитации:
Аккредитовать: Лаборатория соответствует всем критериям Аккредитовать условно: Лаборатория прошла последнее профессиональное тестирование, но не соответствует одному или нескольким критериям
ОПИШИТЕ МЕРЫ, ПРЕДПРИНЯТЫЕ В ОТНОШЕНИИ ИЗОЛЯТОВ, НЕ ПОДТВЕРЖДЕННЫХ РРЛ:
1. Персонал Количество научных и технических сотрудников, работающих в полиомиелитной 1.1.
лаборатории: пожалуйста, перечислите в соответствии с должностными обязанностями и указанием количества лет работы в полиомиелитной лаборатории и процента рабочего времени, затрачиваемого на работу по полиомиелиту в настоящее время
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
Часть IV: Операционные процедуры и методики, используемые в лаборатории
1. Использование помещения (4%) Баллы:
1.1. Помещение используется эффективно:
1.2. Оборудование в лаборатории расположено рационально:
1.3. Конфигурация помещения адекватная и соответствует надлежащей лабораторной практике:
1.4. Помещение содержится в чистоте и порядке
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
2. Персонал (4%) Баллы:
2.1. Распределение персонала эффективно:
2.2. Обязанности сотрудников внесены в их должностные инструкции:
2.3. Количество обученных сотрудников достаточно для существующей рабочей нагрузки:
2.4. Регистрация обучения сотрудников ведется своевременно, информация доступна для ознакомления:
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
4. Клеточные линии (6%) Баллы:
4.1. Имеются распечатанные стандартные операционные процедуры по:
a. замораживанию и восстановлению клеток:
b. пассированию клеток:
c. созданию банка клеток:
Используются RD и L20B линии клеток:
Еженедельно обе линии клеток имеются в наличии для заражения:
Клетки получены из соответствующих запасов ВОЗ:
Клетки с небольшой пассажной историей хранятся в жидком азоте:
Клетки регулярно заменяются новыми, минимум через 3 месяца или через 15 4.6.
Постоянно или периодически осуществляется подсчет клеток с целью 4.7.
определения соответствующей плотности посева при пересеве клеток:
Клетки остаются здоровыми в виде монослоя не менее 5 дней:
Ведение клеток осуществляется в помещении, изолированном от зоны, 4.9.
используемой для обработки и инокуляции образцов:
4.10. Питательные среды и клетки готовятся в разное время:
Постоянно ведутся протоколы пассирования и хранения клеток:
Приготовленные среды и исходные реагенты соответствующим образом 4.12.
промаркированы, с указанием даты изготовления и срока годности, и хранятся при соответствующей температуре:
5. Осуществление регулярной оценки чувствительности клеток Баллы:
(6%) Имеются распечатанные стандартные операционные процедуры по оценке 5.1.
Лабораторные стандарты контроля качества (ЛСКК) приготовлены в 5.2.
соответствии с рекомендованной методикой и достаточное количество промаркированных аликвот хранится при температуре –20oC.
Чувствительность клеток оценивается в отношении всех трех серотипов 5.3.
полиовируса по крайней мере в середине 15 пассажей или каждые 3 месяца:
Протоколы оценки чувствительности сохраняются, результаты оценки 5.4.
обобщаются в формате, позволяющем анализировать тенденции:
При снижении чувствительности клеток предпринимаются корректирующие 5.5.
меры (замена линий клеток, повторное тестирование образцов):
Результаты оценки чувствительности клеток сообщаются региональному 5.6.
лабораторному координатору в течение 48 часов после завершения теста:
УКАЖИТЕ РЕЗУЛЬТАТЫ (log TCID50 для каждой линии клеток и серотипа полиовируса)
6. Образцы стула (10 %) Баллы:
6.1. Имеются соответственные распечатанные стандартные операционные процедуры по обработке образцов:
6.2. Образцы обрабатываются хлороформом в соответствии с протоколами ВОЗ:
6.3. Образцы стула и экстракты хранятся при температуре –20oC в течение рекомендованных сроков:
Исходные образцы хранятся в оригинальных контейнерах при температуре 20oC от 6 (для лабораторий с большой рабочей нагрузкой) до 12 (для лаборатории с низкой рабочей нагрузкой) месяцев :
Экстракты хранятся при температуре –20oC, если они не берутся в работу в тот же день:
Экстракты стула хранятся при температуре –20oC минимум 3 месяца и уничтожаются после подтверждения результатов:
6.4. Работа со всеми потенциально инфекционными клиническими материалами производится в шкафу биологической безопасности:
6.5. Оригинальные образцы стула, экстракты стула, все вирусные изоляты и другие потенциальные инфекционные материалы соответственно промаркированы и хранятся отдельно от неинфекционных материалов в соответствующих морозильниках или холодильниках:
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
7. Изоляция вируса (12%) Баллы:
7.1. Имеются в наличии распечатанные стандартные операционные процедуры по изоляции вируса:
7.2. Первый и второй образец от каждого пациента обрабатываются и инокулируются в культуру клеток отдельно, никогда не смешиваются:
7.3. Инокуляция экстрактов в культуру клеток осуществляется в течение 2-3 дней после приготовления:
7.4. Экстракты инокулируются в культуры клеток RD и L20B одновременно:
7.5. Пассирование культур осуществляется в соответствии с используемым алгоритмом:
Для традиционного алгоритма:
RD(+)/L20B(-) изоляты пассируются в клетках L20:
Два последовательных пассажа по 7 дней каждый осуществляются в двух линиях клеток, прежде чем образец расценивается как отрицательный (минимальное общее время для культивирования – 14 дней):
Для нового алгоритма:
Все L20B(+) изоляты пассируются в клетках RD:
Все RD(+) изоляты пассируются в L20B клетках и затем обратно в клетках
RD, если ЦПЭ воспроизводится:
Два последовательных пассажа по 5 дней каждый осуществляются в двух линиях клеток, прежде чем образец расценивается как отрицательный (минимальное общее время для культивирования – 10 дней):
7.6. Наблюдения за инокулированными клетками с соответствующей записью ведутся ежедневно:
Для лабораторий, использующих новый алгоритм:
Интерпретация результатов исследования проводится в соответствии с рекомендациями ВОЗ:
Регистрируется информация о результатах серотипирования и внутритиповой дифференциации, полученная от лаборатории, в которую изоляты были направлены для изучения:
Вирусные изоляты хранятся в соответственно промаркированных флаконах с 8.3.
указанием идентификационного номера, типа изолята, названия линии клеток и даты сбора:
Изоляты хранятся при температуре –20oC или ниже в течение минимум 12 8.4.
месяцев. Для идентификации местонахождения изолятов ведется соответствующая документация:
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
Биологическая безопасность (10%) Баллы:
10.1. Все сотрудники прошли инструктаж по биологической безопасности:
10.2. Стандартные операционные процедуры по дезинфекции и деконтаминации материалов и поверхностей, утилизации инфекционных отходов, удалению пролитых жидкостей, сообщению об авариях и подверганию воздействия инфекционного материала имеются в наличии:
10.3. Разработано руководство и проведено обучение сотрудников по их действиям в чрезвычайной ситуации (пожар или другие происшествия):
10.4. Внедрены меры биологической безопасности, включая:
a. Мытье рук:
b. Пипетирование с использованием механических приспособлений:
В лабораторных помещениях запрещен прием пищи, напитков, курение и хранение пищевых продуктов:
Применение персональных защитных средств при работе в лаборатории, включая перчатки, лабораторные халаты, маски:
e. Использование лабораторных халатов и перчаток только в лаборатории:
Деконтаминация отходов инфекционных и клинических материалов перед их уничтожением:
g. Деконтаминация рабочих лабораторных поверхностей:
Использование для сбрасывания инфекционных отходов не прокалываемых, не подвергающихся коррозии и автоклавируемых контейнеров соответствующего размера:
i. Иммунизация сотрудников против полиомиелита:
10.5. Персональное защитные средства имеются в достаточном количестве:
10.6. Шкафы биологические безопасности и специально отведенные зоны используются для работы с потенциально инфекционными и чистыми материалами, соответственно:
10.7. Шкафы биологической безопасности обслуживаются в соответствии с рекомендациями, включая ежегодную сертификацию с заменой фильтров в случае необходимости:
10.8. Лабораторные поверхности устойчивы к воздействию воды и дезинфектантов, а также других химикатов:
10.9. Мониторы стерилизации (например, биологические и химические индикаторы) применяются для оценки эффективности автоклавирования, применяемого для деконтаминации инфекционных отходов:
10.10. Знак биологической угрозы размещен на входе в лабораторию и вход в лабораторию разрешен только персоналу, имеющему соответствующий допуск:
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
12. Оборудование (4%) Баллы:
12.1. Руководство по эксплуатации оборудования и распечатанные стандартные операционные процедуры имеются в наличии:
12.2. Ведется инвентаризация оборудования:
12.3. Ежедневно регистрируются температурные показатели для оборудования, чувствительного к колебаниям температуры: морозильников, термостатов, холодильников:
12.4. Оборудование периодически калибруется:
12.5. Периодически производится техническое обслуживание оборудования, и даты проверки регистрируются:
12.6. Оборудование функционирует и находится в хорошем состоянии:
12.7. Расположение оборудования способствует оптимальной организации работы:
12.8. Не функционирующее оборудование, которое невозможно починить, помечено соответствующим образом и удалено из лаборатории:
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
13. Сотрудничество с РПИ и специалистами, осуществляющими Баллы:
надзор за инфекционными заболеваниями (4%)
13.1. Сотрудники лаборатории и РПИ или эпиднадзора встречаются не реже одного раза в месяц:
13.2. Сотрудники РПИ или эпиднадзора уведомляются о случаях доставки образцов в лабораторию без адекватной информации и ЭПИД номера:
13.3. Лаборатория представлена в:
КОММЕНТАРИИ И РЕКОМЕНДАЦИИ:
14. Ведение отчетности и сотрудничество с региональными офисами Баллы:
14.1. Имеются в наличии распечатанные стандартные операционные процедуры по вводу данных, их обработке и отчетности:
14.2. Дубликат данных хранится в безопасном месте:
14.3. Лабораторные отчеты предоставляются в региональный офис ВОЗ в соответствующем формате и с необходимой частотой:
14.4. Следующие данные (см. стр. 16) имеются по всем полио и неполиомиелитным
Читайте также:
- Эпид надзор за сальмонеллезами
- Может быть головная боль при стафилококке
- Сальмонеллез в саду на ленской
- Сальмонеллез на всю жизнь
- Откуда берется золотистый стафилококк в кале
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

