В чем сложность приема арвт при вич
Знать и верить для того, чтобы жить…
Уж коль болезнь послал мне мой жестокий рок,
Лекарство –есть , так учит мой урок…
Всем моим пациентам посвящается.
Часть 1.Немного истории.
Вплоть до 2004 года при выявлении у пациентов ВИЧ-инфекции на последних стадиях болезни мне приходилось только констатировать необратимость ухудшения их здоровья в связи с непрерывно прогрессирующим иммунодефицитом. Назначать при этом огромные дозы антибиотиков, противогрибковых препаратов , витаминные препараты, которые уже были бессильны изменить ситуацию со здоровьем в лучшую сторону, и понимать ,что летальный исход рано или поздно неизбежен. Причём стараться избегать любых прямых разговоров о смерти со своими пациентами.
Появление у нас в стране в 2004 году Проекта ПРООН при поддержке Глобального фонда для профилактики и лечения ВИЧ-инфицировнных граждан Республики Беларусь и внедрение высокоактивной антиретровирусной терапии( АРВТ) для наших пациентов стало настоящим прорывом в оказании им медицинской помощи. Врачи –инфекционисты получили мощное оружие против ВИЧ в виде антиретровирусных препаратов. Тогда стало возможным радикально изменить ход болезни , улучшить качество жизни пациентов и реально продлить им жизнь. ВИЧ-инфекция из ряда смертельных перешла в ряд хронических длительно протекающих болезней.
Часть 2.Что такое АРВТ?
На фоне АРВТ кроме всего уменьшается число осложнений, улучшается качество жизни (пациенты чувствуют себя совершенно здоровыми людьми), значительно продлевается жизнь ВИЧ-положительных пациентов. АРВ-терапия стала неотъемлемой частью комплексной медицинской помощи ВИЧ-положительным пациентам, наряду с профилактикой, лечением сопутствующих болезней.
Основными принципами проведения АРВТ являются:
1.Лечение предоставляется всем пациентам, нуждающимся в нём по медицинским показаниям и выразившим желание лечиться не зависимо от их социального статуса.
2.Лечение представляет собой комбинацию из не менее 3-х антиретровирусных препаратов, схема приёма которых и дозировка подбирается врачом –инфекционистом каждому пациенту индивидуально согласно протоколов лечения, утверждённых Министерством здравоохранения РБ.
3.Лечение должно быть непрерывным, то есть пожизненным. Диспансерное наблюдение, мониторинг за ходом лечения устанавливается лечащим врачом. Основными показателями эффективности лечения являются вирусная нагрузка и количество СД-4 клеток(так называемая иммунограмма).
4. И самое главное: пациент должен быть мотивирован на проведение АРВ -терапии и иметь высокую приверженность к лечению.
Часть 3.Что такое приверженность?
Дословно из толкового словаря приверженность -это привязанность, пристрастие, хорошее отношение к кому-либо, чему-либо.
Приверженность к АРВ-терапии – это приём АРВ препаратов по схеме, назначенной врачом: в определенное время и в определенной дозировке, при соблюдении рекомендуемого режима питания. Таким образом - это хорошее отношение к собственному лечению, полное осознанное понимание важности его для себя, самоконтроль и самодисциплина.
Сюда же можно добавить доверие к лечащему врачу, систематическое добровольное выполнение врачебных рекомендаций по обследованию в ходе лечения.
Приверженность к лечению -это прежде всего хорошее отношение к самому себе и к жизни.
В моей практике за 15 лет работы с ВИЧ-позитивными пациентами не раз возникали случаи полного непринятия АРВ терапии, то есть категорический отказ от неё. При этом пациент охотно обследуется , уточняет свои анализы , данные иммунограмм и даже лечит какие-то другие заболевания. Уверена , что в Интернете или ещё где-либо он получает дополнительную информацию о современных методах лечения ВИЧСПИДа, то есть о своей болезни и её стадии знает немало. Но как только речь заходит о назначении АРВТ , то полный негатив!
Я попыталась проанализировать и как-то систематизировать основные факторы отказа от терапии. Вот что получилось.
На первом месте утверждение пациента ,что он прекрасно себя чувствует, жалоб на здоровье у него нет , анализы в относительной норме. Даже красноречивые иммунограммы ,которые доказывают на продвинутую стадию ВИЧ ни в чём такого пациента убедить не могут.
На втором месте боязнь нанести вред АРВ препаратами своей печени. В основном за свою печень переживают люди с сопутствующим гепатитом. При этом часть из них не оказываются употреблять алкоголь и (или) наркотики, хотя им разъясняется , что вред от них для печени куда более колоссален.
На четвёртом месте страх , что АРВ терапия может убить больного. При этом пациенты иногда приводят примеры , что , дескать , их знакомые жили себе хоть и болели тяжело, но тихо , а вот как начали принимать АРВТ через месяц –второй погибли. Да, к сожалению, такое случалось. Но погибали пациенты не от лечения , а от того , что это лечение было начато очень поздно и помочь им уже оказалось невозможно.
Часть 4.Когда начинать лечение?
Сразу же сделаю одно очень важное пояснение: антиретровирусную терапию чаще всего нет необходимости назначать срочно, то есть по жизненным показаниям. Старт АРВТ- это плановый подход к началу лечения при тщательном дообследовании пациента и с его личного согласия. Исключение составляют ВИЧ-позитивные беременные женщины , АРВ препараты которым назначаются с главной целью - снизить риск вертикальной передачи ВИЧ от матери к ребёнку во время беременности и родов с 16 недель беременности. Даже на последних стадиях СПИДа при тяжёлом состоянии пациента АРВ терапия назначается спустя 2-4 недели от начала клинического обследования больного. Особенно важно за этот промежуток времени исключить у пациента активный туберкулёзный процесс, поскольку лечение туберкулёза начинается первым, а затем к нему присоединяется антиретровирусная терапия против ВИЧ.
В целом, АРВ терапия должна начинаться при наличии у пациента ВИЧ 3 и 4 стадии. Стадия болезни уточняется врачом –инфекционистом по клиническим и лабораторным критериям. В процессе уточнения стадии болезни велика роль иммунологического обследования пациента, так называемый иммунный статус больного. При сопоставлении всех данных обследования схема АРВ терапии назначается врачом-инфекционистом, разъясняется пациенту и ,при наличии письменного согласия пациента на проведение АРВТ ,лечение стартует. Старт терапии осуществляется чаще всего в амбулаторных условиях, реже в условиях стационара , если состояние больного требует госпитализации. Ход лечения мониторируется проведением общеклинических анализов: общего анализа крови и мочи , биохимического анализа крови , иммунограммами и определением вирусной нагрузки вначале ежемесячно , далее не реже одного раза в шесть месяцев. Эффективность схемы АРВ терапии, а также правильность приёма препаратов пациентом, определяется по иммунограмме.
Часть 5.Что такое иммунограмма?
Иммунограмма – это комплексный анализ крови, в котором исследуются компоненты иммунной системы. Для исследования берётся венозная кровь пациента. Основные компоненты для исследования Т-лимфоциты , так называемые СД-4 клетки. Именно они поражаются вирусом иммунодефицита человека (ВИЧ) в ходе болезни, и именно от их количества зависит клиническая картина болезни и состояние больного. Количество СД-4 клеток предъявляется лабораторией лечащему врачу как в абсолютных цифрах , так и в процентном соотношении в пересчёте на микролитр(мкл) крови пациента. Если схема АРВ терапии эффективна , то уровень СД-4 клеток неуклонно повышается, это проявляется в улучшении состояния здоровья пациента. Но основным критерием эффективности лечения служит вирусная нагрузка (ВН) - это количество РНК-копий вируса (ВИЧ) в микролитре крови больного, то есть количество вируса в организме человека. Если образно представить болезнь ВИЧСПИД в виде локомотива, то вирусная нагрузка –это скорость , с которой этот локомотив(болезнь) движется к трагическому финишу .Эффективная АРВ терапия подавляет вирусную нагрузку уже в первую неделю от старта. Желаемые показатели ВН в ходе лечения составляют менее 200-500 РНК копиймкл крови , это так называемая неопределяемая вирусная нагрузка. Такие показатели особенно важны при проведении АРВ профилактики ВИЧ у беременных, поскольку сводят риск передачи ВИЧ от матери к ребёнку практически к нулю. При неукоснительно поддерживаемой высокой концентрации АРВ-препаратов в крови вирусная нагрузка должна оставаться неопределяемой если не всегда, то довольно долго. Необходимая высокая концентрация АРВ препаратов достигается путём их правильного дозирования и режима приёма. Для этого нужно, чтобы пациент принимал назначенную дозу АРВ-препарата строго по часам непрерывно и постоянно, то есть был высоко привержен к лечению.
И ещё важно знать , что самовольное нарушение или прекращение схемы антиретровирусной терапии чревато тем , что вирус ВИЧ приобретает устойчивость (резистентность) к АРВ препаратам, иногда к нескольким сразу, а это приводит к прогрессированию болезни, усложняет подбор новой комбинации АРВ препаратов. В результате эти комбинации от простых становятся сложными , от приёма 2-3 таблеток в сутки увеличиваются до приёма 6-9 таблеток в сутки, что создаёт ещё большие трудности в достижении успеха в лечении.
Вот поэтому так важна приверженность пациента к АРВ терапии.
Кстати будет сказать, что в природе существуют ещё несколько болезней ,при которых необходим пожизненный приём лекарственных препаратов. Одной из таких болезней является сахарный диабет 1 типа, при котором пациент должен получать инсулин по часам всю свою жизнь.
Часть 6.Сложности приёма АРВ-препаратов.
Для того , чтобы понять, что чувствуют хронические больные, когда им приходится пожизненно принимать то или иное лекарство , нужно хотя бы на время встать на их место. Причём не в физическом смысле этого понятия, а, скорее, в психологическом. Тогда будет хоть немного ясно, что собственное лечение –это труд прежде всего над собой, это мужество, терпение и огромная сила воли. Это отказ от некоторых привычек, в первую очередь, вредных!), от традиций, иногда даже отказ от прежнего круга общения. Это непросто. Для ВИЧ-позитивных пациентов пожизненное лечение ещё более психологически сложно , потому что нужно вначале признать свою болезнь, свыкнутся с ней и продолжать жить. Очень многие мои пациенты не посвящают своих близких в тайну своей болезни, а как им тогда объяснить , почему они принимают лекарства?
Поэтому главной сложностью приёма АРВТ я считаю психологический фактор, когда наступает психологическая усталость от непрерывного лечения. Но осознание пользы лечения и огромное терпение позволяет отбросить болезнь далеко назад и продолжать борьбу с болезнью. У меня есть пациенты , которые имеют высокую приверженность к лечению, принимают АРВТ с 2004 года , а это уже более 8 лет. Восемь лет непрерывного почасового приёма таблеток! Более того , есть ВИЧ-позитивные дети , которым уже 12- 14 лет , они принимают АРВ терапию с рождения! Самому старшему юноше, который получил ВИЧ-инфекцию от своей мамы и продолжает АРВТ, уже 20 лет!Это и есть пример высокой приверженности к лечению мам этих детей, но и самих детей ещё в большей степени.
Антиретровирусные препараты –это химические вещества. Зачастую с неприятным вкусом и запахом, причём в одинаковой степени это относится и к таблеткам, и к сиропам. Поэтому вторая сложность приёма АРВТ- это вкусовое восприятие лекарства. Какую –то часть АРВ препаратов нужно принимать натощак , другую часть с едой. Эти рекомендации даются врачом для того , что эффективность всасывания лекарства в желудочно-кишечном тракте была максимальной. Понятно , что весь вкус и запах препарата пациент ощутит сразу. Рекомендую строго придерживаться правилу запивать лекарство достаточным количеством воды , не менее 100 мл, для того чтобы оно быстрее растворилось и всосалось в кровь. Если после приёма лекарства возникла рвота , то не принимайте новую порцию АРВ препарата , а дождитесь следующего приёма очередной дозы. За это время можете съесть или выпить что-то вкусное , но удобоваримое, чтобы уменьшить неприятное послевкусие.
Любой лекарственный препарат имеет побочные эффекты. О них пишут в аннотациях к препарату , о них должен предупреждать лечащий врач. Ещё одна сложность приёма АРВ-препаратов –это боязнь развития побочных эффектов. Поскольку лечение ВИЧ/СПИДа это очень длительный процесс, то побочные эффекты могут возникнуть на всех этапах терапии. Всё это обговаривается с пациентом. Для того , что вовремя заметить побочные эффекты, врач назначает регулярные обследования пациента с исследованием анализов крови и мочи. Чаще всего пациент сам указывает на такие побочные явления как тошнота, понос, головокружение , головная боль ,прибавка в весе, нарушение сна, реже отмечается сыпь. Все эти явления постепенно исчезают самостоятельно , а в случае их затяжного течения врач назначает параллельно другие медикаменты , облегчающие симптомы. Бывает , что врач и вовсе отменяет АРВ-препарат и заменяет его на другой. То или иное решение обсуждается с пациентом и принимается в интересах больного.
Побочные эффекты на фоне АРВТ ,которые могут угрожать жизни больного ,развиваются крайне редко и при отмене препарата имеют обратимый результат.
Хочу предупредить , что употребление алкоголя и(или ) наркотиков, а также курение в ходе АРВТ могут спровоцировать наступление побочных эффектов и утяжеляет их проявления.
Абсолютно все пациенты обычно интересуются побочными эффектами АРВ-препаратов, многие спрашивают о совместимости с другими лекарствами, которые назначаются другими врачами параллельно лечению. И это правильно. Но бывают случаи , когда пациент в большей степени опасается побочных эффектов от терапии , чем последствий , связанных с прогрессированием СПИДа. А вот это большая ошибка! Побочные эффекты можно предупредить , устранить, а вот прогрессию смертельного заболевания без соответствующего лечения –нет. Это надо чётко понимать.
На стартовой фазе АРВТ врач обычно старается назначить эффективную схему , при которой используется минимальное количество таблеток в сутки , чаще всего пять –шесть , а иногда , в случае комбинации двух АРВ-препаратов в одной таблетке, то всего три в сутки. В случае неэффективности АРВ-терапии, схемы лечения должны меняться, а это может привести к увеличению количества таблеток до 8-10 штук в сутки. А неэффективной схема АРВ-терапии может стать и по вине самого пациента ,если он не привержен к лечению и здоровому образу жизни.
Каждый человек –это личность со своими достоинствами и недостатками, со своими страхами и силой. Но всё ,что объединяет людей –это разум и огромная жажда жизни. Жизнь-это бесценный дар , данный нам Богом и природой, ценить его нужно и должно.
Хочу пожелать всем не ошибиться в правильном выборе, продолжать жить и радоваться каждому прожитому дню, дарить заботу и любовь, любить и быть любимыми ,словом ,прожить жизнь так , чтобы всегда оставаться Человеком.
Врач-инфекционист высшей категории Додалева Елена Николаевн Минск.Республика Беларусь.
В настоящий момент антиретровирусная терапия помогает миллионам людей по всему миру жить жизнью без ограничений, не смотря на страшнейшее заболевание. Победить вирус полностью пока не удается, но возможность жить до 70 лет, будучи носителем вируса иммунодефицита – уже большая победа.
Разработки эффективных препаратов антиретровирусной терапии ведутся с самого первого зарегистрированного случая заболевания, однако лишь спустя несколько десятилетий получилось найти удачный подход к контролю заболевания. На сегодняшний день, инфицированный человек может прожить долго и вполне полноценно, завести здоровых детей, не бояться сезонных инфекций и работать практически в любой сфере.
Как действует антиретровирусная терапия?
Давайте разберемся, как действует антиретровирусная терапия? Это не волшебная таблетка, а распорядок, которого пациент должен строго придерживаться под наблюдением врачей. Комплекс противовирусных препаратов подбирается индивидуально, и обычно корректируется на протяжении всего течения болезни.
Высокоактивная антиретровирусная терапия направлена на снижение вирусной нагрузки и на уменьшение проявлений заболевания. Правильно подобранное лечение улучшает качество жизни, снижает вероятность возникновения и развития оппортунистических инфекций. Регулярный прием препаратов существенно продлевает жизнь инфицированному, дает шанс отсрочить наступление терминальной стадии заболевания, а также делает носителя безопасным для половых партнеров и эмбриона беременной зараженной женщины.
Преимущества АРВТ при ВИЧ очевидны: больной может жить точно так же, как и ВИЧ-отрицательные люди. Конечно, для максимального эффекта требуется отказ от вредных привычек, здоровое питание. Не смотря на возможность побочных эффектов, прием лекарств все же является единственной возможностью для активного долголетия.
АРВТ ВИЧ инфицированных должна назначаться врачом после детального обследования. В последние годы взгляды и подход к борьбе изменились, потому настоятельно рекомендуется обращаться к хорошим врачам, которые следят за развитием медицины.
АРВТ побочные эффекты имеет, но коррекция в ходе лечения, а также дополнительные лекарственные средства могут свести неприятные проявления к минимуму. Противовирусные препараты могут оказывать токсичное воздействие на печень и почки, в ряде случаев и на другие органы. Во время лечения может периодически может возникать тошноте, диарея, анемия. Но здоровое питание и дополнительные протекторные лекарства помогут поддерживать все параметры в норме. По статистике, примерно 80% подопечных испытывают неудобства от побочных эффектов.
Как уже было сказано, в последние годы подход к лечению изменился. Раньше лечение назначали сразу после выявления вируса, теперь врачи к выводу, что это ошибочно.
Когда назначается антиретровирусная терапия? Лишь только после того как врач установит стадию болезни, оценит состояние организма пациента. Слишком ранние меры может привести к быстрой мутации вируса и снижению результативности действующего вещества.
Антивирусная терапия при ВИЧ назначается при определенных показателях:
- Т-лимфоциты 350 кл/мл и ниже;
- Вирусная нагрузка 55000/мл и выше;
- Клиническая стадия ВИЧ на 3 или 4 стадии.
Одновременно с назначением ВААРТ, больному дается ряд рекомендаций по поддержанию здоровья. Это может быть спорт, диета, особый режим дня. Рекомендации даются индивидуально, на основании замера жизненных показателей пациента. Несоблюдение рекомендаций снижает плодотворность лечения и ускоряет развитие заболевания.
Схемы АРВ терапии
АРВ терапия при ВИЧ назначается в соответствии с определенной схемой. Подбирает программу только квалифицированный медицинский работник, никакого самолечения быть должно. Условно схемы делятся на 3 типа:
Смена курса лечения происходит только по решению лечащего врача. Следует знать, что любой удачно подобранный комплекс даст временный успех, потому что вирус приспосабливается и вырабатывает резистентность. По этой причине, важно наблюдаться регулярно, следить за состоянием и вовремя делать коррекцию в лечебной программе. Со временем, через некоторое время после начала курса уровень Т-лимфоцитов снова начинает падать, а вирусная нагрузка – расти. Это значит, что вирус мутировал и адаптировался, пора менять дозировку или сам препарат.
Антиретровирусная терапия в лечении ВИЧ инфицированных
Антиретровирусная терапия при ВИЧ дает потрясающие результаты. Препараты все более совершенствуются, что обусловлено и постоянной мутацией вируса, который приспосабливается. Но все же, каждое новое поколение лекарств лучше предыдущего. Эффективность лечения у всех разная, это связано с индивидуальными особенностями организма. Но, тем не менее, практически для каждого зараженного можно подобрать эффективную комбинацию веществ.
Ретровирусная терапия при ВИЧ обычно включает 3 или 4 препарата, плюс дополнительно назначают гепатопротекторные или другие поддерживающие комплексы для улучшения самочувствия. Оценить первые результаты и скорректировать лечение можно через 6-8 месяцев после начала.
Антиретровирусная терапия ВИЧ инфицированных лечение проходит строго под присмотром и контролем, нельзя игнорировать требования сдать анализы или прийти на осмотр.
Не забывайте, что лечение нельзя останавливать, даже если удалось достичь ремиссии и показатели пришли в норму, как у неинфицированных людей. Вирус пока не удается на 100% вывести из организма, потому прием лекарств обязателен, до конца жизни. ВААРТ является обязательной мерой в лечении, остальные таблетки, кроме противовирусных, помогают лишь поддержать силы организма, но на течение заболевания никак не влияют.
Возможные противопоказания АРВТ при ВИЧ и побочные эффекты
В чем сложность приема антиретровирусной терапии, так это в побочных эффектах, которые могут доставить существенный дискомфорт. О появившихся недомоганиях на фоне приема препаратов следует сообщать в центр, где был назначен лечебный курс. Наблюдение пациентов предполагает выявление побочных действий и, по возможности, их устранение тем или иным способом.
Противопоказанием не может послужить никакое отклонение. Линии препаратов разработаны таким образом, чтобы подобрать лекарство для каждого ВИЧ положительного. Если есть противопоказание для приема одного препарата, то подбирается другое, аналогичное по своему воздействию. Так как целю АРВТ является спасение жизни, то абсолютных противопоказаний быть просто не может.
Побочные эффекты не должны останавливать пациента: если прекратить прием, болезнь начнет прогрессировать быстро, и терминальная стадия наступит гораздо скорее, чем без лечения.
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, а значит, специальные лекарства могут тормозить его на различных этапах.
В случае с ВИЧ это выглядит так.
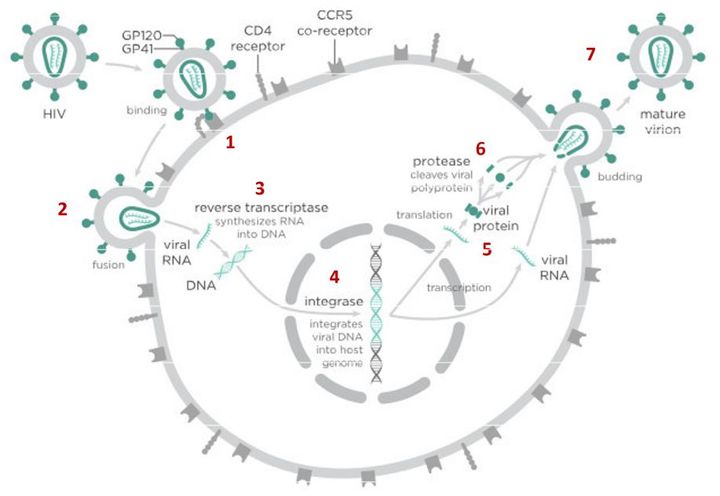

После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме). На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
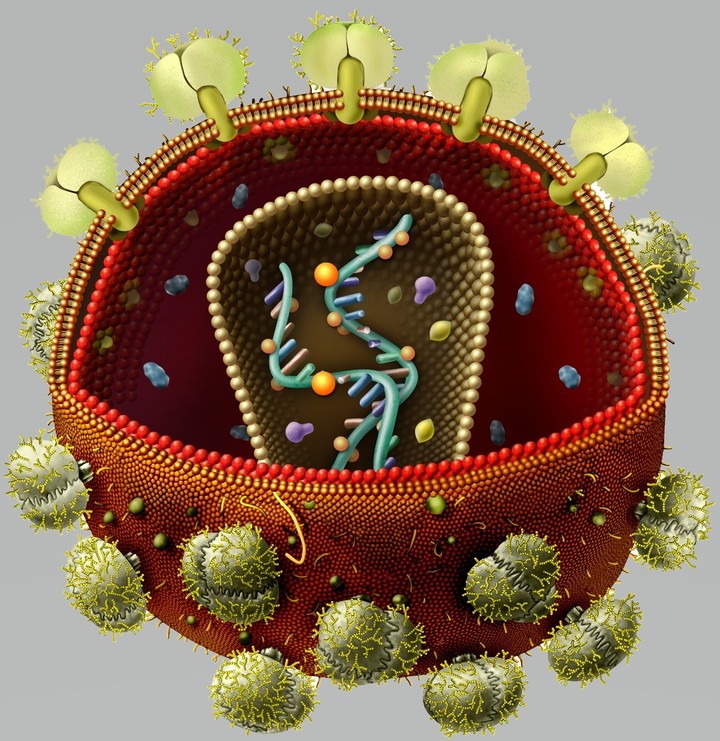
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин). Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы. Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.

После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы, включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.


Определение: фармакокинетическое прощение – это время между приемом следующей надлежащей дозой препарата и временем падения до минимальной эффективной концентрации (МЭК/MEC) антиретровирусных препаратов.
Кратко о некоторых сложностях: их немало, например, мы иногда говорим о концентрации в плазме, а важна внутриклеточная концентрация, которая может отличаться мало или существенно, как в случае с парой тенофовир дизопропил фумарат и тенофовир алафенамид; мы иногда говорим об одной молекуле препарата, а важны совсем другие, которые получаются после метаболических реакций в организме, как в случае с фосфорилированием НИОТ…
В таблице ниже представлены данные хвостовых исследований, показывающие долю участников с концентрациями лекарственного средства в плазме ниже предполагаемой МЭК после прекращения приема лекарственного средства (Dickinson L и др., 2015).
| Препарат* | ATV/r | LPV/r | LPV/r x2 | DRV/r |
| Доза, мг | 300/100 | 400/100 | 800/200 | 800/100 |
| МЭК, нг/мл | 150 | 1000 | 1000 | 550 |
| Источник, PMID | 19043924, (21709075) | 19043924 | 19043924 | 21709075 |
| Время, часы | Участники, n/N с концентрацией препарата в плазме ниже МЭК после последнего приема | |||
| 12 | 0/16 | 0/16 | 0/16 | |
| 16 | 0/16 | 2/16 | 0/16 | |
| 20 | 0/16 | 10/16 | 0/16 | |
| 24 | 0/16 | 13/16 | 7/16 | |
| 30 | 2/16 (0/17) | 15/16 | 15/16 | 3/17 |
| 36 | 5 /16 (8/17) | 16/16 | 16/16 | 8/17 |
| 48 | 11/16 (12/17) | 16/16 | 16/16 | 15/17 |
| 60 | 16 /16 (15/17) | 16/16 | 16/16 | 16/16 |
| 72 | 16 /16 | 16/16 | 16/16 | |
| *Один раз в день во всех случаях, кроме LPV/r x2 (Калетра) ATV/r – атазанавир/ритонавир; DRV/r – дарунавир/ритонавир; LPV/r – лопинавир/ритонавир. | ||||
| Препарат | EFV | EVG/COBI | DTG | RPV |
| Доза, мг | 600 | 150/150 | 50 | 25 |
| МЭК, нг/мл | 1000 | 45 | 64 | 50* |
| Источник, PMID | 23274933 | 26679246 | 26679246 | 26195515 |
| Время, часы | Участники, n/N с концентрацией препарата в плазме ниже МЭК после последнего приема | |||
| 24 | 0/17 | 0/17 | 2/18 | |
| 36 | 11/17 | 6/18 | ||
| 48 | 5/16 | 16/17 | 0/17 | 7/18 |
| 60 | 1/17 | |||
| 72 | 1/17 | 11/18 | ||
| 84 | 8/16 | |||
| **МЭК (минимальная эффективная концентрация) определена для рилпивирина недостаточно точно, интерпретировать с осторожностью. DTG – долутегравир; EFV – эфавиренз; EVG/COBI – элвитегравир/кобицистат; RPV – рилпивирин. | ||||
Хотя МЭК для НИОТ не установлены, фармакокинетические параметры активных внутриклеточных метаболитов тенофовира и эмтрицитабина были установлены в одном хвостовом исследовании, где было установлено, что оба имеют длительные конечные периоды полувыведения – 164 и 39 часов соответственно.
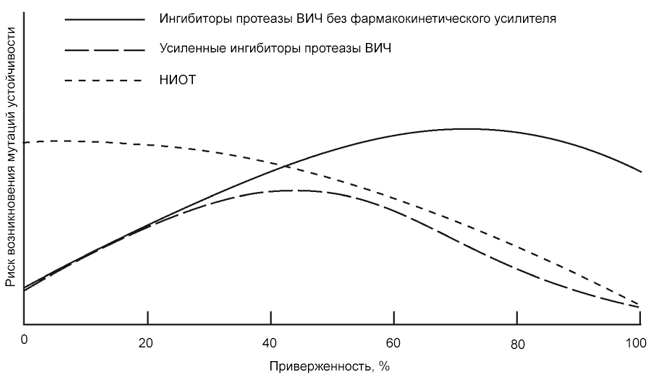
Адаптировано по Bangsberg D.R. и др., 2004. Данная модель иллюстрирует, что у разных классов АРВ-препаратов могут быть весьма различные зависимости рисков формирования резистентности по отношению к приверженности.
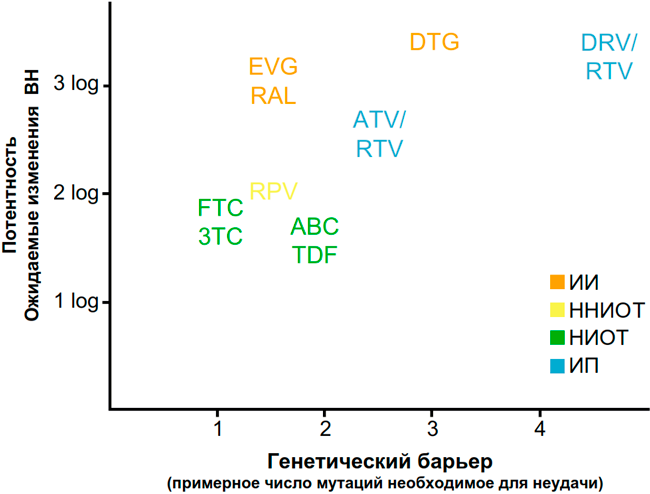
Адаптировано по Clutter D.S. и др., 2016.
В любом случае эскадра движется со скоростью самого медленного корабля, а в схеме терапии мы должны в первую очередь думать о слабом звене, о том препарате, что быстрее всех достигнет минимальной эффективной концентрации, а также о том, что имеет более низкий вирусологический барьер.
В отличие от НИОТ, например, ингибиторы протеазы (ИП) ВИЧ требуют набора мутаций устойчивости, и не все из них могут относиться к лекарственной устойчивости, а иногда направлены на компенсацию изменений, внесенных мутацией устойчивости – оказывается, вирусу не так просто адаптироваться к новым возможностям. Период полувыведения ИП довольно короток, а если препарат скоро покинул организм, то субоптимальные концентрации имели место быть недолго. Мутации к ИП крайне невыгодны для вируса, и при прекращении терапии циркулирующий штамм их довольно быстро теряет, что снижает риски передачи другим людям в виде первичной резистентности.
Полный пропуск терапии
Частота возникновения мутаций устойчивости у людей с подавленной вирусной нагрузкой стремится к нулю. Для изменений уровня вирусной нагрузки нужно некоторое время, а значит, люди со стабильно неопределяемой нагрузкой имеют предельно низкие риски при единичных отклонениях в приверженности. Следствие: – подавленная вирусная нагрузка позволяет одномоментно перенастраивать время приема современной терапии с однократным приемом внутри суток без значимых рисков, естественно, если это происходит лишь изредка; – подавленная вирусная нагрузка практически исключает то, что единичный не систематический полный пропуск терапии повлечет за собой последствия в плане рисков возникновения устойчивости; – упомянутые выше следствия относятся к современным двойным и тройным режимам, но при применении нестандартных режимов, использовании ингибиторов протеазы без бустера, облегченных режимов и монотерапии следует быть предельно осторожным и пунктуальным.
Даже если вирусная нагрузка еще не подавлена ниже уровня 50 РНК ВИЧ копий в мл, справедливым будет утверждать, что единичный полный пропуск терапии, если это не регулярное событие, также не несет никаких измеряемых рисков, во всяком случае в отношении тех случаев, когда применяются стандартные полные и современные режимы терапии с однократным или двукратным приемом.
Как определить, регулярное это событие или нет? Исследования показали, что прием 95% доз препаратов и более не отличается значительно по рискам от приема 100% доз. А значит, высокая приверженность при приеме АРВТ раз в сутки – это пропуск не чаще 1-2 раз в месяц, для приема два раза в сутки – пропуск одного приема не чаще одного случая примерно раз в две недели. Однако приложите все усилия, чтобы иметь 100% приверженность, не стоит сильно полагаться на данные, которые относятся к большим группам.
Потенциал фармакокинетического прощения (Lewis JM и др. 2016)
| Высокий потенциал | Средний потенциал | Низкий потенциал | |||
| Кратность приема | |||||
| Один раз сутки | TDF, ABC, 3TC, FTC, EFV, RPV, ATV/r, DRV/r, EVG/COBI, DTG | LPV/r | |||
| Два раза в сутки | ZDV, LPV/r, RAL, монотерапия DRV/r | монотерапия LPV/r, монотерапия ATV/r, не усиленный ATV | |||
| 3TC–ламивудин; ABC–абакавир; ATV–атазанавир; r–ритонавир; COBI–кобицистат; DRV–дарунавир; DTG–долутегравир; EFV–эфавиренз; EVG–элвитегравир; FTC–эмтрицитабин; RAL–ралтегравир; TDF–тенофовир. | |||||
Прием лишней дозы
Дополнительный прием препаратов возможен при консервативном подходе при смене времени приема режима терапии, но чаще это происходит по той же причине, что и пропуск – забывчивость. Используйте контейнеры для лекарств с ячейками по дням недели, хотя бы записывайте регулярно общее число имеющихся таблеток на определенную дату, чтобы иметь возможность посчитать в случае необходимости.

Принято считать антиретровирусные препараты очень токсичными, однако, тут есть некоторое недопонимание и путаница с разными видами токсичности. Данные о передозировках АРВТ, собранные NPDS (National Poison Data System) в США, говорят о том, что документированных передозировок, в том числе умышленных, происходит в США в год несколько сотен случаев, однако, за период с 2007 по 2011 год лишь одна из более чем 1500 передозировок привела к смерти, тяжелые последствия имели лишь 5 случаев из этих передозировок. Заметим, что в некоторых случаях речь идет о приеме сотен таблеток. Передозировка 270 таблетками Калетры вызывала лишь легкие временные неблагоприятные явления. Однократные дозы 3200 мг дарунавира или 1200 мг атазанавира у здоровых добровольцев не вызывали никаких явных побочных явлений.
Высокие дозы эфавиренза могут у некоторых людей вызывать значимые временные проблемы, связанные с психической деятельностью. Высокие дозы маравирока способны вызвать постуральную гипотензию, то есть падение артериального давления при переходе из сидячего или лежачего положения в положение стоя, что может быть чревато обмороком, падением и травмами.
Таким образом, мы видим, что обычно дополнительный прием одного или всех препаратов вашей схемы терапии не несет никаких измеряемых рисков, за исключением понятных ситуаций с отдельными препаратами, вроде эфавиренза, и то при условии, что препарат переносится именно данным пациентом не идеально. Если по ошибке произошел дополнительный прием препаратов, то не следует предпринимать никаких действий. Время и кратность приема остаются теми же и не требуют никакой коррекции.
Изменение времени приема терапии
Если вы прочитали текст выше, вам уже все ясно. Если ваша терапия - стандартный двойной или тройной режим, смело сдвигайте одномоментно свою терапию на удобное время. Остаетесь вы дома или сменили часовые пояса – не имеет значения. Однако, если вы используете ингибиторы протеазы без усилителя, нестандартные двойные схемы или монотерапию, стоит быть предельно осторожным и производить изменение времени приема мелкими шагами в пределах одного часа каждые сутки.
Заключение
Пунктуальность в приеме препаратов достигается очень просто при правильной организации процесса, и не стоит ей пренебрегать. Следует честно признаться себе в том, что любые поблажки и послабления обычно ведут к другим и еще большим, и в итоге ухудшают приверженность уже критично, к тому же, если это происходит постепенно, то это случается еще и не очень заметно для человека. Все катастрофы – стечение обстоятельств, это относится и к потере вирусологической эффективности режимов АРВТ. Всегда есть некоторые риски наличия или возникновения третьих факторов, в том числе скрытых: полиморфизм системы цитохромов P450 или системы HLA, изменения в параметрах тропности вируса к ко-рецепторам и иной фитнес вируса, некачественный препарат по причинам хранения или брака на производстве, какие-то временные нарушения абсорбции препарата, изменения pH желудочной среды, неучтенные межлекарственные взаимодействия, влияние иных заболеваний… Максимально высокая приверженность достижима, а значит, один фактор всегда в наших, и только в наших руках.
- Lewis JM, Volny-Anne A, Waitt C, Boffito M, Khoo S. Dosing antiretroviral medication when crossing time zones: a review. AIDS. 2016 Jan;30(2):267-71. PMID: 26684823.
- Margolis AM, Heverling H, Pham PA, Stolbach A. A review of the toxicity of HIV medications. J Med Toxicol. 2014 Mar;10(1):26-39. PMID: 23963694.
- Elliot E, Amara A, Jackson A. и др. Dolutegravir and elvitegravir plasma concentrations following cessation of drug intake. J Antimicrob Chemother. 2016 Apr;71(4):1031-6. PMID: 26679246.
- Boffito M, Jackson A, Amara A. и др. Pharmacokinetics of once-daily darunavir-ritonavir and atazanavir-ritonavir over 72 hours following drug cessation. Antimicrob Agents Chemother. 2011 Sep;55(9):4218-23. PMID: 21709075.
- Jackson A, Moyle G, Watson V. и др. Tenofovir, emtricitabine intracellular and plasma, and efavirenz plasma concentration decay following drug intake cessation: implications for HIV treatment and prevention. J Acquir Immune Defic Syndr. 2013 Mar 1;62(3):275-81. PMID: 23274933.
- Dickinson L, Yapa HM, Jackson A. и др. Plasma Tenofovir, Emtricitabine, and Rilpivirine and Intracellular Tenofovir Diphosphate and Emtricitabine Triphosphate Pharmacokinetics following Drug Intake Cessation. 2015 Oct;59(10):6080-6. PMID: 26195515.
- Hermankova M, Ray SC, Ruff C. и др. HIV-1 drug resistance profiles in children and adults with viral load of
Читайте также:


