Первичный инфекционный токсикоз у детей
Острый инфекционный токсикоз — общая реакция организма на вирусную и микробную инфекцию, которая характеризуется рядом функциональных и органических нарушений со стороны центральной нервной системы, органов кровообращения, дыхания, расстройством метаболизма и водно-солевого гомеостаза.
Причина возникновения токсикоза пока до конца не изучена. Предположение о сенсибилизации организма в результате повторных инфекций, ранее высказанное отечественными педиатрами для объяснения гиперергической реакции, в настоящее время получило дальнейшее развитие. Повторная инфекция стимулирует массивную продукцию иммуноглобулинов класса М и образование атипичных комплексов антиген — антитело, которые активируют главным образом 3-ю и 5-ю фракции комплемента, а также свертывающую систему крови. Аналогичным эффектом обладает эндотоксин, действие которого может наслаиваться в случае вторичной бактериальной инфекции. Преимущественная активация комплемента (Сз) способствует высвобождению анафилотоксинов, гистамина, повышению сосудистой и клеточной проницаемости (Д. Александер, Р. Гуд, 1974). Повышенная коагуляция приводит к распространенному микротромбозу, нарушению капиллярной проходимости, в крайних вариантах — к геморрагиям и некрозу (коагулопатия потребления).

Отеку и набуханию мозга большое значение придается в генезе поражения ЦНС (А. В. Чебуркин, Р. В. Громова, 1962). Причиной отека является нарушение внутри- и внеклеточного баланса основных электролитов натрия и калия на фоне повышенной проницаемости клеточных мембран; клетка теряет калий, внутриклеточное осмотическое давление повышается за счет натрия, возникает состояние клеточной гипергидратации (Ю. Е. Вельтищев, 1967; В. И. Кулик, 1947). Следует подчеркнуть, что гипертермия, судороги, менингизм не всегда связаны с отеком-набуханием мозга. Первичная энцефалопатия врожденного и приобретенного характера, гипокальциемия, гипо- магнезиемия, гиповитаминоз, а также различные энзимопатии в сочетании с инфекционным заболеванием могут служить причиной судорог без выраженного отека мозга.
Практическое значение имеет учет фазы инфекционного токсикоза; фаза гиперергии и повышенного катаболизма сменяется фазой функциональной депрессии с глубоким нарушением клеточного метаболизма. Таким образом, чрезмерная активность приводит к истощению функции клетки и в конце концов к ее гибели. Фазность процесса подтверждается клиническими признаками преобладания симпатического отдела нервной системы в начале токсикоза, а в дальнейшем — нарастанием коматозного состояния, шока, гипотермии, симптомами гипоксии и ацидоза.
Клиника. В типичных случаях токсикоз развивается внезапно у внешне здорового ребенка или чаще на 2—
3- и сутки от начала острой респираторной инфекции. Ухудшение состояния прогрессирует параллельно скорости повышения температуры до 4(ГС; нарастает возбуждение, беспокойство, тремор рук, выбухание и напряжение родничка, ригидность затылочных мышц, в тяжелых случаях —клонико-тонические судороги. Со стороны сердечно-сосудистой системы отмечается тахикардия, повышение артериального давления, напряженный частый пульс; границы относительной сердечной тупости определить трудно из-за эмфиземы легких, тоны сердца вначале отчетливы, II тон акцентирован (гипертония малого круга кровообращения), на ЭКГ отмечается синусовая тахикардия. Дыхание учащено, перкуторно определяется коробочный оттенок звука, аускультативно — жестковатое дыхание, сухие хрипы; цианоз незначительный. Указанная клиническая картина соответствует первой (ирри- тативной) фазе токсикоза.
Если состояние больного продолжает ухудшаться, возбуждение сменяется угнетением, то появляются признаки сопорозного и коматозного состояния (вторая фаза токсикоза). Развивается шоковое состояние, кожные покровы приобретают серо-бледный оттенок, артериальное давление снижается, тоны сердца глухие, пульс нитевидный, тахикардия сменяется брадикардией — прогностически неблагоприятный признак. Нарастает парез кишечника, может быть рвота цвета кофейной гущи, парез сфинктеров, жидкий стул. В легких картина отека, пена у рта; дыхание поверхностное, периодическое, усиливается цианоз. Судороги тонического характера, длительные, указывают на поражение ствола мозга.
Инфекционный токсикоз может развиться на фоне четко выраженного воспалительного процесса с гнойнодеструктивными изменениями; эффективность лечения токсикоза в таких случаях зависит от состояния воспалительного очага и этиотропной терапии.
Для проведения направленного неотложного лечения необходимо выделить в каждом случае заболевания доминирующий синдром: гипертермический, синдром недостаточности периферического кровообращения, кардиальный (гипермотильный), легочный (гипервентиляцион- ный), синдром преимущественного поражения органа (энцефалитический, Уотерхауса — Фридериксена, кишечный и Др.). Вариантом острого инфекционного токсикоза можно считать также геморрагический синдром (клинический эквивалент феномена Сенарелли — Швартцманна) и картину внезапной или неожиданной смерти — мало изученный исход инфекционно-токсического стресса, который чаще возникает у детей с лифма- тическим диатезом.
Лечение острого инфекционного токсикоза в основном патогенетическое. Возможности этиотропной терапии ограничены, так как бурно развивающийся патологический процесс зависит не столько от особенностей возбудителя, сколько от вторичных иммунопатологических и нервнорефлекторных реакций на его внедрение. В то же время опасность активизации бактериальной флоры у ребенка, который находится в состоянии тяжелого токсикоза, возможность развития пневмонии и других очагов воспаления являются показанием к применению антибиотиков широкого спектра действия. Целесообразно использовать не менее двух видов антибиотиков, один из них назначают внутривенно. Последнее время широко применяются полусинтетические пенициллины или обычный пенициллин в дозах 250 000—300 000 ЕД/кг в комбинации с ампициллином, гентамицином, цепорином, сукцинатом левомицетина, с учетом общих правил и схемы, позволяющей комбинировать различные антибиотики.
Патогенетическая терапия нейротоксикоза направлена на устранение адренергических эффектов и неадекватной реакции нервной системы (возбуждения, тахикардии, усиленного катаболизма, гипертермии), уменьшение отека-набухания мозга и повышенного внутричерепного давления, устранение тромбообразования и улучшение микроциркуляции, устранение дыхательной недостаточности и недостаточности кровообращения.
Во второй фазе токсикоза большое значение имеет коррекция надпочечниковой недостаточности и борьба с нарастающим коматозным состоянием.
Основной принцип лечения нейротоксикоза предусматривает уменьшение неадекватно высокой реактивности, которая ведет к необратимым изменениям метаболизма. В связи с этим большинство препаратов, применяемых при нейротоксикозе, обладают седативным действием, т. е. являются нарколептиками. Препараты, возбуждающие ЦНС, и стимуляторы (аналептики)—кофеин, камфора, кордиамин, лобелии, цититон противопоказаны и лишь некоторые из них (норадреналин) применяют с осторожностью только в случае прогрессирующего шока, коматозного состояния и депрессии дыхания, т. е. во второй фазе токсикоза.
Важная роль в лечении первой фазы нейротоксикоза отводится нейроплегическим препаратам (транквилизаторам). Широко используют аминазин и дипразин.
Применяют комбинацию нейроплегических препаратов, логическую смесь, которую дополняют промедолом для усиления противоболевого и седативного эффекта. Смесь в составе аминазина (с. 123), дипразина (с. 130) и промедола (с. 118) вводят в одном шприце внутривенно или внутримышечно. Полную разовую дозу смеси вводят в первую фазу токсикоза, т. е. в том случае, если нет нарушения периферического кровообращения. Интервалы введения нейроплегических препаратов определяют в зависимости от состояния больного: если после первого введения прекратились судороги, снизилась температура, уменьшилась частота дыхания, тахикардия и ребенок спокоен, то повторные дозы вводят с интервалом в 4—
6 ч. Если эффект от первого введения недостаточен, разовую дозу можно повторить через 30—40 мин.
При одновременном применении других нейролептических препаратов следует учитывать эффект взаимного потенцирования с возможным последующим нежелательным угнетением центральной нервной системы и депрессией дыхания. В связи с этим разовые дозы препаратов, используемых в комбинации, уменьшают на ‘/з или на V2 и вводят дробно в соответствии с динамикой клинической картины и характером дыхания. К препаратам, обладающим выраженным наркотическим и противосудорожным действием, относятся хлоралгидрат, гексенал, оксибути- рат натрия, дроперидол, диазепам.
При наличии симптомов шока и обезвоживания первоначально проводят мероприятия, направленные на выведение из шока (20 мл/кг коллоидных растворов внутривенно до восстановления диуреза), продолжают регидра- тационную терапию преимущественно гипертоническими глюкозо-солевыми растворами (20% глюкоза с солевыми растворами в соотношении 2:1), из расчета не менее 3 U суточной потребности жидкости в течение 24 часов.
Обязательным компонентом патогенетической терапии является устранение тканевого отека, который достигается применением дегидратационного метода. Момент начала дегидратационной терапии зависит от функции почек. Если функция почек сохранена, дегидратационную терапию проводят одновременно с регидратацией. При отсутствии функции почек дегидратационную терапию начинают только после восстановления диуреза.
При назначении осмотических диуретиков наступает перераспределение жидкости из клетки и интерстиция в сосудистое русло и уменьшается внутричерепное давление. В результате улучшения оксигенации клеток восстанавливается функция. Наиболее быстрый эффект наблюдается от осмодиуретиков: мочевины, маннитола. Сали- уретики (в том числе фуросемид) более инертны. В детской практике чаще используют малотоксичный манни- тол (с. 106).
Активная дегидратационная терапия создает опасность эксикоза со всеми вытекающими отсюда последствиями (ангидремический шок), поэтому наряду с дегидратацией продолжают регидратационную терапию. Оптимальное соотношение противоположных методов лечения определяется на основании клинической картины и лабораторных показателей (гематокрит, уровень электролитов). Необходимость в применении солевых растворов возникает после восстановления диуреза. Иногда, несмотря на эксикоз, приходится лимитировать введение жидкости в связи с возможным усилением клеточного отека. О таком осложнении свидетельствует реакция на капельное введение жидкости — появляется беспокойство, повышается температура и отмечаются судороги. В то же время указанные симптомы могут быть следствием нарастающей ангидремии. До настоящего времени отсутствуют надежные критерии оптимального соотношения дегидратационной и регидратационной терапии, поэтому главным ориентиром остается непрерывная клиническая и лабораторная оценка состояния ребенка после установления капельницы.
Современные представления о внутрисосудистом диссеминированном свертывании и нарушении микроциркуляции являются основанием для включения в комплекс патогенетической терапии нейротоксикоза препаратов, уменьшающих тромбообразование и улучшающих реологические свойства крови. С этой целью в последние годы широко используют гепарин.
Гепарин применяют в дозе 100—200 ЕД/кг в сутки ка- пельно внутривенно. Треть указанной дозы вводят медленно одномоментно с 10 мл изотонического раствора хлорида натрия. С целью контроля за состоянием свертывающей системы крови во время лечения можно ограничиться характеристикой тромбинового времени, тромбо- эластограммы и времени свертывания; под влиянием введения гепарина допускается повышение тромбинового времени в 2—3 раза по сравнению с нормой. Раннее применение гепарина дает убедительный эффект.
В далеко зашедших стадиях шока при наличии тяжелых нарушений микроциркуляции и геморрагиях показано применение фибринолитических препаратов (стрепта- зы, стрептокиназы) под контролем коагулограммы.
Для улучшения циркуляции в мелких сосудах и капиллярах, дезагрегации форменных элементов крови рекомендуется применять низкомолекулярные плазмозаме- нители (реополиглюкин).
Во вторую фазу нейротоксикоза прогрессирует циркуляторная недостаточность, гипоксия и ацидоз. В клинической картине нарастает адинамия, серовато-цианотичный оттенок кожных покровов, появляются признаки периодического дыхания. Вначале централизация кровообращения не сопровождается значительным снижением артериального давления, в дальнейшем артериальное давление снижается, пульс становится нитевидным, нарастает парез кишечника, увеличивается в размере печень, могут появиться отеки.
При нейротоксикозе показано применение гормональных препаратов (преднизолон, триамцинолон и др.).
Метаболический ацидоз при нейротоксикозе как следствие циркуляторной гипоксии в первую фазу компенсируется гипервентиляцией. При наличии декомпенсирован- ного метаболического ацидоза вводят 4% раствор гидрокарбоната натрия и препараты, улучшающие периферический кровоток. Перечисленную патогенетическую терапию дополняют методами, направленными на устранение синдромов поражения отдельных органов (кардиального, легочного, желудочно-кишечного и др.).
Обязательным условием успешной терапии нейротоксикоза является тщательное наблюдение за ребенком. Нельзя допускать рецидива токсикоза. Дозы препаратов варьируют в зависимости от состояния больного и эффективности первых введений. Для устранения ангидремии и циркуляторной недостаточности вводят оптимальное количество жидкости. Длительное возбуждение и беспокойство ребенка недопустимы. Нейролептики применяют для устранения судорог, несмотря на признаки депрессии дыхания. Гипоксическая депрессия дыхания вследствие прогрессирующего судорожного синдрома более опасна, чем медикаментозная. Борьба с чрезмерной тахикардией при доминирующем кардиальном синдроме оправдывает незначительные явления передозировки дигоксина, которые могут быть быстро устранены.
Показания для госпитализации в реанимационное отделение. Число детей с нейротоксикозом резко возрастает в период эпидемических вспышек вирусной инфекции. Степень тяжести и длительность манифестации токсического синдрома весьма вариабельна. После интенсивной терапии, которую можно провести в любой больнице, состояние большинства детей быстро улучшается и лишь немногие из них нуждаются в проведении реанимационных мероприятий. При отсутствии эффекта педиатру приходится решать вопрос о необходимости помещения ребенка в реанимационное отделение или о вызове реанимационной бригады. Решение этого вопроса должно быть квалифицированным и стремление педиатра перепоручить реаниматологу каждого ребенка с токсикозом или, наоборот, чрезмерная уверенность в своих силах ведут к нежелательным результатам. В первом случае теряется время на вызов реаниматолога и транспортировку больного, в то время как интенсивную терапию можно провести на месте, во втором — можно опоздать с проведением реанимационных мероприятий.
При нейротоксикозе наиболее частым показанием для проведения реанимационных мероприятий является прогрессирующая-депрессия внешнего дыхания. Важно быстро разобраться в характере нарушения дыхания.
В первую фазу токсикоза дыхание, как правило, учащается (до 80—100 дыханий в минуту) параллельно нарастанию температуры; в спокойном состоянии дыхание ритмичное, поверхностное с редкими и непродолжительными остановками.
Во время приступа клонико-тонических судорог дыхание задержано, изредка наблюдаются короткие шумные вздохи, напоминающие икоту. Настораживает в первую фазу токсикоза появление периодического дыхания Чейна — Стокса, которое состоит из периодов нарастающих и убывающих дыхательных движений, отделенных друг от друга паузами. Обнаружить периодическое дыхание в первую фазу токсикоза удается только после довольно длительного наблюдения. Применение нейролептиков [аминазин, дипразин, оксибутират натрия (ГОМК), дро- перидол], антигистаминных препаратов и анальгетиков в сочетании с активным охлаждением способствует уреже- нию и нормализации дыхания, которое становится более глубоким и эффективным. Периодическое дыхание Чейна — Стокса в первой фазе токсикоза у большинства больных устраняется путем проведения указанной выше терапии и не требует реанимационных мероприятий.
Поверхностное частое дыхание, прерываемое отдельными вдохами с компенсаторной паузой (апноэ), требует быть осторожным в применении нейролептиков (медикаментозная депрессия дыхания), но еще не дает повода к немедленному вызову реаниматолога.
Выраженное дыхание Чейна — Стокса с длительными паузами возникает во второй фазе нейротоксикоза. Наряду с периодическим дыханием постепенно нарастают периоды замедленных сердцебиений (до 90—100 в минуту), наиболее выраженные на высоте клонико-тонических судорог. Нейролептики в таком состоянии ребенка применять нельзя, его переводят в реанимационное отделение для проведения аппаратного искусственного дыхания и устранения судорожного синдрома.
Безусловным показанием к проведению немедленного искусственного дыхания является гаспинг — судорожное дыхание, которое возникает в предагональном периоде. Редкие и быстрые дыхательные движения с открыванием рта и запрокидыванием головы выступают как следствие аноксического поражения центров ритмического дыхания; гаспинг часто развивается вслед за периодическим дыханием Чейна — Стокса или Биота.
Показанием к переводу ребенка в реанимационное отделение является также выраженная брадикардия, аритмия и нарастающие признаки недостаточности кровообращения.
Немедленного привлечения реанимационной службы требуют редкие случаи выраженного геморрагического синдрома (коагулопатии потребления). Исключительно сложное лечение (переливание крови, применение гепарина и фибринолитических средств, аппаратное дыхание, гемодиализ) проводят одновременно и под непрерывным лабораторным контролем, что, естественно, возможно только в специализированном медицинском учреждении.
У ребенка с установленным диагнозом острой пневмонии важно выявить наличие или отсутствие признаков инфекционного токсикоза и оценить степень его тяжести.
Диагностика токсикоза, как неспецифической системной реакции организма на внедрение инфекционного возбудителя, включает комплексную оценку: тяжести поражения ЦНС (нейротоксикоз); выраженности гемодинамических нарушений; степени дыхательной недостаточности; гемокоагуляционных нарушений - фазы ДВС-синдрома.
Выделяют три степени тяжести токсикоза при пневмонии.
Со стороны ЦНС - снижение эмоционального тонуса, мышечная гипотония, у части детей двигательное возбуждение и гиперестезия. Температура тела от субфебрильной до фебрильной. Кожные покровы бледные с мраморным рисунком или гиперемированы, периоральный цианоз. Проявления дыхательной недостаточности I степени — учащенное дыхание и тахикардия при физической нагрузке. Гемокоагуляционные нарушения характеризуются гиперкоагуляцией - I фаза ДВС-синдрома.
При токсикозе III степени состояние ребенка крайней степени тяжести. Сознание нарушено от сопора до комы, резкая мышечная гипотония, возможны судороги, гипотермия. Кожные покровы серые, мраморный рисунок, разлитой цианоз, геморрагическая сыпь. Симптомы дыхательной недостаточности III степени с брадипное, патологическими типами дыхания. Со стороны сердца - брадиаритмия, глухость тонов, застойные явления в малом круге кровообращения (увеличение количества влажных мелкопузырчатых хрипов в легких, акцент II тона над легочной артерией), гепатоспленомегалия, нарастание периферических отеков, низкое АД, олигоанурия. Парез кишечника. Выражен геморрагический синдром - III фаза ДВС-синдрома (коагулопатия потребления).
У детей с токсической формой пневмонии возможно развитие такого грозного осложнения, как респираторный дистресс-синдром по взрослому типу (РДСВ) - тяжелая форма острой дыхательной недостаточности с характерными изменениями в легких в виде диффузной инфильтрации и интерстициального отека, протекающая с выраженной гипоксемией, рефрактерной к оксигенотерапии, проявлениями полиорганной недостаточности с неврологическими расстройствами, недостаточностью периферического кровообращения, геморрагическим синдромом и с нарушением азотовыделительной функции почек. На развитие РДСВ указывает резистентность проявлений дыхательной недостаточности к традиционной оксигенотерапии со снижением РаО2 менее 60 мм рт. ст. и коэффициента оксигенации (PaO2/FiO2) менее 120 мм рт. ст. При рентгенографии легких - диффузные легочные инфильтраты, признаки интерстициального отека.
Неотложная помощь
Принципы терапии при токсических формах пневмоний:
1. Срочная госпитализация в отделение интенсивного лечения или реанимационное.
2. Этиотропное лечение эмпирически на основе представлений о вероятном возбудителе (таблицы 11 и 12) после забора биологического материала - мокроты на микроскопию, крови на гемокультуру.
Клинические критерии правильного подбора антибиотиков:
• снижение температуры, уменьшение симптомов интоксикации, положительная динамика основных клинических симптомов в течение 48-72 часов;
• положительная динамика общего анализа крови (уменьшение нейтрофильного лейкоцитоза).
3. Инфузионная терапия с целью дезинтоксикации и восполнения ОЦК по следующим принципам:
• суточный объем не должен превышать 30-50 мл/кг;
• соотношение коллоиды/кристаллоиды 1:2; коллоиды - реополиглюкин, свежезамороженная плазма, 10% альбумин; кристаллоиды - 10% раствор глюкозы и 0,9% раствор натрия хлорида в соотношении: у детей в возрасте до 2 мес — 4:1, 3 мес-1 год - 3:1, 1-3 года - 2:1, старше 3 лет - 1:1;
• скорость инфузии 10-15 капель в мин;
• инфузии под контролем диуреза: при снижении объема мочи - 1% раствор лазикса в дозе 0,1-0,2 мл/кг (1-2 мг/кг) в/в струйно.
4. Коррекция острой дыхательной недостаточности:
• поддержание свободной проходимости дыхательных путей;
• оксигенотерапия увлажненным кислородом;
• с целью улучшения бронхиальной проходимости 2,4% эуфиллин в разовой дозе 4 мг/кг в/в капельно (до 3 раз в сутки);
• ингаляционная терапия с мукорегуляторами (лазолван, ацетилцистеин), с раствором эуфиллина, с физиологическим раство- ром натрия хлорида и др.;
• при дыхательной недостаточности III степени перевод на ИВЛ; при РДСВ показано применение специального режима вентиляции — положительного давления в конце выдоха.
5. Проведение симптоматической терапии:
a) при симптомах нейротоксикоза (злокачественная гипертермия, судороги) проведение нейровегетативной блокады препаратами:
• 0,5% раствор седуксена в дозе 0,05 мл/кг (0,3 мг/кг) в/м;
• 2,5% раствор пипольфена в дозе 0,1-0,15 мл/год жизни в/м;
• 0,25% раствор дроперидола в дозе 0,05-0,1 мл/кг в/м.
б) при недостаточности кровообращения:
• сердечные гликозиды ультракороткого действия 0,05% строфантин или 0,06% коргликон в разовой дозе у детей до года - 0,1 мл, прибавляя на каждый последующий год жизни по 0,05 мл (не превышая дозы 0,5 мл) в/в струйно медленно на 10% растворе глюкозы до 3 раз в сут;
• допамин в кардиотонической дозе 3-5 мкг/кг в мин в/в титрованно;
• реполяризующая смесь в/в капельно: 10% раствор глюкозы в дозе 10-15 мл/кг + инсулин из расчета 1 ЕД на 5 г глюкозы + калия хлорид в дозе 1-2 ммоль/кг (доза калия хлорида рассчитывается следующим образом: 1 мл 7,5% раствора содержит 1 ммоль калия, следовательно в 1 мл 4% раствора калия хлорида содержится 0,5 ммоль калия).
Противопоказанием для введения сердечных гликозидов и калийсодержащих растворов является брадикардия и олигоанурия!
в) с противовоспалительной целью в/в капельно ингибиторы протеолиза: контрикал в дозе 1000 ЕД/кг в сут или гордокс (трасилол) в дозе 5000 ЕД/кг в сут;
г) для профилактики ДВС-синдрома: гепарин 100 ЕД/кг в сут в/в струйно через 4-6 часов и дезагреганты (трентал 1-2 мг/кг в сут или курантил в дозе 2-5 мг/кг в сут);
д) при развитии ДВС-синдрома: в фазу гиперкоагуляции доза гепарина увеличивается до 200 ЕД/кг в сут; в фазу гипокоагуляции (коагулопатия потребления) дозу гепарина уменьшают до 50 ЕД/кг в сут и сочетают с трансфузиями свежезамороженной плазмы под контролем коагулограммы и клинических проявлений;
е) с заместительной целью по показаниям назначение преднизолона без учета суточного ритма в дозе 1 мг/кг в сут.
25. Врожденные пороки сердца. Пороки с лево-правым шунтированием (бледного типа). Дефект межжелудочковой перегородки (ДМЖП). Клинические проявления. Гемодинамические осложнения порока (синдром Эйзенменгера). Диагностика. Показания к кардиохирургической коррекции.

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.

Нейротоксикоз у детей – это патологическое состояние, которое возникает у ребенка раннего возраста при генерализации вирусных и/или бактериальных заболеваний и преимущественно проявляется нарушениями функций ЦНС. Клинически данное состояние характеризуется нарушением сознания ребенка, повышением температуры, гипертонусом мышц, увеличением ЧСС и ЧД. Диагностика нейротоксикоза у детей подразумевает сопоставление клинической картины, клинических анализов и результатов исследования ликвора. Лечение включает в себя этиотропные препараты, дезинтоксикацию и симптоматическую терапию, зависящую от клиники.
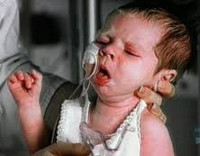
Общие сведения

Причины нейротоксикоза у детей
Нейротоксикоз у детей – это полиэтиологическое явление. Он может возникать на фоне большого количества заболеваний вирусного (ОРВИ, аденовирусная инфекция и т. д.) и бактериального (шигеллез, сальмонеллез, пищевая токсикоинфекция и др.) генеза или их сочетания. Также нейротоксикоз является первым симптом нейроинфекций (менингиты и энцефалиты).
Нейротоксикоз чаще всего развивается у детей раннего возраста благодаря их анатомо-физиологическим особенностям. Для ребенка характерен высокий уровень обмена веществ, который значительно выше такового у взрослых. Строение ЦНС и ее функционирование также отличается. У детей есть склонность к массивным воспалительным реакциям тканей головного мозга. Ткани гипоталамуса более чувствительные к гипоксии и поражаются быстрее, чем у взрослых. В возрасте до 3 лет ГЭБ функционально незрелый, из-за чего он пропускает токсины через себя. Это проявляется повышением внутричерепного давления и отеком головного мозга.
Патогенетически нейротоксикоз у детей обусловлен нарушением микроциркуляторного русла центральной и автономной нервной системы. Экзотоксины, которые выделяют бактерии в процессе жизнедеятельности, и эндотоксины, что попадают в кровь после их гибели, повреждают сосудистую стенку, повышают ее проницаемость для патогенных агентов и провоцируют гипоксию тканей. Вирусы вызывают аналогичный эффект, но другими путями. Они разрушают клетки организма, в результате чего в кровь попадают агрессивные протеолитические ферменты. Также вирусы способны самостоятельно вызывать деструкцию клеток эндотелия сосуда. Благодаря АФО ребенка такие изменения происходят диффузно по всей ЦНС. В развитии нейротоксикоза ведущую роль играет нарушение работы гипоталамуса, т. к. он является высшим вегетативным центром человека и отвечает за терморегуляцию, контролирует работу всех систем и эндокринных желез.
Классификация нейротоксикоза у детей
Различают 3 степени тяжести нейротоксикоза у детей:
Также нейротоксикоз у детей классифицируется согласно вариантам его протекания и ведущим симптомам:
Симптомы нейротоксикоза у детей
Нейротоксикоз у детей возникает остро, клинические проявления развиваются быстро. Токсическая энцефалопатия протекает в 3 периода: продромальный, развернутой клинической симптоматики и восстановления. Для каждого из них характерны свои симптомы.
Продромальный период кратковременный – от 2 до 6 часов. Проявляется ранними симптомами нарушения ЦНС: тошнота, рвота, которая не приносит облегчения и не зависит от приема пищи; нарастание головной боли; чрезмерное беспокойство и капризность; беспокойство, вздрагивания во время сна; сонливость днем; постепенное нарастание температуры тела до 38,5-39°С. Без медицинского вмешательства развивается нарушение сознания (от ступора до комы), дыхательной (повышение ЧД, одышка) и сердечно-сосудистой (повышение ЧСС) систем.
Развернутый нейротоксикоз у детей может иметь различные проявления, которые зависят от степени поражения ЦНС и микроциркуляторного русла. Длительность варьирует от 12 до 72 часов. При интенсивном нарушении кровообращения нейротоксикоз у детей развивается молниеносно. За несколько часов возникает декомпенсация работы сердечно-сосудистой системы, появляются геморрагии, развивается дыхательная недостаточность и отек легких. Нарушения ЦНС выражены в меньшей степени.
При непосредственном поражении ЦНС течение нейротоксикоза у детей более медленное. Нарастает интенсивность симптомов продромального периода, возникают судороги. Сознание ребенка нарушается постепенно – от сонливости до комы, продолжительность которой может составлять до 2 суток. Могут развиваться гипервентиляционный и гипертермический синдромы. Гипервентиляция проявляется увеличением ЧД до 80/мин. без структурных изменений легких или дыхательных путей. Гипертермия при нейротоксикозе достигает 40° С и не снимается обычными жаропонижающими средствами. Без экстренного медицинского вмешательства может возникнуть остановка сердца и дыхания, которые переходят в клиническую и биологическую смерть.
Период восстановления начинается после купирования острого состояния. Восстановление напрямую зависит от тяжести нейротоксикоза, адекватности и своевременности лечения. При легкой степени симптомы нарушения ЦНС исчезают за 12-24 часа. При тяжелых случаях неврологическая симптоматика может сохраняться на протяжении 2-4 суток.
Диагностика нейротоксикоза у детей
При подозрении на нейротоксикоз проводится дифференциальная диагностика с нейроинфекциями, которые сопровождаются синкопе и судорожным синдромом. Для этого выполняется спинномозговая пункция с исследованием ликвора.
Лечение нейротоксикоза у детей
Терапия нейротоксикоза у детей проводится исключительно в условиях реанимационного отделения. Если ребенок на момент развития патологии находится дома – его немедленно госпитализируют. На догоспитальном этапе проводится лечение жизнеугрожающих проявлений: судорожного синдрома и гипертермии.
Этиотропное лечение включает назначение антибиотиков широкого спектра действия, после получения результатов антибиотикограммы – противомикробных препаратов, к которым чувствительна высеянная микрофлора. Допускается использование иммуностимуляторов. При проведении дезинтоксикационной терапии используются 0,9% раствор NaCl, 5% глюкоза, раствор Рингера-лактат. Важно соблюдать небольшой объем и низкую скорость введения растворов, т. к. инфузионная терапия может спровоцировать отек головного мозга.
Прогноз
Прогноз при нейротокискозе зависит от степени тяжести и своевременности лечения. I и II степени при адекватном лечении имеют благоприятный прогноз. При тяжелой (III) степени прогноз для жизни при полноценной терапии благоприятный, для здоровья – сомнительный. При несвоевременном оказании квалифицированной помощи при I-II степени прогноз сомнительный, III степени – неблагоприятный. Без соответствующего лечения – неблагоприятный прогноз нейротоксикоза любой степени тяжести.
Профилактика
Профилактика нейротоксикоза у детей заключается в полноценном лечении основного заболевания по рекомендациям педиатра, соблюдении рациональной диеты и укреплении иммунитета. Лечение инфекционных заболеваний у детей с наличием неврологических нарушений в анамнезе должно проводиться под строгим наблюдением в условиях стационара.
Читайте также:


