Паразиты в крови и вич
Яйца кровяного сосальщика помешали ВИЧ заразить Т‑лимфоциты
Антигены, которые содержатся в яйцах шистосом, меняют работу иммунной системы, мешая ее клеткам связываться с частицами ВИЧ. Помимо этого она стимулирует рост Т-клеток, которые более устойчивы к вирусу иммунодефицита человека.
Шистосомы – это паразитические плоские черви, которые живут в крови и откладывают яйца в венах человека. Яйца шистосом умеют бороться с иммунной системой человека, выделяя вещества, которые изменяют иммунный ответ. Основные цели, против которой работают вещества яиц шистосом – дендритные клетки. Вещества, которые выделяют паразиты, связываются с рецепторами дендритных клеток, мешая им нормально работать.
Дендритные клетки нужны иммунной системе для того, чтобы познакомить с антигенами вторгшейся инфекции Т-клетки (Т-лимфоциты). После того, как дендритные клетки принесли в лимфоузлы антигены, активируются разные типы Т-клеток, которые непосредственно уничтожают угрозу для организма – самостоятельно, либо активируя B-клетки.
ВИЧ заражает именно Т-клетки. Он может делать это двумя путями – цисинфицировать или трансинфицировать их. При первом вирусные частицы непосредственно прикрепляются к мембране Т-клеток и проникают внутрь. При втором способе их приносят к Т-клеткам дендритные клетки, чтобы активировать их, как при любой другой инфекции. Но в случае с ВИЧ все идет не так – вирус переходит с поверхности дендритной клетки на лимфоцит и заражает его. Это значит, что можно помешать заражению Т-клеток, если запретить вирусу прикрепляться к их рецепторам. Именно это и делают вещества, которые выделяют яйца шистосом.
Эстер де Йонг (Esther C. de Jong) из Амстердамского университета, Уильям Пэкстон (William A. Paxton) из Ливерпульского университета и их коллеги решили проверить, могут ли шистосомы помешать дендритным клеткам захватывать ВИЧ и переносить его в лимфоузлы к наивным Т-клеткам. Они сделали из яиц паразитов препарат, который назвали SEA (soluble egg antigen), и стали тестировать его на рецепторах дендритных клеток, самих клетках, Т-лимфоцитах и ВИЧ.
Сначала ученые провели эксперимент с рецепторами дендритных клеток и вируса. Они выдерживали рецепторы в SEA, а затем в растворе вирусного белка. Оказалось, что SEA связывается с рецепторами дендритных клеток и оставляет мало места для вирусных рецепторов – обработка SEA снизила их связываемость с рецепторами дендритных клеток на 70 процентов.

Рецепторы дендритных клеток, связавшиеся с аналогом вирусного белка в присутствии SEA (здесь и ниже рисунки из статьи в PLOS Pathogens).
Затем ученые обработали SEA уже культуру дендритных клеток, а затем поместили к ней Т-лимфоциты и стали заражать их ВИЧ. Выяснилось, что в среде с обработанными дендритными клетками вирус развивается на 80 процентов меньше.
Исследователи выделили из SEA вещество омега-1, основной компонент паразитической смеси, и проверили его. В опыте с ним схему эксперимента немного изменили – теперь обработанные веществом сосальщика дендритные клетки находились в одной среде с наивными Т-клетками без присутствия вируса. Только после того, как Т-лимфоциты активировались в присутствии обработанных дендритных клеток, ученые перенесли их и попробовали заразить ВИЧ. Оказалось, что Т-лимфоциты, активированные обработанными дендритными клетками, заражаются ВИЧ на 60 процентов меньше. Ученые связывают это с тем, что под действием омега-1 активация Т-клеток происходит таким образом, что на их мембране уменьшается количество CCR5-рецепторов, которые необходимы вирусу для связывания с лимфоцитом.

Количество вирусного белка в культуре Т-клеток, зараженных ВИЧ. Т-клетки активированы в присутствии омега-1.
Кроме успехов в этом исследовании есть и неудачи. Так, оказалось, что защита паразита действует только против разновидности вируса, которая использует рецептор CCR5, чтобы проникнуть в клетку. ВИЧ, который пользуется рецептором CXCR4, не замечает никаких помех. Кроме того, исследование проводилось только на ВИЧ-1, а не обоих видах.
Авторы исследования считают, что результаты исследования стоит учесть при испытаниях вакцины против ВИЧ, если они будут проводиться в районах распространения шистосомоза. Кроме того, по мнению авторов, вакцины, разработанные на основе веществ, выделяемых гельминтами, могут помочь в борьбе с ВИЧ.
Иммуноферментный анализ на паразитов (сокращенно ИФА) — лабораторный иммунологический тест, который использует антитела и их способность менять цвет, может диагностировать широкий круг инфекционных заболеваний, вызванных паразитами, выяснить присутствие онкологических маркеров различного происхождения, определять наличие гормонов, пептидов и белков при диагностике репродуктивной способности человека. Сейчас большой популярностью пользуется анализ крови на лямблии. Такие диагностические исследования также используются в качестве аналитического инструмента в области биомедицинских исследований для выявления количественной оценки специфичных антигенов в лабораторном образце.
Иммуноферментный анализ и его использование
Метод ИФА не стоит путать со способом дуоденального зондирования и анализом кала, которые проводятся при помощи микроскопических мероприятий и ставят перед собой цель обнаружить глистные инвазии, микроскопических паразитов или их остатки, яйца и личинки в отобранном или сданном образце фекалии.
Анализ кала может диагностировать наличие гельминтов, паразитирующих не только в кишечнике, но и в печени, желчевыводящих путях, поджелудочной железе и двенадцатиперстной кишке. В данном случае правдивость теста прежде всего зависит от внимательности и квалификации сотрудников лаборатории, возможностей лабораторного оборудования.
Если вредитель не выполнил кладку яиц в период проведения теста и присутствует у человека в минимальном количестве, его наличие сложно определить, даже при особой внимательности лаборанта.
Диагностирование глистов способом соскоба на энтеробиоз считается более эффективным, так как признано достаточно информативным и безболезненным. Но, как и при исследовании фекалий, результаты анализа зависят от присутствия кладки гельминтов, поэтому этот вид исследования требует повторного взятия проб в сомнительных ситуациях.
В последние годы в арсенале лаборантов появился новый, более современный метод иммунологического исследования. Он позволяет по крови больного обнаружить присутствие антигенов и антител к паразитам разных типов. Точность тестов зависит от:
- типа паразита;
- его активности к размножению;
- концентрации в организме.
На чем основан иммуноферментный анализ?
Иммуноферментный анализ использует основы фундаментальной иммунологии и концепцию связывания антигена с его специфическими антителами. Он состоит из 2-х различных составляющих:
- иммунного ответа;
- ферментативной реакции.
Иммунный рефлекс может связывать биологические молекулы, части клетки и микроорганизмы, которые необходимо обнаружить в ходе проведения теста, а ферментативная реакция позволяет визуально оценить и измерить показатели этой реакции.
Другими словами, иммунная реакция является частью сложной методики, которая прямым образом может обнаружить искомый микроб в отобранном образце. А ферментативная реакция — частью, позволяющей перевести полученный результат в форму, которую можно оценить глазом и измерить при помощи доступной биохимической методики.
Что такое иммунная реакция, и как выяснить узнаваемость антигена?
Иммунная реакция — процесс связывания антигена с антителом. В результате реакции образуется иммунный комплекс. Антигены — сложные структуры, которые живут на поверхности клетки и несут в себе сведения о клетке. Антигены у людей индивидуальны, они схожи у различных людей, но всегда отличаются и не имеют копий.

Узнаваемость антигена основана на свойстве клетки распознавать свои и чужеродные клетки ИС. Когда иммунная клетка соединяется с опасной, образуется чужеродная клетка. На поверхности чужеродной клетки образуется антиген, не совпадающий с тем, который присутствовал в памяти здоровой клетки. Когда клетка обнаруживает чужой антиген, она запускает процесс уничтожения подозрительного объекта. Точность иммунологического распознания составляет в среднем 99,97%.
Антитело: какое это вещество, его виды
Антитело — динамичная молекула, которая располагается на теле иммунной клетки. Антитело может соединяться с антигенами опасной клетки и передавать сведения в тело клетки для распознавания своей и чужой клетки. При обнаружении своей клетки антитело убивает связь с антигеном и высвобождает клетку.
В природе выявлено пять классов антител, именуемых также белковыми структурами или иммуноглобулинами. Все типы антител имеют способность связываться с различными антигенами в различных частях организма. Антитела именуются знаками латинского алфавита — A, M, G, D и E и в анализах тестов обозначаются следующими буквенными символами: IgA, IgM, IgG, IgD и IgE.
Как проводится тест ИФА?
Иммуноферментный анализ крови на паразитов проводится путем сдачи венозной крови из локтевой вены в сухую стерильную пробирку. Для получения достоверной информации тестов из вены отбирается от 3 до 5 мл образца. У новорожденных младенцев анализ крови на глисты и лямблии рекомендуется проводить из сохранившейся плаценты или пуповинной вены и отбирать пуповинную кровь.
Перед сдачей крови пациентам рекомендуется воздержание от принятия еды на срок 8 часов, исключить из употребления алкоголь, газированные напитки, прием лекарственных и антибактериальных препаратов.
Расшифровка и описание результатов ИФА
При иммуноферментном анализе крови на гельминты, лямблии, глисты и другие паразиты расшифровка результатов устанавливает наличие в организме различных видов антител (иммуноглобулинов) и антигенов — паразитов и продуктов их жизнедеятельности.
Расшифровка при иммуноферментном анализе крови может быть представлена в табличном виде и внутри себя содержать следующие стандартизованные значения классов антител:
- JgM (-), JgG (-), JgA (-) — отрицательный результат иммунитета к инфекции;
- JgM (-), JgG (+), JgA (-) — присутствие поствакционного (постинфекционного) иммунитета;
- JgM (+), JgG (-/+), JgA (-/+) — диагностирование острой инфекции;
- JgM (+), JgG (+), JgA (+) — диагностирование обострения хронической инфекции;
- JgM (-), JgG (+/-), JgA (+/-) — присутствие хронической инфекции;
- JgM (-) — полное выздоровление.
В иммуноферментном анализе крови в расшифровке знак (+) обозначает положительный результат, а знак (-) — отрицательное значение.
Кроме уточнения классов антител иммуноферментный анализ крови в расшифровке может иметь количественные, цифровые целые или дробные показатели антител. Обширное объяснение значений больному может по требованию предоставить только лечащий врач.
Многократное проведение тестов и исследование наличия и концентрации антител различных классов в некоторых случаях позволяет врачу выяснить стадии инфекционного процесса: начальную, активную, хроническую или запущенную.
Анализ крови или анализ кала на лямблии: что лучше?
Сдачу кала на лямблии до сих пор часто назначают врачи в педиатрической практике детям и взрослым в качестве эффективной диагностики лямблиоза.
Сущность метода достаточно проста: пациент сдает анализ кала в лабораторию. В образце кала при помощи микроскопа лаборант обнаруживает или не обнаруживает цисты лямблий или других паразитирующих микроорганизмов. При обнаружении цист лямблии или инвазий глистов и других паразитирующих организмов лаборант выдает положительный результат и сообщает о тяжести протекания заболевания.
Положительный тест в этом случае ложным не бывает, а вот ложно-отрицательный встречается достаточно часто, так как цисты могут быть не замечены в ходе микроскопического теста.
Помимо анализа кала, лямблии может выявлять анализ крови на паразитов, считающийся более чувствительным. Такой анализ крови позволяет вести поиск не самих паразитов в отобранном материале, а обнаружить присутствие антител и антигенов, которые появились в результате паразитирующей деятельности паразитов.
Положительный результат теста свидетельствует о присутствии паразитов в организме или же сообщать о только что перенесенном инфицировании.
Какой из анализов лучше: иммуноферментный или дуоденальный? На данный вопрос однозначного ответа нет. Лучшим считается тот анализ, который дает положительный результат, а именно обнаруживает присутствие инфекции в организме.
Многие врачи считают лучшим иммуноферментный анализ крови, так как он является более современным и чувствительным. Другие считают этот метод слишком дорогостоящим и бесполезным и отдают предпочтение дуоденальному анализу, основанному на исследовании кала при помощи микроскопа.
Среди множества глистных инвазий (более 300 видов) одной из самых неприятных являются паразиты в крови человека. При этом симптоматика патологии настолько разнообразна, что человек может годами лечить несуществующую болезнь, а врага так и не распознать в лицо. В том, какие виды гельминтов могут жить и размножаться в крови человека, а также какова клиническая картина патологий, разбираемся ниже.
Разновидности паразитов в крови
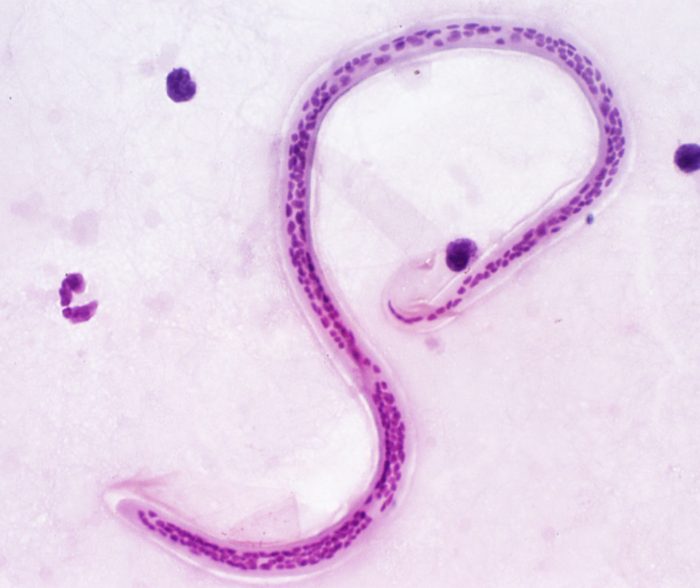
У человека можно выявить несколько видов паразитов в крови. При этом каждый из них несет в себе потенциальный вред для организма. Так, человек может быть биологическим носителем таких гельминтов:
Помимо приведенных видов гельминтов существуют и такие, которые паразитируют в кишечнике, но в определенный цикл своей жизнедеятельности попадают в кровоток, нарушая его. К таким глистам относят:
- Амеба. В основном крепится к стенкам кишечника и питается кровяными клетками.
- Широкий лентец. При попадании в кровь серьезно нарушает кровоток.
- Шистосома. Способна закупоривать просвет сосудов, попадая в кровоток.
- Анкилостома. Не просто циркулирует с кровью по организму, но и выбрасывает в кровь вещество, снижающее ее свертываемость. В результате у человека обнаруживается дефицит белков.
- Эхинококк. Провоцирует малокровие, питаясь кровью человека.
Способы заражения и симптомы

Появление паразитов в крови человека симптомы провоцирует самые разные. Но при этом стоит знать, что инфицирование происходит такими путями:
- Укусы зараженных глистной инвазией животных;
- Укусы кровососущих насекомых;
- Проникновение паразитов через поврежденный эпидермис у человека;
- Переливание зараженной донорской крови;
- Через грязные руки, овощи, фрукты и мясные продукты питания.
При поражении крови глистной инфекцией у пациента формируются такие симптомы:
- Аллергические высыпания на коже ввиду снижения иммунитета и отравления организма продуктами жизнедеятельности гельминтов;
- Болезненность в мышцах и суставах из-за токсинов;
- Малокровие и анемия;
- Расстройства нервной системы и как следствие головокружения, галлюцинации, нервозы, расстройства сна;
- Частые простудные заболевания;
- Болезненность в области сердца, печени, живота;
- Потеря массы тела без других видимых причин;
- Выпадение волос и ломкость ногтей, бледность кожных покровов.
Диагностика глистов в крови человека
Чтобы выявить паразитирующих в крови пациента особей, необходимо использовать один или несколько современных методов диагностики. Таковыми являются:
- Иммуноферментный анализ крови (ИФА). Позволяет выявить паразитов методом реакции антител на антигены в крови. Не является методом определения вида паразитов в организме человека, а лишь позволяет подтвердить предполагаемый лечащим врачом диагноз.
- Серологический анализ крови и кала пациента. Позволяет выявить яйца гельминтов на этапе их размножения. Является информативным лишь на 30%, поскольку биоматериал может быть забран в период отсутствия кладки яиц паразитом.
- Гемосканирование. Анализ, который позволяет оценить состояние эритроцитов и определить их подвижность. Также при данной методике диагностики удается выявить наличие склеенных эритроцитов, что является подтверждением наличия в крови глистов.
Важно: периодическое обследование рекомендуется проходить пациентам из потенциально эндемических районов и лицам, работающим в потенциально опасных условиях (ловля и разделка рыбы, разделка мяса, работа в водоемах и пр.).
Помимо перечисленных методов диагностики лечащий врач обязательно учитывает историю болезни пациента и берет во внимание все условия, которые могли привести к потенциальному заражению глистной инвазией (отдых в Африке и Азии, сыроедение, работа в потенциально опасных условиях).
Лечение глистов в человеческой крови

Чтобы полностью избавиться от паразитов в крови, необходимо пройти сложное многоэтапное лечение противогельминтными препаратами. При этом эффективность терапии зависит как от правильности поставленного диагноза, так и от соблюдения всех предписаний лечащего врача. Принцип действия всех современных препаратов заключается в обездвиживании особей паразита и в их последующем выведении из кровотока. Стоит знать, что оценивать симптомы и лечение назначать может только специалист. При этом дозировку приема препаратов также должен подбирать лечащий врач-паразитолог или инфекционист. Использовать для лечения глистной инвазии в крови можно такие препараты:
- Пиперазин и Вормил;
- Азинокс и Гельминтокс;
- Немозол и Фенасал.
Важно: стоит знать, что большинство противогельминтных препаратов являются токсичными, а поэтому противопоказаны беременным, женщинам в период лактации, пациентам с недостаточностью печени и почек.
На протяжении всей терапии стоит придерживаться специальной диеты, исключающей углеводы (в том числе и простые), мясо и рыбу, алкоголь в любом виде. Пища должна быть максимально простой и легкоусвояемой.
Профилактика
Чтобы избежать глистной инвазии, необходимо соблюдать элементарные правила личной гигиены, которые и будут являться профилактическими мерами заражения. Таковыми правилами являются:
- Тщательное мытье рук после каждого посещения туалета, контакта с животными, работы с мясом и рыбой, а также после работы в саду и огороде.
- Тщательное мытье овощей, фруктов и зелени перед употреблением.
- Борьба с насекомыми в доме (мухи, клопы, тараканы, комары и пр.).
- Своевременная и регулярная обработка домашних животных противогельминтными препаратами.
- Купание только в специальных водоемах, предназначенных для отдыха населения.
- Употребление в пищу качественной чистой воды (кипяченой или специально очищенной).
Соблюдение таких простых правил позволит застраховать свое здоровье и жизнь от серьезных проблем, которые могут спровоцировать паразиты. Помните, ваше здоровье только в ваших руках.
Другие инфекционные и паразитарные болезни при ВИЧ
Другие инфекционные и паразитарные болезни при ВИЧ
1. Криптоспоридиоз — кишечная протозойная инфекция, вызываемая внутриклеточным паразитом Cryptosporidium. Установлено, что сывороточные антитела существенной роли в процессе очищения при этой инфекции не играют, тогда как при поражении Т-клеток формируется затяжное течение. Вероятно, именно этот фактор имеет значение в развитии упорной диареи у ВИЧ-инфицированных, а сочетание развивающегося синдрома малабсорбции с повышенной секрецией жидкости и электролитов в просвет кишечника сопровождается значительной потерей массы тела больным.
2. Изоспороз — протозойное заболевание, вызываемое простейшими Isospora belli и Isospora natalensis.
3. Токсоплазмоз — протозойное зоонозное заболевание, вызываемое паразитом Toxoplasma gondii. При СПИДе на фоне выраженного иммунодефицита наступает активация токсоплазм, находящихся в клетках мозга. Кроме того, токсоплазмы получают возможность более активно распространяться по организму, в том числе и проникать в ЦНС.
Клиническая картина
1. Криптоспоридиоз.
О СПИДе можно говорить лишь при криптоспоридиозной диарее, продолжающейся 1 месяц и более, так как такой процесс уже не способен к самолимитированию. Диарея (постоянная или перемежающаяся) у больных СПИДом может продолжаться месяцы и даже годы, она сопровождается лихорадкой, болью в животе (иногда резкой), на этом фоне истощение может достигать критических степеней. У больных СПИДом диарея может сочетаться с катаральным синдромом, обусловленным размножением криптоспоридий в эпителии дыхательных путей. При аускультации легких в этих случаях выслушиваются рассеянные сухие и влажные хрипы, а рентгенография позволяет выявить данные, характерные для бронхита или пневмонии.
2. Изоспороз.
Размножение изоспор в эпителиальных клетках кишечника приводит к его повреждению, нарушению процессов всасывания жидкости и питательных веществ из просвета кишечника — развивается диарейный синдром, сопровождающийся схваткообразной болью в животе. Стул частый, водянистый, температура чаще субфебрильная. Процесс в иммунокомпетентном организме обычно протекает благоприятно, все явления стихают не позднее чем через 7 — 10 дней даже без лечения. У многих инфицированных диарейный синдром не развивается вообще, хотя изоспоры обнаруживаются в фекалиях. Однако у лиц с иммунодефицитом, в том числе и больных СПИДом, изоспороз приобретает затяжное течение — диарея может длиться месяцы, сопровождаясь малабсорбцией, приводя к истощению больного. Изоспороз с диареей более 1 месяца — индикатор СПИДа. Более того, при тяжелом длительном течении изоспороза возможна диссеминация изоспор.
3. Токсоплазмоз.
Размножение токсоплазм в ЦНС сопровождается развитием очаговых или диффузных поражений. Токсоплазмоз головного мозга у больных старше 1 месяца — маркер СПИДа. Возрастные ограничения (1 месяц) введены потому, что тяжелые поражения ЦНС с развитием гидроцефалии, микроцефалии и другой патологии могут быть следствием внутриутробного инфицирования токсоплазмами плода без признаков иммунодефицита; такой врожденный токсоплазмоз отчетливо проявится в течение 1-го месяца жизни ребенка. Симптоматика при поражении токсоплазмами головного мозга бывает очень пестрой. При диффузном поражении больных беспокоят головная боль, слабость, прогрессирующее снижение работоспособности. Эти явления быстро нарастают, и уже через несколько недель, а иногда и раньше у больных возникают спутанность сознания, дезориентация в окружающем, сонливость или возбуждение, а в дальнейшем наступают потеря сознания, судороги, кома. При очаговых поражениях клинические проявления определяются локализацией процесса. Часто возникает гемипарез, он может быть нерезко выражен и не всегда привлекает внимание из-за наличия других, более ярких симптомов. У больных могут выявляться поражение черепных нервов, афазия, атаксия, тремор и т. д. При поражении токсоплазмами спинного мозга развивается поперечный миелит. Токсоплазмы могут приводить к образованию внутримозговых абсцессов. У некоторых больных выявляют обширные зоны деструкции ткани мозга. Изменения, возникающие в ткани мозга, необратимы. Поражение ЦНС токсоплазмами у больных СПИДом сопровождается лихорадкой, упорной головной болью. Заболевание при отсутствии лечения быстро прогрессирует и может быть непосредственной причиной смерти. На фоне диссеминации токсоплазм при СПИДе возможны токсоплазмозные поражения различных органов: сердца, легких, мужских и женских половых органов (яички, придатки).
Диагностика
1. Криптоспоридиоз.
Диагноз подтверждают обнаружением криптоспоридий в исследуемом материале (обычно исследуют фекалии, при наличии соответствующей клиники — мокроту и дуоденальное содержимое). Существуют специальные методы обработки, хранения и окраски исследуемого материала. Методами РИФ, РЛА можно выявлять антигены криптоспоридий. Имеются серологические методы, позволяющие определять специфические антитела; хотя в борьбе с инфекцией они существенной роли не играют, но могут служить маркером инфекции.
2. Изоспороз.
Диагноз подтверждается обнаружением паразитов в фекалиях; применение метода обогащения повышает вероятность паразитологических находок.
3. Токсоплазмоз.
Токсоплазмозный генез энцефалита подтверждает обнаружение токсоплазм в биоптатах мозга и/или в спинномозговой жидкости. Серологические методы менее надежны, учитывая высокую степень инфицированности населения.
txt by Стани́слав ЛЕМ // published 16/11/2011
У людей, подвергшихся заражению разновидностью паразита, с которой ранее им не приходилось встречаться (обычно — из-за географической изоляции), реакция на прибывших издалека паразитов может оказаться гораздо более резкой, чем у тех, кто с давних пор подвержен инфекции подобного типа. Говорят, что насморк, который испанские конкистадоры завезли в Америку, оказался сущим бедствием для туземцев.
Не подлежит сомнению, что виновником пандемии, обнаруженной около 1981 года (которая, как следует из экстраполяции кривых роста заболеваемости, началась где-то между 1950 и 1960 годами), был первый известный науке ретровирус человека из группы лентивирусов. Он получил название вирус иммунодефицита человека, ВИЧ. Это был возбудитель СПИДа.
Немецкий психолог Дитрих Дернер составил перечень медико-биологических проблем, решать которые труднее всего. Вот их характерные признаки, в несколько модифицированном мною виде:
1. Большое абсолютное число случаев.
2. Экспоненциальный рост.
3. Особенно длительный скрытый, латентный период, при котором целые годы отделяют причину от следствий.
4. Крайне трудно поддающиеся выявлению побудительные причины.
5. Особое место в эмоциональной жизни человека при отсутствии альтернативного поведения, которое
гарантировало бы полную безопасность (в случае СПИДа: человечество не может существовать без сексуальных отношений, а вирус передается преимущественно этим путем).
6. Абсолютная новизна проблемы.
8. Вероятностная неопределенность последовательности неблагоприятных событий; в результате эта последовательность необратима.
10. Неэффективность ранее испробованных методов решения подобного рода проблем.
Эти десять пунктов показывают, перед сколь серьезными проблемами ставит нас ВИЧ; можно было бы подумать, что его породило чье-то необычайно изощренное коварство.
Новизна стратегии ВИЧ заключается, прежде всего, в необычайной длительности латентного периода. Появление вирусов в крови приводит к образованию антител, которые, однако, неспособны успешно справиться с незваным гостем.
ВИЧ отличается высокой способностью к мутациям: в организме одного больного можно обнаружить два или даже три разных мутанта вируса. Подобная мутабильность свойственна многим вирусам, например вирусам обычной простуды (риновирусам) и гриппа. Изменчивость вируса простуды так велика, что делает невозможным создание защитных вакцин. С гриппом дело обстоит несколько лучше.
Стратегия этого вируса и в самом деле кажется совершенно новой. Но я рискну усомниться в том, что она встречается в природной эволюции впервые. Гипотезу, которую я хочу изложить, нельзя пока что проверить путем моделирования на ЭВМ; нельзя также найти хотя бы косвенного ее подтверждения в данных палеонтологии. Тем не менее, я хочу предложить определенную версию событий геологического прошлого Земли в качестве возможной и допустимой. В самом ли деле никогда еще не было вируса, у которого продолжительный латентный период сочетался бы с максимальной вирулентностью? И можно ли представить себе условия, в которых появление вирусов подобного типа становится более вероятным? При помощи какой контрстратегии эволюция может защитить от их вторжения виды, которым угрожает наибольшая опасность?
Сначала замечу (в скобках и предварительно), что у многих млекопитающих, живущих стадно, настоящая панмиксия обычно не наблюдается. Иначе говоря, там нет такого положения, при котором каждый самец копулирует поочередно с каждой самкой: этому мешает иерархическая организация стада, регулирующая, в частности, спаривание животных.
Тут следовало бы поставить вопрос: почему живущие социально насекомые — муравьи, пчелы, термиты, осы — в массе бесполые? Хотя филогенетически термиты не родственны ни муравьям (за которых их иногда ошибочно принимают), ни пчелам, и термиты, и пчелы, и муравьи образуют совокупности бесполых, неспособных к копуляции особей. В каждом пчелином рое, в каждом термитнике и муравейнике (а этих насекомых тысячи видов) родительские функции осуществляет одна-единственная особь, самка, один единственный раз в году, во время брачного полета, оплодотворяемая самцом, а потом оплодотворяющая яички его семенем, содержащимся в специальном receptaculum seminis. Разве в такой анатомии, физиологии и таком поведении не проявляется стратегия минимизации числа актов копуляции?
Быть может, если бы все особи данного вида имели пол и могли копулировать и размножаться, в результате такой панмиксии вероятность появления вирусов, вирулентность которых проявляется с большой задержкой и влечет за собой 100%-ную смертность, приближалась бы к единице, что равнозначно гибели вида. Поэтому под давлением естественного отбора шел процесс устранения способных к размножению особей, однако без снижения численности популяции (ведь рой из пятидесяти пчел или муравейник из ста муравьев были бы нежизнеспособны).
Насекомые тоже имеют иммунную систему, хотя и отличающуюся от иммунной системы высших животных. Среди них также встречаются болезни, вызываемые паразитами, причем здоровые особи устраняют мертвых из улья или муравейника. Лентивирус, который существовал бы в латентном состоянии на протяжении значительного отрезка жизни муравьев, термитов или пчел, убил бы их всех — такая инфекция охватила бы все сообщество как пожар. Поэтому социальные двуполые пранасекомые вымерли.
Читайте также:


