Особенности течения вич инфекции у детей
СПИД — это инфекционное заболевание вирусной природы. Возбудитель заболевания — вирус, названный человеческим Т-лимфотропным вирусом (ВИЧ). Вирус относится к группе ретровирусов и передается через жидкости тела (кровь, сперма) при половом контакте, при повторном использовании нестерильных игл (особенно это относится к наркоманам), а также трансплацентарно. Причем трансплацентарная передача вируса HTLV-I11 может осуществляться уже к 15-й неделе гестации. Именно этот путь передачи является основным для инфицирования детей. Установлено, что 35—65% HTLV-I1I позитивных женщин рожают инфицированных детей.
Таким образом, в зоне особого риска развития СПИДа у детей находятся: а) дети, больные гемофилией, которые для лечения получают концентрат фактора крови УШ, готовящийся более чем из сотен образцов донорской крови; б) дети, которые получали гемотрансфузии от доноров с развившимися у них позднее СПИДом; в) дети, у которых один из родителей имеет СПИД и находится в тесном контакте; г) дети, родившиеся от родителей, имеющих СПИД.
Инкубационный период при СПИДе (т.е. время между инфицированием и клиническими проявлениями иммунодефицита) колеблется от 4 месяцев до 4—5 лет.
Клинические симптомы ВИЧ-инфекции у большинства детей проявляются в возрасте до двух лет. Заболевание у детей характеризуется следующими основными признаками:
1) недостаточная прибавка ребенка в массе, задержка и отставание физического развития;
2) повторные бактериальные инфекции респираторного тракта, возможны сепсис, менингит, а также интерстициальная пневмония с лимфоцитарной инфильтрацией легочной ткани неясной этиологии у детей раннего и преддошкольного возраста;
3) увеличение околоушных слюнных желез, генерализованная лимфоаденопатия, гепатоспленомегалия;
4) упорная рецидивирующая молочница полости рта, хроническая рецидивирующая диарея.
Были предложены следующие критерии диагностики ВИЧ-инфекции у детей;
1) первичные клинические критерии:
— интерстициальная пневмония;
— резистентная к терапии молочница;
— увеличение слюнных желез;
— сепсис или менингит;
— мать или сибсы с подтвержденной ВИЧ-инфекцией;
2) вторичные клинические критерии:
— рецидивирующие бактериальные инфекции;
— генерализованная лимфоаденопатия;
— гепато- и спленомегалия;
— хроническая диарея;
— задержка развития;
3) лабораторные критерии:
— обнаружение антител к ВИЧ, идентификация его антигенов;
— повышенный уровень или IgA;
— снижение соотношения СD4:СD8 (вплоть до исчезновения СD4); а: — увеличение В-лимфоцитов.
ПРОФИЛАКТИКА.
ВИЧ-инфекция, характеризующаяся пандемическим распространением, представляет серьезную опасность для населения. В условиях отсутствия специфических средств профилактики и лечения чрезвычайно важное значение имеют меры по неспецифическому предупреждению заболевания.
В сложившейся обстановке на первое место выступает санитарно-просветительная работа. Однако санитарное просвещение может лишь тогда достичь своих целей, когда в его проведении принимают участие все медицинские работники. Эпидемические особенности заболевания требуют особо настойчиво и целенаправленно проводить санитарно-просветительную работу среди молодых людей как наиболее активных в сексуальном отношении, а также среди представителей групп высокого риска. Их необходимо информировать о путях и факторах передачи инфекции, подчеркивая, что нет никаких данных о возможности распространения возбудителя воздушно-капельным путем, при случайных бытовых контактах, а также через продукты питания. В связи с тем, что возбудитель наиболее часто проникает в организм при половых контактах, целесообразно рекомендовать использование презервативов, особенно при случайных половых контактах. Зараженные женщины должны предохраняться от беременности, так как возбудитель передается плоду. Распространение инфекции происходит также при использовании загрязненных игл и шприцев.
Важное место в предупреждении распространения ВИЧ-инфекции должны занять скрининговые исследования по выявлению инфицированных лиц. Для этого организуется обязательное тестирование всех доноров крови, плазмы, спермы, органов и тканей. Необходимой мерой является обследование представителей групп высокого риска, в частности детей, страдающих гемофилией, которые на протяжении всей жизни подвергаются неоднократным переливаниям крови и ее препаратов. В связи с этим их также следует проверять в отношении инфицированности ВИЧ.
Препараты крови также являются потенциально опасными в отношении инфицирования ВИЧ. Поэтому в технологию производства этих препаратов включают этапы, направленные на инактивацию или удаление вируса.
Решение относительно обучения и ухода за детьми с ВИЧ-инфекцией следует принимать исходя из состояния их нервной системы и физического статуса с учетом риска как для самих детей, так и для окружающих. Большинство детей могут посещать школу и неограниченно общаться со сверстниками. Для дошкольников, а также детей с открытыми мокнущими повреждениями, неврологическими нарушениями, проявляющимися, например, в непроизвольном мочеиспускании или дефекации, рекомендуется создавать условия, исключающие контакт окружающих с их кровью и жидкостями организма. Лица, ухаживающие за инфицированными детьми, должны быть информированы о методах предупреждения заражения. Во всех школьных и детских учреждениях уборка загрязненных жидкостями организма мест должна проводиться с использованием дезинфицирующих растворов. Необходимо постоянно следить за соблюдением инфицированными детьми гигиенических правил и своевременно принимать решение о степени их изоляции от окружающих. Врачи, наблюдающие детей, матери которых страдают ВИЧ или относятся к группам высокого риска, должны рассмотреть вопрос о проведении обследования на ВИЧ и целесообразность иммунизации детей живыми вакцинами (против кори, паротита, краснухи). В перечень медицинских обследований при передаче детей на воспитание приемным родителям необходимо включать исследование на инфицированность ВИЧ. В то же время проведение такого обследования всех детей перед поступлением в школу нецелесообразно.
В настоящее время ведутся интенсивные работы по созданию вакцины против ВИЧ-инфекции, однако препятствием в создании эффективной вакцины является чрезвычайно высокая изменчивость возбудителя, изменение структуры его поверхностных гликопротеидов. Поэтому в настоящее время основные усилия медицинских работников должны быть направлены на всестороннее использование комплекса неспецифических мер профилактики ВИЧ-инфекции.
При общем сходстве течения ВИЧ-инфекции у детей и у взрослых педиатрические наблюдения выявляют ряд существенных особенностей.
Кроме того, такие дети часто рождаются ослабленными, с явными признаками недоразвитости. И.И. Кузнецова обнаружила разницу в состоянии новорожденных, родившихся у ВИЧ-инфицированных и не зараженных ВИЧ женщин, при оценке их по шкале Апгар. Оценка менее 8 баллов при рождении детей от серо-позитивных матерей отмечена в 71% случаев, а у новорожденных контрольной группы (рожденных от не зараженных ВИЧ матерей) — только в 34%. При этом следует учесть, что ВИЧ-инфекция у серопозитивных женщин ведет к снижению жизнеспособности плода даже в том случае, если он не заражается ВИЧ.
Заражение во время родов, видимо, приводит к более позднему появлению признаков инфицирования. Еще позднее эти признаки появляются в том случае, если заражение произошло при грудном вскармливании. Наконец, заражение парентеральным путем, что особенно четко было показано за рубежом у детей, страдающих гемофилией, приводит к более длительному прогрессированию заболевания. Более половины детей, зараженных парентеральным путем во внутрибольничных очагах ВИЧ-инфекции, прожили более Шлет, т.е. длительность заболевания у них не отличалась от средней продолжительности заболевания у взрослых, а возможно, окажется и большей, хотя влияние на течение заболевания у них могла оказать и проводившаяся противоретровирусная терапия. По данным И. И. Поповой и соавт., наиболее существенным фактором, определившим выживаемость ВИЧ-инфицированных детей в очагах инфекции, был их возраст в момент заражения.
В группе с быстрым прогрессированием заболевания возраст детей в момент заражения колебался от 1 до 11 мес, а в группе с медленным прогрессированием — от 18 мес до 11 лет. Установлена также связь ранней смерти детей с тяжелыми сопутствующими заболеваниями во время заражения. Мы предполагаем, что при парентеральном заражении детей старше 1—2 лет прогноз ВИЧ-инфекции может считаться вообще относительно благоприятным по сравнению с таковым в других возрастных группах. Под нашим наблюдением находился ребенок, зараженный еще в 1985 г. в возрасте 4 лет при переливании крови, произведенном в связи с многочисленными пластическими операциями по поводу врожденных пороков развития; в настоящее время этот ребенок оканчивает среднюю школу. Умозаключения о более длительном выживании лиц, инфицированных в молодом возрасте, можно сделать и при анализе статистики выживаемости разных групп ВИЧ-инфицированных, приводимой в справочнике J. Bartlett, из которого явствует, что наиболее благоприятное течение ВИЧ-инфекции отмечается у детей, больных гемофилией, зараженных при введении препаратов крови. Очевидно, что клинические проявления в случае врожденной ВИЧ-инфекции отличаются от таковых при более позднем заражении. Чаще всего, описывая клиническую картину ВИЧ-инфекции у детей, зарубежные авторы пишут о клинической картине, развивающейся у детей, зараженных от ВИЧ-инфицированной матери.
При этом у детей не исключается, а довольно часто наблюдается развитие поражений, типичных для ВИЧ-инфекции у взрослых. По мере прогрессирования заболевания частота и разнообразие поражений нарастают. Нетипичным для детей поражением считают саркому Капоши, реже отмечают и другие опухоли.
При оценке прогноза ВИЧ-инфекции у детей следует учитывать возрастные особенности иммунологических показателей, в частности уровня СD4-лимфоцитов, которые различаются у детей разных возрастов. У детей до 1 года показателем отсутствия снижения иммунитета является уровень СD4-клеток более 1,5-10 9 /л, показателем умеренного иммунного дефицита — менее 1,5•10 9 /л, но более 0,75•10 9 /л, выраженного иммунного дефицита — менее 0,75•10 9 /л.
У детей в возрасте от 1 года до 5 лет признаком умеренного иммунодефицита является уровень СD4-клеток менее 10 9 /л, выраженного — менее 0,5•10 9 /л.
У детей старше 6 лет признаком умеренного иммунного дефицита является уменьшение количества СD4-клеток до 0,5•10 9 /л и менее, выраженного — до 0,2•10 9 /л и менее.
Поскольку количество СD4-клеток в единице объема крови у детей до 6 лет значительно колеблется, следует обращать большее внимание на процентное содержание СD4-клеток. Признаком умеренного снижения этого показателя во всех возрастных группах детей считается его падение до 24% и менее, выраженного — до 15% и менее.








ОСОБЕННОСТИ ТЕЧЕНИЯ ВИЧ ИНФЕКЦИИ У ДЕТЕЙ
Болезнь, вызванная вирусом иммунодефицита человека, или ВИЧ-инфекция – медленно прогрессирующее заболевание с контактным путем передачи, характеризующееся поражением иммунной системы с развитием синдрома приобретённого иммунодефицита (СПИД). Клиническими проявлениями несостоятельности иммунной защиты являются злокачественные новообразования, дистрофические и аутоиммунные процессы, что в конечном итоге, в случае отсутствия специфического лечения, ведет к гибели инфицированного человека.Заражение детей ВИЧ может происходить от инфицированной матери в процессе беременности, во время родов и при кормлении грудью, а также парентеральным путем при медицинских и парамедицинских вмешательствах. Риск передачи ВИЧ детям, рожденным от серопозитивных матерей, составляет по разным данным от 15% до 50%, зависит от стадии ВИЧ-инфекции у матери и увеличивается при грудном вскармливании. Инкубационный период при перинатальном заражении составляет около 12 месяцев. Активация ВИЧ-инфекции в организме ребенка происходит быстрее, чем у взрослого (у детей до 5 лет в среднем 2 года, взрослых и подростков -- 8 лет).
Особенностями патогенеза ВИЧ-инфекции у детей является то, что ВИЧ поражает незрелую иммунную систему. Для детского СПИДа характерна более ранняя недостаточность В-системы иммунитета по сравнению с Т-клеточным звеном. Именно этим объясняется разнообразие и рецидивирование бактериальных инфекций (стрептококковые, гемофильные и др.), которые определяют прогноз болезни. В результате недостаточности В-клеточного звена иммунитета и узкого спектра „знакомых“ АГ у маленького ребенка каждая новая инфекция может дать катастрофическое течение. Следовательно, быстрое развитие тяжелого иммунодефицита следует считать важнейшей особенностью ВИЧ-инфекции у детей раннего возраста.В постнатальном периоде такие дети плохо развиваются, у них постоянно обнаруживаются лимфоаденопатии, гепато- и спленомегалия, длительная субфебрильная температура тела. В отдельных случаях возникает так называемая СПИД-эмбриопатия, проявляющаяся нарушением роста, микроцефалией, отставанием психомоторного развития. Диагностика ВИЧ-инфекции у детей, рожденных от сероположительных матерей, сложна и имеет особенности. Это обусловлено тем, что в крови новорожденного до 12-15 месяцев могут циркулировать материнские анти-ВИЧ АТ. Кроме того, у детей замедлена репликация ВИЧ, поэтому ни вирус, ни его геном могут не выявляться. Вопрос о наличии у них ВИЧ-инфекции решается на основании анализа комплекса клинических, иммунологических и серологических данных.
Симптомы врожденной ВИЧ-инфекции
Дети, рожденные с ВИЧ, отличаются от здоровых малышей. У них обнаруживают следующие внешние признаки:
маленькие вес и рост;
лоб, по форме напоминающий коробку;
плоский и короткий нос;
Кроме этого у таких малышей увеличены лимфатические узлы, селезенка и печень. Лихорадка при внутриутробном заражении ВИЧ наблюдается редко.
Дети, рожденные с ВИЧ-инфекцией, хуже растут и медленнее прибавляют в весе. В дальнейшем у них наблюдается задержка психомоторного развития. Такой ребенок позже начинает держать головку, сидеть, стоять. Причина этих проблем — в том, что вирус поражает нервную систему ребенка.
Дальнейшее развитие болезни идет по нарастающей: дистрофия, рецидивирующий стоматит, пневмония, менингит, септические инфекции. Срок жизни при врожденной ВИЧ-инфекции 1-3 года.
Особенности течения ВИЧ инфекции
В целом наблюдается более быстрая динамика болезни по сравнению со взрослыми.
Характерное развитие хронического пневмонита (интерстициальная лимфоидная пневмония) и хронического паротита с лимфоидной инфильтрацией.
Бактериальные инфекции, особенно менингит, развиваются рано, принимают рецидивирующий характер с нарастанием симптомов от рецидива к рецидиву.
Саркома Капоши и лимфома ЦНС у детей, больных ВИЧ-инфекцией, наблюдаются в порядке исключения.
По сравнению с взрослыми пневмоцистоз у детей значительно реже.
Гипергаммаглобулинемия так же характерна, как и у взрослых, но степень её выраженности выше.
В связи с более быстрым прогрессированием болезни у детей ВИЧ раньше, чем у взрослых, проникает в ЦНС и раньше формируется специфическая энцефалопатия с деменцией.
Тромбоцитопения с геморрагическим синдромом вплоть до опасных для жизни кровотечений характерны для детской ВИЧ/СПИД инфекции.
Обнаружение анти ВИЧ антител в сыворотке ребенка 1 года жизни не является основанием для диагноза. Необходимо убедиться в том, что эти антитела не материнского происхождения. Дети от ВИЧ позитивных матерей наблюдаются не менее 36 месяцев от рождения. Возможно использование ПЦР.
У детей реже наблюдается туберкулез, герпетические в качестве СПИД ассоциированных заболеваний.
У них особенно часто бывают зуд кожи, пятнисто-папуллезная сыпь, нередки геморрагические высыпания в связи с возникающей тромбоцитопенией. Геморрагический синдром может стать причиной смерти больных.
Лекция по детским инфекционным болезням
Тема: ОСОБЕННОСТИ ВИЧ-ИНФЕКЦИИ
Учебные и воспитательные цели:
1. Факторы риска и частота перинатальной трансмиссии ВИЧ
2. Патогенез врожденной ВИЧ-инфекции
3. Клинические классификации ВИЧ-инфекции у детей
4. Естественное течение ВИЧ-инфекции у детей
5. Лечение ВИЧ-инфекции у детей: понятие ВААРТ, группы препаратов, критерии назначения препаратов, мониторинг терапии
РАСЧЕТ УЧЕБНОГО ВРЕМЕНИ
Перечень учебных вопросов
К-во выделяемого времени в минутах
Факторы риска и частота перинатальной трансмиссии ВИЧ
Патогенез и естественное течение ВИЧ-инфекции у детей
Диагностика ВИЧ-инфекции у детей
Классификации ВИЧ-инфекции у детей
Терапия ВИЧ-инфекции у детей
Лекцию подготовила доцент, к.м.н. Матиевская Н.В.
В настоящее время пандемия ВИЧ-инфекции достигла территории Республики Беларусь и постепенно становится все более и более актуальной проблемой здравоохранения РБ. Так, количество зарегистрированных случаев ВИЧ-инфекции на начало 2010 года составило около 11 тысяч, среди них умерло около 2-х тысяч больных. Подавляющее большинство больных это люди молодого работоспособного возраста – до 35 лет. Начиная с 2001-2002 г.г. во всех регионах республики начинает доминировать половой путь инфекции, так как в эпидпроцесс по ВИЧ вовлечены лица репродуктивного возраста. Все большее число случаев ВИЧ-инфекции регистрируется среди молодых женщин при постановке на учет по беременности. Соответственно, вероятность рождения ВИЧ-инфицированных детей возрастает. Течение врожденной ВИЧ-инфекции у детей имеет особенности, связанные с характером иммунного ответа у детей в разные возрастные периоды жизни, знание которых необходимо для осуществления рационального мониторинга ВИЧ-инфекции у детей.
Факторы риска и частота перинатальной трансмиссии ВИЧ
Наиболее значимая причина ВИЧ-инфекции у детей до 15 лет - это вертикальная передача ВИЧ от матери к ребенку во время беременности. Приблизительно 1800 детей во всем мире инфицируются данным путем ежедневно, большинство из них в развивающихся странах. Частота перинатальной трансмиссии (ПТ) ВИЧ в развитых странах составляет около 15-25% в год, в развивающихся – 25-45%.
Использование различных режимов профилактики ПТ ВИЧ позволяет снизить риск вертикальной трансмиссии до 2%.
При отсутствии профилактики риск ПТ составляет 19-36%. Частота зависит от пренатальных, интранатальных и постнатальных факторов, которые необходимо учитывать при проведении профилактики ПТ.
В зависимости от периода частота ПТ распределяется следующим образом:
Пренатальный период, преимущественно на последних стадиях беременности - 25-35%
Интранатальный период (роды) – 70-75%
Постнатальный период (грудное вскармливание) – 10-16%.
При грудном вскармливании (ГВ) наиболее высок риск ПТ в первые 3-4 месяца жизни ребенка
Считается, что если ребенок является позитивным на ВИЧ методом ПЦР в первые 48 часов жизни – он был инфицирован пренатально, если он становиться ПЦР-позитивным после 48 часов – инфицирование произошло во время родов.
Риск постнатального инфицирования, связанного с грудным вскармливанием возрастает в течение времени вскармливания. Отмечается прямая зависимость между риском ПТ и продолжительностью ГВ, уровнем ВН у матери. Высокий уровень антител к ВИЧ в грудном молоке (ГМ) снижает риск передачи. Имеет значение наличие докорма смесями (снижение риска), а также наличие у матери мастита, трещин сосков, абсцессов, инфекционной патологии у ребенка. В развитых странах грудное вскармливание для ВИЧ-позитивных матерей запрещено, в развивающихся странах – вопрос решается с учетом наличия возможности искусственного вскармливания и риска инфицирования для ребенка при переводе на искусственное вскармиливание. Матери, получающие ВААРТ, имеют низкий риск трансмиссии ВИЧ при ГВ.
Факторы, влияющие на ПТ условно могут быть разделены на 5 групп (табл. 1):
1. материнские факторы
2. вирусные факторы
3. акушерские факторы
4. факторы плода
5. факторы ребенка
Табл.1 – Факторы, влияющие на ПТ ВИЧ
Тип влияния фактора
Уровень виремии ВИЧ
Иммунный статус матери
Низкий уровень CD4+или терминальная стадия ВИЧ – увеличение риска ПТ
Инфекции урогенитального тракта
Наличие инфекций, особенно с изъязвлением слизистых УГТ – увеличение риска ПТ
При ВН матери >1000 кп/мл снижает риск ПТ на 50-70%, при ВН 299 000 кп/мл) четко ассоциируется с прогрессированием заболевания и развитием смерти, однако такие показатели ВН у детей встречаются редко.
Иммунологические особенности. Абсолютное значение показателя CD4+лимфоцитов зависит от возраста ребенка и у неинфицированных детей существенно выше, чем у взрослых. Показатели приближаются к уровню взрослого лишь к 4-6 году жизни (табл.2).
Табл.2 - Иммунологические категории при ВИЧ-инфекции у детей (1994)
Отсутствие значимой ИС
0,5см в диаметре
двух и более анатомических групп);
• хронический ВИЧ-паротит 1;
• рецидивирующие или постоянно персистирующие инфекции верхних дыхательных путей, синуситы и средние отиты.
· категория В (умеренная симптоматика): наличие связанной с ВИЧ-инфекцией клинической симптоматики, не входящей в категории А и С; ниже приведен примерный (но не исчерпывающий) список примеров такой симптоматики:
• анемия ( 9 /л), персистирующие более З0 дней;
• бактериальный менингит, пневмония или сепсис (хотя бы 1 эпизод);
• кандидоз орофарингеальный длительностью более 2 месяцев (у ребенка старше 6 месяцев);
• ЦМВ-инфекция (у ребенка старше 1 месяцев);
• диарея рецидивирующая или хроническая;
• герпетический (ВПГ 1 или 2) стоматит рецидивирующий (более 2-х эпизодов в год);
• герпетические (ВПГ 1 или 2) бронхиты, пневмонии, эзофагиты у детей старше 1 месяца;
• опоясывающий лишай (ВПГ 3) более 2-х раз в год или захватывающая дерматома, диссеминированная или осложненная ветряная оспа;
• лимфоидная интерстициальная пневмония (ЛИП) или гиперплазия прикорневых лимфоузлов;
• токсоплазмоз у ребенка старше 1 месяца, диссеминированный или осложненный;
• лихорадка персистирующая более 1 месяца;
• категория С (тяжелая симптоматика): наличие СПИД-ассоциируемых заболеваний (исключая ЛИП):
• серьезные бактериальные инфекции, множественные или рецидивирующие, как минимум 2 раза за двухлетний период, подтвержденные выделением возбудителя из гемокультуры, в виде сепсиса, пневмонии, менингита, остеомиелита, абсцессов различных органов и полостей, исключая отит, поверхностные кожно-слизистые абсцессы и катетер-ассоциированные инфекции;
• кандидоз глубокий (пищевода, бронхов, трахеи, легких);
• криптококкоз внелегочный (как правило, менингит);
• криптоспоридиоз или изоспороз с диареей более 1 месяца;
• ЦМВ-инфекция у ребенка старше 1 месяца (исключая изолированные поражения печени, легких и лимфоузлов);
• энцефалопатии: наличие прогрессирующих симптомов более 2 месяца при отсутствии других заболеваний кроме ВИЧ-инфекции:
а) задержка развития мозга, нарушение интеллекта, подтвержденное нейрофизиологическим тестами, или приобретенная микроцефалия, атрофия мозга, подтвержденная КТ или МРТ, у ребенка старше 2 лет;
б) приобретенные моторные нарушения (2 и более): парез, патологические рефлексы, атаксия или нарушение походки;
• герпетические (ВПГ 1 или 2) инфекции: кожно-слизистые язвы персистирующие более 1мес, или бронхиты, пневмонии, эзофагиты (у детей старше 1мес);
• туберкулез или атипичный микобактериоз диссеминированный или висцеральный;
• сальмонеллезная бактериемия (исключая S. typhi) рецидивирующая;
• токсоплазмозный энцефалит у ребенка старше 1 месяца;
• wasting-синдром (стойкая потеря массы >10% вследствие хронической диареи (стул не менее 3 раз в сутки длительностью не менее 1 месяца у детей старше 5 лет) и документированной лихорадки более 1 месяца постоянной или интермиттирующей) при отсутствии заболеваний, сходных с ВИЧ-инфекцией и объясняющих перечисленные симптомы;
• опухоли ВИЧ-ассоциируемые (саркома Капоши, злокачественные лимфомы: в первую очередь первичная лимфома головного мозга, а также В-клеточная лимфома и лимфома Беркитта);
• прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ).
Особенностью данной классификации является то, что пациент, единожды отнесенный к категории В, не может в последующем перейти в категорию А после излечения соответствующего заболевания. То же относится и к категории С. Все пациенты в группах A3, ВЗ, С1-3 расцениваются как пациенты, потенциально нуждающиеся в антиретровирусной терапии.
При невозможности определнения показателя CD4+ используется клиническая классификация ВИЧ-инфекции, где стадия ВИЧ-инфекции определяется с учетом клинических проявлений заболевания, параметров физического и нейропсихологического развития ребенка.
Пересмотренная клиническая классификация ВИЧ-инфекции у детей
(протоколы ВОЗ, 2006 г.)
Версия для Европейского региона, для детей 18 месяцев, выявление ДНК, РНК или антигена р24 у детей 12 месяцев
В зависимости от содержания CD4 лимфоцитов
В зависимости от содержания CD4 лимфоцитов
Примечание: * В некоторых случаях возможен индивидуальный подход к старту терапии при условии хорошего диспансерного наблюдения за больным.
Как видно из табл. 6, ВААРТ показана при манифестных стадиях ВИЧ-инфекции (3 и 4 стадия) независимо от уровня CD4+лимфоцитов. При 1 и 2 клинической стадии ВИЧ-инфекции вопрос о назначении терапии у детей старше 1 года основывается на данных иммунологического исследований. В то же время у детей с верифицированной врожденной ВИЧ-инфекцией терапия показана практически во всех случаях. Такая позиция связана с постоянно высокой ВН на 1 году жизни и риском развития осложнений, приводящих к смерти.
В то же время иммунологические критерии начала ВААРТ позволяют детям 1-го года жизни с отсутствием иммуносупрессии отложить терапию (табл. 7).
Таблица 7. Иммунологические критерии начала APT у детей (ВОЗ, 2006)
Пороговые значения CD4-лимфоцитов в зависимости от возраста, при которых показано назначение APT
Доля СD4-лимфоцитов плазмы (%)
25% у детей моложе 11 месяцев терапия может быть отложена, при условии тщательного мониторинга состояния здоровья ребенка.
Вирусологические показатели (вирусная нагрузка, ВН) не констатируют стадию ВИЧ-инфекции (как иммунологические и клинические данные), поскольку не отражают состояние организма (сохранность его иммунитета), а говорят только об активности репликации вируса. И если у подростков и взрослых значения ВН могут быть использованы для прогнозирования риска развития иммунодефицита в будущем, то у детей, особенно первого года жизни, это делать трудно из-за постоянно очень высокой ВН.
Тем не менее, ВН следует определять до начала APT, поскольку это объективный и ранний показатель ответа на лечение. Ведь целью APT является снижение ВН до неопределяемого уровня, при котором репликация вируса прекращается и снижается вероятность развития устойчивости к применяемой схеме APT.
АРП классифицируются в зависимости от механизма действия и точек приложения препарата, которые связаны с определенными этапами цикла репликации ВИЧ в клетках инфицированного пациента (рис. 3).
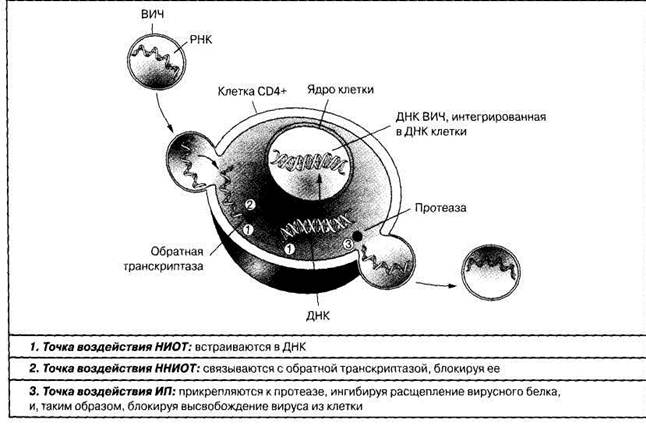
Рис. 3 – Целевые точки приложения АРП
К октябрю 2005 года к применению у взрослых и подростков был сертифицирован 21 антиретровирусный препарат в настоящее время к применению у детей доступны 4 группы АРП:
• Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ и НтИОТ)
• Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ)
• Ингибиторы протеазы (ИП)
• Ингибиторы слияния (ИС)
1 группа. Нуклеозидные ингибиторы обратной транскриптазы (НИОТ)
Существуют в виде монопрепаратов и комбинированных форм.
К монопрепаратам относят:
1. Ретровир (Retrovir, zidovudin, тимазид, азидотимидин, AZT, ZDV, 1987)
2. Ставир (Ставудин, Зерит, d4T, 1994)
3. Дивир (Диданозин, Видекс, ddl, 1991)
4. Зальцитобин (Хивид, Замицид, 1992)
5. Зиаген (Ziagen, Абакавир, АВС, 1998)
6. Эпивир (Epivir, Ламивудин, 3TC, LMV, 1995)
7. Тенофавир (Tenofavir, PMPA, Viread, 2001)
8. Эмтрицитабин (Эмтрива, 2003)
Комбинированные формы НИОТ представлены 6 препаратами:
1. Комбивир – ламивудин + зидовудин
2. Эпзиком – абакавир + ламивудин
3. Тризивир - абакавир + ламивудин+ зидовудин
4. Тенофавир+абакавир+ ламивудин
5. Тенофавир+диданозин + ламивудин
6. Трувада – эмтрицитабин + тенофовир
Комбинированные формы удобны в применении т.к. уменьшают количество таблеток, принимаемых больным.
2 группа. Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) представлены 3 препаратами. В РБ используются 2 препарата:
· Невирапин (Невимун, Viramune, NVP)
· Эфавир (Эфавиренз, Ифавиренц, Сустива, Стокрин, EFZ)
3 группа препаратов. Ингибиторы протеазы (ИП).
· Инвираза (Саквинавир твердые капсулы, SQV-HGC);
· Нелфинавир (Вирасепт, Nelvir, NFP);
· Норвир (Ритонавир, RTV);
· Калерта (Лопиновир/ритоновир, LPV/r);
4 группа. Ингибиторы фузии.
Единственный одобренный на сегодня препарат этой группы энфувиртид (T-20) вводится подкожно.
Принципы комбинации АРВ препаратов:
· Комбинации, основанные на ННИОТ (2 НИОТ и 1 ННИОТ)
· Комбинации, основанные на НИОТ (3 препарата из группы НИОТ)
· Комбинации, основанные на ИП (ИП и 2 НИОТ)
· Не рекомендуется комбинировать 1 НИОТ и 2 ННИОТ
· При неэффективности предложенных схем – ИП и НИОТ и ННИОТ
Особенности применения АРТ у детей.
Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ).
Невирапин. Схемы ВААРТ, включающие Невирапин + 2 НИОТ рекомендуются для широкого применения у детей младше 3 лет и тех, кому требуется жидкая форма препарата , одобрен к применению у детей с 2 месяцев. Препарат хорошо переносится детьми, дозировка препарата хорошо разработана в разных возрастных категориях. К неблагоприятным эффектам относится – возможность гепатотоксичности, возникновение аллергической сыпи, резистентность к препарату, если матери для профилактики ПТ назначался невирапин.
Эфавиренз препарат в капсулах, его жидкая форма проходит клинические испытания. В качестве схемы ВААРТ Эфавиренз+ 2 НИОТ разрешен к назначению в виде стартовой схемы детям старше 3 лет. Позитивными сторонами препарата является возможность назначения в виде однократной суточной дозы, а также способность его потенцировать антивирусный эффект других препаратов в схеме. В то же время доза для детей младше 3 лет не установлена. Препарат способен вызывать неиропсихические нарушения (бред, галлюцинации, возбуждение ит.д.) . Необходимо помнить о тератогенных эффектах препарата при назначении девочкам подросткового возраста.
Делавирдин выпускается только в таблетках и к применению у детей не одобрен, поскольку пока не изучен на детях.
Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ и НтИОТ).
- настоятельно рекомендуемые комбинации для первой схемы антиретровирусной терапии: зидовудин + ламивудин, зидовудин + диданозин и ставудин +ламивудин.
- рекомендуемыекомбинации для первой схемы антиретровирусной терапии: зидовудин + абакавир, ламивудин +абакавир и диданозин + ламивудин.
- не рекомендуются комбинации: зидовудин + ставудин (эти препараты снижают антиретровирусную активность друг друга), а также комбинации зальцитабина с диданозином, ставудином и ламивудином (эти комбинации плохо изучены у детей и все эти препараты нейротоксичны)
Тройные комбинации НИОТ в педиатрической практике.
По результатам нескольких педиатрических исследований тройная комбиниция НИОТ: ABC+ 3TC+ ZDV (Тривир) может рекомендоваться в качестве стартовой терапии у детей, но лишь в тех случаях, когда нет возможности использовать схемы с ННИОТ или ИП. 2 другие тройные комбинированные формы НИОТ (TNF+ ABC+ 3TC и TNF+ddI+3TC) не рекомендуются к применению в педиатрической практике.
Ингибиторы протеазы (ИП).
Наиболее часто используемая стартовая схема с ИП у детей в настоящее время это лопиновир/ритоновир (LPV/r, Калетра) +2 НИОТ. LPV/r имеет высокую антивирусную активность, высокий генетический барьер, хорошо изученную возрастную дозировку (даже у новорожденных), низкую токсичность.
Альтернативная схема: фосампренавир + RTN +2 НИОТ (для детей старше 6 лет). Жидкая форма фосампренавир появилась с 2007 г., рекомендуется у детей старше 2 лет.
Новые группы АРП в педиатрической практике. Ингибитор фузии – Т-20 был изучен на небольшой группе детей старше 6 лет, рекомендуется в режимах альтернативной терапии. Ингибитр интегразы (Ралтегравир) и ингибиторы входа (Маравирок) – не изучались на детях.
Диспансеризация детей получающих пожизненную ВААРТ.
Наблюдение детей, получающих длительные курсы ВААРТ имеет свои особенности. Несмотря на достижение успеха в первые годы терапии, очень часто на более поздних этапах констатируется отсутствие эффекта лечения. В такой ситуации требуется пересмотр терапии и смена стартовых режимов ВААРТ. Причины возникновения неэффективности терапии связаны со многими факторами: несоблюдение режима терапии, плохая переносимость препаратов, лекарственные взаимодействия, неадекватный уровень препарата, низкая противовирусная активность используемой схемы и т.д. Все данные факторы должны быть учтены и проанализированы прежде, чем менять схему терапии.
Необходимо помнить, что спектр выбора АРП у детей меньше, чем у взрослых. Поэтому прежде, чем принять решение о смене схемы лечения необходимо тщательно взвесить все факторы, максимально обследовать ребенка, используя генетические методы и т.д., а также проанализировать приверженность пациента к терапии. Необходимо понимать, что наблюдение ВИЧ-инфицированного ребенка должно проводиться с учетом всех обстоятельств жизни ребенка: социальных, экономических, психологических, культурных, семейных и т.д. Клиницисты должны понимать, что имеют дело с ребенком, страдающим сложным, многокомпонентным хроническим заболеванием, имеющем место в постоянно развивающемся и изменяющемся организме ребенка.
Читайте также:


