Действие вич на лимфоциты
Инфицирование человека ВИЧ происходит путем его попадания в кровь или на поврежденные слизистые оболочки. Возбудитель обладает уникальной способностью поражать разные типы дифференцированных клеток, в первую очередь Т4-лимфоциты (хелперы), а также моноциты/макрофаги и большое количество других чувствительных к нему клеток органов и тканей: фолликулярные дендритные клетки лимфатических узлов, клетки олигодендроглии и астроциты головного мозга, альвеолярные макрофаги легких, эпителиальные клетки кишечника и шейки матки, клетки Лангерганса.
Проникновение вируса внутрь клетки осуществляется связыванием его со специфическим рецептором клеточной оболочки (молекулярной СД4) путем эндоцитоза или прямым внедрением через плазматическую мембрану. Внутри клетки генетическая информация с вирусной РНК переходит на ДНК с помощью обратной транскриптазы. Однонитевая структура ДНК достраивается второй ее нитью, а промежуточная форма ДНК сливается с ядром клетки и интегрируется с ее ДНК, становясь ДНК-провирусом. С этого момента наступает стадия латентной инфекции, которая длительное время не проявляется никакими симптомами болезни, и человек находится в состоянии вирусоносительства.
Главным вопросом механизма патогенеза ВИЧ-инфекции является выяснение причин активации провируса. Допускают, что активация латентной инфекции может происходить под влиянием различных антигенов, цитокинов, собственных клеточных и гетерологичных транскрипционных факторов и других причин. Активация транскрипции и синтез белков-предшественников вируса принимает иногда взрывообразный характер, когда происходит завершающая сборка частиц вируса и выход его из клетки, следствием чего является ее прямая деструкция и цитолиз (цитонекроз), который дополняется образованием синцитиев с другими клетками, пораженными вирусом и не пораженными им, но имеющими на наружной мембране авидитентные молекулы СД4.
Это позволяет вирусу фиксироваться на клетках ЦНС, эпителиоцитах легких, кишечника и т. д. и вызывать развитие хронической (медленной) инфекции.
Уменьшение количества СД4-клеток в крови инфицированных ВИЧ может быть обусловлено действием цитокинов, секретируемых ВИЧ-макрофагами, таких, как фактор некроза опухолей и интерлейкины-1. Повышенная их секреция запускает запрограммированный механизм гибели клетки - апоптоз. СД8-лимфоциты, напротив, способны затормозить процесс гибели клетки с помощью секреции ими других цитокинов, благодаря чему сдерживается развитие инфекции на уровне бессимптомного течения. Прогрессирование ВИЧ-инфекции и цитолиз лимфоцитов определяют темп развития патологического процесса.
Дисгармония взаимодействия цитокинов, вырабатываемых субпопуляциями Т-хелперов 2-го типа (интерлейкин-4 и интерлейкин-10) и уменьшение Т-хелперов 1-го типа (интерлейкин-2, гамма-интерферон) лежат в основе прогрессирования инфекции ВИЧ.
По своей природе ВИЧ является иммунотропным, поэтому в дальнейшем развитии болезни все большую патогенетическую роль приобретает состояние иммунной системы организма. В основе иммунной супрессии лежит не только прямое цитопатическое действие на Т-хелперы - главную мишень ВИЧ, но и ряд опосредованных процессов. Уже в начале болезни идет выработка специфических противовирусных антител, но остановить развитие инфекционного процесса с их участием, как это наблюдается при многих других инфекционных болезнях, не удается. Вирус, первично поражая иммунную систему человека, упреждает ее защитную функцию.
Кроме того, поликлональная активация В-лимфоцитов ведет к общему нарастанию иммуноглобулинов и циркулирующих иммунокомплексов (ЦИК). ЦИК, содержащие антигены и антитела к ним, циркулируя в крови, способствуют генерализации процесса, вовлекая новые клеточные образования, не пораженные ранее вирусом. Развиваются глубокие иммунопатологические процессы, которые преобладают над защитными иммунными реакциями организма. Вследствие иммунодефицита возникают вторичные патологические процессы. Активация собственной микрофлоры тела человека обусловливает развитие оппортунистических инфекций. Иммунодефицит влечет за собой более легкое присоединение экзогенных инфекций и возникновение опухолей. Патологический стресс, возникающий у человека при диагностике у него ВИЧ-инфекции, опосредовано дополнительно угнетает ослабленную иммунную систему организма.
Немалую отрицательную роль при этом играет и поражение самого головного мозга, с состоянием которого связывают общую реактивность организма. Таким образом, снижается участие механизмов естественной регуляции иммунитета и адаптации организма во время болезни. На этом фоне вирус ВИЧ прямо и с дополнительным участием иммунопатологических процессов поражает практически все органы и системы организма, обуславливая полиорганность в стадии развернутой клинической картины СПИДа.
Инфекционные заболевания связаны с проникновением в организм человека бактерий, вирусов и грибковых микроорганизмов. Патогены преодолевают естественные барьеры, проникают во внутреннюю среду и начинают активно размножаться, повреждая ткани и органы пациента. Ученые еще в прошлом веке разработали эффективные лекарства для борьбы с бактериальными и грибковыми инфекциями, однако вирусные заболевания зачастую не поддаются терапии. Это связано с тем, что вирусные частицы не являются самостоятельными единицами жизнедеятельности и выполняют свои функции только внутри клетки. Такими свойствами обладает и вирус иммунодефицита человека, открытый во второй половине прошлого столетия.
Несмотря на отсутствие полноценного лечения, ВИЧ-инфекция не считается самой опасной болезнью. Новые методы терапии предотвращают развитие патологии и существенно улучшают качество жизни пациента. В то же время вирус иммунодефицита обладает значительной изменчивостью, поэтому ученым необходимо постоянно совершенствовать способы терапии инфекции. Кроме того, люди с врожденными и приобретенными патологиями иммунитета подвергаются большей опасности даже при своевременном лечении. На сегодняшний день главной задачей является снижение темпов распространения болезни в мире и улучшение профилактических мер.
Подробнее о заболевании

ВИЧ-инфекция представляет собой распространенное заболевание вирусной природы, поражающее иммунную систему человека. Патология характеризуется прогрессирующим течением: постепенное уничтожение иммунокомпетентных клеток приводит к формированию синдрома приобретенного иммунодефицита (СПИД). При этом на ранних стадиях ВИЧ-инфекция зачастую не вызывает каких-либо симптомов, поэтому у многих пациентов заболевание выявляется слишком поздно. К наиболее опасным осложнениям недуга относят развитие оппортунистических инфекций и злокачественных новообразований. Своевременное медикаментозное лечение позволяет существенно снижать вирусную нагрузку и предотвращать формирование осложнений.
На сегодняшний день во всем мире зарегистрировано более 35 миллионов людей, зараженных вирусом иммунодефицита. От осложнений болезни с каждым годом погибает все меньшее количество пациентов, однако инфекция до сих пор считается смертельно опасной. Важно учитывать, что скорость формирования приобретенного иммунодефицита может варьироваться в зависимости от штамма вируса, возраста и здоровья пациента, поэтому необходима своевременная диагностика. Введение в медицинскую практику скрининговых исследований позволило улучшить выявляемость болезни и уменьшить частоту смертельных исходов. Помимо скрининга пациентам необходимо учитывать способы заражения вирусом и основные методы профилактики.
История открытия
Первые клинические открытия, связанные с синдромом приобретенного иммунодефицита, датируются 1981 годом. В тот момент американские врачи начали выявлять редкие формы оппортунистических инфекций у наркоманов и гомосексуальных мужчин. Вскоре после этого эпидемиологи также отметили частое выявление саркомы Капоши у молодых людей. Это редкий тип злокачественной опухоли, развивающийся у пациентов с патологиями иммунитета. На тот момент врачи еще не догадывались о причинах активного распространения таких заболеваний, однако уже в 1982 году специалисты описали патологию защитных систем организма как синдром приобретенного иммунодефицита (СПИД).
После открытия опасного вируса ученые сконцентрировали свое внимание на изучении этиологии болезни. Предполагалось, что инфекция передается только при анальном сексе или инъекционном введении наркотиков. В 1983 году французские и американские специалисты независимо открыли и описали вирус, провоцирующий развитие болезни. Это было значимое открытие, позволившее в дальнейшем изучить все особенности инфекции и разработать эффективные лекарственные средства.
Происхождение вируса иммунодефицита до сих пор остается спорным вопросом, однако ученые склоняются к теории зоонозиса. Результаты многочисленных исследований показали, что предшественник вируса был распространен среди обезьян Западной и Центральной Африки. Из-за постоянных мутаций у патогена появились более опасные свойства, благодаря которым заболевание не купируется защитными системами организма.
Способы заражения
Пути передачи вируса связаны с биологическими жидкостями, включая кровь, сперму и вагинальные выделения. В этих субстанциях содержится большое количество вирусных частиц, готовых к инвазии. Чаще всего ВИЧ-инфекция передается именно половым путем, однако не следует исключать и другие способы заражения.
Известные пути передачи
- Анальный, вагинальный или оральный секс. Вирус может проникать в новый организм через слизистые оболочки органов.
- Гемотрансфузия. Вирус может проникать в кровеносную систему человека в случае переливания крови. Считается, что такой путь передачи заболевания маловероятен, поскольку специалисты всегда проверяют донорскую кровь на наличие инфекций.
- Совместное использование одноразовых шприцов – основной способ заражения ВИЧ-инфекцией и гепатитом среди наркоманов.
- Беременность, роды и грудное вскармливание. Вирусные частицы легко проникают в развивающийся организм, поэтому ведение беременности обязательно подразумевает скрининг на ВИЧ-инфекцию. Больным женщинам также следует отказаться от лактации, поскольку в слюне и желудочном соке младенцев содержится недостаточное количество агрессивных ферментов.
Патоген не обладает значительной устойчивостью к внешним факторам, поэтому другие пути заражения маловероятны.
Факторы риска
Помимо путей передачи необходимо также учитывать факторы риска. Это определенные состояния и признаки, увеличивающие вероятность заражения. Те или иные формы предрасположенности к болезни необходимо учитывать при профилактике.
Ключевые факторы риска
- Незащищенный секс. Вирусные частицы могут легко передаваться через слизистые оболочки, поэтому обязательно необходимо использовать латексные или полиуретановые презервативы. Эти защитные средства минимизируют риск инвазии.
- Анальный секс. Высокий риск заражения при подобном половом контакте обусловлен большим количеством микроповреждений слизистой оболочки кишечника.
- Наличие венерических заболеваний в индивидуальном анамнезе. Первичные инфекции, поражающие половые органы человека, увеличивают риск инвазии ВИЧ. Также такие патологии нарушают функции иммунной системы пациента.
- Многоразовое использование шприцов и игл. Этот фактор риска в первую очередь связан с наркоманией.
- Необрезанная крайняя плоть полового члена. Исследования показали, что обрезанные мужчины подвержены меньшему риску заражения.
Патогенные частицы могут попасть в организм любого человека независимо от половой принадлежности, расы и возраста. При этом высокая вероятность инвазии также может быть связана с особенностями протекания болезни у полового партнера. При высокой вирусной нагрузке и частом незащищенном сексе передача инфекции является наиболее вероятным исходом.
Особенности вируса
ВИЧ является ретровирусом, принадлежащим к роду лентивирусов. К особенностям этого патогена следует отнести длительный инкубационный период, наличие РНК в качестве генетического материала и способность реплицироваться в неделящихся клетках. После инвазии ВИЧ конвертирует собственную РНК в двухцепочную ДНК и встраивает полученную молекулу в генетическую структуру клетки. Для всех необходимых превращений используются специальные ферменты, включая обратную транскриптазу и интегразу. После встраивания вирусная структура может долго оставаться скрытой, из-за чего иммунная система человека не реагирует на присутствие патологии. Отмечается, что ВИЧ может оставаться бессимптомным даже в течение десяти лет после проникновения в организм.
- ВИЧ-1 – первичный инфекционный агент, открытый и описанный в 1983 году. Именно этот вирус распространился во всем мире в прошлом столетии. В разных странах можно обнаружить неодинаковое соотношение подтипов и групп ВИЧ-1. Так, например, подтип Aосновной группы ВИЧ-1распространен в СНГ и Западной Африке.
- ВИЧ-2 – инфекционный агент, открытый в 1986 году. Отмечаются значительные генетические отличия этого патогена от ВИЧ-1. В странах Европы этот вирус встречается редко.
Через некоторое время после встраивания вирусной ДНК в клеточный геном происходит распространение болезни. ВИЧ использует ресурсы клетки для сборки вирионов. В результате образуется несколько новых патогенов, способных распространяться в организме пациента. При этом зараженная клетка разрушается после высвобождения вирионов. Отмечается, что вирусный геном может проникать в структуру хромосом и оставаться в клетках человека даже после длительной медикаментозной терапии, поэтому ученые возлагают надежды на разработку способов редактирования генетической информации.
14 октября 2013
- 19743
- 15,7
- 2
- 3
Распространенность СПИДа в мире на 2009 год.

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Обратная транскрипция осуществляется вирусным белком обратной транскриптазой [31]. Обратная она потому, что обычно в клетке все наоборот — информация переносится с ДНК на РНК (а с РНК — в последовательность аминокислот белков). РНК по сравнению с ДНК очень нестабильна, и поэтому для ВИЧ характерна огромная скорость мутации — в десятки тысяч раз быстрее, чем для человека. Если скорость нейтральных мутаций для ДНК составляет у различных видов и для различных генов в среднем меньше 10 −9 замен на сайт в год, то скорость мутирования генетического материала РНК-вирусов — около 10 −3 замен на сайт в год (у гена env ВИЧ: 10 −2 –10 −3 замен на сайт в год [21]). Это одна из причин, почему иммунная система не может справиться с ВИЧ — он слишком быстро изменяется.
Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
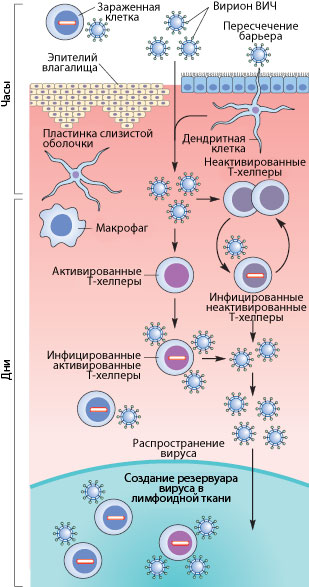
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
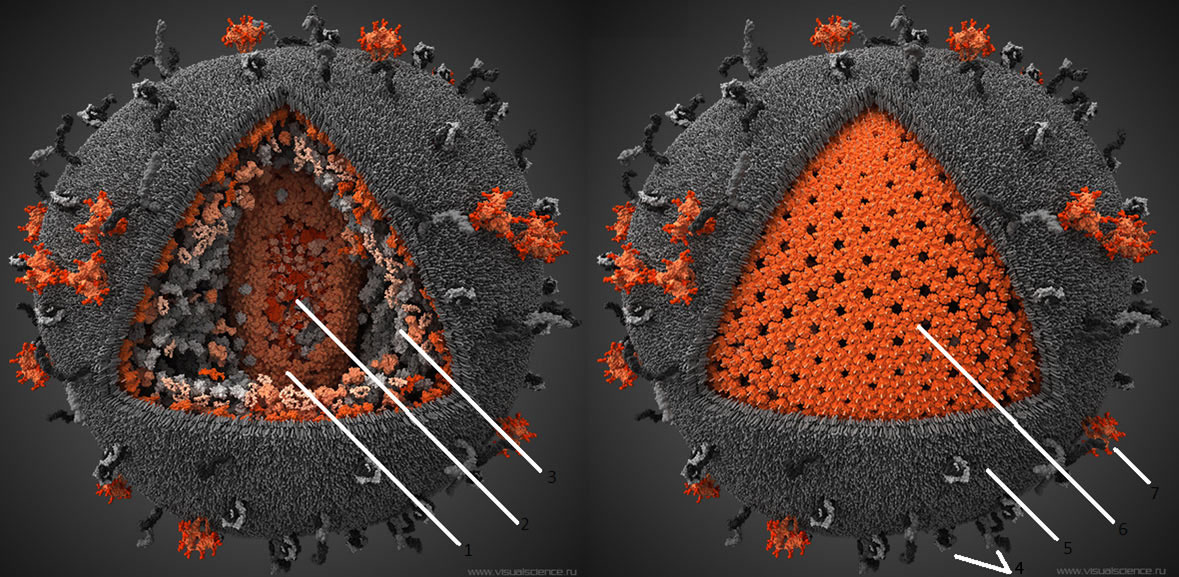
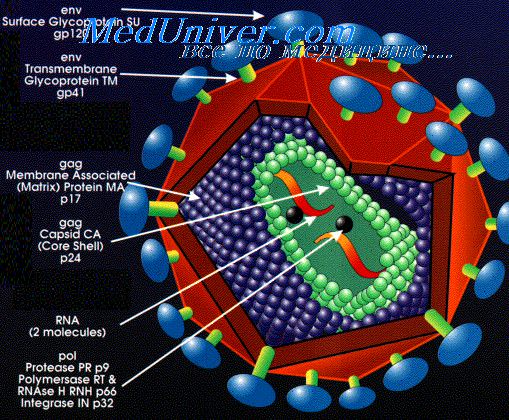
10000 нуклеотидов в каждой. Всего геном включает девять генов, которые в результате альтернативного сплайсинга кодируют 15 различных белков. 3 — Различные белки, захваченные вирусом из хозяйской клетки. 4 — Человеческие белки, обычно находящиеся на поверхности мембраны клеток. Захваченые в результате отпочковывания, они увеличивают вирулентность вируса. 5 — Внешняя оболочка ВИЧ, ведущая свое происхождение от цитоплазматической мембраны клетки, от которой когда-то отпочковался вирион. 6 — Матрикс, образованный тримерами белка р17. 7 — Тримерные комплексы белков gp120 и gp41, при помощи которых вирус проникает в клетку. На поверхности среднего вириона насчитывается около 20 таких тримеров. Чтобы увидеть рисунок в полном размере, нажмите на него.
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Все инфекционные заболевания нуждаются в своевременной точной диагностике. ВИЧ и СПИД — не исключение. Поставленный вовремя диагноз позволяет принять необходимые терапевтические меры и продлить пациенту жизнь. Как же определить наличие или отсутствие заболевания с максимальной точностью?
Диагностика ВИЧ-инфекции и СПИДа
Сегодня, наверное, каждый человек слышал о ВИЧ и СПИДе и знает, что эти заболевания очень опасны, что передаются они в основном во время незащищенного барьерным способом полового акта. А между тем, первые случаи инфицирования были зафиксированы не так давно — в 1978 году (у нескольких мужчин-гомосексуалов из США и Швеции). Сам вирус был открыт в 1983 году.
В первую очередь ВИЧ атакует и разрушает лимфоциты (Т-лимфоциты, или хелперы). Они отвечают за иммунный ответ организма, распознавание и уничтожение инфицированных клеток. В результате заболевший теряет способность противостоять инфекциям.
У здорового человека количество Т-лейкоцитов составляет 1200–3000 клеток/мкл. После ВИЧ-инфицирования число клеток снижается. При этом заболевший продолжает чувствовать себя нормально. Данный период болезни может длиться на протяжении многих лет. Но наступает момент, кода количество клеток-хелперов достигает критической отметки. Это может проявиться следующими проблемами:
- кандидоз полости рта и ЖКТ;
- опоясывающий лишай (герпес);
- неделями не спадающая высокая температура;
- ночная потливость;
- диарея;
- частые ОРЗ и ОРВИ и др.
Если число Т-лимфоцитов снижается до 200 клеток/мкл, то диагностируют СПИД. Организм больного в таком состоянии не может сопротивляться даже простейшим микроорганизмам — от дрожжей до вирусов. У здорового человека к ним развивается резистентность, тогда как страдающего СПИДом они могут довести до летального исхода. Чаще всего возбудителями смертельных заболеваний становятся токсоплазма, криптоспоридии, цитомегаловирус. Кроме того, снижение лимфоцитов провоцирует образование злокачественных опухолей.
При отсутствии должного лечения пациенты с ВИЧ-инфекцией не переступают порог выживаемости в 10 лет. Грамотно и своевременно назначенная терапия затормаживает развитие болезни, в разы увеличивая продолжительности жизни больного. ВИЧ-положительный человек в таком случае может дожить до преклонных лет.
Основной метод диагностики инфекции — анализ крови. С момента заражения до появления антител в крови проходит 1–3 месяца.
Разные виды лабораторных анализов венозной крови, взятой натощак, позволяют обнаружить наличие или отсутствие ВИЧ-инфекции в крови. Рассмотрим виды этих исследований.
- Скрининговое исследование иммуноферментными (ИФА) методами представляет собой выявление антител к антигенам ВИЧ-типов: ВИЧ-1 и ВИЧ-2. Уже со второй недели после инфицирования могут появиться антитела, хотя они способны обнаружиться и позже — через несколько месяцев. В последующее время количество антител растет и сохраняется в крови пациента. При наличии антител в большинстве случаев клинические признаки ВИЧ не проявляются 2–10 лет.
Отметим, что данный тест не всегда точен, возможен ложноположительный результат. В любом случае при положительном результате назначается повторный анализ через 2-3 недели. - Верификационное исследование методом иммуноблота проводится, если описанный выше анализ дважды дал положительный результат. Данное исследование сочетает анализ ИФА и метод электрофореза, который позволяет разделить по молекулярному весу входящие в состав вируса антигены. Данное исследование имеет максимальную точность.
- Полимеразная цепная реакция (ПЦР) с детекцией в режиме реального времени дает возможность определить концентрацию вирусной РНК в плазме крови. Тест проводят в целях ранней диагностики возможного инфицирования после случая повышенного риска (на 7–10 день после предположительного инфицирования).
Также данный анализ назначается для оценки эффективности применяемой терапии, для решения вопроса о начале антиретровирусной терапии, о проведении кесарева сечения у инфицированных беременных за 4 недели до родов.
Такое исследование крови проводят новорожденным детям инфицированных матерей. Полученный дважды положительный ответ говорит о заражении ребенка.
Поводом пройти исследование на ВИЧ-инфекцию может стать множество причин. Тест необходим перед оперативным вмешательством, в случае планирования беременности, риск приобретения данной инфекции несут случайные половые контакты. Отдельная категория граждан (врачи, педагоги, работники пищевых производств, продавцы пищевой продукции и др.) обязана проходить тест в рамках оформления медицинской книжки, являющейся обязательным условием допуска к работе.
Что касается тревожных симптомов, то обычно врачи назначают анализ на ВИЧ при следующих состояниях:
- Резкая потеря веса.
- Диарея, длящаяся более трех недель.
- Лихорадка неясного происхождения.
- Увеличение лимфатических узлов в разных областях.
- Лейкопения и лимфопения.
- Тяжелые инфекционные заболевания: пневмония, кандидоз внутренних органов, туберкулез, манифестный токсоплазмоз, частые случаи обострения герпесвирусной инфекции и другие.
Специальной подготовки перед сдачей венозной крови не требуется. Единственное — это воздержание от приема пищи в течение 8–10 часов. Также накануне рекомендуется избегать физических и эмоциональных нагрузок, отказаться от употребления алкоголя.
Вся процедура забора венозной крови занимает не более пяти минут. После взятия материала место укола дезинфицируют и заклеивают специальным пластырем. Так как анализ берется натощак, во избежание головокружения после забора крови следует выпить сладкий чай или съесть кусочек шоколада.
В государственных поликлиниках, чтобы получить направление на анализ, придется сначала посетить участкового терапевта. В частных же медицинских центрах нужно просто заполнить заявку на анализ. Для этого в клинике попросят предъявить паспорт или какой-либо другой документ, удостоверяющий личность (миграционная карта, водительские права, военный билет и т. д.). Документ позволит идентифицировать результаты анализа. Впрочем, тест на ВИЧ можно сделать и анонимно. В этом случае заявке и образцу крови, который отправляется на анализ в лабораторию, присваивается номер, известный лишь пациенту и медицинскому персоналу. Однако результаты анонимных исследований не могут быть представлены для госпитализации, в женские консультации и не могут быть зарегистрированы в ОРУИБ (Отдел регистрации и учета инфекционных болезней).
Следует помнить, что интерпретировать результаты исследования и поставить точный диагноз способен только врач. Полученный результат ни в коем случае не может быть поводом для самолечения, к тому же одни и те же результаты у разных пациентов могут говорить о противоположной клинической картине.
Показывает объем выявленной РНК вируса иммунодефицита человека, выраженный в C/ml (копии/мл). Интерпретировать результаты следует следующим образом:
- РНК не выявлена, либо значение ниже предела чувствительности метода (20 копий/мл).
- Меньше 20 копий/мл — РНК выявлена в концентрации на пределе чувствительности метода, характеристика с удовлетворительной точностью невозможна.
- От 20 до 10 6 копий/мл — полученное значение находится в пределах линейного диапазона, результат достоверен.
- Больше 10 6 копий/мл — РНК выявлена в указанной концентрации, выходящей за верхний предел линейного диапазона.
Анализы на ВИЧ можно сдать в частных клиниках. В этом случае стоимость скринингового исследования иммуноферментными методами в среднем составит от 400 до 800 рублей. Срок выполнения исследования — один рабочий день, хотя возможна и срочная диагностика, в таком случае ответ будет получен через 2 часа.
Верификационное исследование методом иммуноблота обойдется в 3000–5000 рублей. Результаты станут известны через 3–7 рабочих дней.
Полимеразная цепная реакция с детекцией в режиме реального времени представляет собой более сложный анализ, поэтому его стоимость намного выше — она составляет 10 000–12 000 рублей. Результаты исследования готовятся в среднем 10–14 рабочих дней.
Согласно законодательству все иммунные анализы в государственных медицинских учреждениях проводятся бесплатно. В обязательном порядке проверку на ВИЧ-инфекцию проходят беременные женщины, пациенты, готовящиеся к оперативному вмешательству и госпитализации. В остальных случаях направление на данное исследование назначается по усмотрению врача.
Пройти анализ на ВИЧ-инфекцию сегодня не составляет сложности. Сама процедура практически безболезненна и занимает считанные минуты. Современное оборудование и методики проведения теста позволяют получить максимально точные результаты.

Вопреки некоторым мнениям, ВИЧ не является приговором. Инфицированные люди способны прожить долгую, полноценную жизнь. Они могут иметь семью, детей, без опасений общаться с окружающими. Главное при этом выполнять особые правила гигиены и бытового поведения, знать, как свести к минимуму риск заражения домочадцев. А в случае возникновения сомнительных или спорных ситуаций — обращаться к специалистам: врачам, психологам. Но ни в коем случае не замыкаться и не ставить на жизни крест.
Читайте также:


