Септического и гиповолемического шока

Септический шок является одним из тяжелейших осложнений сепсиса, и сопровождается высоким риском летального исхода. Данное состояние свидетельствует о полном истощении компенсаторных систем организма, его неспособности самостоятельно поддерживать артериальное давление, а также о присоединении полиорганной недостаточности (состояние, при котором органы не способны выполнять свои функции без медицинского вмешательства).
Для септического шока характерно изменение сосудистого русла, а также развитие паралича сосудов. Возможно нарушение сократительной способности сердечной мышцы, хотя и на поздних сроках, а также возможно сгущение крови. Не исключено, что может развиться дыхательная недостаточность.
Что такое септический шок
Септический шок – это тяжелое течение сепсиса , характеризующееся развитием артериальной гипотензии, устойчивой к стандартной реанимации жидкостями и сопровождающейся возникновением тканевой гипоперфузии (нарушение микроциркуляции в тканях) и множественной органной дисфункции.
Артериальная гипотензия, резистентная к инфузионной терапии, является обязательным и важнейшим критерием выставления диагноза септический шок.
Течение сепсиса, сопровождающееся только дыхательной или сердечно-сосудистой дисфункцией, сочетающимися с двумя и более, другими дисфункциями (неврологическая, гематологическая, почечная, желудочно-кишечная, печеночная и т.д.) определяется как тяжелый сепсис без септического шока.

Развитию септического шока предшествует сепсис-индуцированная артериальная гипотония, сопровождающаяся понижением систолического артериального давления ниже 90 мм.рт.ср. для пациентов с исходным нормальным давлением или на 40 мм.рт.ст. ниже привычного рабочего давления для пациентов с гипертонией.
На этой стадии гипотония временно устраняется проведением адекватной инфузионной терапии. О присоединении септического шока будут свидетельствовать падение систолического давления ниже 65 мм.рт.ст., а также отсутствие реакции на проведение инфузионной терапии в возрастной дозировке.
Причины развития септического шока
Септический шок является осложнением тяжелого сепсиса. То есть, вначале развивается синдром системной воспалительной реакции, затем сепсис, далее тяжелый сепсис. Финальным этапом является развитие септического шока. Для его развития требуется наличие предрасполагающих факторов риска, а также тяжелая септицемия, септикопиемия и тяжелейшая интоксикация.
Чаще всего септический шок развивается у:
- ослабленных больных, недавно перенесших длительные инфекционно-воспалительные заболевания, травмы, ожоги и т.д.;
- лиц, с декомпенсированными соматическими заболеваниями (сердечная недостаточность, сахарный диабет, хроническая почечная недостаточность и т.д.);
- лиц, с иммунодефицитами (первичными и вторичными);
- пациентов с выраженными авитаминозами, дефицитом белка (вегетарианцы, лица, придерживающиеся низкобелковых диет);
- новорожденных детей;
- пациентов пожилого возраста;
- больных со злокачественными новообразованиями (в особенности, в период опухолевого распада либо при наличии большого количества метастатических очагов);
- больных, получающих или недавно проходивших курс химиотерапии или лучевой терапии;
- пациентов, принимающих цитостатическую или иммунодепрессивную терапию;
- лиц, с тяжелыми аутоиммунными патологиями;
- пациентов после трансплантации органов.
Септический шок может развиваться при генерализации инфекции на фоне отитов, синуситов, пневмоний, абсцессов в легких, гнойных поражений кожных покровов и подкожно-жировой клетчатки, септических артритов, остеомиелитов, гнойных бурситов, аппендицита, перитонита, аднекситов, сальпингоофорита, миокардитов , эндокардитов, кишечных инфекций, менингитов и т.д.

Спектр основных возбудителей зависит от возраста больного, состояния его иммунной системы, а также первичного очага инфекции.
Причинами пупочного и кожного сепсиса и септического шока, чаще всего, выступают золотистые и эпидермальные стафилококки, эшерихия коли, пиогенные стрептококки.
Легочной сепсис, как правило, развивается из-за пневмококков, клебсиеллы пневмония, гемофильной инфекции типа В, золотистых и эпидермальных стафилококков. У интубированных больных может развиться сепсис и септический шок, вызванных синегнойной палочкой или ацинетобактером.
Кишечный сепсис может быть ассоциирован энтеробактериями (сальмонеллы, шигеллы и т.д.), энтеробактером, эшерихией коли. У детей первых трех лет жизни септический шок может развиваться на фоне тяжелого септического течения сальмонеллеза (у взрослых, генерализированный сальмонеллез встречается гораздо реже).
Септический шок, связанный с гнойно-воспалительными заболеваниями мочеполовой системы, как правило, вызывается эшерихией коли, стафилококками, стрептококками, клебсиеллой, протеем, энтерококком. У пациентов с катетеризированным мочевым пузырем, среди основных возбудителей сепсиса и септического шока выделяют золотистый и эпидермальный стафилококк, энтеробактер и псевдомонады.
- фузобактерией некрофорум (палочкой Шморля),
- гемофильной инфекцией типа В,
- стафилококковой, стрептококковой и пневмококковой флорой.
Сепсис у пациентов с менингитом развивается из-за пневмококков, гемофильной инфекции и менингококков (септический шок на фоне менингококковой инфекции, как правило, встречается у детей, для взрослых более характерно здоровое носительство менингококков или менингококковые назофарингиты).
Причиной септического шока у больных с остеомиелитом, гнойным бурситом или септическим артритом, чаще всего, становятся золотистые стафилококки, пневмококки, пиогенные стрептококки, гемофильная палочка, клебсиеллы.
Септический шок – классификация
Септические шоки принято разделять на:
- теплые компенсированные (гипердинамическая фаза шока);
- холодные декомпенсированные (гиподинамическая фаза);
- рефрактерные к введению дофамина;
- рефрактерный к введению катехоламинов;
- абсолютно рефрактерный шок (картина септического шока продолжает нарастать, несмотря на введение вазопрессорных, вазодилататорных и инотропных препаратов).
По длительности течения септический шок может быть молниеносный, прогрессирующий, стертый, рецидивирующий и терминальный.
В патогенезе развития шока выделяют две основные стадии:
- гипердинамическую, сопровождающуюся снижением периферического сосудистого сопротивления, рефлекторным увеличением работы сердца и компенсаторным повышением сердечного выброса;
- гиподинамическая, характеризующаяся нарушением микроциркуляции в органах и тканях, резким уменьшением периферического кровообращения, гипоксией и ишемией органов и тканей, а также прогрессирующими нарушениями функции органов (сердечная, дыхательная, почечная, печеночная и т.д. недостаточности).
Септический шок – это следствие:
- развития синдрома системной воспалительной реакции;
- массивной септицемии, септикопиемии, токсинемии;
- выброса в кровь большого количества воспалительных медиаторов;
- относительной (развивается за счет расширения сосудов и снижения периферического сопротивления сосудов) и абсолютной (возникающей как результат резко увеличенной сосудистой проницаемости) гиповолемии;
- снижения сократимости миокарда и понижения сердечного выброса (наблюдается при прогрессирующем септическом шоке). При начальных стадиях септического шока при адекватной и ранней инфузионной терапии, характерно компенсаторное повышение сердечного выброса, с целью поддержания периферического кровообращения. При истощении компенсаторных механизмов организма, способность сердечной мышцы к сокращению снижается.

В результате резко выраженной артериальной гипотонии и гипоперфузии в тканях, нарушается кислородный обмен и полноценный метаболизм. Развивается гипоксия, увеличивается процесс анаэробного гликолиза (ферментативные процессы, в результате которых происходит расщепление глюкозы без потребления О2).
Анаэробный гликолиз позволяет некоторое время поддерживать метаболизм в клетках и обеспечивать их энергией, однако прогрессирующая гипоксия приводит к накоплению в клетках молочной кислоты и развитию лактатацидоза.
Лактатацидоз при септическом шоке развивается остро (в течение одного-двух часов). У пациентов появляется:
- сильная мышечная боль,
- боли за грудиной,
- одышка,
- учащенное дыхание,
- боли в животе,
- многократная и не приносящая облегчения рвота,
- заторможенность,
- нарушение сердечного ритма ,
- появление дыхания Куссмауля (шумного, редкого, глубокого дыхания).
Неврологическая симптоматика может проявляться отсутствием рефлексов, либо наоборот гиперкинезами и судорогами. Также характерны симптомы почечной недостаточности (анурия), снижение температуры тела (гипотермия), диссеминированное внутрисосудистое свертывание крови, внутрисосудистый тромбоз. При тяжелом лактатацидозе возможно появление очагов некроза на кончиках пальцев рук и ног.
Кроме симптомов лактатацидоза, септический шок сопровождается развитием острого респираторного дистресс-синдрома, нарушения сознания, ишемией головного мозга, паралитической кишечной непроходимостью, ишемией и некрозом кишечника.
Симптомы и признаки септического шока

Развитию септического шока всегда предшествуют прогрессирующие симптомы сепсиса. Пациенты бледные, вялые, заторможенные, может отмечаться выраженное беспокойство, страхи. Характерен также озноб и профузная потливость. Первыми признаками сепсиса у детей может быть капризность, плаксивость, отказ от еды, частое шумное дыхание, вздутие живота. Характерно появление рвоты, не приносящей облегчения.
Отмечается также снижение диуреза и парез кишечника (отсутствие стула и перистальтики). При пальпации живота обнаруживается увеличение печени и селезенки. У большинства пациентов печень при пальпации болезненна, живот вздут и напряжен.
При развитии компенсированного септического шока (теплый или гипердинамический шок), характерно развитие:
- гипертермии (температура повышается выше 38.5-39 градусов);
- тахикардии, нарушений сердечного ритма;
- ускорения периферического пульса, время наполнения капилляров менее двух секунд (симптом белого пятна оценивается надавливанием пальцем на кисть и подсчетов времени, которое требуется на исчезновение белого пятна);
- олигурии (снижения объема мочеиспускания);
- спутанности сознания, сонливости, заторможенности.
Общие сведения
Гиповолемический шок представляет собой патологическое состояние, развивающееся под влиянием снижения объема циркулирующей крови в кровеносном русле или дефицита жидкости (дегидратации) в организме. Как следствие, снижается ударный объем и степень наполнения желудочков сердца, что приводит к развитию гипоксии, перфузии тканей и расстройству метаболизма. Гиповолемический шок включает:
- Геморрагический шок, в основе развития которого острая патологическая потеря крови (цельной крови/плазмы) в объеме превышающим 15-20% от всего ОЦК (объема циркулирующей крови).
- Негеморрагический шок, развивающийся по причине выраженной дегидратации организма, вызванной неукротимой рвотой, диареей, обширными ожогами.
Гиповолемический шок развивается преимущественно при больших потерях жидкости организмом (при патологическом жидком стуле, потере жидкости с потом, неукротимой рвоте, перегревании организма, в виде явно неощутимых потерь). По механизму развития он близок к геморрагическому шоку, за исключением того, что жидкость в организме теряется не только из сосудистого кровеносного русла, но и из внесосудистого пространства (из внеклеточного/внутриклеточного пространства).
Наиболее часто в медицинской практике встречается геморрагический шок (ГШ), представляющий собой специфический ответ организма на кровопотерю, выражающийся комплексом изменений с развитием гипотензии, гипоперфузии тканей, синдрома малого выброса, расстройств гемокоагуляции, нарушения проницаемости сосудистой стенки и микроциркуляции, полисистемной/полиорганной недостаточности.
Пусковым фактором ГШ служит патологическая острая кровопотеря, развивающаяся при повреждении крупных кровеносных сосудов в результате открытой/закрытой травмы, повреждениях внутренних органов, при желудочно-кишечных кровотечениях, патологий в период беременности и родового акта.
Летальный исход при кровотечении наступает чаще в результате развития острой сердечно-сосудистой недостаточности и гораздо реже, в связи с утратой кровью своих функциональных свойств (нарушения функции кислородно-углекислого обмена, переноса питательных веществ и продуктов метаболизма).
Значение в исходе кровотечения имеют два основных фактора: объём и скорость потери крови. Принято считать, что острая одномоментная потеря циркулирующей крови за короткий промежуток времени в объёме порядка 40% несовместима с жизнью. Однако, встречаются ситуации, когда больные теряют значительный объём крови на фоне хронического/периодического кровотечения, а пациент не погибает. Это обусловлено тем, что при незначительных одноразовых или хронических кровопотерях существующие в организме человека компенсаторные механизмы достаточно быстро восстанавливают объем крови/скорость ее циркуляции и сосудистый тонус. То есть, именно скорость реализации адаптационных реакций определяет возможность сохранения/поддержания жизненно важных функций.
Различают несколько степеней острой кровопотери:
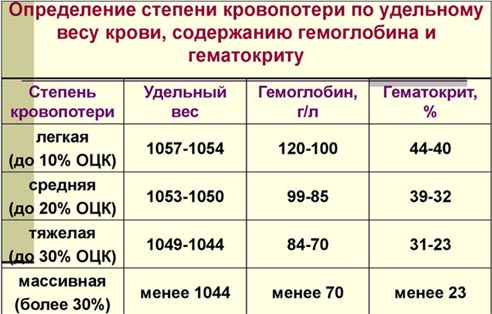
- I степень (дефицит ОЦК до 15%). Клинические симптомы практически отсутствуют, в редких случаях — ортостатическая тахикардия, показатель гемоглобина более 100 г/л, гематокрит 40% и выше.
- II степень (дефицит ОЦК 15-25%). Ортостатическая гипотензия, АД снижено на 15 мм рт.ст. и более, ортостатическая тахикардия, ЧСС увеличен более чем на 20/минуту, показатель гемоглобина в 80-100 г/л, уровень гематокрит 30-40%.
- III степень (дефицит ОЦК 25-35%). Присутствуют признаки периферической дисциркуляции (выраженная бледность кожи, на ощупь холодные конечности), гипотензия (систолическое АД 80-100 мм рт. ст.), ЧСС превышает 100/минуту, частота дыхания более 25/минуту), ортостатический коллапс, сниженный диурез (менее 20 мл/ч), гемоглобин в пределах 60-80 г/л, гематокрит — 20-25%.
- IV степень (дефицит ОЦК больше 35%). Отмечается нарушение сознания, гипотензия (систолическое АД менее 80 мм рт. ст.), тахикардия (ЧСС 120 /минуту и более), частота дыхания более 30/минуту, анурия; показатель гемоглобина менее 60 г/л, гематокрита – менее 20%.
Определение степени кровопотери может проводиться на основании различных прямых и относительных показателей. К прямым методам относятся:
- Калометрический метод (взвешивание излившейся крови путем колориметрирования).
- Гравиметрический метод (радиоизотопный метод, полиглюкинолвый тест, определение с помощью красителей).
К непрямым методам:
- Шоковый индекс Альговера (определяется по специальной таблице по соотношению частоты пульса и систолического давления).
На основании лабораторных или клинических показателей, наиболее доступными из которых являются:
- По удельному весу крови, содержанию гемоглобина и гематокриту.
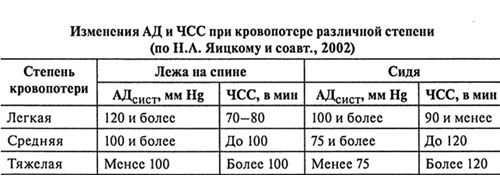
- По изменению гемодинамических показателей (АД и частоты сердечных сокращений).
Величину кровопотери при травмах можно определить ориентировочно и по локализации повреждений. Принято считать, что объем кровопотери при переломах рёбер составляет 100-150 мл; при переломе плечевой кости — на уровне 200-500 мл; большеберцовой кости — от 350 до 600 мл; бедра — от 800 до 1500 мл; костей таза в пределах 1600-2000 мл.
Патогенез
К основным факторам развития геморрагического шока относятся:
- Выраженный дефицит ОЦК с развитием гиповолемии, что приводит к снижению сердечного выброса.
- Снижение кислородной ёмкости крови (уменьшается доставка кислорода к клеткам и обратная транспортировка углекислого газа. Также страдает процесс доставки питательных веществ и вывода продуктов метаболизма).
- Нарушения гемокоагуляции, вызывающие расстройства в микроциркуляторном сосудистом русле — резкое ухудшение реологических свойств крови — повышения вязкости (сгущение), активизация свертывающей системы крови, агглютинация форменных элементов крови и др.
Как следствие возникает гипоксия, чаще смешанного типа, капилляротрофическая недостаточность, обуславливающая нарушения функции органов/тканей и расстройство жизнедеятельности организма. На фоне нарушения системной гемодинамики и уменьшения интенсивности биологического окисления в клетках включаются (активизируются) адаптационные механизмы, направленные на поддержание жизнедеятельности организма.
Механизмы адаптации прежде всего включают в себя вазоконстрикцию (сужение сосудов), которая возникает из-за активации симпатического звена нейрорегуляции (выделение адреналина, норадреналина) и действия гуморально-гормональных факторов (глкокортикоиды, антидиуретический гормон, АКТТ и т.д.).
Вазоспазм способствует уменьшению ёмкости сосудистого кровеносного русла и централизации процесса кровообращения, что проявляется снижением объёмной скорости кровотока в печени, почках, кишечнике и сосудах нижних/верхних конечностей и создаёт предпосылки в дальнейшем для нарушения функции этих систем и органов. В тоже время, кровоснабжение головного мозга, сердца, лёгких и мышц, участвующих в акте дыхания, продолжает сохраняться на достаточном уровне и нарушается в самую последнюю очередь.
Этот механизм без выраженной активации других механизмов компенсации у здорового человека способен самостоятельно нивелировать утрату около 10–15% ОЦК.
Развитие выраженной ишемии большого тканевого массива способствует накоплению в организме недоокисленных продуктов, нарушениям в системе энергообеспечения и развитию анаэробного метаболизма. В качестве адаптационной реакции на прогрессирующий метаболический ацидоз можно считать усиление катаболических процессов, поскольку они способствует более полной утилизации кислорода различными тканями.
К относительно медленно развивающимся адаптивным реакциям относится перераспределение жидкости (её перемещение в сосудистый сектора из интерстициального пространства). Однако, такой механизм реализуется только в случаях медленно происходящего незначительного кровотечения. К менее эффективным приспособительным реакциям относятся увеличение частоты сердечных сокращений (ЧСС) и тахипноэ.
В патогенезе гиповолемического шока необходимо учитывать и роль развивающегося дисбаланса электролитов, в частности, концентрацию ионов натрия в сосудистом русле и внеклеточном пространстве. В соответствии с их концентрацией плазме крови выделяют изотонический тип дегидратации (при нормальной концентрации), гипертонический (повышенная концентрация) и гипотонический (пониженная концентрация) тип обезвоживания. При этом, каждый их этих типов обезвоживания сопровождается специфическими сдвигами осмолярности плазмы, а также внеклеточной жидкости, что оказывает существенное влияние на характер гемоциркуляции, состояние сосудистого тонуса и функционирование клеток. И это важно учитывать при выборе схем лечения.
Классификация геморрагического шока
Классификация геморрагического шока базируется на стадийности развития патологического процесса, в соответствии с чем выделяют 4 степени геморрагического шока:
- Шок первой степени (компенсированный обратимый шок). Обусловлен незначительным объемом кровопотери, которая достаточно быстро компенсируется функциональными изменениями в работе сердечно-сосудистой деятельности.
- Шок второй степени (субкомпенсированный). Развивающиеся патологические изменения компенсируются не полностью.
- Шок третьей степени (декомпенсированный обратимый шок). Выражены нарушения в различных органах и системах.
- Шок четвертой степени (необратимый шок). Характеризуется крайним угнетением жизненных функций и развитием необратимой полиорганной недостаточности.
Причины
Наиболее частой причиной развития геморрагического шока являются:
- Травмы — повреждения (переломы) крупных костей, ранения внутренних органов/мягких тканей с повреждением крупных сосудов, тупые травмы с разрывом паренхиматозных органов (печени или селезенки), разрыв аневризмы крупных сосудов.
- Заболевания, которые могут вызывать кровопотерю – острые язвы желудка/двенадцатиперстной кишки, цирроз печени с варикозным расширением вен пищевода, инфаркт/гангрена легкого, синдром Маллори-Вейса, злокачественные опухоли органов грудной и клетки ЖКТ, геморрагический панкреатит и другие заболевания с высоким риском разрыва кровеносных сосудов.
- Акушерские кровотечения, возникающее при разрыве трубы/внематочной беременности, отслойке/предлежании плаценты, многоплодной беременности, кесаревом сечении, осложнениях в течении родов.
Симптомы
Клиническая картина геморрагического шока развивается в соответствии с его стадиями. Клинически на первый план выступают признаки кровопотери. На стадии компенсированного геморрагического шока сознание, как правило, не страдает, больной отмечает слабость, может быть несколько возбужденным или спокойным, кожные покровы бледные, на ощупь — холодные конечности.
Важнейшим симптомом на этой стадии является запустевание подкожных венозных сосудов на руках, которые уменьшаются в объеме и становятся нитевидными. Пульс слабого наполнения, учащенный. Артериальное давление, как правило, нормальное, иногда повышенное. Периферическая компенсаторная вазоконстрикция обусловлена гиперпродукцией катехоламинов и возникает практически немедленно после кровопотери. На этом фоне, одновременно у пациента развивается олигурия. При этом, количество выделяемой мочи может снижаться наполовину и даже более. Резко снижается центральное венозное давление, что обусловлено уменьшением венозного возврата. При компенсированном шоке ацидоз чаще отсутствует или носит локальный характер и слабо выражен.
На стадии обратимого декомпенсированного шока признаки расстройств кровообращения продолжают углубляться. В клинической картине, для которой характерны признаки компенсированной стадии шока (гиповолемия, бледность, обильный холодный и липкий пот, тахикардия, олигурия) в качестве основного кардинального симптома выступает гипотония, что свидетельствует о расстройстве механизма компенсации кровообращения. Именно в стадии декомпенсации начинаются нарушения органного (в кишечнике, печени, почках, сердце, головном мозге) кровообращения. Олигурия, которая в стадии компенсации развивается вследствии компенсаторных функций, на этой стадии возникает на базе снижения гидростатического давления крови и расстройств почечного кровотока.
На этой стадии проявляется классическая клиническая картина шока: акроцианоз и похолодание конечностей, усиление тахикардии и появление одышки, глухость сердечных тонов, что свидетельствует об ухудшении сократимости миокарда. В ряде случаев отмечается выпадение отдельных/целой группы пульсовых толчков на периферических артериях и исчезновение при глубоком вдохе тонов сердца, что свидетельствует об крайне низком венозном возврате.
Больной заторможен или находится в состоянии прострации. Развивается одышка, анурия. Диагностируются ДВС-синдром. На фоне максимально выраженной вазоконстрикции периферических сосудов происходит прямой сброс в венозную систему артериальной крови через открывающиеся артериовенозные шунты, что позволяет повысить насыщение кислородом венозной крови. На этой стадии выражен ацидоз, являющийся следствием нарастающей тканевой гипоксии.
Стадия необратимого шока качественно не отличается от декомпенсированного шока, но является стадией ещё более выраженных и глубоких нарушений. Развитие состояния необратимости проявляется вопросом времени и определяется накоплением токсических веществ, гибелью клеточных структур, появлением признаков полиорганной недостаточности. Как правило, на этой стадии отсутствует сознание, пульс на периферийных сосудах практически не определяется, АД (систолическое) на уровне 60 мм рт. ст. и ниже, с трудом определяется, ЧСС на уровне 140/мин., дыхание ослаблено, ритм нарушен, анурия. Эффект от инфузионно-трансфузнонной терапии отсутствует. Длительность этой стадии составляет 12-15 часов и завершается летальным исходом.
Анализы и диагностика
Диагноз геморрагического шока устанавливается на основании осмотра пациента (наличие переломов, наружного кровотечения) и клинической симптоматики, отражающей адекватность гемодинамики (цвет и температура кожных покровов, изменения пульса и АД, подсчета шокового индекса, определение почасового диуреза) и данных лабораторного исследования, включающие: определение ЦВД, гематокрита, КОС крови (показатели кислотно-основного состояния).
Следует учитывать, что оценка объема кровопотери является приблизительной и субъективной и при ее неадекватной оценке можно упустить допустимый интервал выжидания и оказаться перед фактом уже развившейся картины шока.
Лечение
Лечение геморрагического шока условно целесообразно разделить на три этапа. Первый этап — неотложная помощь и интенсивная терапия до обеспечения устойчивости гемостаза. Неотложная помощь при геморрагическом шоке включает:
- Остановку артериального кровотечения временным механическим способом (наложение закрутки/артериального жгута или прижатие артерии к кости выше раны выше места травмы/раны, наложение зажима на кровоточащий сосуд) с фиксацией времени выполненной процедуры. Наложение на раневую поверхность тугой асептической повязки.
- Оценку состояния жизнедеятельности организма (степень угнетения сознания, определение пульса над центральными/периферическими артериями, поверка проходимости дыхательных путей).
- Перемещение тела пострадавшего в правильное положение с немного опущенной верхней половиной туловища.
- Иммобилизацию травмированных конечностей подручным материалом/стандартными шинами. Согревание пострадавшего.
- Адекватное местное обезболивание 0,5–1% раствором Новокаина/Лидокаина. При обширной травме с кровотечением — введение Морфина/Промедола 2–10 мг в сочетании с 0,5 мл раствора атропина или нейролептиков (Дроперидол, Фентанил 2–4 мл) или ненаркотических анальгетиков (Кетамин, Анальгин), при тщательном контроле дыхания и показателей гемодинамики.
- Ингаляция смесью кислорода и закиси азота.
- Адекватную инфузионно-трансфузионную терапию, что позволяет как восстановить потерю крови, так и нормализовать гомеостаз. Терапию после потери крови начинают проводить с установки катетера на центральной/крупной периферической вене и оценки объёма кровопотери. При необходимости введения большого объема плазмозамещающих жидкостей и растворов можно использовать 2-3 вены. Для этой цели более целесообразно использовать кристаллоидные и полиионные сбалансированные растворы. Из кристаллоидных растворов: раствор Рингера-Локка, изотонический раствор Натрия хлорида, Ацесоль, Дисоль, Трисоль, Квартасоль, Хлосоль. Из коллоидных: Гекодез, Полиглюкин, Реоглюман, Реополиглюкин, Неогемодез. При слабом эффекте или его отсутствии вводятся синтетические коллоидные плазмозаменители, обладающие гемодинамическим действия (Декстран, Гидроксиэтилкрахмал в объёмах 800-1000 мл. Отсутствие тенденции к нормализации гемодинамических показателей является показанием к внутривенному введению симпатомиметиков (Фенилэфрин, Допамин, Норэпинефрин) и назначения глюкокортикоидов (Гидрокортизон, Дексаметазон, Преднизолон).
- При выраженных нарушениях гемодинамики необходим перевод пациента на ИВЛ.
Второй/третий этапы интенсивной терапии при геморрагическом шоке проводятся в специализированном стационаре, и направлены на коррекцию гемической гипоксии и адекватное обеспечение хирургического гемостаза. Основными препаратами являются компоненты крови и натуральные коллоидные растворы (Протеин, Альбумин).
Интенсивная терапия проводится под мониторингом параметров гемодинамики, кислотно-основного состояния, газообмена, функции жизненно важных органов (почек, лёгких, печени). Большое значение отводится купированию вазоконстрикции, для чего можно использовать как мягко действующие препараты (Эуфиллин, Папаверин, Дибазол) и препараты с более выраженным действием (Клофелин, Даларгин, Инстенон). При этом дозы препаратов, путь и скорость введения подбирают исходя из недопущения артериальной гипотонии.
Алгоритм неотложной помощи при гиповолемическом шоке схематически представлен ниже.
Читайте также:


