Септический шок в анестезиологии
Септический (инфекционно-токсический, бактериемический) шок (СШ) – разновидность шока, при котором пусковым фактором служит инфекция, приводящая в сочетании с особой иммунологической и гуморальной реакцией организма к тяжелым системным расстройствам и прежде всего к нарушению микроциркуляции и адекватной перфузии тканей оксигенированной кровью.
Этиопатогенез. СШ может быть вызван как грамположительными (у 30% больных), так и грамотрицательными бактериями (у 70% больных). Меньшее значение имеют вирусные и грибковые инфекции. Чаще встречается и тяжелее протекает у маленьких детей и лиц старше 60 лет. Летальность при СШ выше, чем при других его формах, и достигает 50 — 60 % в случаях шока, вызванного грамположительными микроорганизмами, и 80— 90 % — грамотрицательными бактериями.

Нарушения гемодинамики при СШ проявляются в виде двух основных синдромов. Гипердинамический синдром характеризуется высокими показателями сердечного выброса, работы сердца и сократимости миокарда. Общее периферическое сопротивление нормальное или повышенное. При гиподинамическом синдроме показатели сердечного выброса, работы сердца и сократимости снижены. Общее периферическое сопротивление высокое, но резко падает в терминальной фазе СШ.
Нарушения функции ЦНС при СШ неспецифичны, однако ее депрессия вплоть до развития коматозного состояния возникает быстрее и чаще, чем при других видах шока.
В развитии дыхательной недостаточности определенное значение имеет ухудшение сократимости дыхательных мышц вследствие их гипоперфузии. Дыхательная недостаточность при СШ усугубляется повышением требований к вентиляции в связи с лихорадкой, ознобами, гиперпродукцией углекислоты и повышением работы сердца. Гипервентиляция при СШ связана с гипертермией, а также с прямым действием токсинов бактерий на дыхательный центр. Кроме того, следует учитывать компенсаторный характер дыхательного алкалоза в ответ на значительный избыток органических кислот в организме, который еще более ухудшает оксиге-нацию тканей вследствие сдвига кривой диссоциации оксигемоглобина влево.
Одним из показателей ухудшения метаболизма является гипергликемия, обусловленная не только и не столько гиперкатехоламинемией, сколько депрессией процесса окисления глюкозы. При СШ снижается продукция высокоэнергических фосфатов, а благодаря развитию гипоксии и действию бактериальных токсинов увеличивается выброс в кровоток протеаз из поджелудочной железы и клеток ретикулоэндотелиальной системы. В общем активация патологических ферментов при сепсисе идет в трех участках: в системе кининов, системе свертывания и системе фибринолиза.
Большое значение при СШ приобретает проблема коагулопатических расстройств, в генезе которых участвуют этиологические факторы шока (токсины бактерий), а также повреждения органов и тканей, связанные с гипоперфузией и гипоксией. Под влиянием бактериемии или эндотоксемии при СШ очень рано возникают спазм печеночных вен, портальная гипертензия и застой. Перфузионная недостаточность печени быстро приводит к нарушениям ее функции, а также к уменьшению образования протромбина и повышению фибринолитической активности крови. Однако, несмотря на это, гиперкоагуляция сохраняется, так как уровень фибриногена в крови остается высоким даже при тяжелой печеночной недостаточности, а содержание эндогенного гепарина — одной из основных систем противосвертывания — снижается. Это и определяет возникновение диссеминированной внутрисосудистой коагуляции у больных. Коагулопатия потребления — ведущая причина геморрагических осложнении СШ.
Нарушения реологии крови и гиперкоагуляция имеют первостепенное значение в развитии почечной недостаточности. Особенностью этого вида шока является более быстрое развитие необратимых изменений в почке вплоть до массивного тубулярного некроза.
В возникновении и развитии СШ существенная роль принадлежит ишемическому повреждению поджелудочной железы. Степень этого повреждения может быть различной — от активации секреторной функции с выбросом протеолитических ферментов в кровоток (трипсин, калликреин) до асептического панкреонекроза. Значительное повышение секреции протеаз в просвет кишечника, застой крови в мезентериальной системе сопровождаются ухудшением кровоснабжения желудка и кишечника и являются ведущими причинами часто возникающего в поздних стадиях СШ геморрагического эрозивного гастроэнтероколита.
Подавление иммунологических сил организма и развитие аутоиммунных реакций на любое травматическое воздействие, в том числе хирургическое вмешательство, в значительной степени определяют возникновение СШ, его тяжесть и высокую летальность больных.
Шок – это форма критического состояния организма, проявляющаяся множественной органной дисфункцией, каскадно развивающейся на основе генерализованного кризиса циркуляции и, как правило, заканчивающаяся летально без лечения.
Шоковый фактор – это любое воздействие на организм, которое по силе превышает адаптивные механизмы. При шоке изменяются функции дыхания, сердечно-сосудистой системы, почек, нарушаются процессы микроциркуляции органов и тканей и метаболические процессы.
Этиология и патогенез
Шок – это заболевание полиэтиологической природы. В зависимости от этиологии возникновения виды шока могут быть различны.
1. Травматический шок:
1) при механических травмах – переломы костей, раны, сдавление мягких тканей и др.;
2) при ожоговых травмах (термические и химические ожоги);
3) при воздействиях низкой температуры – холодовой шок;
4) при электротравмах – электрический шок.
2. Геморрагический, или гиповолемический, шок:
1) развивается в результате кровотечения, острой кровопотери;
2) в результате острого нарушения водного баланса происходит обезвоживание организма.
3. Септический (бактериально-токсический) шок (генерализованные гнойные процессы, причиной которых является грамотрицательная или грамположительная микрофлора).
4. Анафилактический шок.
5. Кардиогенный шок (инфаркт миокарда, острая сердечная недостаточность). Рассмотрен в разделе неотложные состояния в кардиологии.
При всех видах шока основным механизмом развития является вазодилатация, и в результате этого увеличивается емкость сосудистого русла, гиповолемия – уменьшается объем циркулирующей крови (ОЦК), так как имеют место быть различные факторы: кровопотеря, перераспределение жидкости между кровью и тканями или несоответствие нормального объема крови увеличивающейся емкости сосудистого русла. Возникшее несоответствие ОЦК и емкости сосудистого русла лежит в основе уменьшения сердечного выброса и расстройства микроциркуляции. Последнее приводит к серьезным изменениям в организме, так как именно здесь осуществляется основная функция кровообращения – обмен веществ и кислорода между клеткой и кровью. Наступает сгущение крови, повышение ее вязкости и внутрикапиллярное микротромбообразование. Впоследствии нарушаются функции клеток вплоть до их гибели. В тканях начинают преобладать анаэробные процессы над аэробными, что приводит к развитию метаболического ацидоза. Накопление продуктов обмена веществ, в основном молочной кислоты, усиливает ацидоз.
Особенностью патогенеза септического шока является нарушение кровообращения под действием бактериальных токсинов, что способствует открытию артериовенозных шунтов, и кровь начинает обходить капиллярное русло и устремляется из артериол в венулы. За счет уменьшения капиллярного кровотока и действия бактериальных токсинов именно на клетку, питание клеток нарушается, что приводит к снижению снабжения клеток кислородом.
При анафилактическом шоке под влиянием гистамина и других биологически активных веществ капилляры и вены теряют свой тонус, при этом периферическое сосудистое русло расширяется, увеличивается его емкость, что приводит к патологическому перераспределению крови. Кровь начинает скапливаться в капиллярах и венулах, вызывая нарушение сердечной деятельности. Сформировавшееся при этом ОЦК не соответствует емкости сосудистого русла, соответственно снижается минутный объем сердца (сердечный выброс). Возникший застой крови в микроциркуляторном русле ведет к расстройству обмена веществ и кислорода между клеткой и кровью на уровне капиллярного русла.
Вышеперечисленные процессы приводят к ишемии печеночной ткани и нарушению ее функций, что дополнительно усугубляет гипоксию в тяжелых стадиях развития шока. Нарушается детоксикационная, белковообразующая, гликогенобразующая и другие функции печени. Расстройство магистрального, регионального кровотока и микроциркуляции в почечной ткани способствует нарушению как фильтрационной, так и концентрационной функции почек со снижением диуреза от олигурии вплоть до анурии, что приводит к накоплению в организме больного азотистых шлаков, таких как мочевина, креатинин, и других токсических продуктов обмена веществ. Нарушаются функции коры надпочечников, снижается синтез кортикостероидов (глюкокортикоиды, минералокортикоиды, андрогенные гормоны), что усугубляет происходящие процессы. Расстройство кровообращения в легких объясняет нарушение внешнего дыхания, снижается альвеолярный газообмен, возникает шунтирование крови, формируются микротромбозы, и как следствие – развитие дыхательной недостаточности, которая усугубляет гипоксию тканей.
Геморрагический шок представляет собой реакцию организма на возникшую кровопотерю (потеря 25–30 % ОЦК приводит к тяжелому шоку).
В возникновении ожогового шока главенствующую роль играют болевой фактор и массивная плазмопотеря. Быстро развивающаяся олигурия и анурия. Развитие шока и его тяжесть характеризуются объемом и скоростью кровопотери. На основании последнего различают компенсированный геморрагический шок, декомпенсированный обратимый шок и декомпенсированный необратимый шок.
При компенсированном шоке отмечается бледность кожи, холодный липкий пот, пульс становится малого наполнения и частый, артериальное давление остается в пределах нормы или несколько снижено, но незначительно, уменьшается мочеотделение.
При некомпенсированном обратимом шоке кожа и слизистые оболочки приобретают цианотичную окраску, больной становится заторможенным, пульс малый и частый, отмечается значительное снижение артериального и центрального венозного давления, развивается олигурия, индекс Альговера повышен, на ЭКГ отмечается нарушение обеспечения миокарда кислородом. При необратимом течении шока сознание отсутствует, артериальное давление снижается до критических цифр и может не определяться, кожные покровы мраморного цвета, развивается анурия– прекращение мочеотделения. Индекс Альговера высокий.
Для оценки тяжести геморрагического шока большое значение имеет определение ОЦК, объема кровопотери.
Карта анализа тяжести шока и оценка полученных результатов приведены в таблице 4 и таблице 5.
Карта анализа тяжести шока
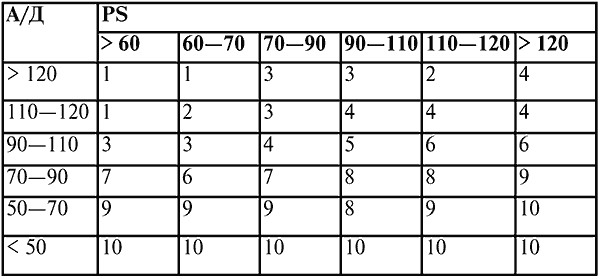
Оценка результатов по сумме баллов

Шоковый индекс, или индекс Альговера, представляет отношение частоты пульса к систолическому давлению. При шоке первой степени индекс Альговера не превышает 1. При второй степени – не более 2; при индексе более 2 – состояние характеризуют как несовместимое с жизнью.
Анафилактический шок – это комплекс различных аллергических реакций немедленного типа, достигающих крайней степени тяжести.
Различают следующие формы анафилактического шока:
1) сердечно-сосудистая форма, при которой развивается острая недостаточность кровообращения, проявляющаяся тахикардией, часто с нарушением ритма сердечных сокращений, фибрилляцией желудочков и предсердий, снижением артериального давления;
2) респираторная форма, сопровождающаяся острой дыхательной недостаточностью: одышкой, цианозом, стридорозным, клокочущим дыханием, влажными хрипами в легких. Это обусловлено нарушением капиллярного кровообращения, отеком легочной ткани, гортани, надгортанника;
3) церебральная форма, обусловленная гипоксией, нарушением микроциркуляции и отеком мозга.
По тяжести течения различают 4 степени анафилактического шока.
I степень (легкая) характеризуется зудом кожи, появлением сыпи, головной боли, головокружения, чувством прилива к голове.
II степень (средней тяжести) – к ранее указанным симптомам присоединяются отек Квинке, тахикардия, снижение артериального давления, повышение индекса Альговера.
III степень (тяжелая) проявляется потерей сознания, острой дыхательной и сердечно-сосудистой недостаточностью (одышка, цианоз, стридорозное дыхание, малый частый пульс, резкое снижение артериального давления, высокий индекс Альговера).
IV степень (крайне тяжелая) сопровождается потерей сознания, тяжелой сердечно-сосудистой недостаточностью: пульс не определяется, артериальное давление низкое.
Лечение. Лечение проводят по общим принципам лечения шока: восстановление гемодинамики, капиллярного кровотока, применение сосудосуживающих средств, нормализация ОЦК и микроциркуляции.
Специфические мероприятия направлены на инактивацию антигена в организме человека (например, пенициллиназы или b-лактамазы при шоке, вызванном антибиотиками) или предупреждающие действие антигена на организм – антигистаминные препараты и мембраностабилизаторы.
1. Внутривенно инфузия адреналина до стабилизации гемодинамики. Можно использовать допмин 10–15 мкг/кг/мин, а при явлениях бронхоспазма и b-адреномиметики: алупент, бриканил капельно внутривенно.
2. Инфузионная терапия в объеме 2500–3000 мл с включением полиглюкина и реополиглюкина, если только реакция не вызвана этими препаратами. Натрия бикарбонат 4 %-ный 400 мл, растворы глюкозы для восстановления ОЦК и гемодинамики.
3. Мембраностабилизаторы внутривенно: преднизолон до 600 мг, аскорбиновая кислота 500 мг, троксевазин 5 мл, этамзилат натрия 750 м г, цитохром-С 30 мг (указаны суточные дозы).
4. Бронхолитики: эуфиллин 240–480 мг, ношпа 2 мл, алупент (бриканил) 0,5 мг капельно.
5. Антигистаминные препараты: димедрол 40 мг (супрастин 60 мг, тавегил 6 мл), циметидин 200–400 мг внутривенно (указаны суточные дозы).
6. Ингибиторы протеаз: трасилол 400 тыс. ЕД, контрикал 100 тыс. ЕД.
Травматический шок – это патологическое и критическое состояние организма, возникшее в ответ на травму, при котором нарушаются и угнетаются функции жизненно важных систем и органов. В течение травматологического шока различают торпидную и эректильную фазы.
По времени возникновения шок может быть первичным (1–2 ч) и вторичным (более 2 ч после травмы).
Эректильная стадия или фаза возникновения. Сознание сохраняется, больной бледный, беспокойный, эйфоричный, неадекватен, может кричать, куда-то бежать, вырываться и т. п. В эту стадию происходит выброс адреналина, за счет чего давление и пульс некоторое время могут оставаться в норме. Длительность этой фазы от нескольких минут и часов до нескольких дней. Но в большинстве случаев носит короткий характер.
Торпидная фаза сменяет эректильную, когда больной становится вялым и адинамичным, снижается артериальное давление и появляется тахикардия. Оценки обёма тяжести травмы приведены в таблице 6.
Оценка объема тяжести травмы

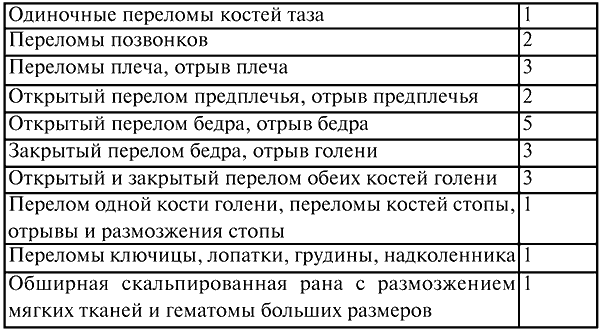
После подсчета баллов получившееся число умножают на коэффициент.
1. При наличии повреждений, не указанных в перечне объема и тяжести травмы, начисляется количество баллов по типу повреждения, по тяжести соответствующего одному из перечисленных.
2. При наличии соматических заболеваний, снижающих адаптационные функции организма, найденную сумма баллов умножается на коэффициент от 1,2 до 2,0.
3. В возрасте 50–60 лет сумма баллов умножается на коэффициент 1,2, старше – на 1,5.
Лечение. Основные направления в лечении.
1. Устранение действия травмирующего агента.
2. Устранение гиповолемии.
3. Устранение гипоксии.
Обезболивание осуществляется введением анальгетиков и наркотиков, выполнением блокад. Оксигенотерапия, по необходимости интубация трахеи. Возмещение кровопотери и ОЦК (плазма, кровь, реополиглюкин, полиглюкин, эритромасса). Нормализация обмена веществ, так как развивается метаболический ацидоз, вводится хлористый кальций 10 %-ный – 10 мл, хлористый натрий 10 %-ный – 20 мл, глюкоза 40 %-ная – 100 мл. Борьба с витаминным дефицитом (витамины группы В, витамин С).
Гормонотерапия глюкокортикостероидами – преднизалон внутривенно однократно 90 мл, а в последующем по 60 мл каждые 10 ч.
Стимуляция сосудистого тонуса (мезатон, норадреналин), но только при восполненном объеме циркулирующей крови. В проведении противошоковой терапии участвуют и антигистаминные препараты (димедрол, сибазон).
Геморрагический шок – это состояние острой сердечно-сосудистой недостаточности, которая развивается после потери значительного количества крови и приводит к уменьшению перфузии жизненно важных органов.
Этиология: травмы с повреждением крупных сосудов, острая язва желудка и двенадцатиперстной кишки, разрыв аневризмы аорты, геморрагический панкреатит, разрыв селезенки или печени, разрыв трубы или внематочная беременность, наличие долек плаценты в матке и др.
По клиническим данным и величине дефицита объема крови различают следующие степени тяжести.
1. Не выраженная – клинические данные отсутствуют, уровень артериального давления в норме. Объем кровопотери до 10 % (500 мл).
2. Слабый – минимальная тахикардия, небольшое снижение артериального давления, некоторые признаки периферической вазоконстрикции (холодные руки и ноги). Объем кровопотери составляет от 15 до 25 % (750—1200 мл).
3. Умеренная – тахикардия до 100–120 ударов в 1 мин, снижение пульсового давления, систолическое давление 90—100 мм рт. ст., беспокойство, потливость, бледность, олигурия. Объем кровопотери составляет от 25 до 35 % (1250–1750 мл).
4. Тяжелая – тахикардия более 120 ударов в мин, систолическое давление ниже 60 мм рт. ст., часто не определяется тонометром, ступор, крайняя бледность, холодные конечности, анурия. Объем кровопотери составляет более 35 % (более 1750 мл). Лабораторно в общем анализе крови снижение уровня гемоглобина, эритроцитов и гематокрита. На ЭКГ обнаруживаются неспецифические изменения сегмента ST и зубца Т, которые обусловлены недостаточной коронарной циркуляцией.
Лечение геморрагического шока предусматривает остановку кровотечения, применение инфузионной терапии для восстановления ОЦК, использование сосудосуживающих средств или сосудорасширяющих средств в зависимости от ситуации. Инфузионная терапия предусматривает внутривенно введение жидкости и электролитов в объеме 4 л (физиологический раствор, глюкоза, альбумин, полиглюкин). При кровотечении показано переливание одногруппной крови и плазмы в общем объеме не менее 4 доз (1 доза составляет 250 мл). Показано введение гормональных препаратов, таких как мембраностабилизаторы (преднизолон 90—120 мг). В зависимости от этиологии проводят специфическую терапию.
Септический шок – это проникновение возбудителя инфекции из его первоначального очага в систему крови и распространение его по всему организму. Возбудителями могут быть: стафилококковая, стрептококковая, пневмококковая, менингококковая и энтерококковая бактерии, а также эшерихии, сальмонеллы и синегнойная палочка и др. Септический шок сопровождается нарушением функции легочной, печеночной и почечной систем, нарушением системы свертывания крови, что приводит к возникновению тромбогеморрагического синдрома (синдром Мачабели), развивающегося во всех случаях сепсиса. На течение сепсиса влияет вид возбудителя, особенно важно это при современных методах лечения. Лабораторно отмечается прогрессирующая анемия (за счет гемолиза и угнетения кроветворения). Лейкоцитоз до 12 109/л, однако в тяжелых случаях, так как формируется резкое угнетение органов кроветворения, может наблюдаться и лейкопения.
Клинические симптомы бактериального шока: озноб, высокая температура, гипотензия, сухая теплая кожа – вначале, а позже – холодная и влажная, бледность, цианоз, нарушение психического статуса, рвота, понос, олигурия. Характерен нейтрофилез со сдвигом лейкоцитарной формулы влево вплоть до миелоцитов; СОЭ увеличивается до 30–60 мм/ч и более. Уровень содержания билирубина крови увеличен (до 35–85 мкмоль/л), что также относится и к содержанию в крови остаточного азота. Свертывание крови и протромбиновый индекс понижены (до 50–70 %), снижено содержание кальция и хлоридов. Общий белок крови снижен, что происходит за счет альбуминов, а уровень глобулинов (альфа-глобулины и b-глобулины) повышается. В моче белок, лейкоциты, эритроциты и цилиндры. Уровень содержания хлоридов в моче понижен, а мочевины и мочевой кислоты – повышен.
Лечение в первую очередь носит этиологический характер, поэтому до назначения антибактериальной терапии необходимо определить возбудитель и его чувствительность к антибиотикам. Антимикробные средства должны использоваться в максимальных дозах. Для терапии септического шока необходимо использовать антибиотики, которые перекрывают весь спектр грамотрицательных микроорганизмов. Наиболее рациональной является комбинация цефтазидима и импинема, которые доказали свою эффективность по отношению к синегнойной палочке. Такие препараты, как клиндамицин, метронидазол, тикарциллин или имипинем применяются как медикаменты выбора при возникновении резистентного возбудителя. Если из крови высеяны стафилококки, нужно обязательно начинать лечение препаратами группы пенициллина. Лечение гипотонии заключается на первом этапе лечения в адекватности объема внутрисосудистой жидкости. Используют кристаллоидные растворы (изотонический раствор хлорида натрия, Рингер-лактат) или коллоиды (альбумин, декстран, поливинилпирролидон). Преимущество коллоидов состоит в том, что при их введении наиболее быстро достигаются нужные показатели давления заполнения и долго остаются такими. Если нет эффекта, то применяют инотропную поддержку и (или) вазоактивные препараты. Допамин является препаратом выбора, поскольку он является кардиоселективным b-адреномиметиком. Кортикостероиды снижают общую реакцию на эндотоксины, способствуют ослаблению лихорадки и дают положительный гемодинамический эффект. Преднизолон в дозе 60к 90 мг в сутки.
, MD, MBA, Stanford University Medical Center
Last full review/revision February 2018 by Paul M. Maggio, MD, MBA

Сепсис представляет собой спектр заболеваний с риском смерти, колеблющимся от умеренного (например, 10%) до значительного (например, > 40%) в зависимости от различных возбудителей и факторов со стороны хозяина, наряду со своевременностью выявления и предоставления соответствующего лечения.
Септический шок является разновидностью сепсиса со значительно повышенным уровнем смертности в связи с серьезными нарушениями кровообращения и/или клеточного метаболизма. Септический шок предполагает наличие персистирующей гипотонии (определяется как потребность в вазопрессорах для поддержания среднего артериального давления ≥ 65 мм рт. ст., и уровень сывороточного лактата > 18 мг/дл [2 ммоль/л], несмотря на реанимационные мероприятия, проведенные в достаточном объеме [1]).
Понятие синдрома системного воспалительного ответа (ССВО), которое определяется специфическими нарушениями жизненно важных функций и результами лабораторных исследований, уже давно используется для выявления сепсиса на ранних стадиях. Однако было обнаружено, что критерии ССВО имеют недостаточную чувствительность и специфичность при повышенном риске смерти, что является основным аспектом использования такой концептуальной модели. Отсутствие специфичности может быть обусловлено тем, что ССВО чаще является адаптивным, а не патологическим ответом.
Справочные материалы
1. Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA 315:801–810, 2016.
Этиология
Большинство случаев септического шока вызвано внутрибольничными грамотрицательными бактериями или грамположительными кокками и часто возникает у пациентов с ослабленным иммунитетом и у пациентов с хроническими заболеваниями. Реже возбудителями являются грибы рода Candida. Следует заподозрить послеоперационную инфекцию (глубокую или поверхностную) в качестве причины септического шока у пациентов, которые недавно перенесли операцию. Неспецифическая, редкая форма шока, вызванная токсинами стафилококков и стрептококков называется синдромом токсического шока.
Септический шок встречается чаще у новорожденных ( Неонатальный сепсис), у пожилых людей и беременных женщин. Предрасполагающие факторы включают:
Лейкопению (особенно, связанную с раком или лечением цитотоксическими лекарственными средствами)
Наличие инвазивных устройств (в том числе эндотрахеальных трубок, сосудистых или мочевых катетеров, дренажей и других инородных материалов)
Первоочередным лечением являются антибиотики или кортикостероиды
К наиболее распространенным локализациям инфекции относятся легкие, мочевые и желчные пути и ЖКТ.
Патофизиология
Патогенез септического шока полностью не изучен. Воспалительные агенты (например, бактериальный токсин) провоцируют выработку провоспалительных медиаторов, включая ФНО и ИЛ-1. Эти цитокины вызывают нейтрофильно-эндотелиальную клеточную адгезию, активируют механизмы свертывания крови и обуславливают образование микротромбов. Они также способствуют высвобождению других медиаторов, включая лейкотриены, липоксигеназу, гистамин, брадикинин, серотонин и IL-2. Им противостоят противовоспалительные медиаторы, такие как IL-4 и IL-10, в результате механизма обратной отрицательной связи.
Сначала артерии и артериолы расширяются, уменьшается периферическое артериальное сопротивление; сердечный выброс, как правило, увеличивается. Этот этап называется тепловым шоком. Позже, сердечный выброс может уменьшиться, падает АД (с или без увеличения периферического сопротивления), и появляются типичные признаки шока.
Даже на стадии увеличенного сердечного выброса, вазоактивные медиаторы приводят к тому, что кровоток минует капилляры (распределительный дефект). Ослабленный капиллярный ток из этого шунтирования наряду с капиллярной обструкцией микротромбами уменьшают доставку кислорода и снижают выведение углекислого газа и других продуктов распада. Гипоперфузия приводит к дисфункции, а иногда и к недостаточности одного или более органов, включая почки, легкие, печень, мозг и сердце.
Коагулопатия может развиться из-за внутрисосудистой коагуляции с участием основных факторов свертывания крови, усиленного фибринолиза, и чаще комбинации обоих.
Клинические проявления
Симптомы и признаки сепсиса могут быть малозаметными и часто легко принимаются за проявления других заболеваний (например, белая горячка, первичная дисфункция сердца, эмболия легочной артерии), особенно у послеоперационных больных. У пациентов с сепсисом, как правило, отмечаются: лихорадка, тахикардия, обильное потоотделение и тахипноэ; АД остается в норме. Также могут присутствовать другие признаки инфекции, являющейся ричиной сепсиса. По мере ухудшения состояния больного с сепсисом или при развитии септического шока ранним симптомом, особенно у пожилых людей и маленьких детей, может быть спутанность сознания или снижение активности. АД снижается, однако кожа остается парадоксально теплой. Позже, конечности становятся прохладными и бледными с периферическим цианозом. Дисфункция органов приводит к появлению дополнительных симптомов и признаков в зависимости от пораженного органа (например, олигурия, одышка).
Диагностика
АД, частота сердечных сокращений и мониторинг кислородного статуса
Общий анализ крови с лейкоцитарной формулой, уровень электролитов, креатинина и лактата
Показания инвазивного центрального венозного давления (ЦВД), Pa O 2 и сатурации кислорода в центральной вене (ScvO2)
Бактериологический посев крови, мочи и других потенциальных очагов инфекции, в том числе из ран у пациентов после операции
Сепсис подозревают, когда у пациента с известной инфекцией развиваются системные симптомы воспаления или органной дисфункции. Аналогичным образом, у пациентов с необъяснимыми признаками системного воспаления необходимо изучить наличие инфекционных заболеваний в анамнезе, провести медицинский осмотр и лабораторные исследования, которые включают общий анализ мочи и бактериологический посев мочи (особенно у пациентов с постоянными катетерами), бактериологический посев крови и посевы других подозрительных жидкостей организма. Пациентам с подозрением на хирургическую или скрытую причину сепсиса может потребоваться УЗИ, КТ или МРТ в зависимости от предполагаемого источника. При тяжелом сепсисе уровни C- реактивного белка и прокальцитонина в крови часто повышены и могут облегчить постановку диагноза, но эти показатели не являются специфичными. Диагноз основывается прежде всего на клинических проявлениях.
Другие причины шока (например, гиповолемия, инфаркт миокарда) должны быть исключены с помощью анамнеза, медицинского осмотра, электрокардиограммы и анализа кардиомаркеров в сыворотке крови. Даже в отсутствие ИМ гипоперфузия, обусловленная сепсисом, может привести к появлению признаков ишемии на электрокардиограмме, включая неспецифические отклонения ST-T, инверсии зубца T, наджелудочковые и желудочковые экстрасистолии.
Важно выявить дисфункцию органа как можно раньше. Был разработан ряд систем оценки, но шкала динамической оценки органной недостаточности (шкала SOFA) и шкала quick SOFA (qSOFA) были одобрены в отношении риска смерти и являются относительно простыми в использовании.
С помощью критериев шкалы qSOFA выявляют пациентов, которым необходимо провести дальнейшие клинические и лабораторные исследования (должны присутствовать все 3 критерия):
Частота дыхания ≥ 22/мин
Систолическое АД ≤ 100 мм рт. ст.
Оценка по шкале SOFA является более надежной, но требует проведения лабораторных исследований ( Шкала динамической оценки органной недостаточности (SOFA)).
≥ 400 мм рт. ст. (53,3 кПа)
12,0 мг/дл (204 мкмоль/л)
САД ≥ 70 мм рт. ст.
САД 15 мкг/кг/мин в течение ≥ 1 ч
Эпинефрин > 0,1 мкг/кг/мин в течение ≥ 1 ч
Норэпинефрин > 0,1 мкг/кг/мин в течение ≥ 1 ч
5,0 мг/дл (440 мкмоль/л)
* Более высокий балл указывает на лучшее состояние неврологических функций.
F IO 2 = фракция вдыхаемого O2; кПа = килопаскали; САД = среднее артериальное давление; Pao2 = парциальное давление кислорода артериальной крови.
По материалам Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA 315:801-810, 2016.
Проводят ОАК, ГСАК, рентгенологическое исследование органов грудной клетки, анализ уровней электролитов в сыворотке, азота, мочевины крови и креатинина, P co 2 и проб печени. Измерение уровня лактата в сыворотке или сатурации кислорода в центральной вене (ScvO2) (или сразу оба анализа) могут помочь в определении лечения. Количество лейкоцитов может быть уменьшено ( 4 000/мкл) или увеличено (> 15 000/ мкл ), а количество ПМЯ-клеток может снизиться до 20%. В ходе развития сепсиса количество лейкоцитов может увеличиваться или уменьшаться в зависимости от тяжести сепсиса или шока, иммунологического статуса пациента и этиологии инфекции. Одновременное использование кортикостероидов может увеличить количество лейкоцитов и, таким образом, маскировать изменения в анализах, связанные с проявлениями болезни.
Гипервентиляция с дыхательным алкалозом (низкий Pa co 2 и повышенный pH крови) появляется рано, как реакция компенсации метаболического ацидоза. Уровень сывороточного бикарбоната обычно низкий, а уровни лактата в сыворотке и крови повышаются. Шок прогрессирует, метаболический ацидоз ухудшается, и снижается pH крови. Раннее развитие гипоксемической дыхательной недостаточности приводит к снижению соотношения PaO2:F IO 2, а иногда и к выраженной гипоксемии с Pa o 2 70 мм рт. ст. Диффузные инфильтраты на рентгенограмме грудной клетки могут появляться вследствие развития острого респираторного дистресс-синдрома (ОРДС). Уровень мочевины и креатинина обычно прогрессивно возрастают в результате почечной недостаточности. Значения билирубина и трансаминазы могут повыситься, хотя клинически выраженная печеночная недостаточность редко встречается у пациентов с нормальными исходными функциональными пробами печени.
У большинства пациентов с тяжелым сепсисом развивается относительная недостаточность коры надпочечников (т. е. нормальный или немного повышенный исходный уровень кортизола, который не увеличивается в значительной степени в ответ на дальнейший стресс или экзогенный АКТГ). Функция надпочечников может быть проверена путем измерения сывороточного кортизола в 8 часов утра , уровень 5 мг/дл считается неадекватным. При другом подходе уровень кортизола можно измерять до и после введения 250 мкг синтетического AКТГ; повышение уровня 9 мкг/дл считают недостаточным. Тем не менее, при резистентном септическом шоке проведение анализов на кортизол не требуется перед началом кортикостероидной терапии.
Измерения гемодинамики с помощью центрально-венозного или легочно-артериального катетера ( Мониторинг и обследование тяжелобольных пациентов : Методика) могут использоваться, когда неясен тип шока или необходимы большие объемы жидкости (например, > 4–5 литров 0,9% физиологического раствора в течение более, чем 6–8 ч). Эхокардиография, проведенная у постели больного в ОИТ, является практичным и неинвазивным альтернативным методом контроля гемодинамики. При септическом шоке сердечный выброс увеличивается, а периферическое сосудистое сопротивление уменьшается, в то время как при других формах шока сердечный выброс, как правило, снижается, а периферическое сосудистое сопротивление увеличивается. Показатели ЦВД и давления заклинивания в лёгочной артерии (ДЗЛА) вероятнее всего будут в норме при септическом шоке, в отличие от гиповолемического, обструктивного или кардиогенного шока.
Читайте также:


