Септический шок клиника диагностика интенсивная терапия

Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
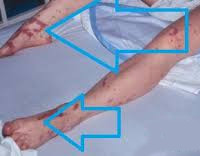
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
- при тяжелой септицемии с лейкоцитозом эффективно сочетание карбенициллина с цефалоспоринами и гентамицином;
- при септическом очаге в брюшной полости или в малом тазу: гентамицин с линкомицином и ампициллином;
- в случае генерализованной инфекции, вызванной бактероидами, эффективны линкомицин или клиндамицин;
- уремические формы инфекции лечатся гентамицином с пенициллином или цефалоспоринами с канамицином и левомицетаном.
Pneumococcus или стрептококки групп А,В,С,G
Цефалоспорины*, ванко мицин, эритромицин
— инфекция мочевых путей
— эндокардит и другие серьезные инфекции
Ампициллин или амоксициллин
Норфлоксацин, ципро флоксацин
Ванкомицин + гентами цин
— метициллин-
чувствительные
— метициллин-
резистентные
Полусинтетические
пенициллины
Ванкомицин
Триметоприм-сульфа-метоксазол
Клиндамицин, ванко мицин
Аэробные грамотрицательные бактерии:
Klebsiella, Enterobacter, Serratia, Proteus (индолполо жительные)
Ампициллин или триметоприм -сульфаметоксазол
Цефотаксим или цефтриаксон
Цефотаксим или цефтриаксон
Азтреонам, аминогли козиды
или
амоксициллин
сульфа-метоксазол,
цефотаксин,
цефтриаксон
Тикарциллин или цефтазидим + аминогликозид
Азтреонам или имипе нем + аминогликозид
- метилпреднизолон вводится в дозе 30 мг/кг болюсно, затем 4—5мг/кг — поддерживающая доза.
- дексаметазон — 5 мг/кг в/в;
- ретаболил или феноболил 1 мл в/ м 1 раз в неделю;
Несмотря на все успехи теоретической и практической медицины, сепсис остается одной из нерешенных проблем XX века. Об этом красноречиво свидетельствуют следующие цифры: летальность при септическом шоке в 1909 г. была 41%, в 1985 г. она составила 40% (Sanford J., 1985).
Синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) представляет собой приобретенное расстройство гемостаза, при котором одновременно или последовательно наблюдается массивное микротромбообразование, избыточное потребление факторов свертывания, активация фибринолиза и кровоточивос.
Артериальная гипертония относится к числу основных причин сердечно-сосудистой смертности и распространенность ее среди населения, согласно современным критериям, составляет около 50%. Опасность вынашивания беременности на фоне гипертонической болезни определяется риском развития сочетанного гестоза.
Лечение ДВС-синдрома зависит от стадии процесса. В первую очередь необходимо устранить причину, вызвавшую активацию тромбокиназы (тромбопластина). Если видимая причина отсутствует, то необходимо начать посиндромную терапию, направленную на восстановление адекватной гемодинамики, микроциркуляции, дых.
Прежде всего, для дальнейшего изложения материала надо определиться терминологически, поскольку это в значительной степени упорядочивает представление материала и придает ясность его восприятию. К примеру, преэклампсию называли родильными судорогами, родильным нефритом, эклампсией и преэкламптическо.
Для диагностики ДВС-синдрома не существует одного простого теста, необходимо использование комплекса лабораторных методов для выявления данной патологии. Диагностика синдрома диссеминированного внутрисосудистого свертывания должна быть срочной, информативной, основанной на системе простых и легко вы.
Важным моментом, определяющим лечебную тактику и прогноз при массивных кровотечениях, является правильное измерение кровопотери в родах и при кесаревом сечении. Существует несколько способов измерения кровопотери в родах и при кесаревом сечении.
, MD, MBA, Stanford University Medical Center
Last full review/revision February 2018 by Paul M. Maggio, MD, MBA

Сепсис представляет собой спектр заболеваний с риском смерти, колеблющимся от умеренного (например, 10%) до значительного (например, > 40%) в зависимости от различных возбудителей и факторов со стороны хозяина, наряду со своевременностью выявления и предоставления соответствующего лечения.
Септический шок является разновидностью сепсиса со значительно повышенным уровнем смертности в связи с серьезными нарушениями кровообращения и/или клеточного метаболизма. Септический шок предполагает наличие персистирующей гипотонии (определяется как потребность в вазопрессорах для поддержания среднего артериального давления ≥ 65 мм рт. ст., и уровень сывороточного лактата > 18 мг/дл [2 ммоль/л], несмотря на реанимационные мероприятия, проведенные в достаточном объеме [1]).
Понятие синдрома системного воспалительного ответа (ССВО), которое определяется специфическими нарушениями жизненно важных функций и результами лабораторных исследований, уже давно используется для выявления сепсиса на ранних стадиях. Однако было обнаружено, что критерии ССВО имеют недостаточную чувствительность и специфичность при повышенном риске смерти, что является основным аспектом использования такой концептуальной модели. Отсутствие специфичности может быть обусловлено тем, что ССВО чаще является адаптивным, а не патологическим ответом.
Справочные материалы
1. Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA 315:801–810, 2016.
Этиология
Большинство случаев септического шока вызвано внутрибольничными грамотрицательными бактериями или грамположительными кокками и часто возникает у пациентов с ослабленным иммунитетом и у пациентов с хроническими заболеваниями. Реже возбудителями являются грибы рода Candida. Следует заподозрить послеоперационную инфекцию (глубокую или поверхностную) в качестве причины септического шока у пациентов, которые недавно перенесли операцию. Неспецифическая, редкая форма шока, вызванная токсинами стафилококков и стрептококков называется синдромом токсического шока.
Септический шок встречается чаще у новорожденных ( Неонатальный сепсис), у пожилых людей и беременных женщин. Предрасполагающие факторы включают:
Лейкопению (особенно, связанную с раком или лечением цитотоксическими лекарственными средствами)
Наличие инвазивных устройств (в том числе эндотрахеальных трубок, сосудистых или мочевых катетеров, дренажей и других инородных материалов)
Первоочередным лечением являются антибиотики или кортикостероиды
К наиболее распространенным локализациям инфекции относятся легкие, мочевые и желчные пути и ЖКТ.
Патофизиология
Патогенез септического шока полностью не изучен. Воспалительные агенты (например, бактериальный токсин) провоцируют выработку провоспалительных медиаторов, включая ФНО и ИЛ-1. Эти цитокины вызывают нейтрофильно-эндотелиальную клеточную адгезию, активируют механизмы свертывания крови и обуславливают образование микротромбов. Они также способствуют высвобождению других медиаторов, включая лейкотриены, липоксигеназу, гистамин, брадикинин, серотонин и IL-2. Им противостоят противовоспалительные медиаторы, такие как IL-4 и IL-10, в результате механизма обратной отрицательной связи.
Сначала артерии и артериолы расширяются, уменьшается периферическое артериальное сопротивление; сердечный выброс, как правило, увеличивается. Этот этап называется тепловым шоком. Позже, сердечный выброс может уменьшиться, падает АД (с или без увеличения периферического сопротивления), и появляются типичные признаки шока.
Даже на стадии увеличенного сердечного выброса, вазоактивные медиаторы приводят к тому, что кровоток минует капилляры (распределительный дефект). Ослабленный капиллярный ток из этого шунтирования наряду с капиллярной обструкцией микротромбами уменьшают доставку кислорода и снижают выведение углекислого газа и других продуктов распада. Гипоперфузия приводит к дисфункции, а иногда и к недостаточности одного или более органов, включая почки, легкие, печень, мозг и сердце.
Коагулопатия может развиться из-за внутрисосудистой коагуляции с участием основных факторов свертывания крови, усиленного фибринолиза, и чаще комбинации обоих.
Клинические проявления
Симптомы и признаки сепсиса могут быть малозаметными и часто легко принимаются за проявления других заболеваний (например, белая горячка, первичная дисфункция сердца, эмболия легочной артерии), особенно у послеоперационных больных. У пациентов с сепсисом, как правило, отмечаются: лихорадка, тахикардия, обильное потоотделение и тахипноэ; АД остается в норме. Также могут присутствовать другие признаки инфекции, являющейся ричиной сепсиса. По мере ухудшения состояния больного с сепсисом или при развитии септического шока ранним симптомом, особенно у пожилых людей и маленьких детей, может быть спутанность сознания или снижение активности. АД снижается, однако кожа остается парадоксально теплой. Позже, конечности становятся прохладными и бледными с периферическим цианозом. Дисфункция органов приводит к появлению дополнительных симптомов и признаков в зависимости от пораженного органа (например, олигурия, одышка).
Диагностика
АД, частота сердечных сокращений и мониторинг кислородного статуса
Общий анализ крови с лейкоцитарной формулой, уровень электролитов, креатинина и лактата
Показания инвазивного центрального венозного давления (ЦВД), Pa O 2 и сатурации кислорода в центральной вене (ScvO2)
Бактериологический посев крови, мочи и других потенциальных очагов инфекции, в том числе из ран у пациентов после операции
Сепсис подозревают, когда у пациента с известной инфекцией развиваются системные симптомы воспаления или органной дисфункции. Аналогичным образом, у пациентов с необъяснимыми признаками системного воспаления необходимо изучить наличие инфекционных заболеваний в анамнезе, провести медицинский осмотр и лабораторные исследования, которые включают общий анализ мочи и бактериологический посев мочи (особенно у пациентов с постоянными катетерами), бактериологический посев крови и посевы других подозрительных жидкостей организма. Пациентам с подозрением на хирургическую или скрытую причину сепсиса может потребоваться УЗИ, КТ или МРТ в зависимости от предполагаемого источника. При тяжелом сепсисе уровни C- реактивного белка и прокальцитонина в крови часто повышены и могут облегчить постановку диагноза, но эти показатели не являются специфичными. Диагноз основывается прежде всего на клинических проявлениях.
Другие причины шока (например, гиповолемия, инфаркт миокарда) должны быть исключены с помощью анамнеза, медицинского осмотра, электрокардиограммы и анализа кардиомаркеров в сыворотке крови. Даже в отсутствие ИМ гипоперфузия, обусловленная сепсисом, может привести к появлению признаков ишемии на электрокардиограмме, включая неспецифические отклонения ST-T, инверсии зубца T, наджелудочковые и желудочковые экстрасистолии.
Важно выявить дисфункцию органа как можно раньше. Был разработан ряд систем оценки, но шкала динамической оценки органной недостаточности (шкала SOFA) и шкала quick SOFA (qSOFA) были одобрены в отношении риска смерти и являются относительно простыми в использовании.
С помощью критериев шкалы qSOFA выявляют пациентов, которым необходимо провести дальнейшие клинические и лабораторные исследования (должны присутствовать все 3 критерия):
Частота дыхания ≥ 22/мин
Систолическое АД ≤ 100 мм рт. ст.
Оценка по шкале SOFA является более надежной, но требует проведения лабораторных исследований ( Шкала динамической оценки органной недостаточности (SOFA)).
≥ 400 мм рт. ст. (53,3 кПа)
12,0 мг/дл (204 мкмоль/л)
САД ≥ 70 мм рт. ст.
САД 15 мкг/кг/мин в течение ≥ 1 ч
Эпинефрин > 0,1 мкг/кг/мин в течение ≥ 1 ч
Норэпинефрин > 0,1 мкг/кг/мин в течение ≥ 1 ч
5,0 мг/дл (440 мкмоль/л)
* Более высокий балл указывает на лучшее состояние неврологических функций.
F IO 2 = фракция вдыхаемого O2; кПа = килопаскали; САД = среднее артериальное давление; Pao2 = парциальное давление кислорода артериальной крови.
По материалам Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA 315:801-810, 2016.
Проводят ОАК, ГСАК, рентгенологическое исследование органов грудной клетки, анализ уровней электролитов в сыворотке, азота, мочевины крови и креатинина, P co 2 и проб печени. Измерение уровня лактата в сыворотке или сатурации кислорода в центральной вене (ScvO2) (или сразу оба анализа) могут помочь в определении лечения. Количество лейкоцитов может быть уменьшено ( 4 000/мкл) или увеличено (> 15 000/ мкл ), а количество ПМЯ-клеток может снизиться до 20%. В ходе развития сепсиса количество лейкоцитов может увеличиваться или уменьшаться в зависимости от тяжести сепсиса или шока, иммунологического статуса пациента и этиологии инфекции. Одновременное использование кортикостероидов может увеличить количество лейкоцитов и, таким образом, маскировать изменения в анализах, связанные с проявлениями болезни.
Гипервентиляция с дыхательным алкалозом (низкий Pa co 2 и повышенный pH крови) появляется рано, как реакция компенсации метаболического ацидоза. Уровень сывороточного бикарбоната обычно низкий, а уровни лактата в сыворотке и крови повышаются. Шок прогрессирует, метаболический ацидоз ухудшается, и снижается pH крови. Раннее развитие гипоксемической дыхательной недостаточности приводит к снижению соотношения PaO2:F IO 2, а иногда и к выраженной гипоксемии с Pa o 2 70 мм рт. ст. Диффузные инфильтраты на рентгенограмме грудной клетки могут появляться вследствие развития острого респираторного дистресс-синдрома (ОРДС). Уровень мочевины и креатинина обычно прогрессивно возрастают в результате почечной недостаточности. Значения билирубина и трансаминазы могут повыситься, хотя клинически выраженная печеночная недостаточность редко встречается у пациентов с нормальными исходными функциональными пробами печени.
У большинства пациентов с тяжелым сепсисом развивается относительная недостаточность коры надпочечников (т. е. нормальный или немного повышенный исходный уровень кортизола, который не увеличивается в значительной степени в ответ на дальнейший стресс или экзогенный АКТГ). Функция надпочечников может быть проверена путем измерения сывороточного кортизола в 8 часов утра , уровень 5 мг/дл считается неадекватным. При другом подходе уровень кортизола можно измерять до и после введения 250 мкг синтетического AКТГ; повышение уровня 9 мкг/дл считают недостаточным. Тем не менее, при резистентном септическом шоке проведение анализов на кортизол не требуется перед началом кортикостероидной терапии.
Измерения гемодинамики с помощью центрально-венозного или легочно-артериального катетера ( Мониторинг и обследование тяжелобольных пациентов : Методика) могут использоваться, когда неясен тип шока или необходимы большие объемы жидкости (например, > 4–5 литров 0,9% физиологического раствора в течение более, чем 6–8 ч). Эхокардиография, проведенная у постели больного в ОИТ, является практичным и неинвазивным альтернативным методом контроля гемодинамики. При септическом шоке сердечный выброс увеличивается, а периферическое сосудистое сопротивление уменьшается, в то время как при других формах шока сердечный выброс, как правило, снижается, а периферическое сосудистое сопротивление увеличивается. Показатели ЦВД и давления заклинивания в лёгочной артерии (ДЗЛА) вероятнее всего будут в норме при септическом шоке, в отличие от гиповолемического, обструктивного или кардиогенного шока.
Многие годы сепсис и септический шок остаются одной из самых актуальных проблем интенсивной терапии. Частота тяжелого сепсиса среди пациентов ОРИТ составляет от 2% до 18%, а септического шока -3-4%. Примечательно, что в ОРИТ сепсис развивается почти в 30 раз чаще, чем в других клинических отделениях больниц.
Увеличению частоты возникновения сепсиса и септического шока способствуют постарение населения, рост продолжительности жизни лиц с тяжелыми хроническими заболеваниями, значительная частота иммунодефицитных состояний у населения, рост штаммов микроорганизмов, резистентных к антибактериальной терапии, связанный с неконтролируемым назначением антибиотиков, применение в интенсивной терапии препаратов, снижающих иммунитет (цитостатаки, гормоны), повышением инвазивности лечения (расширением показании к обширным операциям, длительная катетеризация сосудов, использование экстракорпоральной детоксикации), нарушение правил асептики и антисептики.
Частота грамположительного и грамотрицательного сепсиса встречается практически одинаково - в 39 и 40% случаев соответственно. В 21% случаев диагносцируются полимикробные ассоциации. Это произошло в результате увеличения роли таких бактерий, как Streptococcus spp., Enterococcus spp., Staphylococcus spp., причем среди них отмечается рост метициллинрезистентных штаммов. Выросла частота сепсиса, вызванного рефрактерными к антибактериальной терапии бактериями (Р. Aeruginosa, Acinetobacter spp., Klebsiella spp.), которые, как правило, выступают в качестве возбудителей нозокомиальной инфекции. Увеличение продолжительности жизни больных, перенесших критические состояния, широкое использование комбинаций цефалоспоринов с ами-ногликозидами обусловили появление новых "ужасов" иифектологии -Enterococcus faecium, Stenothrophamonas maltophylia, Flavobacterium spp. и др. У больных, находящихся в стационаре более трех недель и получавших глюкокортикостероиды и парентеральное питание, сеансы гемодиализа, возросла частота грибкового (кандидозного) сепсиса.
Наиболее вероятная этиология сепсиса в зависимости от локализации очага инфекции представлена в таблице.
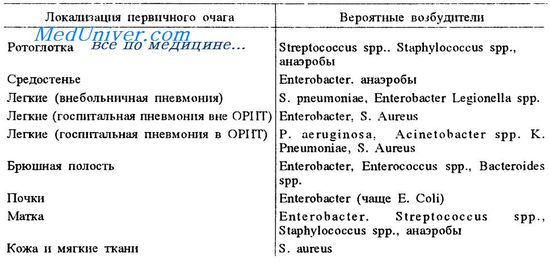
Несмотря на использование самых современных методов интенсивной терапии, достаточно высокой остается летальность, которая при тяжелом сепсисе и септическом шоке составляет 60-70%.
Высокой летальности способствуют поздняя диагностика, неадекватное хирургическое лечение и антибактериальная терапия, полимикробные инфекции, грибковая суперинфекция.
Сепсис классифицируется по темпу развития, по локализации, по виду возбудителя и стадии компенсации.
В 1992 году была сформулирована концепция сепсиса на основе синдрома системного воспалительного ответа (ССВО), которая вошла в клиническую практику большинства стран мира, включая Россию. Главными достоинствами концепции являются простота диагностических критериев, четкое определение реально встречающихся в клинической практике ситуаций, возможность установления диагноза в короткий срок в лечебном учреждении любого уровня.
Бактериемия является одним из возможных, но необязательных признаков сепсиса. Даже при самом скрупулезном соблюдении техники забора крови и использовании современной технологии, как правило, в среднем высев микроорганизмов не превышает 45%, причем при сепсисе положительные результаты посева достигают 17%, при тяжелом сепсисе - 25%, при септическом шоке - 60-70%.
Клиническое значение результатов высева заключается в подтверждении диагноза и определении этиологии инфекционного процесса, обоснованности схемы и оценке эффективности интенсивной терапии, доказательстве механизма развития сепсиса (например, катетеризация).

Обнаружение микроорганизмов в крови у пациентов без признаков ССВО должно расцениваться как транзиторная бактериемия, часто возникающая после различных диагностических процедур.
Одним из первых проявлений ранней стадии септического шока (гипердинамическая фаза) является гипертермия (до 40-41 °С) с ознобами, сочетающаяся с тахипноэ и тахикардией. Лихорадке часто сопутствует изменение психического статуса в виде неадекватности поведения, возбуждения, двигательного беспокойства. Дыхание у больных частое, поверхностное. Артериальное давление нормальное или несколько снижено, тахикардия до ПО ударов в минуту. Темп диуреза снижен до 25 мл/ч. В крови отмечается леГпсоцитоз с высоким уровнем ЛИИ, лимфо- и тромбоцитопения, гипохромия, пойкилоцитоз, компенсированный метаболический ацидоз.
В поздней стадии септического шока (гиподинамическая фаза) гипертермия сменяется гипотермией, отмечается нарушение сознания, вплоть до комы. Кожные покровы бледные с мраморным рисунком. Бледно-цианотичная, холодная кожа, влажные кисти и стопы являются неблагоприятным признаком исхода заболевания. В легких при аускультации определяются рассеянные влажные хрипы, тахипноэ достигает 40-50 в минуту. Систолическое артериальное и пульсовое давление снижено, тахиаритмия выраженная - до 120 ударов в минуту и более.
Со стороны ЖКТ наблюдается развитие пареза кишечника. Уровень билирубина, АЛТ, ACT, ЛДГ возрастает.
Олигурия (менее 10 мл/ч) сопровождается ростом азотемии, снижением концентрационного индекса по осмолярности до 1,0, возрастанием фракционной экскреции натрия выше 2%.
В крови определяется анемия, выраженный лейкоцитоз, лимфопения. Метаболический ацидоз становится декомпенспровапным. Гипергликемия сменяется гипогликемией.
Септический шок - это шок, вызванный грамположительными,грамотрицательными бактериями, вирусами, риккетсиями, паразитами или грибками.
Этиология септического шока.
Предрасполагающие факторы: Инфекция мочевых путей, заболевания печени, пневмония, перитонит включая бактериемию, септический аборт, послеродовые осложнения, иммунологические заболевания.
Наиболее часто вызывают:
- Грам-отрицательные бактерии: E.coli, Klebsiella, Proteus.
- Грам-положительные бактерии: S.aureus, S.epidermidis, Enterococcus spp., S.pneumoniae.
В ранней стадии: гипердинамический шок с теплой сухой кожей, респираторный алкалоз, увеличение сердечного выброса,снижение периферического сопротивления сосудов, нормальное или повышенное центральное венозное давление и нормальное левожелудочковое давление.
В поздней стадии: потенциальная транзиторная гиподинамия с холодной цианотической плохо перфузируемой кожей, метаболический ацидоз, сниженный сердечный выброс, повышение периферического сосудистого сопротивления, снижение ОЦК и склонность к ДВС.
Диагностика септического шока
Признаки септического шока:
- симптомы бактериальной инфекции (лихорадка, озноб)
- гипервентиляция
- нарушение общего состояния
- спутанность сознания, признаки делириума
- факторы предрасполагающие к септическому шоку: послеоперационный период, постоянный катетер в мочевом пузыре, постоянное в/венное введение, трахеостомия, диабет, цирроз печени, ожоги, малигнизация, лейкемия, агранулоцитоз, терапия кортикостероидами или цитотоксическими медикаментами.
- Клинические:выраженный шок и признаки сепсиса (лихорадка, бактериальная инфекция)
- Лабораторные данные:
- кровь: лейкоцитоз или лейкопения но со сдвигом влево, тромбоцитопения, гипофосфатемия.
- бактериологический контроль крови, мочи, мокроты, и стула или отделяемого из раны.
- свертывающая система в случае ДВС: угнетение тромбоцитоза, фибриноген, свертывающие факторы 11,У и Х, активация фибриногена и снижение прекалликреина в плазме.
Лечение септического шока.
Интенсивная терапия
- Горизонтальное положение.
- Внутривенные инфузии: восполнение ОЦК: плазма или растворы декстранов, переливание крови только в случае кровопотери. Центральное венозное давление не выше 14 см в.с.
Антибиотики
- известный патоген: антибиотики внутривенно (с проверкой на чувствительность)
- неизвестный патоген: комбинация бактерицидных антибиотиков с аминогликозидами и антибиотики с активностью к анаэробным микробам.
Гемодинамическое восполнение ОЦК объем переливания 250 мл/15 мин. под контролем центрального венозного давления не выше 14 см вод.ст. доза не увеличивается больше чем на 5 см вод.ст. для объем/время. Давление в легочной артерии до 16-18 мм.рт.ст.
Кортикостероиды: в случае низкого периферического сосудистого сопротивления после восполнения ОЦК метилпреднизалон 30 мг/кгМТ внутривенно, в дальнейшем 2 г. каждые 6 часов до 48 часов, или дексаметазон 40 мг внутривенно, в дальнейшем 20-40 мг каждые 4-6 часов. Продолжение кортикостероидной терапии: 24-72 часа. Гепарин 1000 ед капельно.
Вазоактивные медикаменты
Если основное лечение (восполнение ОЦК, оксигенация, компенсация ацидоза) оказывается не в состоянии контролировать шок:
- допамин в увеличивающейся дозе 200-400-600 мг/мин. Если не увеличивается сердечный выброс то доза недостаточна:
- дополнительно добутамин в увеличивающейся дозе 200-400-600 мг/мин. Если циркуляция нестабильна:
- увеличить комбинацию допамин-добутамин в дозе 800-1000 мг/мин до эффекта. Если дозировка не увеличивает систолическое давление до 100 мм.рт.ст и давление 120-130 уд/мин:
- дополнительно вводят норадреналин в увеличивающейся дозе 10-100 мг/мин.
Хирургическое лечение при септическом шоке проводят: при стабильной гемодинамике хирургическое лечение локальное удаление инфекционного очага.
Если фокус инфекции не удален окончательно стабилизация септического больного невозможна. Интенсивная терапия направлена на уменьшение септического очага. Удаление септического очага одна из мер интенсивной терапии.
Прогноз при септическом шоке
Очень важно если:
- источник инфекции не удален
- ухудшение основного заболевания
- перемежающаяся или прогрессирующая гиперлактацидемия в настоящее время может иметь место полиорганные нарушения (острая почечная недостаточность, острая дыхательная недостаточность, желудочно-кишечные кровотечения, острая печеночная недостаточность).
Читайте также:
- Бруцеллез в тогучинском районе
- Кто вылечил стрептококк агалактия бактериофагами
- Что при коклюше вам помогло
- Септический шок лечение перитонита
- Через сколько дней пройдет прививка от столбняка
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.





