Септическая пневмония у наркоманов
Актуальность проблемы объясняется и тем, что для этой группы пациентов характерна высокая летальность (33,7%), в то время как в среднем по России летальность от пневмонии у пациентов молодого и среднего возраста составляет 1-3% [5].
У всех поступивших больных была ВИЧ-инфекция: 19 человек с IVA стадией, 31 человека с IVБ стадией, причем специфическую антиретровирусную терапию получали только 5 человек (10%). Остальные пациенты за медицинской помощью в СПИД-центр не обращались или самостоятельно прервали назначенный им курс специфической терапии. Вирусные гепатиты В, С наблюдались у 86% пациентов. Для верификации диагноза использовалось общеклиническое, лабораторно-инструментальное исследование, посев мокроты и крови на микрофлору и чувствительность к антибиотикам; проводилось рентгенографическое исследование грудной клетки в динамике, трансторакальное ЭХОКГ, УЗИ внутренних органов, по показаниям –диагностическая фибробронхоскопия и компьютерная томография легких. При необходимости больные консультировались инфекционистом, невропатологом, кардиохирургом.
Результаты исследования. Все больные поступили в стационар в поздние сроки от начала заболевания (через 1-1.5 месяца от появления первой симптоматики) и до госпитализации лечения антибиотиками не получали. При поступлении в стационар у всех больных была лихорадка (температура тела повышалась до фебрильных цифр). Также наблюдалась выраженная одышка при незначительной физической нагрузке, тахикардия, кашель чаще со скудной мокротой, боли в грудной клетке у 15 больных (30%), у 18 больных (36%) отмечалось кровохарканье. Большинство больных (92%) при поступлении имели I-II степень дыхательной недостаточности, определяемую с помощью пульсоксиметрии (SaO2 в %), 8% имели III степень дыхательной недостаточности. У 28 больных (56%) наблюдался лейкоцитоз до 19,0 х109 /л. со сдвигом лейкоформулы влево (палочкоядерные до 54%), значительное ускорение СОЭ. Лейкопения наблюдалась у 3 больных (6%) до 2,5 х109 /л.
По данным объективного исследования укорочение перкуторного тона наблюдалось у 16% больных, появление тупого перкуторного звука над областью инфильтрации у 74%. При аускультации чаще определялись мелкопузырчатые хрипы на вдохе или крепитация над местом поражения.
Посев мокроты на флору и чувствительность к антибиотикам удалось взять у 14 больных (28%), остальные больные поступили с сухим, малопродуктивным кашлем либо в крайне тяжелом состоянии. Анализ показал наличие бактериальной микрофлоры (St.Haemolyticus, M.catarrhalis), часто выявлялись грибки рода Candida.
При рентгенологическом исследовании инфильтрация легочной ткани с одной стороны отмечалась у 24 больных (48%), в остальных случаях отмечалась двусторонняя локализация процесса. У 5 больных (10%) пневмония осложнилась пневмотораксом, у 2 больных – экссудативный плеврит (4%). Деструктивные изменения в легких отмечались у 14 больных (28%). Подобное осложнение в виде множественных полостей распада у наркоманов с пневмонией, обнаруживалось и другими исследователями [1]. Нетипичное течение пневмонии (рецидивирующие множественные очаги деструкции с незначительной перифокальной реакцией (рис.1), несмотря на массивную антибиотикотерапию, а также появление клиники сердечно-сосудистой и легочной недостаточности) позволило заподозрить инфекционный эндокардит, который был выявлен у 18 больных (36%).
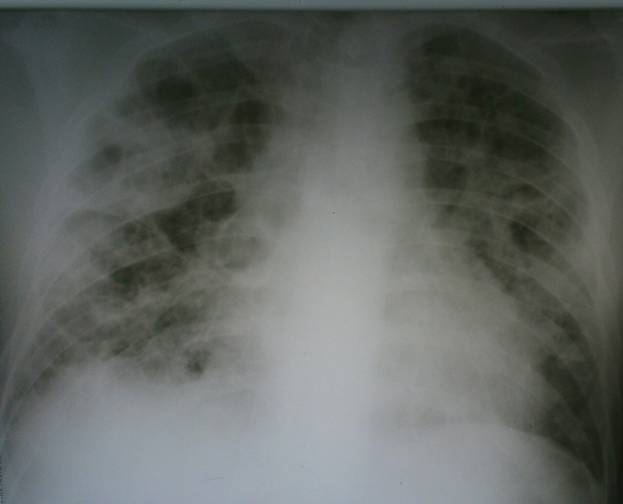
Рис. 1. Рентгенограмма органов грудной клетки:септическая пневмония - множественные очаги деструкции с обеих сторон
По данным ряда авторов, диагностика инфекционного эндокардита во многих случаях запаздывает, поскольку наркоманы поздно обращаются за медицинской помощью[4]. Трудности в диагностике инфекционного эндокардита объясняются еще и тем, что разрушение трехстворчатого клапана может долго не сопровождаться шумами в сердце и недостаточностью кровообращения (впервые шумы в области сердца могут появиться через 2-3 недели от начала терапии).
При проведении ЭХОКГ у наблюдаемых пациентов вегетации на трикуспидальном клапане с различной степенью регургитации обнаружены у 8 больных (44,4%) от всех случаев выявленного бактериального эндокардита), вегетации на митральном клапане у 5 больных (27,8%), вегетации на аортальном клапане у 2 больных (11,1%) и вегетации на всех клапанах у 3 больных.
Все больные с инфекционным эндокардитом были проконсультированы кардиохирургом, для определения дальнейшей тактики лечения. Помимо высокой стоимости лечения инфекционного эндокардита, другой проблемой для инъекционных наркоманов является необходимость протезирования клапанов. По данным статистики, даже при проведении оперативного лечения у этой категории больных сохраняется неблагоприятный прогноз. Через год после оперативного лечения погибают 55% наркоманов, через 3 года – 89%, поскольку при продолжающейся наркомании (и даже при ее прекращении) возникает новая проблема – инфекционный эндокардит протезированных клапанов [4].
У большинства больных помимо поражения легких, наблюдаются изменения внутренних органов [2]. Поражение печени наблюдалось у 12 больных, которое проявлялось гепатоспленомегалией (24%) по данным УЗИ и повышением уровня аминотрансфераз у 50% больных, у 3 больных (6%) обнаружены признаки цирроза печени. Признаки хронического панкреатита обнаружены у 46%больных.
Признаки токсической почки по данным УЗИ и изменению мочевого осадка отмечались у 9 больных (18%). Максимальный подъем уровня креатинина у этих пациентов составил 146мкмоль/л. Признаки ХПН диагносцированы у 2 пациентов (4%) и у 4 пациентов (8%) был диагностирован пиелонефрит с лейкоцитурией.
Явления хронической сердечной недостаточности определялись у больных с бактериальным эндокардитом: СН I стадии у 4 больных , СН II А стадии – 8 больных и CHII Б – 6 больных.
Поражение ротовой полости в виде орофарингеального кандидоза и микоза пищевода наблюдалось у 7 больных (14%). Анемия различной степени тяжести при поступлении выявлена у 24 больных (48%). У 6 пациентов (12%) наблюдался постинъекционный тромбофлебит различной локализации на фоне самостоятельного введения наркотических средств, требующий хирургического лечения.
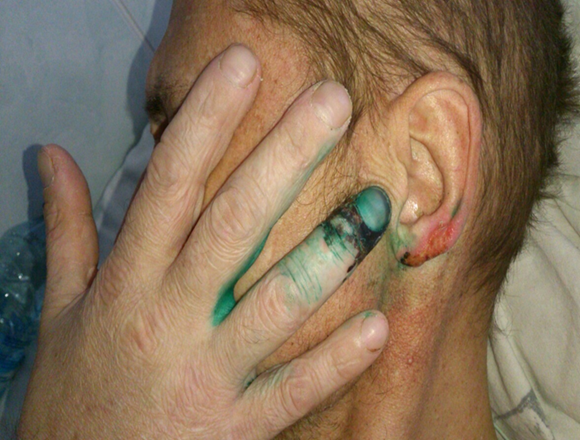
Летальность в наблюдаемой группе составила 16 % (умерли 8 пациентов). У 5 человек смерть наступила от тяжелой (деструктивной, абсцедирующей пневмонии) на фоне ВИЧ- инфекции. Трое больных умерли в результате септического эндокардита трехстворчатого клапана и множественных септических инфарктов в легких.
Как известно, на выбор антибиотиков при лечении внебольничной пневмонии оказывают влияние три основных фактора: наиболее вероятный возбудитель заболевания, резистентность наиболее вероятных возбудителей к антибиотикам и спектр антибиотиков, реально доступных для пациента [6].
После установления возбудителя выбор адекватной терапии значительно упрощается. Однако у ряда больных установление возбудителя невозможно из-за отсутствия мокроты.
В лечении пациентов использовали комбинации антибиотиков, преимущественно бактерицидного действия, вводимые парентерально. При неустановленной этиологии использовали цефалоспорины, преимущественно III поколения в комбинации с макролидами или фторхинолонами. При установлении возбудителя лечение корректировали в соответствии с чувствительностью к антибиотикам. В случаях неэффективности терапии использовались антибиотики резерва: меропенем по 1г 2 раза в сутки в/в капельно, сульперацеф по 2г 2 раза в сутки в/в капельно. При бактериальном эндокардите использовали комбинацию цефалоспоринов I-III поколения с аминогликозидами (цефазолин +гентамицин, цефтриаксон +гентамицин). В случае неэффективности этой комбинации, при подозрении на MRSA инфекцию (метициллин-резистентный стафилококк), использовался ванкомицин в дозе 0,5 г 3-4 раза в сутки в/в капельно. Суточную дозу препаратов корректировали с учетом недостаточности функции почек и печени.
Всем больным, помимо антибактериальной терапии проводили симптоматическое лечение: дезинтоксикационную терапию, назначение гепатопротекторов, нестероидных противовоспалительных средств, ферментов, препаратов железа, мочегонных, иАПФ, антикоагулянтов и антиагрегантов.
Антибактериальную терапию можно считать эффективной у 84% больных. Клиническое улучшение у пациентов наступало, как правило, в конце 1 недели лечения, однако у многих больных наблюдалось медленное разрешение очагово-инфильтративных изменений на рентгенограмме. По мнению ряда авторов, пневмония у лиц с иммунодефицитом, практически всегда сопровождается синдромом затяжного рентгенологического разрешения [3]. Рентгенологически, первое улучшение, в среднем, наступало на 14 день лечения. По окончанию лечения у многих больных (42%) наблюдалось формирование фиброзных изменений в легких.
Сроки пребывания больного в стационаре составили от 2 до 42 дня, в среднем 22 к/дня. Причем 8 больных (16%) полный курс лечения не прошли, самостоятельно покинув отделение, или были выписаны за нарушение режима (употребление очередной дозы наркотика в стационаре).
Данные нашей работы показывают, что для получения благоприятного исхода заболевания и сокращения сроков госпитализации необходимо своевременное применение комбинации современных антибиотиков. Успешное лечение пациентов в стационаре позволяет перейти к следующему этапу – психологической и социальной реабилитации.
Рецензенты:
Сайфутдинов Р.И., д.м.н., профессор, заведующий кафедрой факультетской терапии и эндокринологии ГБОУ ВПО ОрГМУ Минздрава России, г. Оренбург;
Иванов К.М., д.м.н., профессор, заведующий кафедрой пропедевтики внутренних болезней ГБОУ ВПО ОрГМУ Минздрава России, г. Оренбург.
Д. Б. Утешев А. А. Карабиненко Е. Н. Филатова Г. И. Сторожаков, член-корр. РАМН, доктор медицинских наук, профессор РГМУ НО МФ МСЧ № 1 АМО ЗиЛ, Москва По официальным данным
РГМУ НО МФ
МСЧ № 1 АМО ЗиЛ, Москва
 |
| Рисунок 3. ЭхоКГ больной Л., 22 года |
 |
| Рисунок 4. Рентгенограмма больной Л., 22 года |
Как показывают наши примеры, встречаемость инфекционного эндокардита среди наркоманов увеличивается в связи с широким распространением внутривенного употребления наркотиков. Наиболее часто поражается трикуспидальный клапан. По данным литературы, в процесс могут также вовлекаться и другие клапаны [3]. В кантональном госпитале Цюриха было проведено проспективное исследование 22 пациентов с инфекционным эндокардитом (средний возраст 23 года). Период наблюдения составил три года [3]. Трикуспидальный клапан был поражен у 13 человек, митральный клапан — у четырех, комбинированное трикуспидально-митральное поражение наблюдалось у пяти пациентов и аортальный клапан был поражен у одного больного. Золотистый стафилококк оказался наиболее частым возбудителем (у 15 человек). Потенциальными факторами его патогенности, определяющими клиническую картину септического процесса, являются следующие энтеротоксины: SEA, SEB, SEC, SED и токсин синдрома токсического шока (TSST-1). Эти вещества связываются белками интерстицильного матрикса: фибронектином, колллагеном I и II типа и костным сиалопротеином (BSP). Однако эти факторы не являются преобладающими среди больных с инфекционным эндокардитом, вызванным Staphylococcus aureus [2]. BSP преобладает у больных с кожными поражениями, в то время, как у больных с эндокардитом чаще всего выделяются штаммы микроорганизмов, не вырабатывающие энтеротоксины. На наш взгляд, исходя из такой особенности выработки патогенов, можно предположить, что клинические проявления септического процесса, связанные с первичным очагом инфекции в коже (например, фурункулез), являются по своей картине однородными, в то время как при стафилококковом эндокардите факторы патогенности разнородны или вообще отсутствуют. Это может быть причиной отрицательного результата посевов крови.
Streptococci, по данным швейцарских врачей, являлись причиной бактериального эндокардита у четыреx пациентов, Corynebacteria — у двуx и в одном случае имелась смешанная инфекция [3]. Шесть пациентов были ВИЧ-инфицированы и 17 имели хронический вирусный гепатит. Десять пациентов (трое из них ВИЧ-инфицированные) подверглись хирургическому лечению. При кардиохирургическом лечении было проведено: рассечение трикуспидального клапана с заменой (у одного больного) или без замены (у четыреx больных) клапана, удаление вегетаций и замена клапана (у двух больных), замена митрального клапана (у двуx больных), протезирование аортального клапана (у одного больного). В случае эндокардита трехстворчатого клапана тактика оперативного вмешательства (выполнить резекцию, удалить вегетации или осуществить замену клапана) была выбрана с учетом тяжести поражения клапана и состояния психосоциального статуса пациента. В случае если вегетации присутствуют только на одной створке клапана и могут быть легко удалены, используется вегетоэктомия с аннулопластикой аутологичным перикардом. Удаление клапана без его протезирования является средством выбора среди тех пациентов, у которых нельзя исключить употребление наркотиков в будущем. Протезирование биопротезом используется в том случае, когда налицо полное разрушение клапана и доказано, что пациент воздерживался от употребления наркотиков в течение длительного времени до операции.
1. Медицинская микробиология / Гл. ред. В. И. Покровский, О. К. Поздеев. М.: Гэотар Медицина, 1999. 1200 с.
2. Carrel T., Schaffner A., Pasic M. et al. Surgery of endocarditis in the drug dependent and HIV patient. A prospective comparison with conservative treatment // Helv. Chir. Acta. 1993. Vol. 60. №3. Р. 439-445.
3. Hogevik H., Soderquist B., Tung H. S. et al. Virulence factors of Staphylococcus aureus strains causing infective endocarditis a comparison with strains from skin infections // APMIS. 1998. Vol. 106. № 9. P. 901-908.
Пневмония Септическая пневмония – патологическое состояние, которое правильнее называть септическая эмболия легких, возникающая в результате закупорки инфицированными эмболами мелких ветвей легочной артерии. Эти эмболы проникают в легкие из инфекционных очагов в органах брюшной полости, коже, костях, правых камер миокарда (инфекционный эндокардит). Также источником инфекции может быть инфицированный центральный венозный катетер.
Наиболее часто септическая пневмония возникает у лиц, принимающих наркотические средства путем внутривенного введения.
Таким образом, септическая эмболия легких – одна из форм осложнения сепсиса, при которой эмболии формируют участки инфарктов в легких. Из-за присоединения инфекционного процесса на протяжении нескольких часов в пораженных участках происходит гнойный распад.
При септической пневмонии на рентгенограмме легких определяются множественные инфильтраты неправильно-округлой или округлой формы, возможно образование субплевральных треугольных затемнений, похожих на инфаркт легкого при тромбоэмболии легочной артерии. По мере развития патологии в инфильтратах образуются участки распада и появляются тонкостенные полости (в некоторых полостях определяется небольшое количество содержимого – менискообразные или горизонтальные уровни содержимого; рисунок 1).
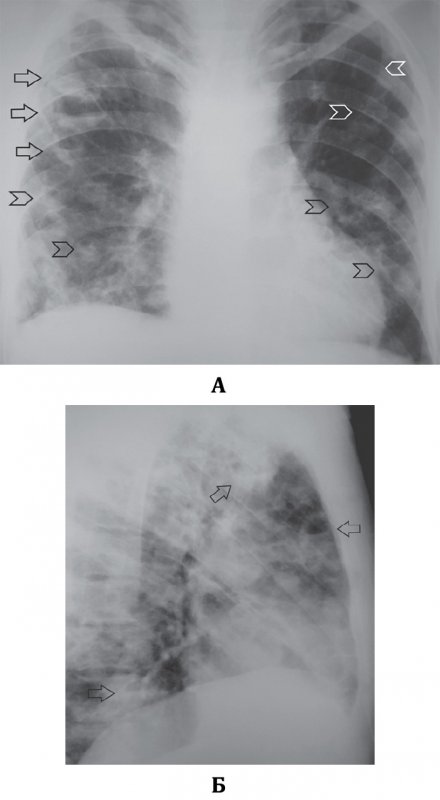
Септическая пневмония (Септическая эмболия легких)
Рисунок 1. Септическая пневмония (Септическая эмболия легких). Рентгенограмма в прямой проекции: определяются множественные тонкостенные полости в обоих легких на фоне усиленного рисунка. А – в правом легком определяется часть полостей с содержимым (см стрелки); указателями отмечены полости без содержимого (множественные полости без содержимого дифференцируются хуже, создавая картину крупноячеистой деформации рисунка в нижних отделах легких. Б – рентгенограмма в правой боковой проекции (тот же пациент): полости с содержимым отмечены стрелками.
Отметим, что инфильтраты находятся на разных стадиях развития. Процесс развития инфильтратов происходит достаточно быстро (на протяжении нескольких дней). При этом на рентгенограмме в легких определяется динамичная и полиморфная картина – одновременно обнаруживаются как полостные образования, так и инфильтраты (см рисунок 2). Осложнения в виде эмпиемы плевры или пневмоторакса могут возникать в случае прорыва полостей с содержимым в плевральную полость. Благоприятное течение заболевания характеризуются спаданием полостей и их бесследным исчезновением или образованием участков фиброза.
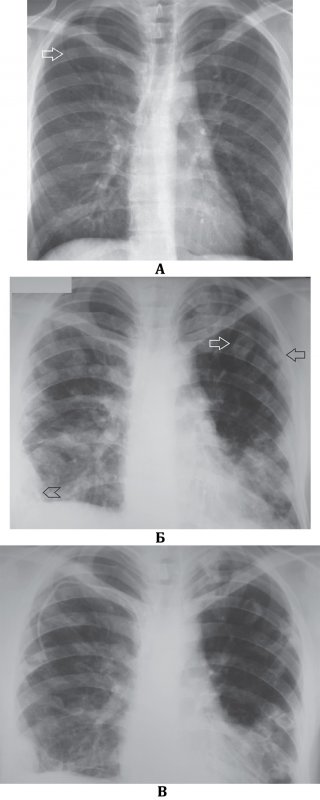
Септическая пневмония (Септическая эмболия легких)
Рисунок 2. Динамика септической эмболии легких. А – в проекции 1 межреберья справа определяется небольшое количество инфильтрата (см стрелка) и усиление сосудистого рисунка в обоих легких. Б – рентгенограмма того же пациента через 7 дней терапии: с обеих сторон в легких определяются множественные инфильтраты на фоне усиленного рисунка; в верхней доле слева отмечаются инфильтраты с полостями распада (см стрелки); эти полости имеют относительно толстые стенки. В плевральной полости справа определяется небольшое количество содержимого (см указатель). В – рентгенограмма того же пациента на 14 день терапии: большинство инфильтратов образовали тонкостенные полости; в верхней доле слева в полостях отмечаются менискообразные уровни содержимого
Пневмония может сопровождаться следующими осложнениями: экссудативный плеврит (характеризуется рентгенологической картиной гидроторокса), абсцедирование, деструкция легких (деструктивная пневмония), пневмоторакс, эмпиема плевры. В случае обструкции крупного бронха вязким секретом может возникать ателектаз сегмента или доли легкого.
Контрольную рентгенографию при положительной клинической динамике рекомендовано проводить не ранее чем через 14 дней. Однако на практике, в условиях стационара контрольное рентгенологическое исследование, как правило, проводят через 10 дней терапии. В случае ухудшения клинической картины или при возникновении осложнений также показана повторная рентгенография. Благоприятное течение характеризуется положительной рентгенологической динамикой – уменьшение площади и однородность инфильтрата, а также полного рассасывания инфильтрации (рисунок 3). В ряде случаев на месте инфильтрации может обнаруживаться только усиленный рисунок (рисунок 4).
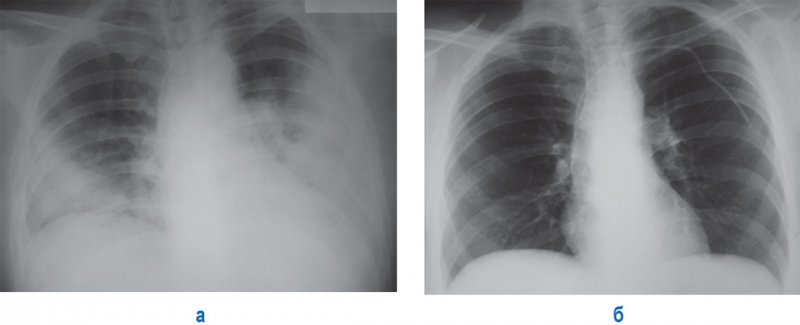
Септическая пневмония (Септическая эмболия легких)
Рисунок 3. А – тяжелый случай двусторонней полисегментарной пневмонии (пациент проходил лечение в отделении интенсивной терапии и был подключен к аппарату искусственной вентиляции легких). Б – рентгенограмма того же пациента через 14 дней терапии: определяется положительная динамика в виде полного рассасывания инфильтрации
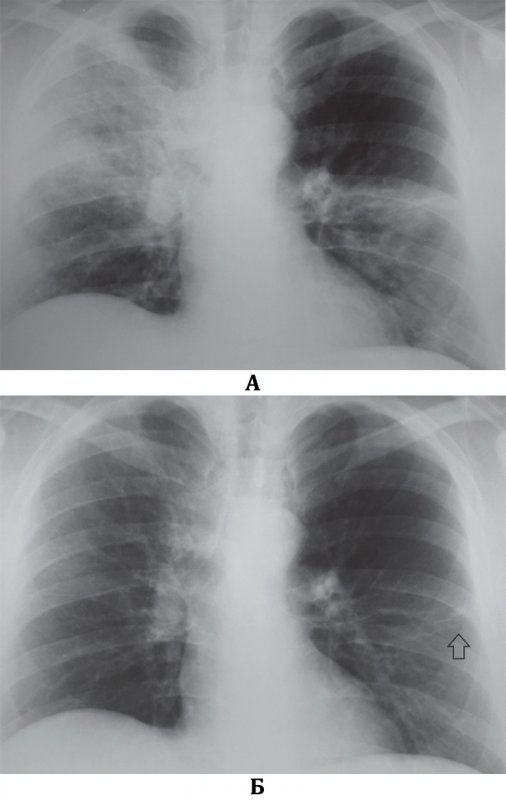
Двусторонняя полисегментарная пневмония
Рисунок 4. Двусторонняя полисегментарная пневмония. А – на рентгенограмме определяется инфильтрация в правой верхней доле и в среднем отделе левого легочного поля. Б – рентгенограмма того же пациента через 10 дней терапии: в верхней правой доле инфильтрация не определяется; слева отмечаются остаточные явления (см стрелка) в виде линейных теней и небольшого участка сниженной прозрачности (остаточные воспалительные изменения в легком или наслоения на плевре, которые могут исчезнуть или сохраниться с течением времени, в этом случае их следует оценивать как фиброз)
Если по истечении 28 дней с момента начала терапии инфильтрация сохраняется – это затяжная пневмония. Затяжное течение пневмонии может быть обусловлено следующими факторами риска:
- Тяжелое течение пневмонии
- Многодолевая инфильтрация
- Иммунодефицитные состояния
- Высоковирулентные возбудители – грамотрицательные бактерии, Legionella, Staphylococcus
- Сопутствующая патология: сахарный диабет, застойная сердечная недостаточность, почечная недостаточность, хроническая обструктивная болезнь легких и др
- Возраст пациента (старше 55 лет)
- Вредные привычки – курение, злоупотребление алкоголем
В случае развития затяжной пневмонии положительная рентгенологическая динамика отмечается через более длительные сроки – до 6-8 месяцев. При этом часто отмечаются уменьшения сегмента или доли легкого в результате фиброза, формирование локального пневмосклероза и бронхоэктазов.
Важно обратить внимание на постпневмонический пневмосклероз, который имеет следующие формы:
Затяжное течение пневмонии требует проведения рентгеновской компьютерной томографии, фибробронхоскопии (ФБС) и других методов диагностики с целью исключения наличия других возможных патологий, которые имеют похожую с пневмонией рентгенологическую картину (в первую очередь – туберкулез легких. Похожую с пневмонией рентгенологическую картину имеют вторичные изменения легких при обструкции бронха инородным телом или опухолью, а также сдавление бронха увеличенными лимфоузлами. Дифференциально-диагностический ряд иногда может включать абсцесс легкого, бронхоэктазы, тромбоэмболия легочной артерии с инфарктом легкого.
В ряде случаев рентгенограмма при грибковом поражении легких может быть похожа на бактериальную пневмонию, которая не разрешается в обычные сроки. Патологию легких могут вызывать грибки Actinomyces, Aspergillus, Candida, Cryptococcus и др. Наиболее часто грибковое поражение легких отмечается у лиц с иммунодефицитными состояниями (СПИД, онкогематологические патологии: лейкоз, лимфома). Предрасполагающими факторами к грибковому поражению легких являются туберкулез, сахарный диабет, длительный прием иммунодепрессантов, антибиотиков, глюкокортикостероидов.
Грибковое поражение легких
К неинвазивным формам аспергиллеза относятся аспергиллома и аллергический бронхолегочный аспергиллез.
К редким патологиям, вызывающим инфильтративные изменения легких, относят криптогенная организующаяся пневмония, лекарственное поражение легких, бронхиолоальвеолярный рак легкого.
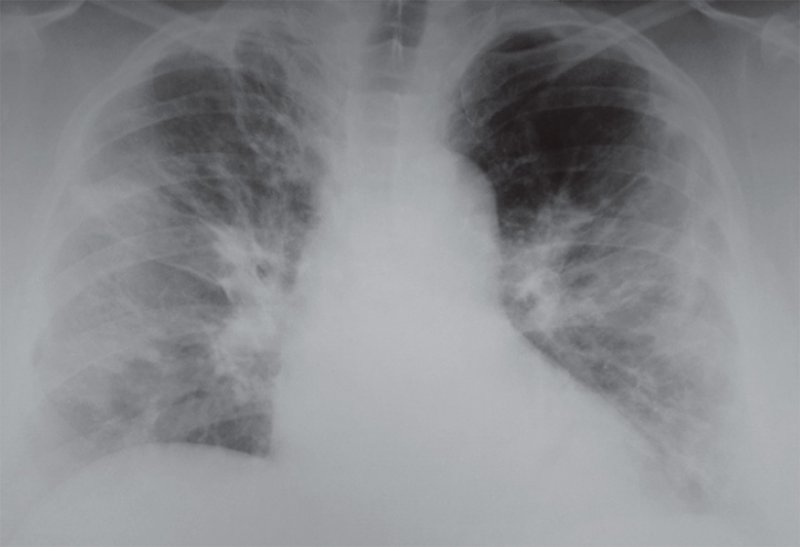
Рентгенограмма легких при респираторной вирусной инфекции
Рисунок 6. Рентгенограмма легких при респираторной вирусной инфекции: с обеих сторон в легких определяются линейные тени, преимущественно радиально расходящиеся от бесструктурных корней легких. Отмечается сниженная прозрачность в субплевральных отделах легочных полей. Учитывая клинические показатели, вероятно, что изменения на этом снимке вызваны не только вирусной инфекцией, но и вторичной бактериальной
В случае присоединения бактериальной инфекции на рентгенограмме часто обнаруживаются участки альвеолярной инфильтрации. Отметим, что после ветряночной пневмонии, перенесенной во взрослом возрасте, в легких могут обнаруживаться множественные мелкие кальцинаты, расположенные преимущественно в нижних и средних отделах легочных полей.
Сепсис является одним из наиболее тяжелых осложнений, возникающих при воспалении легких. Оно характеризуется попаданием в кровяное русло различных токсинов и инфекций. В результате, микробы разносятся кровью в органы, среди которых, и легкие. Это приводит к появлению в легочной ткани множественных небольших воспалительных очагов, нередко сливающихся друг с другом в абсцессы.
- Симптоматика заболевания
- Терапия заболевания
- Особенности профилактики недуга
Основные положения и причины возникновения
Сепсис при пневмонии – это состояние, при котором происходит проникновение инфекции в кровяное русло. В таком случае возбудитель начинает разноситься по всему организму больного, выделяя в кровь токсины, которые затем попадают во все органы и ткани.
В официальной классификации заболеваний данный термин отсутствует. Наиболее подвержены септической пневмонии следующие группы людей:
![]()
Больные, страдающие иммунодефицитом.- Люди преклонного возраста, находящиеся в домах престарелых.
- Пациенты, проходящие стационарное лечение.
- Новорожденные дети, которые находятся на первых месяцах жизни, а также дети, страдающие гипотрофией.
- Инъекционные наркоманы.
Основными возбудителями заболевания являются стрептококки, стафилококки, пневмококки и т. д. При этом, от того, к какой группе относится пациент, во многом зависит тип возбудителя болезни:
- у стационарных больных и детей септическая пневмония чаще всего возникает из-за деятельности стафилококка,
- у наркоманов основным провокатором заболевания является гемофильная палочка (в некоторых случаях – пневмококки),
- провокатором заболевания у больных СПИДом являются пневмоцисты.
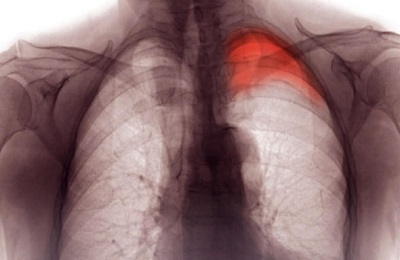
В некоторых случаях сепсис при пневмонии развивается под влиянием смешанной микрофлоры.
Наиболее частыми осложнениями данного заболевания считается образование полостей в легких и некрозы. Появление полостей происходит вследствие гнойных процессов в тканях легких, которые попросту разлагаются некротической жидкостью. Возможен также и абсцесс, выявить расположение которого позволяет рентген.
Если болезнь не лечится в течение длительного времени, то возможно возникновение легочной паренхимы с последующей деформацией бронхов. Образуются множественные полости гнойного характера, которые отделяются от здоровой ткани фиброзной стенкой. При отсутствии лечения легкие начинают постепенно отмирать.
Для сепсиса при пневмонии характерен выраженный синдром интоксикации, при котором наблюдается озноб, повышение температуры и потемнение кожи. Это свидетельствует о наличии во внутренних органах множественных очагов кровоизлияния в слизистые и кожные покровы.
Течение септического воспаления сопровождается симптомами, похожими на туберкулез или актиномикоз.
Проявления сепсиса в клинической картине болезни преобладают следующие симптомы:
- Общее состояние пациента является весьма тяжелым. Наблюдается адинамия, бледность и даже синеватый оттенок кожи, заторможенность.
![]()
Полное отсутствие аппетита, из-за которого пациент начинает интенсивно терять вес.- Наличие несильного кашля, который усиливается при абсцедировании. Начинается выделяться большое количество мокроты (около 200 мл в сутки).
- Ввиду затрудненности дыхания, пациент дышит открытым ртом, появляются приступы удушья.
- Высокая, не сбивающаяся температура, сильный озноб, лихорадочное состояние.
- В виде осложнений могут проявляться признаки гнойного отита, плеврита, менингита, перикардита, абсцедирования и т. д.
При наличии нескольких вышеописанных симптомов, необходимо немедленно обратиться за помощью к специалисту. Клиническая картина данного заболевания предполагает наличие трех фаз:
- Гнойная инфильтрация.
- Гной проникает в бронхи.
- Образование рубцов.

Если у больного выявлена абсцедирующая форма септической пневмонии, то заболевание имеет следующие симптомы:
В качестве осложнений заболевания могут наблюдаться цианоз и одышка. Осложнениями данного заболевания являются гнойный плеврит и пиопневмоторакс. Такая форма болезни имеет неблагоприятный прогноз.
Особенности диагностики
На первой стадии заболевание проявляется в виде грудных болей, лихорадки, кашля и сильного озноба. Диагностика обычно осуществляется на второй неделе после заражения. Основными методиками проведения диагностики является перкуссия и аускультация. Еще одной важной процедурой является рентген, позволяющий определить динамику заболевания.
Осматривая пациента, врач может заметить увеличенную частоту дыхания. При прослушивании становятся заметными влажные и сухие хрипы, которые и являются одними из основных симптомов заболевания.
Берется анализ мокроты с целью проведения бактериологического и микроскопического исследований. Целью первого из них является установление типа возбудителя для эффективного приема антибиотиков. Микроскопическое исследование позволяет определить число лейкоцитов и эластичных волокон. В некоторых случаях пациенту назначается ежедневный сбор мокроты для выявления динамики заболевания.
Также диагностика включает в себя забор крови для проведения общего, клинического и биохимического анализа.
По результатам данных исследований определяется тип воспаления. Биохимия позволяет определить функции печени и почек.
Определение очагов, а также динамики заболевания, происходит при рентгенологическом исследовании. Если болезнь находится на начальной стадии, то на рентгене проявляются затемненные очаги. Далее они развиваются в абсцессы (полости с тонкими стенками, в которых содержится жидкость).
В ряде случаев рентгенограмма не позволяет распознать очаги воспаления. Они могут иметь незначительные размеры и глубокое расположение, а потому требуют использования при исследованиях дополнительных методик диагностики. К ним относится томография, ангиография и сцинтиграфия легких.
При острой форме недуга, пациенту назначается исследование с помощью компьютерного томографа. Помимо этого применяется серологическое, микробиологическое, гистологическое обследование и бронхоскопия.
Если пациенту необходимо проведение операционного вмешательства, то диагностика предусматривает также и взятие функциональных проб печени и почек.
Благодаря данным исследованиям специалистам удается установить диапазон той нагрузки, которая сказывается на сердце и сосуды в ходе операции.
Методики лечения болезни определяются ее этиологией. Но вне зависимости от тяжести заболевания, пациент в обязательном порядке помещается на стационар. При отсутствии абсцессов, лечением больного занимаются такие специалисты, как терапевт и пульмонолог.
Одной из основных методик, применяемых при лечении сепсиса при пневмонии, является антибактериальная терапия. Консервативное лечение предусматривает также дезинтоксикацию организма и прием антибиотиков. Чаще всего пациентам прописываются медикаменты группы макролидов (Азитромицин).
При наличии запущенной формы заболевания введение антибиотика осуществляется внутривенно. Когда состояние пациента стабилизируется, то можно перейти на пероральный прием.
Если медикаментозная терапия не дает результатов, и у пациента начинает развиваться абсцесс, то его переводят в отделение торакальной хирургии, где он проводит около двух недель.
Если данным лечением пренебречь, то болезнь может перейти в хроническую форму с развитием следующих осложнений:

В случаях, когда возбудитель проявляется невосприимчивость к применяемым препаратам, специалисты назначают прием следующих медикаментов:
- Респираторные фторхинолоны.
- В качестве препаратов, для улучшения отхаркивания, применяется Бромгексин и Месна.
- Гепарин позволяет улучшить кровоснабжение.
Помимо медикаментозной терапии, очень важным является правильное, сбалансированное питание. В рацион больного обязательно должны входить легкие супы, куриные бульоны, овсяные кисели, сваренные на молоке. Рацион пациента не должен включать в себя любые жирные блюда.
Спиртные напитки и курение также являются неприемлемыми. Больной должен содержаться в теплом помещении с хорошей вентиляцией.
Поскольку септическая пневмония является очень тяжелым заболеванием, то лучше предотвратить ее, нежели впоследствии заниматься лечением. По этой причине необходимо прислушаться к нескольким советам от специалистов:
![]()
Для людей пожилого возраста желательно систематически проводить вакцинацию от стрептококка.- Для детей, которые входят в группу риска данного заболевания, желательно проводить вакцины от пневмонии. Для этого следует проконсультироваться с педиатром.
- Поскольку септическая пневмония может возникнуть в качестве осложнения гриппа, то противогриппозные прививки также будут кстати.
Помимо медикаментозной профилактики, необходимо уделить особое внимание вопросу гигиены. Руки следует мыть тщательно и с мылом.
Для укрепления иммунитета в ежедневный рацион следует включать продукты, содержащие большое количество витаминов и микроэлементов.

Одной из важных профилактических мер данного заболевания для взрослых является отказ от курения. Дело в том, что табак способен снизить устойчивость бронхов и легких к инфекциям. Поскольку сепсис при воспалении легких имеет значительную тенденцию к рецидивам, то людям, единожды переболевшим данным заболеванием, ни в коем случае нельзя возвращаться к курению.
Заразность септической пневмонии определяется причиной, вызвавшей недуг. Поэтому далеко не во всех случаях при прямом контакте с носителем, здоровый человек обязательно заболеет. Но даже если пневмония окажется заразной, крепкий иммунитет может предотвратить возможное заражение. Именно поэтому профилактические меры являются столь важными.
Септическая пневмония является крайне тяжелым заболеванием, которому свойственно длительное течение и высокая вероятность к рецидивам. К сожалению, данная болезнь очень часто имеет неблагоприятный прогноз. Примерно в 40-70% случаев такое заболевание приводит к летальному исходу.

По этой причине очень важным является своевременное выявление заболевание. Диагностика должна быть проведена максимально оперативно, поскольку лечение сепсиса при пневмонии не терпит никаких отлагательств.
Очень важным для специалиста является правильное постановление диагноза и определение точного курса лечения. Поэтому для диагностики данного заболевания необходим комплексный подход.
Читайте также: