Сепсис статистика в россии
Основные факты
- Сепсис развивается, когда ответ организма на инфекцию приводит к повреждению его собственных тканей и органов, и может привести к смерти или серьезному ухудшению состояния.
- Глобальное эпидемиологическое бремя сепсиса не поддается точной оценке. Согласно расчетам, он ежегодно развивается более чем у 30 миллионов человек и, возможно, уносит жизни 6 миллионов человек(1). Проблема сепсиса, по всей вероятности, больше всего распространена в странах с низким и средним уровнем доходов.
- Согласно оценкам, каждый год сепсисом страдает 3 миллиона новорожденных и 1,2 миллиона детей (2). Три из десяти случаев смерти в результате неонатального сепсиса предположительно вызваны лекарственно устойчивыми патогенами.
- Каждая десятая смерть в связи с беременностью и родами происходит по причине материнского сепсиса, при этом 95% случаев смерти от материнского сепсиса происходят в странах с низким и средним уровнем доходов (4). Каждый год в связи с материнскими инфекциями, в частности материнским сепсисом, умирает один миллион новорожденных (5).
- Сепсис может быть клиническим проявлением инфекций, приобретенных как за пределами медицинских учреждений, так и внутри их. Инфицирование в связи с оказанием медицинской помощи является одной из наиболее распространенных, если не самой распространенной разновидностью неблагоприятных событий, происходящих в ходе оказания такой помощи, и ежегодно затрагивает миллионы пациентов по всему миру (6). Поскольку такие инфекции нередко устойчивы к антибиотикам, они могут вызывать быстрое ухудшение клинического состояния.
Общая информация
Сепсис — это опасная для жизни дисфункция внутренних органов, вызванная нарушением регуляции ответа организма на инфекцию (7). Если сепсис не распознать на ранней стадии не обеспечить своевременное лечение, он может вызвать септический шок, полиорганную недостаточность и смерть. Сепсис может быть вызван любым типом инфекционного патогена. Устойчивость к противомикробным препаратам является ведущим фактором, вызывающим отсутствие клинического ответа на лечение и быстрое развитие сепсиса и септического шока. Среди пациентов с сепсисом, вызванным лекарственно-устойчивыми патогенами, наблюдается повышенный риск больничной летальности.
Кто подвергается риску?
Сепсис может развиться у любого человека с инфекцией, однако повышенному риску подвергаются уязвимые группы населения,такие как пожилые люди, беременные женщины, новорожденные, госпитализированные пациенты и лица с ВИЧ/СПИДом, циррозом печени, раком, заболеваниями почек, аутоиммунными заболеваниями и удаленной селезенкой (8) .
Признаки и симптомы
Сепсис является неотложным состоянием. Однако признаки и симптомы сепсиса у пациентов могут быть различными в различные моменты времени, поскольку такое клиническое состояние, как сепсис, может вызываться множеством возбудителей и менять свой характер на различных этапах. К тревожным признакам и симптомам относятся повышение или понижение температуры тела и озноб, изменение психического состояния, затрудненное/учащенное дыхание, учащенное сердцебиение, ослабление пульса/низкое кровяное давление, олигурия, синюшность или мраморность кожи, похолодание конечностей и сильные боли или дискомфорт в теле (9-11) . Возникновение подозрения на сепсис является первым шагом к его раннему распознаванию и диагностике.
Профилактика
Существует два основных пути профилактики сепсиса:
1. предотвращение передачи микроорганизмов и инфицирования;
2. недопущение осложнения инфекции до состояния сепсиса.
Профилактика инфекций среди населения предусматривает соблюдение эффективных правил гигиены, таких как мытье рук и безопасное приготовление пищи, улучшение качества и доступности водоснабжения и средств санитарии, обеспечение доступа к вакцинам, особенно лиц, подверженных высокому риску развития сепсиса, а также надлежащее питание, включая грудное вскармливание новорожденных.
Профилактика внутрибольничных инфекций, как правило, обеспечивается наличием функционирующих программ по профилактике инфекций и инфекционному контролю, а также соответствующих групп персонала, применением эффективных методов соблюдения гигиены, в том числе гигиены рук, наряду с чистотой в помещениях и правильной работой оборудования.
Профилактика развития сепсиса как среди населения, так и в медицинских учреждениях предполагает надлежащее лечение инфекций с применением антибиотиков, в том числе регулярную оценку состояния больных для рационального применения антибиотиков, быстрое обращение за медицинской помощью и раннее обнаружение признаков и симптомов сепсиса.
Эффективность профилактики инфекций однозначно подтверждается научными данными. Например, при строгом соблюдении правил гигиены рук в учреждениях здравоохранения уменьшение числа случаев инфицирования может составить до 50% (12) , а в общественных местах эти меры могут сократить риск возникновения диареи как минимум на 40% (13) . Меры по улучшению водоснабжения, санитарии и гигиены (ВСГ) способны привести к сокращению общего бремени заболеваний во всем мире на 10% 14 . Каждый год вакцинации помогают предотвратить 2–3 миллиона случаев смерти, связанных с инфекциями (15) .
Диагностика и клиническое ведение
Чтобы выявить сепсис на ранних этапах и своевременно организовать его надлежащее клиническое ведение, крайне важно распознать и не игнорировать перечисленные выше признаки и симптомы, а также выявить определенные биомаркеры (в частности прокальцитонин). На этапе после раннего выявления важное значение имеют диагностические процедуры, помогающие выявить возбудитель вызвавшей сепсис инфекции, поскольку от этого зависит выбор целенаправленного противомикробного лечения. Устойчивость к противомикробным препаратам (УПП) может препятствовать клиническому ведению сепсиса, поскольку оно нередко требует подбора антибиотика эмпирическим путем. Поэтому необходимо понимать эпидемиологические параметры распространения УПП в данных условиях. После определения источника инфекции важнейшей задачей является его ликвидация, например, путем дренирования абсцесса.
На раннем этапе ведения сепсиса важное значение также имеет инфузионная терапия для нормализации объема циркулирующей жидкости. Кроме того, для улучшения и поддержания перфузии тканей может потребоваться применение сосудосуживающих препаратов. Дальнейшие мероприятия по правильному ведению сепсиса выбираются исходя из данных повторных обследований и диагностических мероприятий, включая контроль основных показателей жизнедеятельности пациента.
Проблема сепсиса и Цели в области устойчивого развития
Сепсис является крайне актуальной причиной материнской смертности, а также смертности новорожденных и детей в возрасте до пяти лет. По этой причине борьба с сепсисом будет очевидным образом способствовать выполнению задач 3.1 и 3.2 в рамках Целей в области устойчивого развития (ЦУР).
Сепсис является крайне актуальной причиной материнской смертности, а также смертности новорожденных и детей в возрасте до пяти лет. По этой причине борьба с сепсисом будет очевидным образом способствовать выполнению задач 3.1 и 3.2 в рамках Целей в области устойчивого развития (ЦУР).
Показателями выполнения этих двух задач ЦУР являются коэффициенты смертности матерей, новорожденных и детей младше пяти лет. Сепсис занимает важное место среди причин, вызывающих эти предотвратимые виды смертности. Именно он нередко является клиническим состоянием, вызывающим, в конечном счете, смерть пациентов, страдающих ВИЧ, туберкулезом, малярией и другими инфекционными заболеваниями, упомянутыми в задаче 3.3, но при этом он, как правило, не регистрируется в качестве причины смерти таких пациентов и не включается в статистику по показателям выполнения задачи 3.3 ЦУР.
Проблема сепсиса также имеет важное, хотя и более опосредованное значение для других связанных со здоровьем задач в рамках ЦУР 3. Так, профилактика и/или надлежащая диагностика и ведение сепсиса имеют также отношение к надлежащему охвату вакцинами, всеобщему охвату качественными услугами здравоохранения, возможностям для соблюдения Международных медико-санитарных правил, обеспечению готовности и предоставлению услуг водоснабжения и санитарии. Вместе с тем, обеспечение повсеместной профилактики, диагностики и ведения сепсиса остается сложной задачей.
Деятельность ВОЗ
В мае 2017 г. Семидесятая сессия Всемирной ассамблеи здравоохранения на основании доклада Секретариата ВОЗ приняла резолюцию о сепсисе.
Резолюция WHA70.7. Совершенствование профилактики, диагностики и клинического ведения сепсиса
Доклад Секретариата ВОЗ A70/13. Совершенствование профилактики, диагностики и клинического ведения сепсиса
В настоящее время в рамках нескольких программ уровня штаб-квартиры ВОЗ, осуществляемых в сотрудничестве и координации с региональными бюро ВОЗ, изучаются вопросы воздействия сепсиса на общественное здравоохранение, а также предоставляются руководящие указания и поддержка на уровне стран по вопросам профилактики, ранней и правильной диагностики, а также своевременного и эффективного клинического ведения сепсиса в интересах комплексного решения этой проблемы. Глобальная группа по вопросам профилактики инфекций и инфекционного контроля, работающая в штаб-квартире ВОЗ при Департаменте предоставления услуг и обеспечения их безопасности, обеспечивает координацию деятельности по проблеме сепсиса и руководит мероприятиями в области его профилактики.
Библиография
(1) Fleischmann C, Scherag A, Adhikari NK, et al. Assessment of Global Incidence and Mortality of Hospital-treated Sepsis. Current Estimates and Limitations. Am J Respir Crit Care Med 2016; 193(3): 259-72.
(2) Fleischmann-Struzek C, Goldfarb DM, Schlattmann P, Schlapbach LJ, Reinhart K, Kissoon N. The global burden of paediatric and neonatal sepsis: a systematic review. The Lancet Respiratory medicine 2018; 6(3): 223-30.
(3) Laxminarayan R, Matsoso P, Pant S, et al. Access to effective antimicrobials: a worldwide challenge. Lancet 2016; 387(10014): 168-75.
(4) Say L, Chou D, Gemmill A, et al. Global causes of maternal death: a WHO systematic analysis. The Lancet Global health 2014; 2(6): e323-33.
(5) Reproductive, Maternal, Newborn, and Child Health: Disease Control Priorities, Third Edition (Volume 2). In: Black RE, Laxminarayan R, Temmerman M, Walker N, eds. Reproductive, Maternal, Newborn, and Child Health: Disease Control Priorities, Third Edition (Volume 2). Washington (DC): The International Bank for Reconstruction and Development / The World Bank(c) 2016 International Bank for Reconstruction and Development / The World Bank.; 2016.
(6) World Health Organization. WHO Report on the burden of endemic health care-associated infection worldwide. 2017-11-21 15:11:22 2011.
(7) Singer M, Deutschman CS, Seymour CW, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA 2016; 315(8): 801-10.
(8) Gotts JE, Matthay MA. Sepsis: pathophysiology and clinical management. British Medical Journal 2016.
(9) United States Centers for Disease Control and Prevention. Healthcare Professional (HCP) Resources : Sepsis. 2018-02-01T06:23:15Z.
(12) Luangasanatip N, Hongsuwan M, Limmathurotsakul D, et al. Comparative efficacy of interventions to promote hand hygiene in hospital: systematic review and network meta-analysis. British Medical Journal. 2015;351:h3728.
(14) Pruss-Ustun A, Bartram J, Clasen T, et al. Burden of disease from inadequate water, sanitation and hygiene in low- and middle-income settings: a retrospective analysis of data from 145 countries. Tropical medicine & international health : TM & IH 2014; 19(8): 894-905.
(15) World Health Organization. Fact sheet: Immunization coverage. 2018-04-10 14:55:37.
В настоящее время дать сравнительный анализ летальности при сепсисе на основании литературы сложно. Это объясняется неоднозначной трактовкой различными авторами понятия "сепсис" и значительной разнородностью в связи с -угим анализируемых групп больных. Общая летальность, по данным современных авторов, остается высокой и достигает 40-60% (А.И. Трещинский, 1974, 1994; М.И. Кузин, Б.М. Костюченок, 1991). Однако общая летальность отражает усредненные цифры весьма разнородных наблюдений и поэтому вряд ли может служить критерием оценки тяжести течения сепси.са и методов его лечения. Летальность резко меняется в зависимости от возраста больных, вида возбудителя, степени тяжести септического процесса (наличие или отсутствие различных осложнений сепсиса, локализация первичного и метастатических гнойных очагов и их доступность для хирургического лечения, и сопутствующих заболеваний - сердечная недостаточность, сахарный диабет и др.).
Влияние возраста больных на заболеваемость сепсисом и летальность при нем общеизвестны. Наиболее тяжело заболевание протекает у детей младшего возраста и у престарелых. Наибольшая летальность имеет место v больных старше 60 лет, в то время как у детей старшего возраста она составляет 13-15%, а у больных среднего возраста - 25-27%. Летальность среди больных старше 50 лет составляет 30% (J. Nolle, 1977).
Очень велико влияние на летальность вида возбудителя. Общепризнанным является мнение о значительно меньшей летальности при граположи-тельном сепсисе, чем при грамогрикательном. Более высокий процент летальности при грамотрицательном, чем при грамположительном многие авторы объясняют значительно чаще встречающимися осложнениями сепсиса в первом случае. Наиболее тяжелым осложнением является септический шок, при котором летальность достигает 70-80% (B.C. Савельев и со-авт. 986; О.С. Шкроб, М.И. Кузин и др., 1976; М.И. Кузин, Б.М. Костюченок, 1991 и др.). Известно также, что при грамотрицательном сепсисе шок наблюдается в 20-25% случаев, в то время как при грамположительном лишь в 5% . При септическом эндокардите летальность достигает 90% (С. Попки-ров,1977).
Вне зависимости от микробного возбудителя большое значение при оценке летальности имеет локализация гнойных метастазов. При определенной локализации метастазов (легкие, сердце печень, почки и др.) с учетом крайне тяжелого общего состояния больного, хирургическое воздействие на метастатический гнойник становится пракгически невозможным, что значительно ухудшает прогноз заболевания.
Очень важным фактором, влияющим на исход заболевания, по мнению некоторых авторов, является качество проводимой антибактериальной терапии. Нерациональное проведение антибактериальной терапии может вдвое увеличить летальность при сепсисе, по в связи с появлением в клинической практике высокоэффективных антибиотиков широкого спектра действия и рационального их применения удается снизить общую летальность до 21-30,1% (М.И. Кузин, Б.М. Костюченок, 1991; Ю.Л. Шевченко, Н.Н. Шихвер-диев, 1996 и др). О снижении летальности при септическом шоке до 39% в результате разработки и проведения интенсивной терапии сообщают B.C. Савельев и соавт. (1986). Наибольшая зависимосгь результатов лечения наблюдается от состояния больного при "оступлении, возможности проведения полноценной хирургической обработки гнойного очага, возраста больного и вида микрофлоры.
Среди больных, поступающих в крайне тяжелом состоянии (нетранспортабельные, септический шок, выраженная интоксикация или токсико-аллергический синдром, обширные и множественные гнойники, тяжелые сопутствующие заболевания или сочетание этих факторов), летальность достигает 55,3%.
Летальность резко нарастает в зависимости от фазы течения сепсиса. В табл.6 приведены данные о летальности в зависимости от фазы сепсиса (М.И. Кузин, Б.М. Костюченок, 1991).
Летальность в зависимости от фазы сепсиса
| Фаза сепсиса | Число больных | Летальность % % | Число оперированных | Летальность % % |
| Начальная | ||||
| Септицемия | Л Д | 24,^ | ||
| Септикопиемия | 43,2 | 41,1 |
Большое влияние на летальность оказывает возможность или невозможность хирургического лечения септических очагов: среди оперированных летальность составила 26,9%: а среди неоперированных - 57,1%.
Особенно большое влияние на летальность оказывают качество хирургического лечения септических очагов и сроки закрытия раны. Там, гдк в процессе лечения удается произвести радикальную хирургическую обработку раны и закрыть ее в ближайшее время после операции (швами или кожной пластикой) летальность снизилась до 11,1%. В случаях, когда этого сделать не удалось и у больных длительное время существовали гнойные раны (лечение общепринятыми методами), летальность оказалась наибольшей - 71,8% (табл.7).
Таблица 7 Летальность при сепсисе в зависимости от сроков закрытия раны
| Оперативное вмешательство | Число оперированных | Летальность (абс- число) | Летальность (% %) |
| Радикальное | 11,1 | ||
| а) ранние швы | 1,4 | ||
| б) поздние швы и кожная пластика | 34,6 | ||
| Нерадикальное | 71,8 |
Обращает внимание резкое снижение летальности (до 1,4%) у больных, которым удалось произвести полноценную хирургическую обработку и закрыть рану или сразу на операционном столе (первичными швами) или в ближайшие дни после операции (первичными отсроченными или ранними вторичными швами). Цифры летальности, приведенные в таблице.еще раз доказывают целесообразность быстрейшей ликвидации гнойных очагов при сепсисе.
Анализируя причины летальности (по данным литературы) следкет отметить , что у абсолютного большинства погибших больных ведущей была тяжелая гнойная интоксикация, связанная с обширными или множественными гнойными очагами, как поверхностными, так и локализующимися во внутренних органах. На вскрытии у таких больных, помимо гнойных метастазов, обнаруживались типичные для сепсиса дистрофические и дегенеративные изменения во внутренних органах. Непосредственной причиной смерти чаще всего были тромбоэмболия легочной артерии, поражение головного мозга, обширные двусторонние поражения легких с развитием пневмоторакса и кровотечение (в область ствола мозга и забрюшинное пространство).
ЗАКЛЮЧЕНИЕ
В этиологии хирургического сепсиса в последнее время далеко не последнюю роль играет внутригоспитальная инфекция (стафилококк и грамот-рицателвная флора). Нередко при этом непосредственными причинами заболевания служат хирургические операции, диагностические и лечебные манипуляции (хирургическая ятрогепня).
Течение хирургического сепсиса, как правило, находится в прямой зависимости от состояния первичного и вторичных очагов инфекции. В связи с этим у больных необходимо проводить активное хирургическое лечение очагов местной гнойной инфекции на фоне интенсивной общей терапии. Активное хирургическое лечение гнойных очагов направлено на быстрейшую их ликвидацию путем хирургической обработки, дренирования, длительного промывания и раннего закрытия раны. Ликвидация местного гнойного очага значительно улучшает течение сепсиса и создает предпосылки для излечения.
Комплексное лечение больных хирургическим сепсисом и тяжелыми формами гнойной инфекции, направленное на осиоииыс иаюшиетическис факторы, способствует значительному ch.'-cw!!'!!" летальное'". ',' данных больных.
По-прежнему весьма актуальной остается проблема реабилитации больных, перенесших сепсис, ибо он нередко поражает самый работоспособный возраст. Сепсис встречается в практике врачей различных специальностей (хирургов, акушеров-гинекологов, инфекционистов, педиатров, терапевтов). Каждый врач, принимая активное участие в лечении больного сепсисом, ставит перед собой задачу не только сохранить жизнь больному, но и вернуть его к активной профессиональной и общественной деятельности- Решение этого вопроса требует, помимо узко специального подхода, знания основных направлений реабилигационцых мероприятий. Однако до настоящего времени ни в одном из руководств но вопросам реабилитации больных и врачебной трудовой экспертизе нетрудоспособности этот раздел не освещен.
Больной- перенесший острый или подострый сепсис, с первых дней постгоспитального лечения требует к себе серьезного внимания в связи с медленной компенсаторной приспособляемостью к оружающсй среде При составлении индивидуального плана реабилтящш шкого ''"пыкчо следует исходить не только из тяжести перенесенного заболевания, ею особенностей и характера, но и из оценки степени имеющихся компснсаторных проявлении. Иным;:; словами, следует учитывать не только то, ч го угрйЧсни в ири-цессе болезни, а в первую очередь и то, что сохранилось и что может бьпь использовано для построения новых взаимоотношений как во внутренней среде организма, так и в его связях с внешней средой.
В основе нормализации отдельных функции организма в период реабилитации лежит разрушение сформировавшихся в ходе болезни на тологичс-ских условных связей и восстановление свойственной здоровому человеку условно-безусловной их регуляции. Поэтому в период активною ямбунитол-ного наблюдения над больным, перенесшим сепсис, стоят задачи не только пассивного контроля путем исследования лабораторных и функциональных показателей интенсивности воссгановления жизнсобсспсчивпющих систем организма, но и активное влияние на процессы адаптации.
Особое значение с первых дней после выписки 6o.iii.noi о из стационара приобретает вопрос о том, кто должен наблюдать больною, перенесшего сепсис. Очевиден тот факт, что один специалист не можсг полностью решить все вопросы, возникающие в период реабилитации такого больного Динамическое наблюдение над больным должны осуществлять хирург, невропатолог, терапевт и специалист по лечебной физкультуре. Только общими усилиями можно добиться положительных результатов. Причем следует подчеркнуть, что и здесь большое внимание должно уделяться вопросам адаптации к условиям не только физической, но и социальной Среды.
В Э101 период наблюдения над больным нельзя назначать чрезмерное количество лекарственных препаратов (особенно антибактериальные средства), поскольку это еще более снизит адаптационные возможности организма. В первые 2-3 нед после выписки из стационара необходимо вообще отказаться от лекарственной терапии (за исключением симптоматической терапии сердечными средствами) и внушить больному полезность прогулок на свежем воздухе, особенно вблизи лесных массивов по нескольку часов в день, или занятий лечебной физкультурой по индивидуальному плану в зависимости от состояния больного.
Через 2-3 нед, если возникнет в этом необходимость, рационально назначение средств, активизирующих тканевой обмен (женьшень, апилак, пантокрин, экстракт левзеи и т.д.). Однако их назначению должна предшествовать беседа лечащего врача с больным, цель которой - убедить больного в том, что данные средства являются лишь симптоматическими и не следует рассматривать их как панацею в лечении.
Пища должна быть разнообразной, богатой витаминами и соответствовать вкусам больного. Однако в этот период показано и назначение веществ, улучшающих процессы тканевого обмена: оротат калия, инозин, фосфаден, янтарная кислота, сукцинат аммония. Они, участвуя в различных видах обмена, существенно улучшают пластические процессы в организме и способны активно противостоять развитию хронической сердечной недостаточности, дистрофических процессов в печени вследствие длительной токсемии.
Следующим важным моментом реабилитационного периода таких больных является выбор физико-терапевтического и санаторно-курортного лечения. И если первое целесообразно начинять (по согласованию со специалистами-физиотерапевтами) уже вскоре после выписки больного из стационара, то второе - лишь спусгя 6-8 мес с момента выписки в санаториях местной зоны.
Как свидетельствуют исследования К.А. Цыбырне и Л.Г. Андон (1972), при гнойной инфекции происходит значительная иммунная перестройка механизмов защиты, поэтому такие больные нуждаюгся в ежегодном сана-торно-курортном лечении в течение 3-5 лет. Причем профиль санатория в этот период времени может меняться для каждого больного индивидуально, в зависимости от превалирования тех или иных патологических проявлений.
Весьма ответственным моментом является оценка трудоспособности больного. Эдесь следует подходить ciporo индивидуально, учитывая форму перенесенного заболевания, возраст больного, лабильность ЦНС, квалификацию больного и выполняемую работу до заболевания. Необходимо отметить, что во всех случаях вопрос о рациональном трудоустройстве не должен решаться ранее 6 мес с момента заболевания. Кроме того, такие больные требуют перевода на работу, не связанную с охлаждением, сквозняками, тяжелым физическим трудом и нервно-психическим напряжением, что одновременно служит и эффективным средством профилактики хрониосепсиса или рецидива дремлющей инфекции.
Особое значение приобретают меры, направленные на ликвидацию дремлющей инфекции после перенесенного ссисиса.Установлено, что вспышки дремлющей инфр.кцим прртек-яют чя фоне выраженного снижения иммунной защиты организма ив 1,5 раза чаще встречаются после гнойных операций. На фоне вспышки дремлющей инфекции у больных сепсисом вполне вероятно развитие или рецидива заболевания, или переход его в хроническую форму, что вызывает большие сложности в лечении, а порой и является причиной длительной инвалидности. Эти вопросы находятся в ведении ВКК и ВТЭК и должны решаться в срочном порядке.
Что касается лиц молодого возраста, то здесь следует шире ставить вопрос о профессиональной переквалификации больного, если в этом есть объективная необходимость, без ущерба для здоровья. 13 этих случаях целесообразным является оставление за больным 111 группы инвалидности до полной стабилизации процесса.
На основе предоставленных региональными службами статистики данных РБК подсчитал, какие субъекты Федерации в 2018 году вышли в лидеры по количеству умерших от ВИЧ. Официально Росстат и Минздрав пока эти данные не раскрывают.
Лидером по смертности от вируса иммунодефицита человека стала Кемеровская область. Всего в 2018 году там умерли 38,2 тыс. человек, из них 1750 — от ВИЧ, сообщили РБК в территориальном управлении Федеральной службы по государственной статистике в Кемеровской области.
Коэффициент смертности от ВИЧ составляет 65,1 случая на 100 тыс. жителей региона — это больше, чем от всех отравлений алкоголем, самоубийств, убийств, утоплений и ДТП вместе взятых. Для сравнения: по данным ВОЗ за 2017 год, в Зимбабве и ЮАР — странах с самой высокой смертностью от вируса — этот показатель составил 133 и 190 умерших на 100 тыс. жителей соответственно.
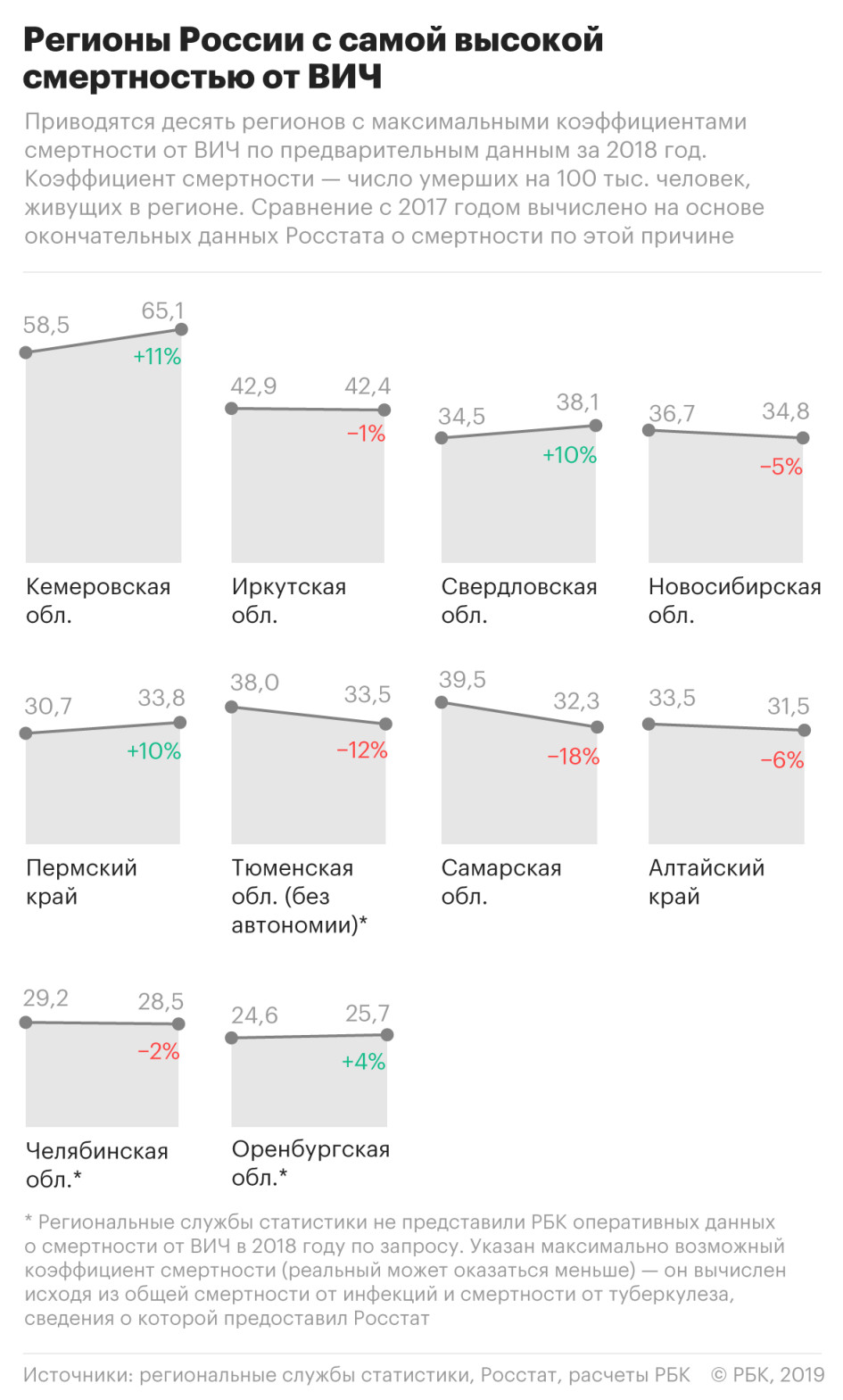
В Иркутской области коэффициент смертности от ВИЧ — 42,4 случая на 100 тыс. жителей, или порядка четырех человек из каждой сотни умерших. В Свердловской области от ВИЧ умерли более 1,6 тыс. человек, коэффициент смертности составил 38,1 случая на 100 тыс. В этих регионах смертность от ВИЧ также больше, чем от всех произошедших в регионе убийств, самоубийств и ДТП вместе взятых.
В 2017 году в тройку регионов с самым высоким коэффициентом смертности от ВИЧ входила Самарская область, но за 2018 год этот показатель у нее упал на 18% — с 39,5 случая на 100 тыс. населения до 32,2. При этом регион по-прежнему входит в топ-10 по смертности от ВИЧ.
В апреле 2018 года главный государственный санитарный врач России Анна Попова заявляла, что лидеры по числу носителей ВИЧ — Свердловская, Иркутская, Кемеровская, Самарская, Оренбургская области, Ханты-Мансийский автономный округ, Ленинградская, Челябинская, Тюменская, Новосибирская области. Причина, как полагает Попова, в том, что в 1990-е годы через эти регионы проходил наркотрафик. А основной способ передачи ВИЧ до недавнего времени — через зараженную иглу.
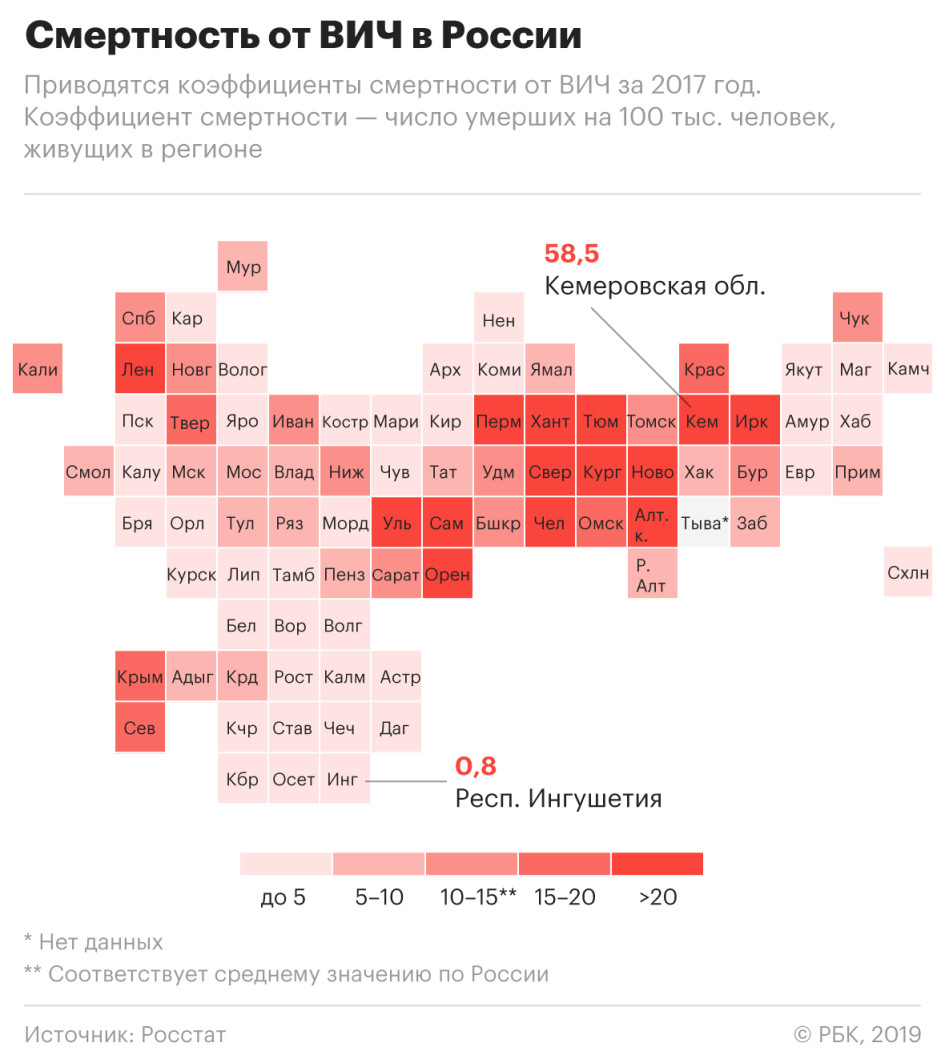
Зависимость смертности от ВИЧ от наркотрафика
Регионы, смертность в которых от ВИЧ была максимальной по России в 2018 году, частично пересекаются с регионами, где в 2018 году было изъято максимальное количество наркотических средств опийной группы. Это Москва, Еврейская автономная область, Московская область, Челябинская область, Самарская область, Кемеровская область, Омская область, Свердловская область, Башкирия, Иркутская и Новосибирская области.
Смертность от ВИЧ в России выросла
Всего в 2017 году от ВИЧ умерли 20 тыс. человек, на 1,5 тыс. больше, чем годом ранее.
Официальных данных по смертности за 2018 год пока нет (Росстат не предоставил РБК предварительные сведения о смертности от ВИЧ в 2018 году), но можно сделать вывод, что в целом по России она выросла. Основная смертельная инфекция в России на протяжении нескольких лет помимо ВИЧ — туберкулез. В 2018 году смертность от этого заболевания, по предварительным данным, снизилась на 11,6%, а общая смертность от инфекций уменьшилась на 0,9%. Из этого следует, что выросла смертность либо от ВИЧ, либо от других инфекций, о которых Росстат не сообщает в оперативных данных. При этом смертность от всех остальных инфекций, за исключением туберкулеза и ВИЧ, на протяжении многих лет была стабильной, а в 2017 году даже снизилась.
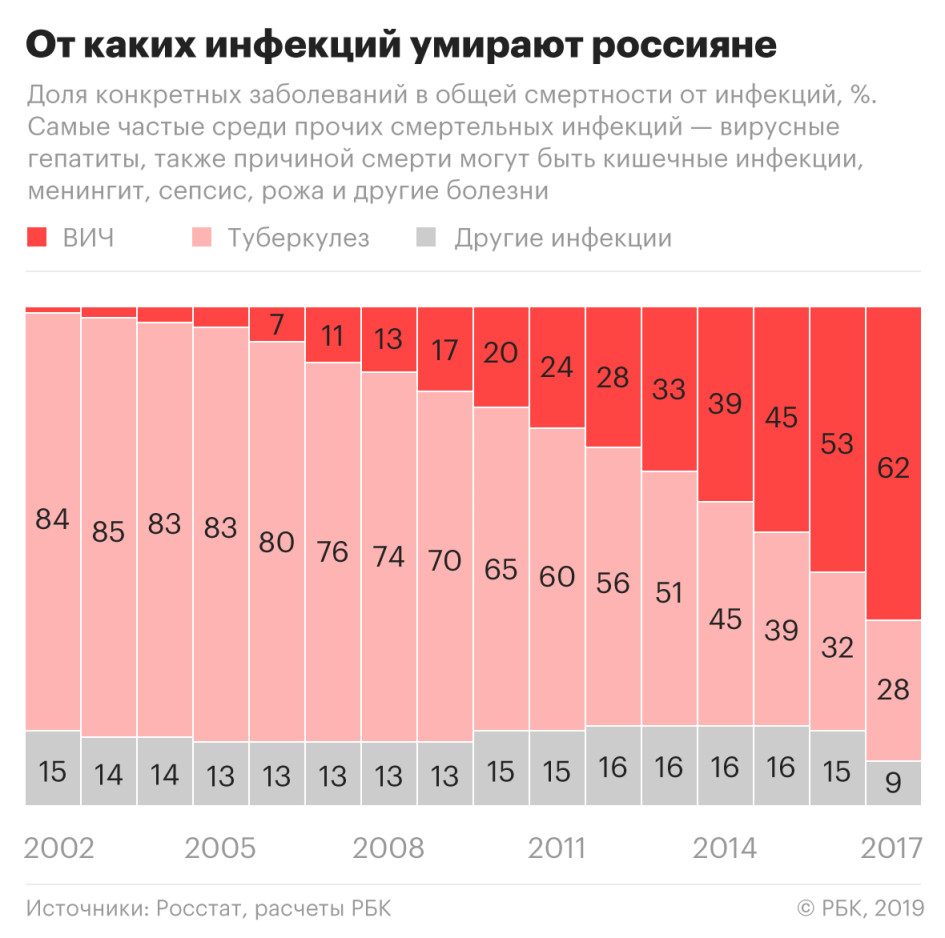
Что входит в другие инфекции
Среди других инфекций, заканчивающихся смертью, в статистике Минздрава проходят гепатиты, кишечные инфекции, менингит, сепсис, рожа. Хотя смерть от гепатита случается чаще, замечает Михайлов, чем от кишечных инфекций, Росстат и Минздрав не публикуют статистику заболеваемости и смертности от гепатитов.
В России растет смертность от инфекций
На основе предоставленной территориальными органами Росстата статистики о смертности можно также сделать вывод, что в 2018 году в каждых двух из пяти российских регионов выросла смертность от инфекций.
Сильнее всего смертность от инфекций выросла в Марий Эл и Удмуртии — на 22% в каждом субъекте. В Марий Эл это связано с ростом смертности от туберкулеза — в 2018 году там от него умерли 37 человек против 25 годом ранее. В Удмуртии рост смертности от инфекций связан с ВИЧ и гепатитами — как сообщили РБК в Удмуртстате, от ВИЧ умерли 219 человек, что на 38% больше, чем в 2017 году. От вирусных гепатитов умерли 17 человек против трех годом ранее.
Рост смертности от инфекций обусловлен ВИЧ и гепатитами и в Тульской области. В региональной службе статистики сообщили, что, по предварительным данным, от этих инфекций в 2018 году умерли 163 человека против 146 годом ранее.
В Москве смертность от инфекций за год выросла на 15%, хотя смертность от ВИЧ и туберкулеза уменьшилась. От каких инфекций москвичи умирали в 2018 году, в Мосгорстате не сообщили.
В Омской области рост смертности от инфекций составил 13%, от ВИЧ — 26%. В Саратовской области рост смертности от инфекций также обусловлен смертностью от ВИЧ — она выросла на 13%. И в том и в другом регионе смертность от туберкулеза при этом упала, как и по всей России.
Об этом же говорит Покровский. Академик заметил, что последние три года смерти от турбович стараются фиксировать как смерти от ВИЧ.
РБК направил в Министерство здравоохранения запрос с просьбой прокомментировать статистические данные.
РБК получил в Росстате данные о смертности от ВИЧ в регионах России в 2017 году. В территориальных органах статистики были запрошены оперативные данные о смертности от ВИЧ. Запросы были отправлены в регионы, в которых были наибольшие показатели смертности от ВИЧ в 2017 году, а также в регионы, в которых резко выросла смертность от инфекций, но не за счет туберкулеза. Всего РБК запросил сведения в 18 регионах, которые в 2017 году дали две трети всей смертности от ВИЧ в России.
Не все региональные службы статистики смогли предоставить сведения о смертности от ВИЧ за январь—декабрь 2018 года. Исходя из опубликованных ранее Росстатом данных о числе умерших от всех инфекций в каждом регионе в 2018 году и оперативных сведений о смертности от туберкулеза был вычислен максимальный возможный коэффициент смертности от ВИЧ для каждого региона. Например, в Тюменской области в 2018 году от инфекций умерли 595 человек, из них от туберкулеза — 92 человека. Следовательно, от ВИЧ умерли не более 503 человек, и коэффициент смертности от ВИЧ в регионе составит не более 33,5 на 100 тыс. живущих (исходя из того, что в регионе живут 1,5 млн человек).
Читайте также:


