Отек легких при сепсисе
Отек легких является неотложной ситуацией, требующей немедленной медицинской помощи.
Отек легких МКБ 10 имеет код J81.
Патофизиология
В нормально функционирующих легких имеется небольшой приток жидкости из альвеолярных капилляров в интерстициальное пространство легких, чему способствуют гидростатические силы и наличие микроскопических щелей между капиллярными эндотелиальными клетками. Скорость поступления жидкости ограничивается градиентом осмотического давления белка, способствующим перемещению жидкости из интерстициального пространства обратно в циркулирующую плазму. В результате относительно небольшое физиологическое перемещение жидкости из сосудистой сети в легкие обычно компенсируется оттоком жидкости из интерстициального пространства легкого через легочную лимфатическую систему, которая в конечном счете возвращается в системный венозный кровоток. Поскольку жидкость проходит через интерстициального пространства легких, она отграничивается от альвеолярного пространства плотными окклюзирующими соединениями между альвеолярными эпителиальными клетками. В отсутствие острого повреждения легких (например капиллярного повреждения) изменение скорости потока жидкости через легкие определяется, прежде всего, изменением гидростатического давления. Давление заклинивания легочных капилляров (ДЗЛК), регистрируемое с баллончика катетера в момент его заклинивания в сегменте легочной артерии, является отражением давления наполнения левого предсердия и считается наиболее полно отражающим гидростатическое давление микроциркуляции легкого.
- Q = Чистая фильтрация жидкости через сосудистую стенку в направлении интерстициального пространства (поток жидкости, фильтрующийся через стенку капилляра в интерстициальное пространство)
- К = Коэффициент фильтрации
- Ppmv = Гидростатическое давление в околососудистом интерстициальном пространстве
- Pmv = Гидростатическое давление внутри капилляров (ДЗЛК)
- πmv = Осмотическое давление белка сосудистом русле
- πpmv = Осмотическое давление белка в околососудистом интерстициальном пространстве
Хотя уравнение Старлинга полезно для понимания механизмов, благоприятствующих образованию отека легких, клинически является нецелесообразным точно измерять большинство из этих параметров. Тем не менее базовое понимание этого уравнения полезно для клиницистов, работающих с пациентами с отеком легких.
При кардиогенном отеке легких гидростатическое давление в легочных капиллярах приводит к увеличению фильтрации жидкости через сосудистую стенку и чаще всего вызывается объемной перегрузкой или нарушением функции левого желудочка, приводящей к повышенному легочному сосудистому давлению. Умеренное повышение давления в левом предсердии, выражаемое в виде ДЗЛК 18-25 мм рт. ст., вызывает образование отеков в периваскулярном и перибронхиальном интерстициальных пространствах. При дальнейшем повышении давления в левом предсердии (ДЗЛК > 25 мм рт. ст.), емкость лимфатических сосудов и интерстициального пространства (ориентировочно 500 мл жидкости) превышается, и жидкость преодолевает легочный эпителиальный барьер, заполняя альвеолы жидкостью, содержащей белок. Клиника гипоксимии обусловлена накоплением альвеолярной жидкости, дестабилизацией альвеолярных ацинусов (нарушением функции сурфактанта) и, следовательно, нарушением вентиляционно-перфузионного отношения (V/Q).
Некардиогенный отек легких относится к любому состоянию, способствующему аномальному увеличению проницаемости сосудов легких, тем самым способствует увеличению потока жидкости и белка в интерстициальное пространство и воздушные пространства легких. Что касается уравнения Старлинга, то повреждение легочных сосудов приравнивается к увеличению коэффициента фильтрации и увеличению осмотического давления в интерстициальном пространстве легкого, что способствует формированию отека легких. Другой фактор, способствующий нарушению газообмена при некардиогенном отеке легких, связан с нарушением альвеолярного эпителиального барьера, например, когда давление в интерстициальном пространстве легких достаточно высокое, чтобы нарушить плотные контакты, или при прямом воспалительном или токсическом повреждении эпителиальной оболочки альвеол. Поврежденный альвеолярный эпителий обладает пониженной способностью к активному переносу жидкости из альвеолярного пространства в интерстициальное пространство легкого и вызывает нарушение продукции сурфактанта (снижение активной поверхности), благоприятствующее альвеолярному коллапсу при нормальном дыхании. Примером служит прямое повреждение альвеолярного эпителия за счет аспирации содержимого желудка или пневмонии. Условия, которые способствуют острому капиллярному эндотелиальному повреждению легких, включают системные инфекции (сепсис), тяжелые ожоги, травму и другие системные воспалительные состояния. Повреждение эндотелия капилляров легких и/или альвеолярного эпителия является отличительной чертой острого повреждения легких (ОПЛ) и острого респираторного дистресс-синдрома (ОРДС), которые представляют собой прогрессирующие некардиогенные повреждения легких, связанные с нарушением газообмена (шунтирование, нарушение V/Q отношений) и снижением легочной растяжимости (повышенная работа дыхания).
Причины
Отек легких по ричинам наиболее часто подразделяется на:
- кардиогенный (повышенное гидростатическое давление),
- некардиогенный (повышенная микрососудистая проницаемость).
Однако у пациентов в критическом состоянии обычно встречается отек легких, обусловленный комбинацией кардиогенной и некардиогенной причин. Отек легких является серьезной проблемой для здоровья, которая обуславливает 10% случаев поступлений в отделение реанимации и интенсивной терапии (ОРИТ) и сопровождается ожидаемой госпитальной летальностью в 10-25 %, при этом смертность в течении года превышает 40%.
Для медицинского персонала важно быстро установить причину отека легких для быстрейшего начала соответствующей терапии и избегания серьезных жизнеугрожающих осложнений. Например, пациент с острым отрывом хорд митрального клапана будет нуждаться в сокращении постнагрузки (например, при использовании периферических вазодилататоров, внутриаортальной баллонной контрпульсации) и экстренной операции на митральном клапане, тогда как пациент с ОРДС, связанной с сепсисом, требует высоких концентраций кислорода на вдохе, вентиляции с положительным давлением и раннего назначения антибиотиков. К сожалению, причину отека легких в условиях критического состояния бывает трудно установить, и для этого требуется квалифицированный врач с соответствующими диагностическими методами.
Симптомы
Общие клинические проявления отека легких (любой причины) включают острое появление одышки, беспокойство, ортопноэ, а в некоторых случаях пенистую мокроту (кровянистого цвета). При обследовании у пациентов наблюдаются признаки повышенного симпатического тонуса (тахикардия, гипертония), усиленная работа дыхания (например участие вспомогательных мышц и повышенное потоотделение), на вдохе инспираторные хрипы в легких и периферический цианоз.
Помимо ранее описанных клинических симптомов отека легких, анамнестические данные, такие как недавний инфаркт миокарда, вновь развившиеся сердечные аритмии, набухание яремных вен, третий тон сердца (S3), новые шумы и/или отеки соответствующей локализации (отек на конечностях, зависимые от положения тела), будут свидетельствовать больше в пользу диагноза кардиогенного отека легких, нежели некардиогенного. Наличие кардиомегалии по результатам рентгенографии органов грудной клетки, картина интерстициальных и альвеолярных теней центральной локализации и/или наличие плевральных выпотов дополнительно подтверждают диагноз кардиогенного отека легких. Другие доказательства включают в себя повышенный уровень мозгового натрийуретического пептида (BNP > 1200 пг/мл) или тропонина — маркер острого повреждения миокарда. Однако эти биомаркеры не обладают диагностической специфичностью. Визуализация сердца, особенно эхокардиография, весьма полезна для диагностики и, как показано, меняет тактику ведения большого процента пациентов в критическом состоянии с острым отеком легких. Использование инвазивных способов измерения давление наполнения левого желудочка может быть полезным в сложных случаях (например, при лечении рефрактерного отека легких), но в значительной степени заменено менее инвазивными подходами (например, мониторинг центрального венозного давления (ЦВД), транспульмональная термодилюция).
ОПЛ и ОРДС охватывают спектр аномалий газообмена от умеренной до тяжелой степени, возникающих вследствие измененной проницаемости легочных сосудов, что часто осложняется альвеолярным эпителиальным повреждением. Дифференциальный диагноз ОПЛ/ОРДС основывается на классификации процессов, вызывающих прямое или непрямое повреждения легких, наиболее распространенными прямыми причинами являются тяжелые легочные инфекции и аспирационная пневмония, тогда как тяжелые инфекции (сепсис), множественные переливания крови и травмы являются частыми причинами непрямого ОПЛ
Согласно Берлинским дефинициям, термина ОПЛ более не существует!
Высоко специфические диагностические тесты для ОПЛ/ ОРДС отсутствуют, и дифференциация ОПЛ/ОРДС от кардиогенного отека легких во многом опирается на клиническую проницательность персонала отделений критической медицины. В связи с этим детали анамнеза данного заболевания в связи с известными факторами риска ОПЛ часто представляют собой ключевые точки диагностики, а некоторые объективные исследования и результаты лабораторных исследований (например BNP Нейрогенный отек легких
Нейрогенный отек легких происходит вследствие обширного повреждения центральной нервной системы и чаще всего вызывается состояниями, связанными с быстрыми и экстремальным повышением внутричерепного давления (ВЧД), а также при остром повреждении спинного мозга, внутричерепном кровоизлияния или во время эпилептического статуса. Первичными механизмами являются активация симпатической нервной системы и высвобождение катехоламинов. Состояние обычно разрешается в течение 48 часов после нормализации ВЧД.
Это осложнение переливания компонентов крови, содержащих плазму, которое характеризуется острым (в течение 6 часов) появлением одышки, гипоксемией и двусторонними легочными инфильтратами, которые опосредованы наличием анти-HLA антител (HLA — Human Leukocyte Antigen — человеческий лейкоцитарный антиген — ЧЛА), активацией нейтрофилов и связанным с ней поражением эндотелиального барьера. Диагноз TRALI-синдрома устанавливается клинически при исключении кардиогенного отека или перегрузки жидкостью. Кроме того, низкий уровень BNP ( Отек легких на фоне быстрого расправления
Обычно это происходит в течение нескольких часов после дренирования большого по объему плеврального выпота в случаях длительно существующего (> 72 часов) коллапса легких. Сопутствующие симптомы варьируют от легких до жизнеугрожающих, включая одышку, кашель с пенистой мокротой, дискомфорт в грудной клетке и гипоксемическую дыхательную недостаточность. Для отека легких подобного типа типичен односторонний характер картины на рентгенографии органов грудной клетки, но иногда он может отмечаться в контралатеральном легком или в обоих легких. Большинство пациентов полностью восстанавливаются на фоне поддерживающей терапии в течение нескольких дней. Стратегия профилактики включает прекращение удаления плевральной жидкости при появлении любых признаков дискомфорта в грудной клетке, ограничение объема удаляемой жидкости до Отек легких на фоне отрицательного давления (ОЛОД)
Отек легких на фоне отрицательного давления редко проявляется непосредственно в постэкстубационном периоде после острого появления отрицательного внутригрудного давления, возникающего при попытках вдоха и при наличии обструкции верхних дыхательных путей. ОЛОД встречается менее чем в 0,1 % всех плановых операций и наиболее часто встречается у молодых, здоровых и атлетически сложенных пациентов во время постэкстубационного ларингоспазма. Другими причинами ОЛОД являются странгуляция (или повешение), тяжелые формы сонного апноэ, окклюзия эндотрахеальной трубки или эпиглотит. Как и при отеке легких на фоне быстрого расправления, ОЛОД обычно разрешается в течение нескольких дней.
Диагностика и дифференциальная диагностика отека легких

В таблице выше приведены типичные клинические симптомы, которые отличают кардиогенный от некардиогенного отека легких. По иронии, катетеризация легочной артерии, наиболее точная диагностическая методика, более не используется в повседневной практике из-за частых осложнений (например кровотечение, пневмоторакс, аритмии, инфекции, травмы сосудов) и ее ненадежности из-за неправильной калибровки или неправильной интерпретации данных. Таким образом, менее инвазивные методы в значительной степени заменили катетеры легочной артерии для рутинной оценки кардиогенных причин отека легких в условиях ОРИТ.
Чреспищеводная эхокардиография (ЧПЭхоКГ) является наиболее широко распространенной методикой для оценки критических пациентов с подозрением на сердечную недостаточность. В контексте отека легких, с использованием ЧПЭхоКГ можно быстро обнаружить серьезные сердечные заболевания, связанных с повышенным давлением наполнения левого желудочка, в том числе нарушенную фракцию выброса левого желудочка из-за ишемических (как правило, вызывающих аномалии движения в участках стенок) или неишемических (с диффузными нарушениями движения стенок) заболеваний миокарда, значимыми поражениями клапанов или перикардиальным выпотом, вызывающим патофизиологический механизм тампонады.
Для оценки отека легких появились два альтернативных метода.
- Система постоянной оценки сердечного выброса по пульсовой волне (PiCCO) оценивает индекс сосудистой проницаемости в легких у пациентов, находящихся в критическом состоянии.
- Количественный компьютерно-томографический анализ (ККТ) с термодилюцией также применялся для диагностики отека легких на фоне ОРДС.
На данный момент ни одно исследование не показало преимущества PiCCO или ККТ по сравнению с традиционными подходами (например с ЦВД-ориентированными) для оценки отека легких, как осложнения ОРДС.
Лечение
Подходы к лечению отека легких разделяются как вмешательства на сердце и сосудах или вмешательства на легких. Сердечно-сосудистые вмешательства направлены на уменьшение потока капиллярной жидкости в легкие за счет уменьшения давления в легочных капилляров. Такие вмешательства направлены на снижение постнагрузки (например петлевые диуретики, нитраты или ультрафильтрация при почечной недостаточности), снижение преднагрузки (системные вазодилататоры, включая нитраты, ингибиторы ангиотензинпревращающего фермента (и-АПФ), ингибиторы фосфодиэстеразы), или оптимизацию сердечной сократимости при нарушении функции левого желудочка (катехоламины, ингибиторы фосфодиэстеразы (иФДЭ), внутриаортальная баллонная контрпульсация). Наиболее эффективное, в условиях кардиогенного отека легких, снижение гидростатического давления в капиллярном русле может также уменьшить тяжесть отека и при некардиогенном отеке легких.

Лечение кардиогенного отека легких
Коррекция функции легких предназначена для оптимизации газообмена, особенно оксигенации, путем рекрутирования нестабильных, коллабированных или заполненных жидкостью альвеол, главным образом, путем использования положительного давления в конце выдоха (ПДКВ). ПДКВ, как правило 5-15 см вод. ст., противодействует альвеолярному коллапсу во время цикла вентиляции за счет увеличения V/Q отношения и, следовательно, диффузии кислорода из альвеол в кровь. Стабилизация альвеол также уменьшает работу дыхания, улучшая обмен CO, (то есть снижая частоту вентиляции) и растяжимость легких. В дополнение к ПДКВ для поддержания адекватной оксигенации часто необходимо увеличить фракцию вдыхаемого кислорода (FiO2). ПДКВ может быть обеспечено плотно прилегающей лицевой маской в виде постоянного положительного давления в дыхательных путях (СРАР) или неинвазивной вентиляции с положительным давлением (НВПД), при котором инспираторная поддержка дополняется ПДКВ (двухуровневая вентиляция). Вентиляция с положительным давлением дополнительно уменьшает кардиогенный отек легких, снижая как пред-, так и постнагрузку. Раннее использование НВПД при респираторном дистрессе на фоне кардиогенного отека легких должно быть хорошо продумано, поскольку оно обеспечивает поддержку в ожидании эффектов вышеупомянутых медицинских вмешательств. Было показано, что НВПД уменьшает как необходимость эндотрахеальной интубации, так и риск ранней летальности, а также уменьшает продолжительность пребывания в ОРИТ. НВПД является полезным дополнением к медикаментозной терапии, однако неясно, может ли двухуровневая NIPPV превосходить СРАР для уменьшении одышки, улучшения работы дыхания, оксигенации и поддержания PaCO2. Пациентам с чрезвычайно высокой работой дыхания или измененным психическим статусом могут потребоваться эндотрахеальная интубация и седация.
В случае необходимости искусственной вентиляции легких в условиях некардиогенного отека легких, рекомендуется использовать стратегию вентиляции легких низкими дыхательными объемами (6 мл/кг идеальной массы тела или менее), чтобы минимизировать повреждение легких и тяжесть отека легких.
- Отек легких классифицируется на кардиогенный (повышенное гидростатическое давление) или некардиогенный (повышенная микрососудистая проницаемость). Однако у критических пациентов обычно наблюдается отек легких за счет комбинации обеих причин.
- Общими клиническими проявлениями отека легких (любой причины) являются острое начало одышки, беспокойство, ортопноэ, а в некоторых случаях — розовая (окрашенная кровью) пенистая мокрота. При обследовании у пациентов наблюдаются признаки повышенного симпатического тонуса (тахикардия, гипертония), усиленная работа дыхания (например, использование вспомогательных мышц и потоотделение), инспираторные хрипы в легких и периферический цианоз.
- В дополнение к анамнезу и осмотру, лабораторные исследования (тропонин, BNP) и визуализация (РГК, эхокардиография) могут быть полезными при дифференцировке кардиогенных и некардиогенных причин отека легких.
- Лечение должно быть направлено на устранение причины отека легких. Кроме того, при респираторном дистрессе на фоне кардиогенного отека легких следует как можно раньше использовать режим NIPPV, поскольку он обеспечивает поддержку, пока другие медицинские вмешательства не станут доступны.
Beth Y. Besecker и Elliott D. Crouser (перевод: Г. Саед)
Общие сведения
Отек легких — это клинический синдром, в основе которого избыточная транссудация жидкости из венул/капилляров в интерстициальную легочную ткань, а затем — в альвеолы и сопровождающийся выраженным нарушением газообмена в легких с развитием гипоксии различных тканей, ацидоза, угнетением функций ЦНС. Код отек легких по МКБ-10: J81. Этот клинический синдром может быть осложнением различных кардиологических, пульмонологических урологических, гинекологических, неврологических, гастроэнтерологических заболеваний.
В клинической практике чаще встречается кардиогенный отек легких, являющийся осложнением ОСН. В большинстве случаев кардиогенный отек развивается при ИБС, ХСН, острых нарушений сердечного ритма, патологии клапанов при которых развиваются застойные явления в легких. В пожилом возрасте преобладает ИБС, а в молодом — превалируют пороки сердца, дилатационная кардиомиопатия, миокардиты.
Относится к жизнеугрожающим осложнениям, требующим принятия неотложных мер. Промедление с оказанием врачебной помощи при отеке легких, приводит к летальному исходу.
В основе развития патологического процесса — повышение давления (постепенное/резкое) в малом круге кровообращения. При этом, важнейшее значение имеет непосредственно скорость развития патологического процесса, поскольку вероятность возникновения кардиогенного отека значительно выше при остро возникших нарушениях, так как в таких ситуациях компенсаторные механизмы не срабатывают (не успевают купировать/уменьшить их последствия). В случаях более постепенного развития процесса недостаточности кровообращения и нарастаниях клинических проявлений последствия чаще не столь драматические.
Некардиогенный отек легких развивается как при прямом повреждении легких (ингаляция токсинов/токсичных газов, аспирация содержимого ЖКТ, воды, крови, ожоги, пневмонии), так и при внелегочных заболеваниях (шок, тяжелая политравма, сепсис, массивная кровопотеря, панкреатит/панкреонекроз, гемотрансфузия, уремия) встречается значительно реже. Еще одним синдромом, проявляющимся некардиогенным отеком легких и острой дыхательной недостаточностью является ОРДС — острый первичный/вторичный респираторный дистресс-синдром (синоним мокрое легкое, шоковое легкое). Развитие этого типа отека обусловлено преимущественно нарушением функции/структуры альвеолокапиллярной мембраны.
Согласно современным представлениям о первичном ОРДС повреждающий фактор оказывает влияние непосредственно на альвеолоциты, сурфактант, приводящих к повреждению эпителия альвеол и нарушению целостность альвеолокапиллярной мембраны в результате чего происходит трансфузия жидкой составляющей крови в альвеолярные пространства. При вторичном ОРДС в основе лежит внелегочный фактор, формирующийся на фоне синдрома воспалительной реакции в организме (сепсис, бактериемия). Отек такого типа (шоковое легкое) не подчиняется законам транспорта жидкости и не зависит от уровня гидростатического давления.
Его особенностью является резкое снижение вентиляции/оксигенации организма, вызывающее застой в легких, кислородную недостаточность тканей головного мозга и сердца с быстрым развитием состояний, угрожающих жизни. При неадекватной/несвоевременно оказанной помощи летальность достигает 65-80%.
Патогенез
Патогенез отека легких определяется его типом (кардиогенный/некардиогенный). Соответственно различают гидростатический и мембраногенный механизм развития отека.
Основным этиологическим фактором являются заболевания сердечно-сосудистой системы, при которых происходит повышение внутри капиллярного гидростатического давления. При достижении давления 15 мм рт. ст. происходит трансфузия плазмы крови в интерстиций в объеме, который превышает физиологическую возможность удаления её путем лимфооттока. При росте давления до 20 мм рт. ст. и выше жидкость поступает на поверхность альвеол. Механизм развития отека этого типа основан на законе Франка-Старлинга, описывающего закономерности обмена жидких сред в тканях легких. В рамках статьи нет возможности расшифровки каждого из действующих факторов формулы. Выделим лишь основные последовательно сменяющиеся взаимосвязанные этапы патологического процесса:
- Повышение гидростатического давления в малом круге кровообращения, способствующее повышению давления в легочной артерии и затем внутри капилляров легких.
- Повышение фильтрации жидкости из лёгочных сосудов непосредственно в ткань.
- Образование избыточного отрицательного давления в интерстициальном пространстве легких и развитие интерстициального отека.
- Декомпенсация оттока жидкости через лимфопути.
- Развитие альвеолярного отека (наблюдается развернутая клиника отека легких).
- Сокращение площади газообмена и дезорганизация механизма газообмена между наружной воздушной средой и кровью.
- Состояние гипоксии, которое, в свою очередь, провоцирует продуцирование гормонов стресса, катехоламинов, что приводит к еще большему нарастанию артериального давления и снижению проницаемости сосудов, дополнительно увеличивая нагрузку на левый желудочек сердца, формируя тем самым порочный круг.
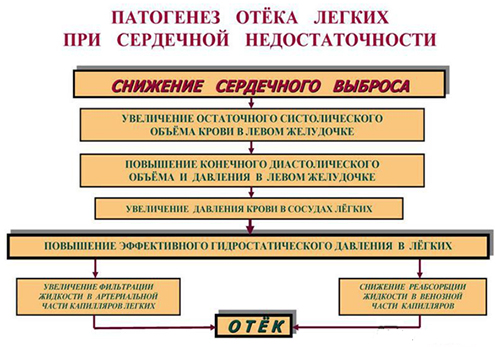
На рисунке схематически представлен патогенез отека легких кардиогенного типа
Его развитие обусловлено первичным повышением проницаемости и нарушением функции альвеолярно-капиллярной мембраны, что вызвано повреждением эпителия альвеол и эндотелия капилляров. Повышение проницательности происходит под воздействием токсичных кислородных радикалов, протеиназ, простагландинов, лейкотриенов, гистамина, образующихся или освобождающихся в ткани под воздействием на нее различного рода раздражителей.
Повышение проницаемости легочных капилляров быстро приводит к появлению большого количества отечной жидкости, в которой содержится много белка. При этом, изменения проницаемости альвеолярной и капиллярной части барьера происходит не одночастно. Вначале повышается проницаемость эндотелиального слоя, что приводит к пропотеванию сосудистой жидкости в интерстиций, где она временно накапливается (интерстициальный отек легких). При этом, интерстициальный отек частично компенсируется за счет ускорения лимфооттока. В большинстве случаев эта приспособительная реакция является недостаточной, и постепенно отечная жидкость проникает через поверхность деструктивно измененных клеток альвеол в их полость, заполняя весь объем.
Развивается альвеолярный отек легких. Выключение из процесса газообмена части альвеол компенсируется растяжением (эмфиземой) еще оставшихся неповрежденных альвеол, что приводит к сдавливанию лимфатических сосудов и капилляров легких. Альвеолярный отек развивается при заполнении альвеол жидкостью и характеризуется появлением выраженных нарушений со стороны дыхательной системы, развитием артериальной гипоксемии/гиперкапнии.
На этом фоне изменяется микроциркуляция/повышается вязкость крови (развитие ДВС-синдрома). Нарушается реактивность сосудов и тонус мышечной ткани бронхов, снижается активность сурфактанта, что приводит к развитию микроателектаз. Нарастает гиповентиляция альвеол, приводящая к несоответствию между перфузией и вентиляцией, изменению диффузии углекислого газа/кислорода и снижению снабжения тканей кислородом с развитием гипоксии и метаболического ацидоза.
Мембраногенный отёк лёгких развивается при воздействии различных типов повреждающих факторов, одним из которых являются токсиканты различного генеза, на примере которых более подробно рассмотрим патогенез токсического отека.
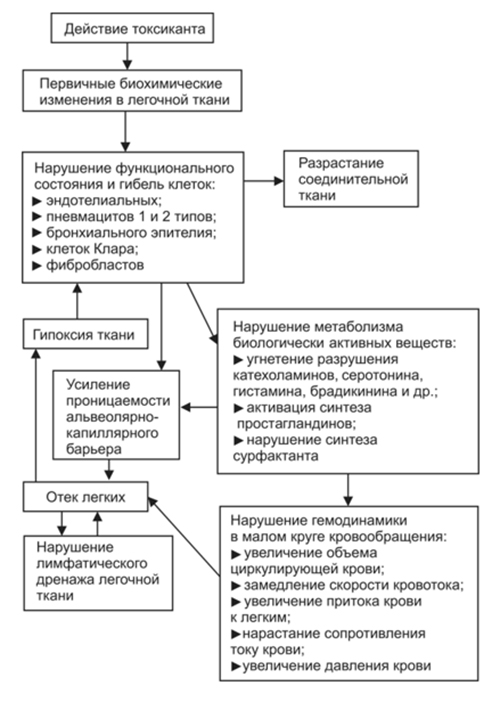
На рисунке схематически представлен патогенез токсического отека легких
Токсический отек легких. Патогенез отека легких такого типа обусловлен воздействием токсикантов непосредственно на клетки альвеолярно-капиллярного барьера с нарушением их функции. Токсический отек имеет различные механизмы повреждения клеток легких, но развивающиеся за этим патологические процессы достаточно схожи. При повреждении/гибели клеток происходит усиление проницаемости барьера и резкому к усилению процессов выработки в легочной ткани биологически активных веществ (гистамина, норадреналина, ангиотензина, ацетилхолина, серотонина, простагландинов) что способствует дальнейшему повышению проницаемости/нарушению функции альвеолярно-капиллярного барьера и развитию нарушений гемодинамики в легких (уменьшается скорость кровотока, растет давление в малом круге кровообращения). По мере прогрессирования отека респираторные и терминальные бронхиолы заполняет жидкость, а под действием турбулентности, возникающей при движении воздуха, образуется пена в дыхательных путях.
Отек легких смешанного типа. В основе развития сочетание механизмов отека обоих типов.
Классификация
Единой общепринятой классификации отека легких нет. Общепризнанным является разделение отека легких на кардиогенный и некардиогенный.
Кардиогенный отек легких в свою очередь разделяют по нескольким признакам.
По наличию/отсутствию в анамнезе ХСН:
- Впервые возникший (без наличия в анамнезе ХСН).
- Декомпенсированный (острая декомпенсация ХСН).
По причине возникновения:
- Левожелудочковая недостаточность (аритмии; острый коронарный синдром; миокардит/перикардит/эндокардит; дисфункции клапанов — митральная недостаточность, аортальный стеноз и др.).
- Увеличение внутрисосудистого объема (почечная недостаточность, объемная перегрузка).
- Легочная венозная обструкция (стеноз митрального клапана).
Некардиогенный отек разделяют на:
- Первичный — связанный с наличием повреждающего фактора непосредственно в легочной ткани.
- Вторичный — развивающегося при наличии внелегочного фактора и выраженном системном воспалении.
По течению выделяют:
- Молниеносный отек – бурное развитие на протяжении нескольких минут, летальный исход.
- Острый отек – быстро нарастает (на протяжении до 4-х часов). Развивается преимущественно при инфаркте миокарда, анафилаксии, черепно-мозговых травмах. Даже при своевременно проведенных реанимационных мероприятиях высокий риск летального исхода.
- Подострый отек – характеризуется волнообразным течением с постепенным нарастанием симптоматики и ее стиханием. Наблюдается чаще при эндогенной интоксикации организма различного генеза (печеночной недостаточности, сепсисе, уремии).
- Затяжной отек – период развития от 12 часов до 1-3 суток. Часто протекает стерто, с невыраженной симптоматикой без характерных клинических признаков. Встречается чаще при хронических заболеваниях легких, ХСН.
Причины отека легкого
Основной причиной отека легкого при болезни сердца (кардиогенного отека) является увеличение гидростатического давления в капиллярной системе легочной артерии. Наиболее частой причиной, от чего бывает отек является застойная сердечная, чаще левожелудочковая недостаточность, обусловленная снижением сократительной возможности миокарда, перегрузкой объемом/давлением или патологией клапанов сердца. Нарастающий дисбаланс артериального/венозного кровенаполнения, развитие в малом кругу кровообращения выраженного венозного застоя является неблагоприятным прогностическим признаком. Венозный застой в легких что это такое? Это нарушение гемодинамики малого круга кровообращения, характеризующийся переполнением венозного участка кровеносного русла кровью, обусловленное расстройствами сердечной деятельности.
Причинами развития некардиогенного отека легких могут быть: ингаляция токсических субстанций, тяжелая травма грудной клетки, острые вирусные заболевания легких (пневмонии), сепсис, аспирационный синдром, радиационное повреждение легких, переливание крови, панкреонекроз, политравма, кровопотеря.
Симптомы отека легких
Относится к той группе состояний, диагностировать которую можно практически уже на расстоянии, поскольку симптомы отека легких у взрослых относятся к весьма характерным: выраженная одышка, преимущественно инспираторная, значительно реже — смешанная; ортопноэ (одышка в положении лежа); кашель с выделением мокроты; число дыханий превышает 30/мин.; холодный обильный пот; цианоз кожных покровов/слизистых; наличие в легких хрипов; тахикардия (ритм галопа), аускультативно — акцент 2 тона над легочной артерией.
Признаки отека легких у человека определяются патогенетическими процессами. Условно клинически выделяют несколько стадий:
- Диспноэтическая. Проявляется сухими хрипами, диспноэ, что связано с началом отека преимущественно интерстициальной легочной ткани, единичные влажные хрипы.
- Стадия ортопноэ. Характерно нарастание влажных хрипов, которых превалируют над сухими хрипами.
- Стадия развернутой клиники. Выраженное ортопноэ, хрипы отчетливо слышны на расстоянии.
- Тяжелая стадия. Множество разнокалиберных хрипов, выделение пены, обильный холодный пот, прогрессирующий диффузный цианоз.
В практике чрезвычайно важно различать интерстициальную и альвеолярную стадию развития отека. Интерстициальному отеку легких соответствует клиническая симптоматика сердечной астмы, что обусловлено резким ухудшением обмена кислородом и углекислотой между кровью и воздухом альвеол, способствующее повышению сосудистого и бронхиального сопротивления.
Приступ сердечной астмы, как правило, развивается в ночной период времени. Больной просыпается от сильного ощущения недостатка воздуха, вынужденно принимает положение сидя, пытается открыть окно, появляется страх смерти, возбуждение, на вопросы не отвечает, сосредоточившись на борьбе за воздух.
Продолжительность приступа сердечной астмы варьирует от 5-10 минут до 1-3 часов. При аускультации— сухие хрипы, в нижних отделах легких ослабленное дыхание. В случаях хронической сердечной недостаточности, митрального стеноза, сопровождаемых гиперволемией малого круга кровообращения для диагностики интерстициального отека большее значение имеет рентгенологическое обследование. На рентгенограмме отмечаются характерные признаки — усиление легочного рисунка, который особенно выражен в прикорневых зонах, что обусловлено наличием лимфатических пространств и отечной инфильтрации перибронхиальной/периваскулярной и межуточной ткани; наличие линии Керли и субплеррального отека.
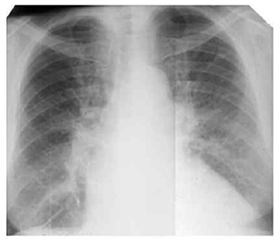
Рентген-снимок. Интерстициальной отек
Далее жидкость из интерстиция поступает в альвеолы, что вызывает альвеолярный отек легких со спаданием альвеол, разрушением сурфактанта, затоплением альвеол транссудатом. На этой стадии может происходить образование стойкой белковой пены, которая перекрывает просвет бронхов/бронхиол, что приводит к гипоксемии и гипоксии.
Острый альвеолярный отек легких относится к более тяжелой форме проявления левожелудочковой недостаточности. Переход интерстициального отека к альвеолярному зачастую происходит достаточно быстро – на протяжении нескольких минут. Бурно протекающий альвеолярный отек чаще развивается в дебюте инфаркта миокарда или на высоте гипертонического криза.
Характерным является громко клокочущее дыхание с выделением белой или из-за примеси эритроцитов розовой пены. На этом фоне резко нарушается оксигенация крови и присутствует высокий риск асфиксии. Как правило, развернутая клиническая симптоматика альвеолярного отека является ярко выраженной и не вызывает затруднений с постановкой диагноза. Дополнительным характерным признаком является появление значительного количества влажных разнокалиберных хрипов, иногда присутствуют и сухие хрипы. Альвеолярный отек, как и сердечная астма, наблюдается преимущественно в ночное время. Приступ может быть как кратковременным, который проходит самостоятельно, так и длительным, продолжающимся несколько часов. В случаях сильного пенообразования может быстро наступить смерть от асфиксии, буквально на протяжении 5-10 минут после появления первых клинических проявлений.
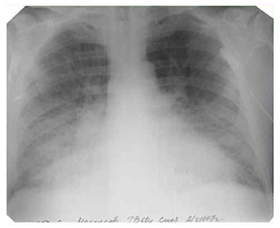
Рентген-снимок. Альвеолярный отек легких.
При альвеолярном отеке легких типичная рентгенологическая картина обусловливается пропитыванием транссудатом симметрично в обоих легких с локализацией отека преимущественно в базальных и прикорневых отделах.
Лабораторные данные клинического значения не имеют и сводятся преимущественно к резким изменениям в газовом составе (гипоксемия) и кислотно-щелочном состоянии крови (метаболический ацидоз). На ЭКГ — тахикардия, повышение/деформация амплитуды зубца Р, снижения сегмента ST.
При застойной сердечной недостаточности, обусловленной снижением сократительной возможности левого желудочка отек чаще развивается при нарушениях сердечного ритма/повышении АД, приводящих к снижению минутного объема крови.
Анализы и диагностика
Диагностическими критериями являются жалобы на резкое ощущение нехватки воздуха, сухой/влажный кашель, позже выделение пенистой мокроты; наличие в анамнезе различных заболеваний сердца (ХСН, ИБС, кардиомиопатии, АГ) или некардинальных причин.
Физикальное обследование: к основным признакам острой левожелудочковой недостаточности относятся пароксизмальная ночная одышка, ортопноэ, двусторонние легочные хрипы, влажные холодные конечности, головокружение, спутанность сознания, олигурия, низкое пульсовое давление.
Вероятные признаки наличия ОСН: тахикардия (ЧСС> 120 уд./мин.)/брадикардия (ЧСС 25/мин. с вовлечением в дыхательный процесс вспомогательных мышц.
Лабораторные критерии постановки диагноза кардиогенного отека легких:
- Низкая сатурация кислорода (при пульсоксиметрии SaO2 45 мм.рт.ст. в артериальной крови).
- Дыхательная недостаточность гиперкапнического типа.
- Метаболический ацидоз.
- Рентгенография легких – признаки легочного застоя.
- ЭКГ – наличие нарушений проводимости, пароксизмальных нарушений ритма и ОКС, признаки структурного поражения сердца.
- Пульсоксиметрия — сатурации кислорода 25 в мин) проводится неинвазивная вентиляция легких специальными аппаратами в режиме CPAP/BiPAP.
Медикаментозное лечение проводится в зависимости от показателей артериального давления. Именно уровень АД у больных с ОСН имеет наибольшее значение в выборе лечебных препаратов при неотложных мероприятиях.
Читайте также:


