Хеликобактер пилори во рту и влагалище

Helicobacter pylori представляет собой болезнетворную бактерию, которая обитает в основном в пилорическом (антральном) отделе желудка.
На фото ниже видно, что микроорганизм имеет форму спирали, к которой прикреплены жгутики. Такое строение помогает ей крепко держаться за стенки пищеварительного органа, передвигаться по нему вместе со слизью и существовать в кислой среде, которую многие патогенные микроорганизмы не переносят и гибнут.
Попадая в организм человека, хеликобактер пилори вызывает опасное заболевание – хеликобактериоз. Бактерии стремительно размножаются, и в процессе своей жизнедеятельности производят много токсинов, разъедающих слизистую оболочку желудка (двенадцатиперстной кишки), а затем и сами стенки пищеварительного органа. Подобное воздействие опасно тем, что создаёт благоприятную среду для гастрита, язвы, а также злокачественных новообразований.
Что это такое?
Хеликобактер пилори — это всего лишь бактерия, которую обнаруживаются у пациентов с различными заболеваниями желудка и кишечника, двенадцатиперстной кишки в частности.
В попытке подтвердить правоту своей догадки, Барри Маршалл провел эксперимент на себе, выпив содержимое чашки Петри, в которой культивировался хеликобактер пилори. Спустя буквально несколько дней у ученого обнаружился гастрит. Вылечить его удалось, принимая на протяжении двух недель метронидазол. И уже в 2005 году авторы этого открытия ученые за свое открытие получили в области медицины Нобелевскую премию. Весь мир признал, что язвы и гастриты, со всеми вытекающими и сопутствующими заболеваниями, появляются именно из-за хеликобактерии.
Как можно заразиться?
Инфицирование происходит при передаче бактерий от одного человека к другому фекально-оральным или орально-оральным путем. Кроме этого, существуют гипотезы о передаче это бактерии от кошек к человеку, а также об их механическом переносе мухами.
Чаще всего заражение происходит в детском возрасте. Самым вероятным путем заражения считается передача хеликобактер пилори от человека к человеку, которая может происходить тремя способами:
- Ятрогенный (обусловленный медицинскими процедурами) путь. При этом пути заражение обусловлено использованием эндоскопического или другого медицинского инструмента, который контактировал со слизистой оболочкой желудка инфицированного пациента, у другого человека.
- Фекально-оральный путь. H. pylori выделяются со стулом зараженных людей. Источником инфицирования могут быть загрязненные каловыми массами вода или продукты питания.
- Орально-оральный путь. Существуют данные, что хеликобактер пилори может находиться в ротовой полости. Поэтому возможна передача бактерий при совместном использовании столовых приборов и зубных щеток, поцелуях.
Что происходит в организме?
На начальном этапе после попадания в желудок H. pylori, быстро двигаясь при помощи жгутиков, преодолевает защитный слой слизи и колонизирует слизистую оболочку желудка. Закрепившись на поверхности слизистой, бактерия начинает вырабатывать уреазу, благодаря чему в слизистой оболочке и слое защитной слизи поблизости от растущей колонии растёт концентрация аммиака и повышается pH. По механизму отрицательной обратной связи это вызывает повышение секреции гастрина клетками слизистой желудка и компенсаторное повышение секреции соляной кислоты и пепсина, с одновременным снижением секреции бикарбонатов.
Муциназа, протеаза и липаза, вырабатываемые бактерией, вызывают деполимеризацию и растворение защитной слизи желудка, в результате чего соляная кислота и пепсин получают непосредственный доступ к оголённой слизистой желудка и начинают её разъедать, вызывая химический ожог, воспаление и изъязвление слизистой оболочки.

Заблуждения, связанные с Helicobacter pylori
Нередко, при обнаружении Helicobacter pylori, пациенты начинают беспокоиться об их эрадикации (уничтожении). Само наличие Helicobacter pylori в желудочно-кишечном тракте не является причиной для немедленной терапии с применением антибиотиков или других средств. В России количество носителей Helicobacter pylori достигает 70 % населения и подавляющее большинство из них не страдает какими-либо заболеваниями желудочно-кишечного тракта. Процедура эрадикации предполагает прием двух антибиотиков (например, кларитромицина и амоксициллина).
Helicobacter pylori однозначно требует эрадикации, если у больного имеется язва желудка или двенадцатиперстной кишки, МАLТома или если у него была резекция желудка по поводу рака. Многие авторитетные гастроэнтерологи (не все) в этот список включают также атрофический гастрит. Эрадикация Helicobacter pylori может быть рекомендована для снижения риска развития рака желудка. Известно, что как минимум 90% случаев рака желука связаны с H. pylori-инфекцией (Старостин Б.Д.).
Симптомы и первые признаки
Развитие инфекции в пищеварительном тракте длительное время протекает практически бессимптомно. Бактерии прикрепляются к слизистой кишечника и 12-перстной кишки, вырабатывают токсичный фермент, который постепенно разъедает клетки эпителиальных тканей.
Только когда на стенках органа появляются эрозии и язвочки, пациента начинают тревожить неприятные симптомы Helicobacter pylori:
- чувство вздутия и переполненности желудка после приёма пищи;
- частая отрыжка с привкусом кислоты во рту;
- регулярно болит желудок;
- наблюдается жжение в пищеводе, горьковатый вкус во рту;
- регулярные приступы тошноты, рвотные позывы;
- повышенное газообразование, которое провоцирует колики и дискомфорт.
У взрослых неприятные признаки бактерии хеликобактер пилори появляются чаще всего после еды и не проходят даже после опорожнения кишечника. Пациента одолевает вялость, упадок сил, сонливость, раздражённость. Наличие helicobacter pylori в желудке или двенадцатиперстной кишке может сопровождаться мелкой кожной сыпью, в частности, на лице. При гастрите или язве, вызванными хеликобактериозом, пациент жалуется на изменения в стуле (запор или понос), неприятный запах изо рта, ломкость ногтевой пластины и постоянное общее недомогание.
Какие заболевания может спровоцировать H. pylori
Наличие H. pylori в желудке само по себе не является заболеванием. Однако эти бактерии повышают риск развития различных болезней пищеварительного тракта.
Хотя колонизация слизистой желудка хеликобактери вызывает гистологический гастрит у всех зараженных людей, лишь у небольшой части из них развивается клиническая картина этого заболевания. По оценкам ученых, у 10-20% людей, зараженных хеликобактер пилори, развивается язва, а у 1-2% — рак желудка.
Заболевания, развитие которых связано с хеликобактерной инфекцией:
- Гастрит – это воспаление слизистой оболочки желудка. Вскоре после инфицирования H. pylori у человека развивается острый гастрит, связанный иногда с диспепсией или тошнотой. Острый воспалительный процесс поражает весь желудок и приводит к снижению секреции кислоты. Через определенный период времени после острого гастрита развивается хронический.
- Язва желудка и двенадцатиперстной кишки. Согласно научным данным, 70-85% всех язв желудка и 90-95% всех язв двенадцатиперстной кишки вызваны бактерией
- Функциональная диспепсия – это боль в верхней части живота, не вызванная язвой или другими поражениями желудка. Результаты научных исследований показали, что некоторые виды диспепсии связаны с инфекцией. Лечение, направленное на эрадикацию бактерий, облегчает состояние у многих пациентов с функциональной диспепсией, а также снижает риск развития язв и рака желудка в будущем.
- Рак желудка. Хеликобактер пилори – признанный учеными этиологический фактор развития рака желудка. По одной из гипотез, бактерии способствуют выработке свободных радикалов и увеличивают риск возникновения мутаций в клетках желудка.
- MALT-лимфома желудка. О связи инфекции с этим заболеванием впервые сообщили в 1991 году. Считается, что эта бактерия вызывает 92-98% MALT-лимфом желудка.
Диагностика
Для обнаружения инфекции в организме используются различные методы обследования, каждый из которых имеет свои преимущества, недостатки и ограничения. Традиционно все методы разделяют на неинвазивные и инвазивные.
Инвазивные методы обнаружения:
- Гистологическое исследование – изучение специально окрашенных образцов тканей желудка, полученных с помощью биопсии во время эндоскопического обследования, под микроскопом.
- Микробиологический посев и выделение культуры хеликобактери. Для получения материала для посева используют биопсию или образец желудочного сока, которые получают во время эндоскопического обследования.
- Полимеразная цепная реакция (ПЦР) – позволяет обнаружить инфекцию в небольших образцах тканей, полученных с помощью биопсии.
- Быстрый уреазный тест – во время этого метода используется способность бактерии к переработке мочевины. Образец тканей, полученный с помощью биопсии, помещают в среду, содержащую мочевину и индикатор рН. Бактерии расщепляют мочевину на двуокись углерода и аммиак, из-за чего повышается рН среды и изменяется цвет индикатора.
Неинвазивные методы обнаружения:
- Серологические анализы крови, с помощью которых можно обнаружить антитела к хеликобактери.
- Дыхательный тест с мочевиной. Во время этого обследования пациенту дают выпить раствор с мочевиной, молекула которой содержит меченый изотоп углерода. Хеликобактери расщепляет мочевину на аммиак и углекислый газ, который содержит меченый атом углерода. Этот газ проникает в кровоток и выводится через легкие с воздухом. Через полчаса после употребления раствора с мочевиной пациент выдыхает в специальный мешочек, в котором с помощью спектрометрии обнаруживают меченый атом углерода.
- Выявление антигенов H. pylori в кале.

Как избавиться от Helicobacter pylori?
В 2019 году приемлемой схемой эрадикации Helicobacter pylori у взрослых считается лечебный режим, обеспечивающий не менее чем 80 % эффективно подтверждённого повторным обследованием излечения от хеликобактерной инфекции и заживления язвы или гастрита, имеющий продолжительность не более 14 суток и обладающий приемлемо низкой токсичностью (побочные эффекты должны развиваться не более чем у 10—15 % больных и в большинстве случаев не быть столь серьёзными, чтобы требовать досрочного прекращения лечения).
Постоянно разрабатываются новые схемы и протоколы эрадикации хеликобактера. При этом преследуется несколько целей:
В 2019 году экспертами Маастрихтом-IV были рекомендованы следующие эрадикационные схемы Helicobacter pylori:
Трёхкомпонентная терапия, была предложена на первой Маастрихтской конференции и стала универсальной схемой лечения инфекции H. pylori. Она рекомендована всеми мировыми согласительными конференциями.
Схема включает препараты:
При этом показано, что схемы ИПН + кларитромицин + метронидазол (тинидазол) и ИПН + кларитромицин + амоксициллин эквивалентны. Установлено, что эффективность тройной терапии повышается, при увеличении её продолжительности до 10 или 14 дней (в зависимости от степени обсеменённости Helicobacter pylori и переносимости терапии пациентом).

В связи с различной резистентностью к антибиотикам в разных регионах мира, распространённостью различных штаммов Нр, генетическими особенностями населения, в разных странах или группах стран вырабатываются свои рекомендации в отношении эрадикации Нр. Некоторые из этих параметров, в частности, резистентность Нр к определенным антибиотикам, меняется с течением времени. Выбор конкретной схемы определяется также индивидуальной непереносимостью больного к препаратам, а также чувствительностью штаммов Нр, которыми инфицирован больной.
На съезде Научного общества гастроэнтерологов России были приняты следующие схемы эрадикации Нр, они актуальны на 2019 год:
1) Первые вариант . Трёхкомпонентная терапия, включающая перечисленные ниже препараты, которые принимаются в течение 10-14 дней:
2) Второй вариант . Четырёхкомпонентная терапия, включающая в дополнении к препаратам варианта 1 препарат висмута, её продолжительность также 10—14 дней:
3) Третий вариант . Если у больного имеется подтверждённая внутрижелудочной рН-метрией атрофия слизистой оболочки желудка с ахлоргидрией и ему, таким образом, нецелесообразно назначать кислотоподавляющие препараты (ИПН или Н2-блокаторы), применяется третий вариант (продолжительностью 10—14 дней):
- амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день) +
- кларитромицин (500 мг 2 раза в день), или джозамицин (1000 мг 2 раза в день), или нифурател (400 мг 2 раза в день) +
- висмута трикалия дицитрат (120 мг 4 раза в день или 240 мг 2 раза в день).
4) Четвертый вариант . Если пожилым больным невозможна полноценная эрадикационная терапия, применяют усечённые схемы:
Другой способ: висмута трикалия дицитрат по 120 мг 4 раза в день в течение 28 дней. При наличии болей в области желудка — короткий курс ИПН.
Возможные осложнения от лечения антибиотиками
Факторы, повышающие риск появления побочных эффектов при проведении эрадикционной терапии:
- Индивидуальная непереносимость препаратов;
- Наличие соматических патологий;
- Негативное состояние микрофлоры кишечника в начальный период лечения.
Осложнения эрадикционной терапии – побочные действия:
- Аллергическая реакция на компоненты препаратов, исчезающая после отмены;
- Диспепсические явления ЖКТ (дискомфорт в желудке и кишечнике, привкус горечи и металла, тошнота и рвота, диарея, метеоризм). Обычно все эти явления самопроизвольно проходят спустя короткое время. В редких случаях (5-8 %) врач назначает средства против рвоты или диареи, или отменяет курс.
- Дисбактериоз. Чаще проявляется у пациентов, ранее имевших нарушения функции ЖКТ, развивается при лечении препаратами тетрациклинового ряда или при терапии макролидами. Кратковременный курс не способен нарушить баланс микрофлоры кишечника, для профилактики дисбактериоза нужно чаще употреблять кисломолочную продукцию: йогурт, кефир.

Питание и диета
Безусловно, основным пунктом при лечении данной патологии выступает прием медицинских препаратов, но не менее важную роль играет правильное питание. Чтобы легко избавиться от хеликобактериоза, следует соблюдать следующие рекомендации:
- не делать больших интервалов между приемами пищи;
- употреблять пищу небольшими порциями;
- соблюдать 5-6 разовый режим питания, есть при этом нужно медленно, хорошо пережевывая еду и запивая ее достаточным количеством жидкости;
- пациенту следует отказаться от чересчур жирной, жареной или острой пищи, газированных напитков, маринованных блюд, алкоголя.
В действительности это только общие рекомендации, в каждом отдельном случае питание должно рассчитываться исходя из уровня кислотности (пониженная, повышенная) и назначаться только специалистом, проводящим лечение.
Профилактика
Полностью вылечиться от хеликобактериоза можно, если помимо терапии придерживаться профилактических мер:
- Соблюдение гигиены. Мыть руки перед приёмом пищи, не употреблять грязные овощи и фрукты, сомнительную воду. Не использовать чужие предметы обихода.
- Своевременное обнаружение болезни. При плохом самочувствии или подозрении на присутствие в организме патогенной бактерии важно немедленно обратится к врачу, пройти нужные тесты.
- Укрепление иммунитета. Здоровый образ жизни (плаванье, бег, пешие прогулки) повышает защитные силы и препятствует проникновению болезнетворных микробов в организм.
- Правильное питание. Дробный приём пищи, малые дозы и отказ от жареного, солёного, острого, копчёного, алкоголя и курения.
Основная опасность helicobacter pylori в том, что она может спровоцировать гастрит, язву даже новообразования злокачественного характера. От вредоносных бактерий невозможно избавиться без антибиотиков. Поэтому важно строго придерживаться специальных схем лечения и соблюдать профилактические меры.
Какой врач лечит хелиобактериоз?
При появлении болей и других негативных симптомов в желудке, а так же при диагностировании бактерии нужно обращаться к врачу-гастроэнтерологу. Если сходные проблемы появились у детей, следует проконсультироваться с детским гастроэнтерологом.
При отсутствии этих специалистов нужно обратиться к терапевту, при лечении детей — к педиатру.
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Сейчас мы передаем слово профессору Юрию Павловичу Успенскому. Юрий Павлович расскажет о хеликобактер пилори и о грибах рода Candida, что их объединяет у гастроэнтерологического больного.
Юрий Павлович Успенский, профессор, доктор медицинских наук:
– Дорогие коллеги, мы с вами прекрасно знаем, что благодаря эпохальному открытию колоссальной роли пилорического хеликобактера в развитии хронического гастрита, язвенной болезни, рака желудка, уже к концу 90-х годов стало очевидным, что количество вновь выявленных случаев язвенной болезни уменьшается, что даже дало возможность гастроэнтерологам заявить о том, что XX век – это век уходящей язвенной болезни, а XXI – это век рождающейся гастроэзофагеальной рефлюксной болезни.
Однако, к сожалению, тенденции последнего времени оказались не столь оптимистичны и основные проблемы связаны все-таки с уменьшающейся эффективностью эрадикационной терапии. Причины этого лежат в плоскости возрастающей резистентности хеликобактер пилори к антибактериальным препаратам, которые входят в состав схем традиционной эрадикационной терапии.
Так один из патриархов, профессор Мегро (F.Megraud), отметил, что резистентность к кларитромицину, согласно молекулярно-генетическим методам, в Европе достигает 46%. Что же происходит при этом? При этом происходит драматическое снижение эффективности эрадикационной терапии, которая не превышает 18%. Что касается Российской Федерации, то диапазон вариаций резистентности к кларитромицину весьма широк. Почему-то в нашем северо-западном регионе наиболее высока резистентность к кларитромицину в Санкт-Петербурге. Причем это были абсолютно независимые исследования: педиатрический анклав профессора Корниенко Е.А., наши исследования доктора Барышниковой Н.В., исследования института Пастера. Причем были разные методы, и все они дали крайне высокие (более 30%) цифры резистентности к кларитромицину.
Коллеги, говоря о новых антибактериальных препаратах как варианте преодоления резистентности к антибиотикам, повышения эффективности эрадикационной терапии, хотелось бы сказать, что все-таки этот путь достаточно опасный, а может быть, даже и тупиковый, потому что тем самым мы способствуем воспитанию полирезистентных штаммов к антибиотикам хеликобактер пилори.
И на самом деле неконтролируемое потребление антибиотиков, это глобальная проблема человечества. Не столь давно, 18 ноября 2012 года, состоялся Европейский день осведомленности о проблеме резистентности и потребления антибиотиков, когда была предложена мировая стратегия борьбы с распространением резистентных форм микроорганизмов.
Непосредственное влияние препаратов висмута на хеликобактер пилори было продемонстрировано в виде целого ряда грамотно организованных исследований, и связаны были эти действия с блокированием адгезии хеликобактера с прямым ингибированием энзимов и уреазы этого микроорганизма.
Кроме того, в последние годы утвердилась концепция активно разрабатываемой школы профессора Кононова в Омске о том, что даже в случае успешно проведенной эрадикационной терапии формируется воспалительный инфильтрат (из-за продукции цитокинов, из-за продукции активных форм кислорода), и он сохраняется достаточно долго – от 1 до 12 месяцев. Поэтому и в этой связи включение препаратов висмута в комплекс эрадикационной терапии является оправданным с клинической точки зрения, потому что при этом происходит подавление ассоциированного воспаления из-за уменьшения продукции цитокинов, увеличения продукции цитопротективных простагландинов, и, соответственно, увеличение эпидермального фактора роста.
Какая же висмутсодержащая схема эрадикации является предпочтительной? Право на существование имеет и та схема, о которой мы сейчас говорили, когда висмут добавляется к стандартной терапии, и 10-дневная схема, о которой говорила Татьяна Львовна (висмут, метронидазол, тетрациклин и ингибитор протонного насоса). Все они обеспечивают достаточно высокий и эффективный уровень эрадикации.
А какая же связь между пилорическим хеликобактером и грибами рода Candida? Согласно нашим исследованиям, оказалось, что у одних и тех же больных экспрессируются гены, которые кодируют как факторы патогенности хеликобактер пилори, так и факторы адгезии и инвазии грибов рода Candida. А грибы рода Candida albicans действительно обладают факторами вирулентности, факторами адгезии, инвазии. Связь между концентрацией грибов рода Candida в толстой кишке и степенью обсемененности хеликобактер пилори антрального отдела желудка достаточно четко выражена и была продемонстрирована еще 10 лет назад в работах М.М. Захарченко.
Что происходит под влиянием антибактериальной терапии с грибами рода Candida? Их популяция неуклонно растет как следствие прямого стимулирующего действия (есть данные, что больные с кандидемией, то есть с кандидосепсисом, получали 4 и более антибиотиков), а также вследствие ингибирующего влияния на бактерии-антагонисты грибов рода Candida.
Что же такое грибы рода Candida? Посмотрите, вот эти данные показывают, что, оказывается, это транзиторные микроорганизмы, они обнаруживаются и в мороженом, и в других кисломолочных и молочных продуктах. То есть, на первый взгляд, нет ничего страшного в их присутствии, они транзитом проходят через организм человека. Но так происходит лишь тогда, когда иммунологическая реактивность макроорганизма достаточно высока. А если она низка, если это человек, страдающий иммунодефицитом, получающий гормональную терапию, если это ослабленный больной, тогда реален риск инвазии грибов рода Candida в слизистой оболочке, развития кандидоза пищевода, толстой кишки, транслокации микроба через кишечную стенку вплоть до развития кандидемии и кандидосепсиса.
В ряде случаев при пониженной иммунной резистентности макроорганизма инвазивный кандидоз не развивается, но возможно развитие неинвазивного кандидоза, когда увеличивается концентрация грибов рода Candida в просвете кишечника. Но и при этом ситуация далека от благополучной, потому что в этих условиях имеет место сенсибилизация, интоксикация организма, формирование вторичного иммунодефицита и присоединение микст-инфекции. Потому что грибы рода Candida обладают целым рядом ферментных, полисахаридных и иных факторов агрессии и патогенности.
Критерием диагностики неинвазивного кандидоза кишечника и повышенной пролиферации грибов рода Candida является снижение числа нормобиоты ниже 100 миллионов колониеобразующих единиц на грамм фекалий и рост грибов рода Candida ssp. при посеве кала выше 1000 колониеобразующих единиц на грамм фекалий.
Наличие тесной патогенетической взаимосвязи между грибами и хеликобактером подтверждает то, что в 98% образцов грибов рода Candida, выделенных из слизистой, детектируется хеликобактер пилори. И в большинстве образцов содержится ген острова патогенности cag A.
В другой работе показано, что также из грибов, выделенных из ротовой полости, идентифицируется присутствие генов хеликобактер пилори и почти в 100% случаев наблюдается гомологичность между генами грибов и генами контрольной популяции хеликобактера.
Согласно отечественной работе у детей с HP-ассоциированным гастродуоденитом с возрастом увеличивается число высокопатогенных штаммов микроорганизма хеликобактер пилори. Но при этом имеется сопряженность роста таких штаммов с увеличением гена sap2. Это ген, который кодирует синтез фактора вирулентности грибов рода Candida с 41,2% до 100% у детей, достигших 17-18 лет.
Таким образом, в последние годы сформировалась концепция, что дрожжеподобные микромицеты являются естественным биологическим резервуаром для грибов рода Candida. То есть что же при этом происходит? Татьяна Львовна уже говорила сегодня о стратегиях выживания пилорического хеликобактера. Но они не ограничиваются одной лишь уреазной активностью. Дело в том, что хеликобактер – это вообще весьма уязвимый организм, крайне чувствительный и к температурным условиям, и к пищевым, и желчным детергентам. Поэтому для своего выживания он способен пенетрировать капсулу и клеточную стенку гриба рода Candida, адгезировать плазменную мембрану гриба с образованием вакуоли и располагаться внутри этого организма, приобретая устойчивость к изменяющимся условиям среды, в том числе температурным, пищевым и желчным детергентам.
Вот и очень интересная работа, которая была выполнена 10 лет назад. Она показывает, что взаимоотношения между грибами и хеликобактером являются, по сути, эквипотенциальными. Их такая комбинация увеличивает и вирулентность грибов рода Candida. А проведенная эрадикационная терапия, даже в случае своей успешности, достоверно уменьшает частоту выявления хеликобактера в желудке, но увеличивает частоту выявления грибов рода Candida.
Что же делать в этой ситуации? По всей видимости, необходим поиск инновационных подходов к диагностике коррекции кандидозы такого рода пациентов. И сложность заключается в том, что среди традиционно принятого в гастроэнтерологии методов лечения, методы, направленные на предотвращение экспансии Candida spp., по сути, отсутствуют. Равно как и отсутствует антикандидозная активность у всех антибактериальных средств, входящих в состав классической эрадикационной терапии. А между тем такие пути необходимо искать, потому что грибы, как мы уже с вами говорили, способны помимо кишечника заселять другие анатомические и экологические ниши организма и в полной мере проявлять свои патогенные свойства.
К путям минимизации риска развития и прогрессирования кандидоза органов пищеварения при использовании эрадикационной терапии можно отнести исключение из эрадикационного комплекса антибиотика с потенциально высокой резистентностью к ним и включение в терапию первой линии препаратов висмута. Кроме того, у ряда пациентов требуется дополнительное назначение нерезорбцируемых антимикотических препаратов.
Пока же позвольте сделать заключение о том, что кандидоз органов пищеварения – это междисциплинарная проблема и для ее решения нужна интеграция усилий гастроэнтерологической и микологической службы. Высокое представительство грибов рода Candida в составе желудочно-кишечной микрофлоры связано с плотностью бактериального обсеменения и вирулентностью микроорганизма в хеликобактер пилори. Перспективным же путем повышения эффективности и безопасности эрадикационной терапии, а также элиминации грибов рода Candida и профилактики прогрессирования кандидоза органов пищеварения является дополнительное включение в схемы эрадикационной терапии тем контингентам пациентов, о которых мы с вами выше говорили, препаратов висмута и нерезорбцируемых антимикотиков.
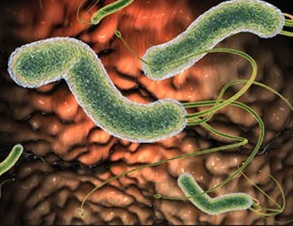
Хеликобактер пилори – микроаэрофильная, грамотрицательная бактерия, что паразитирует в человеческом организме и провоцирует заболевания пищеварительного тракта.
Эта бактерия на сегодняшний день является самой изучаемой в мире, так как она единственная среди микроорганизмов способна выжить в агрессивной среде желудка.
Доказано, что 2/3 населения Земли инфицировано данным микробом.
Как можно заразиться Helicobacter pylori?
Точный механизм заражения не известен. Предполагается, что хеликобактер пилори передается фекально-оральным и орально-оральным (через поцелуи) путем. Инфицироваться можно при:
- использовании общей посуды;
- тесном физическом контакте;
- плохой обработке медицинской техники (эндоскоп);
- чихании и кашле;
- несоблюдении гигиенических правил.
Исходя из всего, хеликобатериоз можно считать семейной инфекцией. Если заразился один член семьи, то есть большая вероятность инфицирования всех домочадцев.
Симптомы хеликобактер пилори
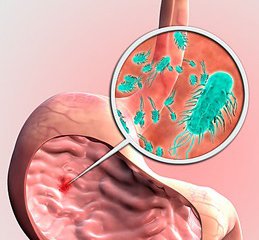
После того как хеликобактер пилори попадает в желудок она начинает выделять продукты своей жизнедеятельности и повреждать эпителий желудка, тем самым вызывая неприятные симптомы.
Можно обозначить несколько форм хеликобактериоза:
1) Латентная форма. У многих людей микроорганизм не вызывает болезненных симптомов при достаточно крепком иммунитете. Бактерия может приобретать неактивную форму и активизироваться при благоприятных условиях. Также существуют менее или более вредоносные штаммы, которые способны в разной степени поражать слизистую.
Даже при бессимптомном носительстве наблюдается функциональное нарушение не только желудка, но и поджелудочной железы. А при длительном (больше десяти лет) нахождении микроорганизма в желудке человека могут развиваться тяжелые последствия, возможно перерождение в рак.
2) Острый гастрит проявляется болями в эпигастральной области, рвотой. Обычно переходит в хроническую форму.
3) Хронический гастрит. Встречается у большей части населения земного шара и есть основным проявлением хеликобактериоза.
Часто беспокоят:
- периодические боли в области желудка;
- тошнота;
- ощущение переполненного желудка;
- изжога;
- повышенная кровоточивость десен;
- плохой привкус во рту;
- отрыжка.
5) Язвенная болезнь развивается под влиянием различных факторов (курение, алкоголь, стрессы), но далеко не у всех. Язвы и эрозии появляются, когда поражаются более глубокие слои желудочных стенок. Клиника симптомов многообразна. Боль в верхней части живота обычно связана с приемом пищи. Также присутствует тяжесть в подложечной области, изжога, тошнота, рвота, отрыжка.
Хеликобактер пилори симптомы на лице - фото
У 85% людей страдающих заболеванием розацеа, симптомы которого проявляются в виде прыщей на лице, была обнаружена бактерия Хеликобактер пилори. Кроме этого, она способна провоцировать возникновение неприятного запаха изо рта.
Методы диагностики и анализ на хеликобактер пилори
Есть несколько методов обследования на наличие хеликобактерной инфекции.
Один из самых распространенных и надежных – фиброгастроскопия с взятием биопсии. Ткань слизистой оболочки исследуют на наличие уреазы и антигенов хеликобактер пилори. Результативность зависит от места взятия биопата.
Для диагностики используются также и другие обследования:
- анализ кала на H. pylori антиген. Частицы бактерий обнаруживаются в кале и на основании этого можно судить о наличии их в желудке;
- обнаружение бактерии в слюне и транссудате десен;
- выделение культуры хеликобактер пилори (бактериологический метод);
- респираторный тест на хеликобактериоз помогает выявить продукты жизнедеятельности микроорганизма в выдыхаемом воздухе;
- полимеразная цепная реакция (молекулярно-генетический метод);
- анализ крови на антитела lgG. Данное обследование не всегда информативно, так как антитела сохраняются еще длительное время после перенесенной инфекции.
Диагностику следует проводить до и после проведения терапии для контроля. Контроль успешности должен осуществляться через 4-6 недель после применения медикаментов с использованием как минимум двух диагностических методов.
Как лечить хеликобактер пилори?
Если обследование показало наличие бактерии нужно обязательно обратиться к гастроэнтерологу, ибо только квалифицированный специалист может подобрать схему лечения хеликобактер пилори.
Современная терапия заболеваний связанных с данной бактерией строится с учетом тяжести течения, фазы процесса и этиологических факторов. Инфекция устраняется только при комплексном, эрадикационном лечении антибиотиками.

Как лечить хеликобактер пилори? Эрадикация подразумевает полное уничтожение бактерий хеликобактер пилори в любой их форме и способствует стойкой ремиссии. Наиболее удачной считается комбинация амоксициллина, кларитромицина и рабепразола. Это схема первой линии, включающая три компонента.
В случае неудовлетворительных результатов предлагается использовать четырехкомпонентную схему второй линии, состоящую из рабепразола, висмута субсалицилата, метранидазола и тетрациклина. Продолжительность лечения не более 14 суток.
Параллельно с эрадикационной терапией следует принимать пробиотики (Линекс, Бифиформ), которые уменьшают побочные реакции и повышают эффективность лечения.
Результативность терапии зависит от формы болезни, от правильности лечения и от чувствительности бактерии к антибиотикам. Антибактериальное лечение при остром гастрите или язве обычно приводит к полному выздоровлению без последствий для здоровья.
Хронический гастрит, сопровождаемый атрофическими изменениями, лечится сложнее, но, хотя атрофированные участки не восстанавливаются, риск перерождения их в раковую опухоль снижается.
Лечение хеликобактер пилори народными средствами
Эффективность многих народных методов лечения хеликобактер пилори не проверена официальной медициной. Средства для лечения подбираются в зависимости от течения болезни. Из рациона исключается тяжелая, острая, жирная еда и спиртные напитки.
Перед основными приемами пищи рекомендуется принимать настой, имеющий в своем составе цветки груши, земляники и яблони, а также листья брусники. На 1 литр кипяченой воды нужно взять 4 ст.л. сырья (по столовой ложке от каждого растения), 30 минут настоять, процедить и принимать по полстакана. Составы чаев могут меняться.
Рекомендуется также зверобой, тысячелистник и календула или зверобой, корень девясила и золототысячник.
В качестве противомикробного средства можно использовать спиртовую настойку прополиса. Принимать надо по 20 капель трижды в день в течение 7 дней.
Иммунитет к хеликобактериозу не вырабатывается, и заболевание имеет обыкновение рецидивировать. Профилактика лежит в соблюдении личной гигиены, поддержании здорового образа жизни, своевременном исследовании и лечении всей семьи, при условии выявления инфекции у кого-то из родных.
Есть правила, которых нужно придерживаться:
- средства личной гигиены должны быть индивидуальными;
- нельзя пользоваться общей посудой;
- перед едой нужно мыть руки;
- не целоваться с незнакомыми людьми;
- не злоупотреблять алкоголем;
- не курить как активно, так и пассивно.
Кроме того, при тестировании оральной вакцины у многих людей возникла диарея. Поэтому на данный момент вакцинация – это вопрос будущего, что нуждается в значительных доработках.
К какому врачу обратиться для лечения?
Если после прочтения статьи вы предполагаете, что у вас характерные для этого заболевания симптомы, то вам стоит обратиться за консультацией к гастроэнтерологу.
Читайте также:


