Гост 33675-2015 методы диагностики бруцеллеза
| Статус документа: | Введен впервые |
| Дата начала действия: | 01 янв. 2017 г. |
| Количество страниц: | 20 стр. |
| Когда и где опубликован: | Бюллетень нормативных актов федеральных органов исполнительной власти от 20 апреля 2009 г. N 16 |
| Страна-разработчик: | Российская Федерация |
| Разработан: |
|
| Издан: |
|
| Утвержден: |
|
| Содержание: | 1 Область применения 2 Нормативные ссылки 3 Термины, определения и сокращения 4 Условия выполнения исследований и требования безопасности 5 Средства измерений, оборудование, питательные среды, реактивы, посуда, животные и материалы 6 Отбор проб 7 Бактериоскопический метод 8 Культуральный метод 9 Идентификация выделенных культур 10 Биологический метод 11 Молекулярно-генетический метод исследований Приложение А (справочное) Дифференциальные свойства видов и биоваров рода Brucella |
| Ссылки в документе: |
|
| Разделы классификатора: |
|
Отзывы
Нет отзывов, пока еще.
ГОСТ 33675-2015 Животные. Лабораторная диагностика бруцеллеза. Бактериологические методы
Стандарт распространяется на все виды млекопитающих животных и устанавливает бактериологические методы лабораторной диагностики бруцеллеза.
– Олег Дмитриевич, чем продиктовано принятие нового ГОСТа?
– Если быть точным, то в действие введен ГОСТ 34105-2017 (Межгосударственный стандарт. Животные. Лабораторная диагностика бруцеллеза. Серологические методы). Его появление обусловлено не только внедрением в российскую ветеринарную диагностическую практику новых серологических тестов, в частности, реакции непрямой гемагглютинации, вариантов иммуноферментного и иммунохроматографического анализа, но и целесообразностью совершенствования диагностики – прежде всего повышения ее оперативности и специфичности.
Разрабатывать этот ГОСТ начинали одновременно с подготовкой по распоряжению Минсельхоза России новых Ветеринарных правил осуществления профилактических, диагностических, ограничительных и иных мероприятий, установления ограничений, направленных на предотвращение возникновения, распространения и ликвидацию очагов бруцеллеза животных в России (далее – новые правила). Сейчас проект правил проходит стадию согласования различными ведомствами.
Разумеется, оценка диагностических титров серологических реакций при диагностике бруцеллеза в ГОСТе и новых правилах будет одинаковой. Поэтому считаю, что до выхода в свет этих правил ветеринарные диагностические лаборатории не должны переходить на работу по ГОСТ 34105-2017.
– Потому что между ГОСТом и действующими в настоящее время Ветеринарными правилами по борьбе с бруцеллезом (ВП 13.3.1302-96) сохраняются существенные различия.
– На какие положения стандарта вы хотели бы обратить внимание специалистов в первую очередь?
– К сожалению, несмотря на то, что ГОСТ34105-2017 согласовывался специалистами стран Евразийского экономического союза, в нем сохраняются недочеты.
– Одним из таких недочетов является предписание проводить дополнительное исследование образцов сыворотки в РИД и ИФА с ОПС-антигеном в случае выявления в группах животных, иммунизированных и не иммунизированных против бруцеллеза и положительно реагирующих по результатам серологических исследований в ряде реакций. Такое требование предусмотрено пп. 8.2, 8.3 и 8.4 данного ГОСТа в целях уточнения диагноза.
– Если речь идет об уточнении диагноза, то почему вы называете это недочетом?
– Дело в том, что, по состоянию на сегодняшний день, диагностические тест-системы для иммуноферментного анализа в рамках госзаказа выделяются в ограниченном количестве. Представители большей части ветеринарных диагностических лабораторий утверждают, что им такие тест-системы будут недоступны. Соответственно, непроведение серологического тестирования в ИФА, согласно ГОСТу, будет расценено представителями надзорных учреждений как нарушение.
С учетом разницы в диагностической чувствительности между РИД с ОПС-антигеном и ИФА с ОПС-антигеном исследование последним методом является принципиальным. В противном случае при выполнении серологического исследования только в РИД с ОПС-антигеном объективность его результатов может быть сомнительной.
Не буду вдаваться в подробности других имеющих принципиальное значение недочетов, отмечу лишь, что после их обсуждения и согласования с диагностическими ветеринарными лабораториями должно быть инициировано внесение изменений в ГОСТ 34105-2017.
– Какие ошибки чаще всего допускают при лабораторной диагностике бруцеллеза?
– О существенных ошибках мне неизвестно. К тому же мы не контролируем работу лабораторий. Однако, когда специалисты ряда лабораторий обращаются к нам, чтобы обсудить спорные результаты исследований, кажется, что некоторые из них не знакомы со всеми документами, регламентирующими диагностику болезни. Впрочем, большинство специалистов проявляют инициативу и демонстрируют познания, достаточные для диагностики болезни. Не менее важно и то, что они заинтересованы в получении объективных результатов.
– Какова сегодня эпизоотическая ситуация по бруцеллезу среди крупного и мелкого рогатого скота на территории России?
В период с 2013 по 2017 годы количество неблагополучных по бруцеллезу мелкого рогатого скота пунктов, остававшихся на конец года, составляло 30, 28, 22, 17 и 14. Число заболевших животных – 1,9; 2,5; 2,2; 1,22 и 1,01 тыс. голов.
– Можно утверждать, что динамика положительная?
– Система контроля бруцеллеза животных в стране несовершенна?
– Сложившуюся систему контроля бруцеллеза животных в Российской Федерации можно считать удовлетворительной. Однако это не исключает необходимости ее совершенствования. Прежде всего в части сокращения временных затрат при установлении диагноза за счет более широкого применения средств дифференциальной диагностики болезни, а именно реакции иммунодиффузии и иммуноферментного анализа с ОПС-антигеном, возможно, за счет сочетания средств диагностики.
Важным представляется проведение исследований и установление возможных, максимально ранних сроков серологического исследования вакцинированных животных, особенно мелкого рогатого скота, иммунизированного агглютиногенными вакцинами. В настоящее время этим никто не занимается.
Не стоит забывать, что самый эффективный способ оздоровления неблагополучного хозяйства предусматривает ликвидацию всего поголовья в таком хозяйстве. Однако данный способ не слишком широко применяется в нашей стране. (Должен отметить, что в проекте новых правил его применение регламентировано в большем количестве случаев, нежели в Ветеринарных правилах 13.3.1302-96.) Поэтому перед проведением вакцинации животных в рамках оздоровления путем вакцинации и последующих периодических серологических исследований особенно важно максимально полно удалять инфицированных особей из групп животных.
– В нынешних условиях это реально?
– Я бы сказал, что это возможно за счет введения животным неблагополучных по бруцеллезу хозяйств провоцирующих неагглютиногенных антигенов, в отличие от применяющихся вакцин, с последующим серологическим исследованием и удалением выявленных больных животных.
При этом не могу не отметить, что организации-производители, планировавшие выпускать такие антигены, зарегистрированные ими ранее в Российской Федерации, пока не справляются со своими планами и не понятно, справятся ли.
– Что препятствует повышению эффективности системы контроля бруцеллеза?
– На мой взгляд, совершенствование этой системы не представляется возможным без решения целого ряда задач. Во-первых, нужно создавать в регионах, неблагополучных по бруцеллезу, мясокомбинаты и бойни, обеспечивающие убой больных животных, что решает проблему неполного, несвоевременного и антисанитарного убоя. При этом следует компенсировать владельцам убыток. К сожалению, он неизбежен при изъятии больных животных, прежде всего в условиях ведения отгонного животноводства.
Во-вторых, следует запретить введение нетелей и ярок в стада и отары взрослых животных. В-третьих, нужно ограничить концентрацию поголовья в хозяйствах молочного направления, которые находятся на территориях, неблагополучных по бруцеллезу. В-четвертых, необходимо оперативно завершать реализуемую в стране программу идентификации (мечения) животных.
– Несложно предположить, что для решения этих задач требуются немалые финансовые вложения.
– Конечно, но если эти задачи не решить, то искоренить бруцеллез на территории нашей страны не получится.
– Лаборатория качества и стандартизации бактерийных лекарственных средств ВГНКИ как структурное подразделение Россельхознадзора разрабатывает образцы сыворотки, которая применяется для диагностики бруцеллёза. Соответствует ли она эталонным стандартам МЭБ?
– Более 30 лет тому назад в лаборатории была разработана Национальная стандартная сыворотка анти-Бруцелла абортус, активность которой составляет 1000МЕ агглютинирующих антител/см 3 . Сыворотка предназначена для стандартизации антигена для реакции агглютинации (РА), применяемой при серологической диагностике бруцеллеза. Периодически с интервалом в пять-семь лет лаборатория готовит очередную серию сыворотки взамен предыдущей. Каждая серия стандартизуется по международной эталонной сыворотке с использованием международного стандарта антигена, предоставляемых Международным эпизоотическим бюро.
Национальная стандартная сыворотка используется и для оценки активности антигенов для других серологических реакций. Но в этой части с учетом современных требований и рекомендаций МЭБ она нуждается в совершенствовании и в изменении ее статуса.
– В заключение расскажите, пожалуйста, о приоритетных задачах вашей лаборатории.
– Традиционно лаборатория выполняет регистрационные и сертификационные испытания, осуществляет инспекционный контроль сертифицированной продукции, а также лекарственный мониторинг и выборочный контроль качества образцов средств специфической профилактики и диагностики бруцеллеза животных. Наряду с этим предполагается выполнение научно-исследовательской работы, цель которой – разработка национальных стандартных образцов сыворотки anti-Brucella abortus для стандартизации антигенов для реакции агглютинации, реакции связывания комплемента, кольцевой реакции с молоком, метода поляризации флуоресценции и иммуноферментного анализа. В частности, речь идет о трех образцах сыворотки anti-Brucella abortus для непрямого ИФА, конкурентного ИФА и поляризации флуоресценции ИФА, стандартизированных по международным стандартным сывороткам с использованием международных стандартных антигенов бруцелл.
Разработка и применение национальных стандартных образцов сыворотки анти-бруцелла абортус для стандартизации бруцеллезных антигенов, используемых в разных серологических тестах, обеспечивает объективную оценку результатов диагностики бруцеллеза в стране, а также международную гармонизацию диагностического тестирования болезни.
Возбудители бруцеллеза (Brucella melitensis, Brucella abortus, Brucella suis и Brucella canis) высоко контагиозны и работа с ними проводится в специализированных лабораториях особо опасных инфекций. Постановку серологических реакций и аллергических проб для диагностики бруцеллеза производят соответственно в обычных микробиологических лабораториях и больничных условиях.
Главным резервуаром бруцелл являются домашние сельскохозяйственные животные, а также другие виды животных, от которых человек заражается преимущественно контактным или контактно-бытовым, реже алиментарным путем. Клинические проявления бруцеллеза многообразны, поражаются лимфатическая, сосудистая, гепато-лиенальная системы и особенно опорно-двигательный аппарат Методы микробиологической диагностики бруцеллеза представлены в схеме 7.
Схема 7. Микробиологическая диагностика бруцеллеза
|
|
Серологический метод- постановка РА с сывороткой крови больного (реакция Райта, ставят в начале 2-й недели болезни, диагностический титр 1:200 и выше), ускоренной РА на стекле (реакция Хеддльсона), РСК и ИФА.
Диагностикумом в реакции Райта и Хеддльсона является взвесь убитых бруцелл с красителем генциановым фиолетовым или метиловым фиолетовым.
Реакцию агглютинации Хеддльсона ставят на стеклянной пластинке, на которую наносят микропипеткой неразведенную исследуемую сыворотку в количествах 0,08; 0,04; 0,02; 0,01 и 0,02 мл, добавляют по 0,03 мл бруцеллезного диагностикума, кроме последней дозы, в которую вносят 0,03 мл ФР (контроль сыворотки). Контролем диагностикума является смесь из 0,03 мл антигена и 0,03 мл ФР. Все капли перемешивают стеклянной палочкой или бактериологической петлей и после легкого покачивания стекла наблюдают за появлением мелкозернистого окрашенного агглютината. Отсутствие агглютинации во всех пробах сыворотки оценивается как отрицательная реакция, наличие агглютинации в 1-й пробе (0,08 мл сыворотки) - сомнительная, во 2-й (0,04 мл) - слабоположительная, в 3-й или 4-й пробах (0,02-0,01 мл) - положительная, во всех пробах - резко положительная реакция. Поскольку реакция агглютинации Хеддльсона иногда бывает положительной у здоровых людей за счет нормальных антител, она обязательно подтверждается реакцией Райта.
РИФ, РНГА, РСК и особенно ИФА более чувствительны, чем реакция агглютинации. Для ранней диагностики бруцеллеза особую ценность имеет ИФА, позволяющий выявить в сыворотке больных антибруцеллезные антитела класса IgM,которыев отличие от IgG появляются в ранние сроки болезни, свидетельствуя о свежем инфицировании.
Аллергический метод –постановка внутрикожной аллергической пробы Бюрне с 15-20 дня заболевания. Учет реакции проводится через 24-48 часов, положительной считается реакция в случае появления на месте введения аллергена (бруцеллина) болезненности, гиперемии и инфильтрации кожи диаметром 3 см и более. Положительная аллергическая реакция на бруцеллин сохраняется в течение длительного времени после перенесенного бруцеллеза, а также после прививки.
Бактериологический метод- посев крови для выделения гемокультуры в 2 флакона с 50 мл печеночного или асцитического бульона (рН 7,1-7,2) или МПБ с добавлением 1 % глюкозы, 2 % глицерина и антифаговой сыворотки (для инактивации бруцеллезного бактериофага) в первые дни болезни при наличии лихорадки. При отрицательных результатах исследование повторяют, т.к. бактериемия наблюдается в течение 1 года и более.
Один флакон выращивают в обычных аэробных условиях, другой — в герметично закрытом сосуде с 10 % углекислого газа (или СО2-инкубаторе) при температуре 37 0 С до 1 месяца, делая пересевы на скошенный печеночный агар или эритрит-агар каждые 4-5 дней. На жидких средах бруцеллы растут с образованием легкого помутнения и небольшого слизистого осадка, на плотных средах в виде округлых, диаметром до 5 мм, серовато-белых, блестящих, прозрачных с янтарным оттенком в проходящем свете колоний. Типичные колонии пересевают на скошенный агар и идентифицируют выделенную культуру до уровня вида.
Выполняются также посевы исследуемого материала в желток свежего куриного яйца или в желточный мешок куриного эмбриона с последующей их инкубацией в течение 5 дней при 37 0 С и пересевом содержимого желточного мешка на плотные и жидкие питательные среды для выделения чистой культуры бруцелл.
Бруцеллы идентифицируют на основании изучения морфологических (рис. 13 - грамотрицательные коккобактерии), культуральных, биохимических (они не ферментируют уг-
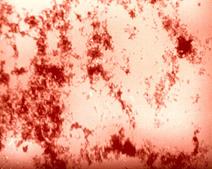
Рис. 13. Возбудитель бруцеллеза (Brucella melitensis). Окраска по Граму. Мелкие грамотрицательные коккобактерии.
леводы, не свертывают молоко и не разжижают желатину, выделяют сероводород), антигенных свойств (постановка РА с моноспецифическими сыворотками против антигеновА, М, R), чувствительности к специфическому бактериофагу и бактериостатическому действию анилиновых красителей (табл. 8).
Таблица 8.Дифференциация основных видов бруцелл
| Признак | Вид бруцелл | ||
| Br. melitensis | Br. abortus | Br. suis | |
| Условия культивирования | аэробные | 10% СО2 | аэробные |
| Рост на средах с красителями: | |||
| фуксином 1:50000 | + | + | - |
| тионином 1:25000 | + | - | + |
| пиронином 1:200000 | + | + | - |
| Образование Н2S | - | ± | ± |
| РА с монорецепторными сыворотками | |||
| А | ± | ± | + |
| М | ± | ± | ± |
| Чувствительность к бруцеллезному фагу | - | + | ± |
– Олег Дмитриевич, чем продиктовано принятие нового ГОСТа?
– Если быть точным, то в действие введен ГОСТ 34105-2017 (Межгосударственный стандарт. Животные. Лабораторная диагностика бруцеллеза. Серологические методы). Его появление обусловлено не только внедрением в российскую ветеринарную диагностическую практику новых серологических тестов, в частности, реакции непрямой гемагглютинации, вариантов иммуноферментного и иммунохроматографического анализа, но и целесообразностью совершенствования диагностики – прежде всего повышения ее оперативности и специфичности.
Разрабатывать этот ГОСТ начинали одновременно с подготовкой по распоряжению Минсельхоза России новых Ветеринарных правил осуществления профилактических, диагностических, ограничительных и иных мероприятий, установления ограничений, направленных на предотвращение возникновения, распространения и ликвидацию очагов бруцеллеза животных в России (далее – новые правила). Сейчас проект правил проходит стадию согласования различными ведомствами.
Разумеется, оценка диагностических титров серологических реакций при диагностике бруцеллеза в ГОСТе и новых правилах будет одинаковой. Поэтому считаю, что до выхода в свет этих правил ветеринарные диагностические лаборатории не должны переходить на работу по ГОСТ 34105-2017.
– Потому что между ГОСТом и действующими в настоящее время Ветеринарными правилами по борьбе с бруцеллезом (ВП 13.3.1302-96) сохраняются существенные различия.
– На какие положения стандарта вы хотели бы обратить внимание специалистов в первую очередь?
– К сожалению, несмотря на то, что ГОСТ34105-2017 согласовывался специалистами стран Евразийского экономического союза, в нем сохраняются недочеты.
– Одним из таких недочетов является предписание проводить дополнительное исследование образцов сыворотки в РИД и ИФА с ОПС-антигеном в случае выявления в группах животных, иммунизированных и не иммунизированных против бруцеллеза и положительно реагирующих по результатам серологических исследований в ряде реакций. Такое требование предусмотрено пп. 8.2, 8.3 и 8.4 данного ГОСТа в целях уточнения диагноза.
– Если речь идет об уточнении диагноза, то почему вы называете это недочетом?
– Дело в том, что, по состоянию на сегодняшний день, диагностические тест-системы для иммуноферментного анализа в рамках госзаказа выделяются в ограниченном количестве. Представители большей части ветеринарных диагностических лабораторий утверждают, что им такие тест-системы будут недоступны. Соответственно, непроведение серологического тестирования в ИФА, согласно ГОСТу, будет расценено представителями надзорных учреждений как нарушение.
С учетом разницы в диагностической чувствительности между РИД с ОПС-антигеном и ИФА с ОПС-антигеном исследование последним методом является принципиальным. В противном случае при выполнении серологического исследования только в РИД с ОПС-антигеном объективность его результатов может быть сомнительной.
Не буду вдаваться в подробности других имеющих принципиальное значение недочетов, отмечу лишь, что после их обсуждения и согласования с диагностическими ветеринарными лабораториями должно быть инициировано внесение изменений в ГОСТ 34105-2017.
– Какие ошибки чаще всего допускают при лабораторной диагностике бруцеллеза?
– О существенных ошибках мне неизвестно. К тому же мы не контролируем работу лабораторий. Однако, когда специалисты ряда лабораторий обращаются к нам, чтобы обсудить спорные результаты исследований, кажется, что некоторые из них не знакомы со всеми документами, регламентирующими диагностику болезни. Впрочем, большинство специалистов проявляют инициативу и демонстрируют познания, достаточные для диагностики болезни. Не менее важно и то, что они заинтересованы в получении объективных результатов.
– Какова сегодня эпизоотическая ситуация по бруцеллезу среди крупного и мелкого рогатого скота на территории России?
В период с 2013 по 2017 годы количество неблагополучных по бруцеллезу мелкого рогатого скота пунктов, остававшихся на конец года, составляло 30, 28, 22, 17 и 14. Число заболевших животных – 1,9; 2,5; 2,2; 1,22 и 1,01 тыс. голов.
– Можно утверждать, что динамика положительная?
– Система контроля бруцеллеза животных в стране несовершенна?
– Сложившуюся систему контроля бруцеллеза животных в Российской Федерации можно считать удовлетворительной. Однако это не исключает необходимости ее совершенствования. Прежде всего в части сокращения временных затрат при установлении диагноза за счет более широкого применения средств дифференциальной диагностики болезни, а именно реакции иммунодиффузии и иммуноферментного анализа с ОПС-антигеном, возможно, за счет сочетания средств диагностики.
Важным представляется проведение исследований и установление возможных, максимально ранних сроков серологического исследования вакцинированных животных, особенно мелкого рогатого скота, иммунизированного агглютиногенными вакцинами. В настоящее время этим никто не занимается.
Не стоит забывать, что самый эффективный способ оздоровления неблагополучного хозяйства предусматривает ликвидацию всего поголовья в таком хозяйстве. Однако данный способ не слишком широко применяется в нашей стране. (Должен отметить, что в проекте новых правил его применение регламентировано в большем количестве случаев, нежели в Ветеринарных правилах 13.3.1302-96.) Поэтому перед проведением вакцинации животных в рамках оздоровления путем вакцинации и последующих периодических серологических исследований особенно важно максимально полно удалять инфицированных особей из групп животных.
– В нынешних условиях это реально?
– Я бы сказал, что это возможно за счет введения животным неблагополучных по бруцеллезу хозяйств провоцирующих неагглютиногенных антигенов, в отличие от применяющихся вакцин, с последующим серологическим исследованием и удалением выявленных больных животных.
При этом не могу не отметить, что организации-производители, планировавшие выпускать такие антигены, зарегистрированные ими ранее в Российской Федерации, пока не справляются со своими планами и не понятно, справятся ли.
– Что препятствует повышению эффективности системы контроля бруцеллеза?
– На мой взгляд, совершенствование этой системы не представляется возможным без решения целого ряда задач. Во-первых, нужно создавать в регионах, неблагополучных по бруцеллезу, мясокомбинаты и бойни, обеспечивающие убой больных животных, что решает проблему неполного, несвоевременного и антисанитарного убоя. При этом следует компенсировать владельцам убыток. К сожалению, он неизбежен при изъятии больных животных, прежде всего в условиях ведения отгонного животноводства.
Во-вторых, следует запретить введение нетелей и ярок в стада и отары взрослых животных. В-третьих, нужно ограничить концентрацию поголовья в хозяйствах молочного направления, которые находятся на территориях, неблагополучных по бруцеллезу. В-четвертых, необходимо оперативно завершать реализуемую в стране программу идентификации (мечения) животных.
– Несложно предположить, что для решения этих задач требуются немалые финансовые вложения.
– Конечно, но если эти задачи не решить, то искоренить бруцеллез на территории нашей страны не получится.
– Лаборатория качества и стандартизации бактерийных лекарственных средств ВГНКИ как структурное подразделение Россельхознадзора разрабатывает образцы сыворотки, которая применяется для диагностики бруцеллёза. Соответствует ли она эталонным стандартам МЭБ?
– Более 30 лет тому назад в лаборатории была разработана Национальная стандартная сыворотка анти-Бруцелла абортус, активность которой составляет 1000МЕ агглютинирующих антител/см 3 . Сыворотка предназначена для стандартизации антигена для реакции агглютинации (РА), применяемой при серологической диагностике бруцеллеза. Периодически с интервалом в пять-семь лет лаборатория готовит очередную серию сыворотки взамен предыдущей. Каждая серия стандартизуется по международной эталонной сыворотке с использованием международного стандарта антигена, предоставляемых Международным эпизоотическим бюро.
Национальная стандартная сыворотка используется и для оценки активности антигенов для других серологических реакций. Но в этой части с учетом современных требований и рекомендаций МЭБ она нуждается в совершенствовании и в изменении ее статуса.
– В заключение расскажите, пожалуйста, о приоритетных задачах вашей лаборатории.
– Традиционно лаборатория выполняет регистрационные и сертификационные испытания, осуществляет инспекционный контроль сертифицированной продукции, а также лекарственный мониторинг и выборочный контроль качества образцов средств специфической профилактики и диагностики бруцеллеза животных. Наряду с этим предполагается выполнение научно-исследовательской работы, цель которой – разработка национальных стандартных образцов сыворотки anti-Brucella abortus для стандартизации антигенов для реакции агглютинации, реакции связывания комплемента, кольцевой реакции с молоком, метода поляризации флуоресценции и иммуноферментного анализа. В частности, речь идет о трех образцах сыворотки anti-Brucella abortus для непрямого ИФА, конкурентного ИФА и поляризации флуоресценции ИФА, стандартизированных по международным стандартным сывороткам с использованием международных стандартных антигенов бруцелл.
Разработка и применение национальных стандартных образцов сыворотки анти-бруцелла абортус для стандартизации бруцеллезных антигенов, используемых в разных серологических тестах, обеспечивает объективную оценку результатов диагностики бруцеллеза в стране, а также международную гармонизацию диагностического тестирования болезни.
Читайте также:


