Гнойно септические заболевания в хирургии
Гнойно-септические заболевания – группа недугов, которые провоцируют патогенные бактерии. Неприятная симптоматика чаще всего развивается на фоне ослабленного иммунитета пациента. При попадании в организм бактерии начинают стремительно размножаться. В результате у больного развиваются признаки воспаления, требуется немедленная медицинская помощь. Гнойно-септические инфекции в хирургии занимают особое место. Большая часть экстренных пациентов обращается за помощью именно с такими заболеваниями.
Грамположительные бактерии
Гнойно-септическая инфекция – это большая группа патогенных микроорганизмов, которые в норме могут присутствовать в теле любого человека. Неприятная симптоматика развивается тогда, когда патогенная микрофлора начинает стремительно размножаться на фоне снижения иммунитета пациента.

Наиболее распространенными являются стафилококки. Это условно-патогенные микробы, которые могут вызывать септические, респираторные и кишечные заболевания. Стафилококковой инфекцией могут поражаться любые органы и ткани при снижении защитных сил. Инфекция чаще всего протекает в виде местного гнойного воспалительного процесса. При попадании патогенного микроба в ЖКТ проявляются симптомы отравления. Может приводить к развитию неприятных осложнений стафилококк. Что это за болезнь? По сути, это целый спектр недугов. Стафилококк может вызывать сепсис с повышенным риском летального исхода. Поэтому при появлении любых неприятных симптомов необходимо обращаться за помощью.
Стрептококки – это также потенциально патогенные микроорганизмы, которые могут стремительно размножаться в условиях сниженного иммунитета. Особенно хорошо они растут при повышенном уровне глюкозы в крови. От стрептококковой пневмонии нередко страдают пациенты с сахарным диабетом. Источником инфекции чаще всего выступает больной человек. Однако тесный контакт еще не значит, что придется столкнуться с неприятными симптомами. Большое значение имеет иммунитет.
При стафилококковой инфекции также могут поражаться любые органы и ткани. Нередко на фоне инфицирования развивается сепсис.
Энтерококки – это бактерии, которые относятся к разряду грамположительных. По физиологическим характеристикам они очень схожи со стрептококками. Нередко энтерококки провоцируют заболевания мочевыводящих путей (цистит, уретрит), бактериальный эндокардит. Хотя в норме энтерококки даже полезны. Они принимают участие в поддержании нормальной микрофлоры кишечника, подавляют деятельность других патогенных микроорганизмов.
Грамотрицательные бактерии
Сальмонеллы – это опасные микроорганизмы. Именно они выступают в роли возбудителя брюшного тифа. Это род неспороносных бактерий, имеющих форму палочек. Эти организмы являются грамотрицательными. При попадании в организм человека они вызывают опасные симптомы. Несвоевременно оказанная помощь может привести к смерти пациента.
Множество грамотрицательных бактерий может продолжительное время существовать в организме человека, не давая о себе знать. Любой удар по иммунитету – отличная возможность для условно-патогенной микрофлоры. Такие бактерии начинают стремительно размножаться при переохлаждении, стрессовой ситуации, эмоциональном перенапряжении, переутомлении и т. д.
Существует множество подвидов грамотрицательных бактерий. Основные возбудители ГСИ были рассмотрены выше. Реже встречаются следующие микроорганизмы: псевдомонады, спирохеты, бруцеллы, франциселлы и т. д. Они могут нарушать работу желудочно-кишечного тракта, сердечно-сосудистой и дыхательной систем. Наиболее опасными являются грамотрицательные палочки и кокки, хламидии, хеликобактерии.
ГСИ окружают человека повсюду. Обезопасить себя от развития опасных заболеваний помогут простые меры профилактики, которые будут описаны ниже.
Лабораторная диагностика
Квалифицированный специалист при появлении у пациента неприятных симптомов может поставить предварительный диагноз. Однако начать терапию не удастся до тех пор, пока не будет выявлен возбудитель, которым спровоцирован патологический процесс. Методы диагностики инфекции существуют разные. При выявлении гнойного воспаления обязательно проводится микробиологическое исследование. Это нужно для того, чтобы определить чувствительность патогенной микрофлоры к выбранному антибиотику. Диагностика проводится с помощью реакции иммунофлюоресценции.
Особым образом проводится забор биологического материала для проведения исследования при гнойных инфекциях кожных покровов. Все манипуляции выполняются в условиях полной стерильности во время операции или оперативного вмешательства. Кожа вокруг пораженной поверхности обрабатывается антисептиком. Из основного очага поражения отбирается отделяемое с помощью шприца.

При подозрении на стрептококковую пневмонию проводится бактериологическое исследование бронхиального секрета. Бактериальный посев при этом важно проводить еще до начала терапии с использованием антибиотиков. Разовая порция мокроты собирается в утреннее время натощак.
Определить, есть ли в организме инфекция, поможет также экспресс-тест на стрептококк. Исследование может быть назначено, если у пациента появился упадок сил, больной часто жалуются на головокружения. От стрептококковой инфекции часто страдают дети дошкольного возраста. Микробиологическое исследование может проводиться, если ребенок страдает от ОРЗ больше пяти раз в год.
Тест на стрептококк выполняется очень просто. Все манипуляции могут проводиться в амбулаторных условиях прямо в кабинете врача. Все, что нужно сделать, - это взять мазок со слизистой рта пациента. Биологический материал далее исследуется в лабораторных условиях с использованием специальных реактивов.
Исследования при заболеваниях ЖКТ
Боли в животе, тошнота, нарушение аппетита – эти симптомы могут свидетельствовать о присутствии инфекции в организме. Чаще всего пациентам в первую очередь назначаются общие анализы мочи, крови и кала. Если уровень условно-патогенных микроорганизмов превышен, это удастся выяснить.
Менингит, хронический гастрит, эндокардит – при всех этих патологиях содержание энтерококка в кале будет превышено. В этом случае актуальным будет лечение с использование антибиотиков. Нередко проблемы выявляются у малышей грудного возраста, которые употребляют искусственное питание.
При кишечных инфекциях выделение возбудителя производится из рвотных и каловых масс. В некоторых случаях бактерии удается выявить в воде, которую используют для промывания желудка. Идентификацию возбудителя удается провести благодаря посеву на питательные среды.
Факторы передачи гнойно-септической инфекции
Условно-патогенная микрофлора в норме присутствует в организме любого человека. Если у одного члена семьи присутствуют симптомы инфекционного процесса, это не значит, что заболеют и остальные. Однако тесный контакт с больным рекомендуется ограничить. Помещение, где находиться пациент, рекомендуется чаще проветривать.
Гораздо больше риск заразиться при внутриполиклиническом инфицировании. Ведущий путь передачи – контактный. Это руки медицинского персонала, текстильные изделия, предметы обстановки. В связи с этим особое внимание уделяется санитарно-гигиеническим мероприятиям. Медицинский персонал должен соблюдать правила личной гигиены – мыть руки с мылом и обрабатывать их антисептиком после контакта с каждым новым пациентом. Важно также исключить занос инфекции в стационар. После приема пациента клеенка на кушетке обрабатывается дезинфицирующим раствором.

Гнойно-септические инфекции (ГСИ) легко передаются контактным способом. В группу риска попадают пациенты с ослабленным иммунитетом, которые находятся в условиях госпиталя. Поэтому особое внимание уделяется чистоте рук медицинского персонала. Гигиенические процедуры необходимо проводить до и после любых манипуляций с больным. Дополнительно следует использовать специальные стерильные перчатки.
Как остановить распространение гнойно-септической инфекции? Гигиенические требования медицинским персоналом должны соблюдаться обязательно. В этом случае удастся значительно сократить стремительное распространение патогенной микрофлоры.
Стрептококковые инфекции
Это целая группа заболеваний, которые развиваются вследствие стремительного размножения стрептококковой флоры. Эти патологии очень опасны своими осложнениями. Минус в том, что стрептококки устойчивы к окружающей среде. Эти микроорганизмы без проблем могут существовать при пониженных и высоких температурах. Погибают они в горячей среде лишь через 30 минут. Под действием химических дезинфекторов (антисептиков) стрептококки погибают лишь через 15 минут.
Носителем стрептококковой инфекции является больной человек. Патогенная микрофлора передается воздушно-капельным путем. Больной выделяет бактерии при кашле, чиханье. Заразиться можно даже во время разговора с переносчиком инфекции. Наиболее заразными являются пациенты, у которых поражены верхние дыхательные пути. Легко заразиться можно ангиной, скарлатиной. При этом на расстоянии более трех метров патогенная микрофлора передаваться уже не будет. Поэтому ограничение контакта с пораженным человеком – лучшая мера профилактики. На пациента можно надеть специальную стерильную маску.
Значительно повышается риск развития гнойных осложнений у пациентов с ожогами, ранениями. Стрептококковая инфекция нередко развивается у больных после операций. Поэтому в условиях стационара особенно важно соблюдать все гигиенические нормы. В группу риска попадают также беременные женщины и новорожденные из-за ослабленного иммунитета.
Стрептококк может проявляться по-разному. Гнойно-септические инфекции часто встречаются на верхних дыхательных путях, слуховом аппарате. Особенно часто такие заболевания встречаются в педиатрии. Дети могут страдать от гнойного отита, гайморита, ангины. Особого внимания заслуживает стрептодермия. При этом заболевании клинические проявления стрептококковой инфекции наблюдаются на коже пациента в виде везикул, пятен, гнойных элементов.

При отсутствии качественного лечения патогенная микрофлора начинает стремительно развиваться на внутренних органах. Особую опасность для жизни представляет стрептококковая пневмония. В этом случае инфекция поражает слизистую оболочку легких. Заболевание может быть следствием недолеченной ОРВИ. Особенно часто с такой патологией встречаются пациенты осенью или весной. В сырой среде патогенные микроорганизмы размножаются быстрее.
Клинически стрептококковая пневмония проявляется сильным кашлем, симптомами общей интоксикации организма, болью в груди. Во время кашля выделяется мокрота с гнойным содержимым. Заболевание может стать причиной серьезных осложнений, угрожающих жизни больного. Поэтому за медицинской помощью необходимо обращаться незамедлительно.
Стафилококковая инфекция
Что это за болезнь - стафилококк? По сути, это не само заболевание, а условно-патогенная микрофлора, провоцирующая развитие неприютных симптомов. Чаще всего стафилококк является причиной развития гнойных поражений кожи. Фурункулез – распространенное заболевание, при котором воспаляется волосяной фолликул, а также окружающая ткань. Заболевание чаще развивается у пациентов, не соблюдающих гигиенические нормы. Также в группу риска попадают ослабленные люди, перенесшие другие опасные заболевания. Фурункулез может развиваться на фоне гриппа, ОРЗ.
Снижение иммунитета может быть обусловлено также хроническими заболеваниями, эндокринными нарушениями, продолжительной гормональной терапией и т. д. Проникновение патогенной микрофлоры в волосяной мешочек может быть вызвано механическим повреждением кожных покровов. В связи с этим любую рану важно правильно обработать антисептиком. Повышается риск развития стафилококковой инфекции на кожи у пациентов с гипергидрозом (повышенным потоотделением). Спровоцировать инфицирование могут и другие дерматологические патологии – экземы, псориаз, дерматит.
В некоторых случаях наличие инфекции в организме может никак не проявляться. Выявить стафилококк в крови удается во время очередного профилактического обследования. Такая ситуация является потенциально опасной и оставлять без внимания ее нельзя. С током крови патогенная микрофлора может распространяться по всему организму. Возрастает риск обширного заражения – сепсиса. При значительном снижении иммунитета инфекция может поражать мозговые оболочки. Менингит – опасное заболевание, которое часто заканчивается летальным исходом.
Стафилококковую инфекцию в запущенной стадии не всегда удается быстро вывести из организма. Антибиотики подбираются с учетом чувствительности патогенной микрофлоры. В некоторых случаях приходится менять препарат по несколько раз, а само лечение длится месяцами.
Брюшной тиф
Это острая кишечная инфекция, которая приводит к развитию опасных симптомов. Поражаются преимущественно лимфатическая система и кишечник. Возбудителем брюшного тифа выступает сальмонелла. Патогенная микрофлора может сохранять жизнеспособность в окружающей среде несколько месяцев. Благоприятной средой для размножения сальмонеллы являются некоторые пищевые продукты – молоко, яйца, мясной фарш. Эта патогенная грамотрицательная палочка легко переносит замораживание. А вот химическая и термическая обработка действует губительно на бактерии.
Как и в случае с другими гнойно-септическими инфекциями, выделение возбудителя происходит с мочой и калом. Источником тифа является больной человек. Выделение возбудителя в окружающую среду происходит уже в конце инкубационного периода, когда у самого пациента еще нет неприятных симптомов. В редких случаях заболевание приобретает хронический характер. При этом человек будет распространять инфекцию на протяжении всей жизни.

Легко передаются в бытовой среде гнойно-септические инфекции. Гигиенические требования следует соблюдать обязательно. Путь заражения сальмонеллой – водный и пищевой. Так, после каждого посещения туалета необходимо тщательно мыть руки с мылом. Заражение может происходить также при употреблении воды, загрязненной фекалиями (речки, озера, другие водоемы). В летне-осенний период отмечается пик заболеваемости.
Инкубационный период недуга не превышает двух недель. Первые неприятные симптомы могут появиться уже через пять дней после заражения. У больного появляется лихорадка, симптомы общей интоксикации организма. Но общим ухудшением самочувствия гнойно-септические инфекции не ограничиваются. Тиф сопровождается побледнением кожных покровов, высыпаниями. У пациента появляются проблемы с дефекацией, внутренние органы увеличиваются.
Брюшной тиф опасен своими осложнениями. У некоторых пациентов наблюдаются кишечные кровотечения, развивается острая анемия. Больной даже с незначительными проявлениями тифа обязательно подлежит госпитализации. Терапия проводится с использованием антибиотиков. Параллельно может быть назначена вакцинация.
Энтерококковая инфекция
Существует более 15 различных видов энтерококков. Эти микроорганизмы не всегда приводят к развитию неприятных симптомов. Однако их уровень в организме следует контролировать. Если выявлены энтерококки в кале, может быть назначено дополнительное обследование. Нередко повышение показателей наблюдается у детей дошкольного возраста. Такая ситуация может быть обусловлена снижением защитных сил организма на фоне переохлаждения, приема лекарственных препаратов. Значительное увеличение числа энтерококков в организме может стать причиной таких заболеваний, как цистит, менингит, отит, гастрит и т. д.
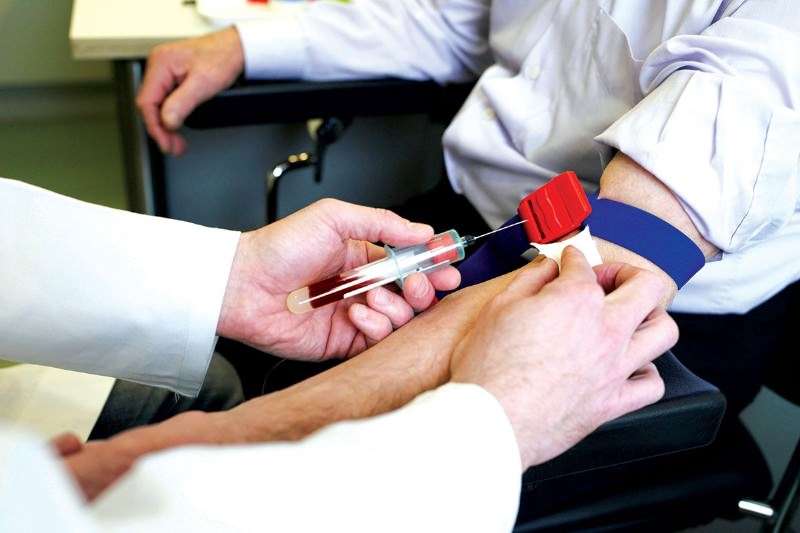
Анализ кала – не единственная методика определения того или иного расстройства. Дополнительно исследуют мочу и кровь пациента. Могут использоваться также инструментальные методики.
Чтобы начать адекватную терапии, изначально необходимо определить вид энтерококка, которым спровоцировано заболевание. Медикамент подбирают с учетом чувствительности микрофлоры, а также индивидуальных особенностей организма пациента, обязательно учитывается возраст.
Профилактика гнойно-септических инфекций
Развитие любых заболеваний легче не допустить, нежели потом проводить терапию. Общая характеристика гнойно-септических инфекций показывает, что пути передачи патогенной микрофлоры могут быть разными. Это и воздушно-капельный путь, и тесный контакт, и кровь. Чтобы исключить развитие эпидемий, должна проводиться как индивидуальная, так и общая профилактика.
Индивидуальная профилактика заключается в ведении здорового образа жизни. Человеку следует укреплять защитные силы организма – правильно питаться, больше времени проводить на свежем воздухе, полноценно отдыхать, отказаться от вредных привычек. Важное значение имеет соблюдение правил личной гигиены и своевременная влажная уборка помещения, в котором большую часть времени проводит человек.
Общественная профилактика включает создание условий, при которых коллективы могут полноценно выполнять свою деятельность. На заводах, в учебных учреждениях, в офисах могут выполнять иммунопрофилактические прививки. При выявлении одного зараженного объявляется карантин, позволяющий ограничить распространение инфекции. Риск развития эпидемий будет снижен, если простые меры профилактики будут соблюдать абсолютно все.
Что такое гнойная хирургия
Понятие "гнойная хирургия" является собирательным термином, который включает в себя лечение заболеваний и осложнений, протекающих с участием патогенных микроорганизмов и требующих хирургического вмешательства. Присоединение инфекции может осложнить течение широкого круга заболеваний и хирургических операций.
Трудно найти область медицины, в которой не работают специалисты по хирургической инфекции:
Травматология: инфицированные посттравматические и ожоговые раны, посттравматический остеомиелит, гнойные осложнения металлоостеосинтеза
Ортопедия: гнойные артриты, гнойные осложнения протезирования суставов и других ортопедических вмешательств
Абдоминальная хирургия: осложненные варианты интраабдоминальной инфекции, инфицированный панкреонекроз, гнойные осложнения после "открытых" и лапароскопических операций на органах брюшной полости
Ревматология: инфицированные трофические язвы на фоне системных васкулитов и заболеваний соединительной ткани.
Эндокринология: инфицированные формы синдрома диабетической стопы
Ангиология: гангрены на фоне критической ишемии конечностей
Флебология: трофические язвы нижних конечностей на фоне хронической венозной недостаточности
Дерматология: инфекции кожи, осложненные абсцедированием
Онкология: осложнения после хирургического и лучевого лечения опухолей различной локализации
Пластическая и эстетическая хирургия: гнойные осложнения после использования медицинских имплантатов, а также применение методов пластической хирургии для закрытия обширных ран.
Инфекционные болезни: заболевания, протекающие с некрозом и воспалением мягких тканей
Неврология: пролежни различной локализации
Формы заболеваний
Острые гнойные заболевания мягких тканей:
- абсцесс - ограниченный очаг воспаления с образованием гнойной полости;
- флегмона - разлитое гнойное воспаление мягких тканей, не имеющее сформированной капсулы. Наиболее грозным вариантом флегмоны является некротизирующая инфекция мягких тканей, которая стремительно, в течение нескольких часов поражает обширные участки соединительной ткани, мышц или подкожной клетчатки. В этих случаях жизнь пациента напрямую зависит от скорости и радикальности выполненной хирургической операции, а также от грамотно проведенной интенсивной терапии в условиях специализированного учреждения. Раньше эти заболевания называли газовой гангреной или анаэробной инфекцией.
Хронические гнойные заболевания:
- трофические язвы, инфицированные раны, гнойные свищи, гангрены - являются, по сути, не самостоятельными нозологическими формами, а осложнениями самых разных заболеваний. Успех в их лечении в первую очередь зависит от правильно установленного диагноза и от возможности воздействовать на причину образования раны и нарушения ее заживления.
При генерализации инфекции (переход местного процесса в общий, развитие вторичных очагов) развивается сепсис, который сопровождается дисфункцией внутренних органов и систем и при неблагоприятном течении может привести к смерти пациента.
Симптомы заболеваний
- Боль в пораженном участке - главный симптом острых гнойных заболеваний мягких тканей.
- Нарушение целостности кожных покровов – характерные, но не обязательный симптом, так называемые "входные ворота" инфекции.
- Болезненная припухлость.
- Кожа над очагом гнойного воспаления часто бывает горячей, покрасневшей, иногда с багровым оттенком.
- Повышение температуры тела, нарастание признаков интоксикации.
Следует отметить, что яркая клиническая картина наблюдается не всегда, и иногда обширные гнойные процессы протекают со скудными местными проявлениями. Особенно это характерно для пожилых и ослабленных пациентов.
Симптомы хронических гнойных заболеваний: образование незаживающих ран, язв, свищей или некроза кожи и мягких тканей.
Причины заболеваний
Комплекс причин, вызывающих образование и длительное существование гнойных очагов, включает в себя:
- Инфекцию, то есть локальную и системную воспалительную реакцию организма на патогенную микрофлору. Инфицирование, как правило происходит:
- при нарушении целостности кожных покровов (при травмах, хирургических операциях, инъекциях),
- контактно (через неповрежденный кожный покров или слизистые оболочки),
- гематогенно (с током крови).
Особенно упорно протекает инфекция при наличии эндопротезов, имплантов и других инородных материалов.
- Ишемию, или нарушение питания тканей вследствие нарушенного кровоснабжения. Некротизированные ткани становятся идеальной питательной средой для раневой микрофлоры, что делает патологический процесс неконтролируемым. Добиться купирования гнойного процесса без восстановления кровоснабжения бывает чрезвычайно трудно.
- Венозную недостаточность, которая приводит к формированию длительно незаживающих трофических язв.
- Сахарный диабет, сопровождающийся нарушением кровоснабжения, иннервации и иммунного ответа. Хирургическая инфекция, протекающая на фоне сахарного диабета, отличается упорным течением и требует комплексного подхода с участием различных специалистов.
Наиболее распространенные возбудители раневых инфекций - грам-положительные (стафилококки, стрептококки и др.) и грам-отрицательные (синегнойная палочка, протей, клебсиелла) микроорганизмы.
Следует отметить, что в последние годы отмечается возрастание числа устойчивых к антибиотикам штамммов возбудителей раневой инфекции. Это делает чрезвычайно ответственным назначение стартовой антибактериальной терапии и определяет необходимость бактериологического контроля за микрофлорой раны.
Диагностика
Современные методы диагностики основаны на определении состояния тканей, обнаружении очагов деструкции (разрушения тканей), скоплений патологического содержимого, наличия воспалительных изменений.
Для оценки распространенности гнойного процесса используется ультразвуковое исследование мягких тканей, компьютерная томография (КТ), магнито-резонансная томография (МРТ), радиоизотопное сканирование с использованием меченых аутолейкоцитов. Обязательным является исследование клеточного состава крови для выявления общей реакции на воспаление, бактериологическое исследование для установления характера микрофлоры и определения чувствительности возбудителей к антибиотикам.
Особенности лечения
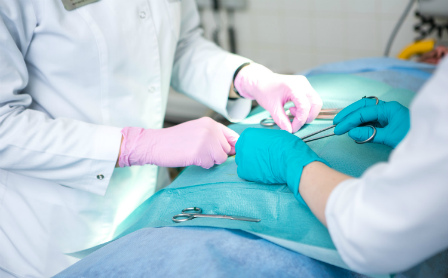
Основа лечения всех вариантов хирургической инфекции - радикальная хирургическая обработка гнойного очага, включающая удаление некротизированных тканей и адекватную санацию раны. В послеоперационном периоде проводят антибактериальную терапию, местное лечение раны с применением современных мазей, раневых покрытий и перевязочных материалов. После купирования воспаления и перехода раны в стадию регенерации решают вопрос о хирургическом закрытии раны (швами, перемещенными полнослойными лоскутами, либо свободными кожными лоскутами). Возможно и самостоятельное заживление небольших ран под повязкой, хотя это удлиняет сроки лечения и приводит к формированию более грубого рубца.
Профилактика
Профилактика хирургической инфекции заключается, прежде всего, в контроле над "входными воротами" инфекции, применении методов антисептики для обработки случайных ран. Важным является своевременное лечение заболеваний, усугубляющих течение инфекции, в первую очередь сахарного диабета, заболеваний артерий и вен нижних конечностей.
Новые технологии диагностики и лечения ран
В последние годы разрабатываются и входят в практику новые методы лечения ран.
К методикам, позволяющим существенно улучшить результаты лечения, можно отнести применение лечения ран локальным отрицательным давлением (NPWT – negative pressure wound treatment, V.A.C. - vacuum assisted clossure). Применение этого метода позволяет оптимизировать течение всех фаз раневого процесса, добиться быстрого купирования воспаления, снизить бактериальную обсемененность раны и способствует быстрому сокращению глубины и размеров раны. Данный метод лечения не требует частых болезненных перевязок, смена повязки производится 1 раз в 3 – 7 дней в зависимости от фазы раневого процесса.
Кардинально улучшить результаты лечения пациентов с синдромом диабетической стопы удается с помощью эндоваскулярных методов восстановления магистрального артериального кровотока в нижних конечностях. Применение баллонной ангиопластики и стентирования позволяет сохранить конечность даже при начинающейся гангрене.
Преимущества гнойной хирургии в ЕМС
Клиника ЕМС является современным лечебным учреждением, обладающим всеми современными возможностями диагностики и лечения. Круглосуточная работа лечебно-диагностического комплекса позволяет комплексно решать проблемы, возникающие при тяжелой хирургической инфекции мягких тканей, в кратчайшие сроки выполнить полноценное обследование и предоперационную подготовку. Радикальное хирургическое лечение производится в кратчайшие сроки в современных операционных, оборудованных лучшей хирургической и анестезиологической аппаратурой.
Перевязки ран выполняются с применением обезболивания. Используются раневые покрытия, препараты для местного лечения ран и перевязочные материалы ведущих производителей.
Использование вакуум-ассистированных повязок позволяет максимально ускорить заживление ран и снизить число перевязок. Возможно амбулаторное лечение локальным отрицательным давлением с редкими (1 раз в 3 – 7 дней) визитами в клинику.
Доступность в стенах одной клиники современных методов обследования и лечения, а также ведущих специалистов позволяет оперативно производить восстановление кровоснабжения, купировать фоновые и сопутствующие заболевания одновременно с контролем за состоянием очага инфекции и комплексным лечением ран.
Хирургическое закрытие ран производится с применение методов пластической хирургии для достижения максимально функционального и эстетического результата.
B.C. Савельев
далекого прошлого — термин введен Гиппократом - сепсис остается проблемой медицинского, демографического и экономического значения. К сожалению, в нашей стране отсутствуют обобщающие эпидемиологические и статистические данные, поэтому приходится ссылаться на зарубежные. В конце XX века США ежегодно регистрировали около 700 000 случаев сепсиса. Во Франции частота сепсиса составляет 6 случаев на 1000 больных в обычных отделениях и 119 случаев на 1000 пациентов, находящихся в отделениях интенсивной терапии.
Метанализ показал, что летальность, связанная с сепсисом, за последние 50 лет снизилась лишь на 20%, и к началу XXI века в среднем составляет около 40%.
Большое значение для организации здравоохранения имеют данные об отдаленных результатах лечения сепсиса. Так, через 8 лет после успешного непосредственного лечения умерли 82% больных, перенесших сепсис. Прогнозируемая продолжительность жизни после перенесенного сепсиса в среднем составляет 5 лет (Quartin AA et al, 1997). При этом качество жизни выживших больных значительно ниже нормы для соответствующих попу-ляционных групп.
Концептуальные вопросы сепсиса - как в отношении понимания его этиопатогенеза и нозологической сущности, так и диагностики и лечения — всегда были предметом противоречий и дискуссий. В последнее время благодаря достижениям фундаментальных наук и клинической медицины получены новые данные об этиологии, патогенезе и та-натогенезе этого патологического процесса. Выяснение новых закономерностей взаимосвязи микроб - человек и общебиологических механизмов ответа на повреждение позволило прийти к заключению, что в основе сепсиса как генерализованного процесса лежит общая, системная реакция макроорганизма, связанная с выбросом различных медиаторов воспаления под действием микроорганизмов. Иначе говоря, сепсис - это проявление системной воспалительной реакции в ответ на микробную агрессию. Однако при сепсисе возникает не просто гиперпродукция про- и противовоспалительных медиаторов и активация других регуля-торных систем - от апоптоза и коагуляции до выброса гормонов. При сепсисе происходит дисрегу-
Координация усилий в исследовании сепсиса позволила унифицировать его диагноз. О сепсисе свидетельствуют клинические признаки системной воспалительной реакции при наличии очага инфекции. Такой унифицированный подход в диагностике сепсиса создает основу для определения эффективности и стандартов лечения, оценки прогноза, а также позволяет проводить эпидемиологические исследования.
хирургическая инфекция и гнойно-септическая хирургия
процесс, начальные проявления которого могут быстро перейти в фатальную стадию полиорганной недостаточности и необратимого инфекционно-токсического шока.
В августе 2001 г. исполнилось 10 лет со времени Согласительной конференции по сепсису, которая предложила стандартизировать терминологию, касающуюся синдрома системной воспалительной реакции (ССВР) и сепсиса. Десятилетний опыт показал, что концепция системной воспалительной реакции имеет не только клиническое, но и общебиологическое значение.
Признаки ССВР являются чувствительными критериями для выявления популяции риска инфекционных осложнений и служат основой опережающего принципа диагностики сепсиса и других критических состояний. При адекватной клинической трактовке симптоматика ССВР имеет существенное дифференциально-диагностическое значение. Частота выявления признаков ССВР в отделениях интенсивной терапии весьма высока — до 75%. Лишь у 25-50% больных с признаками ССВР подтверждается его инфекционная этиология. При этом вероятность ее инфекционной причины четко коррелирует с количеством выявляемых признаков.
В последние годы произошли определенные изменения в микробиологической структуре сепсиса. Если 15-20 лет назад в этиологии хирургического сепсиса доминировали грамотрицательные бактерии и золотистый стафилококк, то сейчас существенно возросла роль сапрофитных стафилококков, энтерококков и грибов. Увеличилась частота выделения микробов, наименования которых ранее были вообще неизвестны клиницистам.
Причина этого - селекция резистентных микробов под влиянием антибиотиков, широкое применение инвазивных методов диагностики и лечения, влияние различных факторов, вызывающих иммунодепрессию.
Сепсис является одной из основных причин летальности хирургических больных и может осложнять течение различных заболеваний и локальных воспалительных процессов.Септическая реакция возникает при перитоните, пневмонии и уроинфекции, нагноении раны, инфицировании внутрисосудистых устройств и катетеров. Выявление первичного очага важно для успешного лечения сепсиса любого ге-неза. Особое значение это имеет для хирургической практики, где успешная оперативная санация невозможна без топического диагноза.
Абдоминальный сепсис, осложняющий течение различных внутрибрюшных воспалительных и деструктивных процессов, представляет наиболее сложную проблему как в диагностическом и лечебном плане, так и в экономическом отношении. В нозологической структуре абдоминального сепсиса приоритетное место занимают различные формы перитонита и гнойно-воспалительные осложнения деструктивного панкреатита. Большая частота развития сепсиса объясняет весьма высокую летальность при этих заболеваниях. Отличительные особенности абдоминального сепсиса, связанные со сложнейшей анатомией, физиологией и биоэкологией органов брюшной полости, включают:
наличие многофокусных и крупномасштабных очагов инфекции, быстрое включение механизма эндогенного инфицирования, сверхактивацию медиаторов и других каскадов системной воспалительной реакции, ускоренное развитие полиорганной недостаточности и септического шока, трудности топической и дифференциальной диагностики. Частое возникновение при абдоминальном сепсисе дистантных и метахронных очагов инфекции, в частности нозокомиальной пневмонии и ан-гиогенного инфицирования, вносят свою лепту в танатогенез этой формы хирургического сепсиса. С учетом особенностей приоритетного спектра возбудителей, путей инфицирования, динамики развития патологического процесса, классификация хирургического сепсиса с учетом локализации первичного очага имеет важное клиническое значение и позволяет обосновать стратегию и тактику различных направлений лечения.
Полиорганная недостаточность, патогномонич-ная для сепсиса, особенно абдоминального, включает поражение различных систем и органов, практически у 60% больных.
Нарушения кровообращения и транспорта кислорода в начальных стадиях сепсиса носят гипердинамический характер с последующим возникновением гиподинамии, синдрома малого сердечного выброса с резким падением доставки и потребления кислорода.
В последние годы уточнена роль различных звеньев коагуляционного каскада в патогенезе и тана-тогенезе тяжелого сепсиса и септического шока. В частности, установлено, что потребление протеина С при ССВР не только приводит к нарушениям гемокоагуляции, но и является причиной дисрегу-ляции системного воспаления, резкого нарушения функции клеток, повреждению эндотелия сосудов и недостаточности органов-мишеней.
Огромную роль в патогенезе сепсиса играет возникновение кишечной недостаточности. Под влиянием медиаторов воспаления, гиперкатаболизма, нарушений системного и висцерального кровотока быстро нарастает повреждение энтероцитов, нарушаются практически все функции желудочно-кишечного тракта — барьерная, метаболическая, иммунозащитная, эндокринная. Кишечная недостаточность - важнейший компонент порочного круга при сепсисе, поскольку транслокация бактерий и их токсинов поддерживает воспалительную реакцию, усугубляя нарушения обмена веществ.
Разрыв порочного круга и успешное лечение больных с сепсисом зависят от своевременной и комплексной реализации 3 стратегических направлений: устранения очагаи блокады дальнейшей генерализации инфекции, воздействия на воспалительные каскадные реакции и
хирургическая инфекция и гнойно-септическая хирургия
комплексной интенсивной поддержки функции органов-мишеней.
Первостепенное значение для хирургического сепсиса имеет инвазивная, хирургическая санация инфекционного очага. Для его выявления нам часто приходится прибегать к различным методам лучевой диагностики, а в ряде случаев даже к радиоизотопным методам исследования. Невозможность одномоментной санации очага, особенно при абдоминальном сепсисе, диктует необходимость неоднократных оперативных вмешательств, которые сами по себе могут быть дополнительным фактором поддержания системной воспалительной реакции.
Важнейшую роль играет адекватная и своевременная антимикробная терапия. Выбор антибиотиков зависит не только от спектра их действия и фармакокинетических характеристик, но и определяется тяжестью состояния больного. Чем тяжелее больной, тем рациональнее должна быть тактика антибактериальной терапии. Фактор времени решает многое. Неадекватная антибактериальная терапия существенно повышает летальность больных с сепсисом. Рациональное использование антибактериальных препаратов,как показывает наш опыт, позволяет на 20% сократить расходы на лечение.
Основа интенсивной терапии - коррекция тканевой гипоксии, оптимизация доставки кислорода, респираторная поддержка.
В отношении коррекции кишечной недостаточности наши возможности пока весьма ограничены, но и их необходимо использовать в полной мере.
Особое значение в ведении больных с сепсисом играет профилактика тромбоза глубоких вен и фатальных тромбоэмболических осложнений. Как правило, у больных с сепсисом выявляют один или несколько факторов риска этих осложнений. По данным доказательных исследований, фармакологическая профилактика ТЭО с помощью нефрак-ционированного или низкомолекулярного гепарина в 2-3 раза снижает частоту фатальных тромбоэмболических осложнений и существенно влияет на летальность больных с сепсисом.
Важную роль в борьбе за жизнь больного играет метаболическая, нутритивная поддержка с приоритетным использованием энтерального питания.
Что касается новых экспериментальных направлений лечения сепсиса, направленных на блокаду и связывание токсинов бактерий, цитокинов и других медиаторов воспаления, то убедительных данных об их эффективном влиянии на летальность при сепсисе пока не получено. Дело, по-видимому, не только в том, что гуморальная воспалительная реакция в силу ее многокомпонентности, разнонаправленное™ и лабильности похожа на китайскую головоломку. Определение активности циркулирующих в крови медиаторов - лишь верхушка айсберга, под водой скрыто много неизвестного. Генетический полиморфизм цитокиногенеза, его зависимость от вида возбудителя не дают пока нам четкого и клинически значимого маркера для целенаправленного лечебного воздействия на медиатор-ном уровне. Сепсис - намного более сложный патологический процесс, чем известная нам сейчас сумма его составляющих. Клинических и лабора-
торных критериев сепсиса достаточно, чтобы своевременно его заподозрить и сформулировать диагноз. Но этих критериев мало для эффективного и своевременного вмешательства в каскады ме-диаторной бури.
Новые данные о роли нарушений гемокоагуля-ции в патогенезе сепсиса привели к разработке нового препарата - активированного человеческого протеина С (АРС). Многокомпонентное благоприятное действие АРС подтверждено результатами только что проведенных международных клинических испытаний. Под влиянием этого препарата удалось улучшить шансы выживания больных с тяжелым сепсисом на 38%. Впервые за 10 лет получен столь значительный успех при применении нового направления лечения сепсиса. По мнению экспертов, вполне вероятно включение АРС в стандарт лечения этой тяжелой категории больных.
На сегодняшний день эффективность применения препаратов иммуноглобулинов в отношении снижения летальности больных доказана как в рандомизированных испытаниях, так и путем ме-танализа опубликованных данных. В настоящее время изучается также эффективность энзимоте-рапии в лечении больных с сепсисом (вобэнзим, флогэнзим).
Особые проблемы связаны с ангиогенным инфицированием, ангиогенным сепсисом. Основная причина этих осложнений - широкое использование для лечения и мониторного контроля длительной катетеризации сосудов. Масштабы этой проблемы отражают эпидемиологические данные. Летальность при ангиогенной инфекции (не атрибутивная, а общая) составляет 25-60%. Следует иметь в виду, что почти 75% случаев бактериемии в послеоперационном периоде связано именно с инфицированием внутрисосудистых катетеров. Кроме того, ангиогенные инфекционные осложнения могут возникнуть при имплантации любого жизнеспаси-тельного устройства в сердечно-сосудистую систему - от клапанов сердца до кава-фильтров для профилактики тромбоэмболии легочных артерий. Следует подчеркнуть, что диагностика и лечение ангиогенной инфекции и сепсиса - крайне сложная проблема.
Значительные трудности связаны с диагностикой и лечением нозокомиальной пневмонии, в частности у хирургических больных. Особенно высока частота возникновения такой пневмонии при проведении искусственной вентиляции легких -до 50%.
Участие в этиологии нозокомиальной пневмонии проблемных микроорганизмов ограничивает арсенал эффективных антибактериальных препаратов, и это осложнение вносит свой весомый вклад в танатогенез хирургических больных. Сле-
хирургическая инфекция и гнойно-септическая хирургия
дует отметить, что целенаправленная антимикробная терапия позволила нам существенно - почти на 20% - ограничить фатальный потенциал, связанный с нозокомиальной пневмонией.
В проблеме госпитальной инфекции есть и существенные достижения. В частности, совершенствование хирургической техники прежде всего и применение так называемой интраоперационной профилактики антибиотиками привело к значительному снижению частоты раневых инфекционных осложнений после операций различных категорий - как чистых, так и контаминированных. И к концу XX века проблема послеоперационной раневой инфекции стала в определенной степени контролируемой.
Основные клинические достижения инфектоло-гии и учения о сепсисе касаются многих аспектов диагностики и лечения, оценки прогноза, внедрения новых антибиотиков, иммунокорригирующих средств, новых фундаментальных представлений о патогенезе и взаимоотношений микроба с челове-
ком. Не менее значительными выглядят нерешенные проблемы.
Особо отметим резистентность бактерий ко многим антибиотикам, возрастание роли грибковой инфекции, сохранение высокой летальности при сепсисе, несостоятельность лечебных воздействий на уровне септического медиаторного каскада.
Перспективным является решение ряда задач научного и организационно-методического плана. Необходимо продолжить разработку современной концепции сепсиса и углубить наши представления о взаимоотношениях микроб—человек Весьма существенным является стандартизация диагностики и лечения госпитальных инфекций на основе доказательных микробиологических, фармакологических и клинических исследований. Решение этих задач невозможно без тесного сотрудничества представителей фундаментальных, прикладных и клинических наук.
ИЛ. Ерюхин
ложность и драматизм проблемы перитонита "растворяются" в клинической неопределенности обобщающего понятия. Диагноз перитонита в общем смысле подразумевает любую форму и любую степень выраженности воспаления брюшины. В данной связи еще И.И. Греков с горькой иронией замечал, что "исправить" угнетающую статистику исходов перитонита довольно просто: стоит лишь "разбавить" наблюдения истинного перитонита теми его формами, для излечения которых достаточно одной адекватной и своевременно выполненной операции без каких-либо дополнительных усилий. Опыт показывает, что подобные тенденции проявляются и поныне. Они служат причиной сосуществования оптимистических заключений некоторых диссертационных исследований и отдельных публикаций с серьезной озабоченностью большинства клиницистов в связи с сохраняющейся высокой летальностью при перитоните. Согласно публикуемым сводным данным Б.КЩуркалина (2000), средние показатели летальности удерживаются на уровне 20-30%, а при наиболее тяжелых формах перитонита, к примеру, послеоперационном перитоните — достигают 40 - 50%.
Перитонит остается хирургической, общеклинической и общепатологической проблемой, актуальность которой не снижается, несмотря на несомненные успехи клинической медицины, вооруженной новыми перспективными технологиями. Поэтому вновь, далеко не в первый раз, прослеживается необходимость более четкого определения и рационального ограничения проблемы перитонита с тем, чтобы сконцентрировать внимание на
профилактике и лечении тяжелых его форм. Начинать обсуждение лечения перитонита каждый раз приходится с уточнения позиций относительно клинической его классификации, имея в виду три исходных положения.
Во-первых, всякая классификация условна и потому не способна полностью исключить те или иные дискуссионные разногласия. Во-вторых, клиническая классификация должна быть краткой, удобной в использовании и ориентированной на решение вполне конкретной практической задачи: обеспечения дифференцированного подхода к лечебно-диагностической тактике. В-третьих, не идеальная, но согласованная общепринятая классификация всегда имеет преимущества перед прочими, возможно и более точными по общепатологическому смыслу, но не получившими широкого признания классификационными вариантами.
Читайте также:


