Синдром умственной отсталости при токсоплазмозе
Токсоплазмоз как одна из причин пренатального поражения мозга впервые описан в 1939г. у ребенка 1 мес с картиной энцефаломиелита.
Частота. Среди больных с глубоким интеллектуальным дефектом частота врожденного токсоплазмоза составляет менее 1%. Среди больных с легкой умственной отсталостью он встречается значительно реже.
Роль врожденного токсоплазмоза в генезе умственной отсталости долгое время значительно переоценивалась. Это обусловлено широкой распространенностью скрытой инфицированности токсоплазмой и, следовательно, большой частотой положительных иммунологических реакций и кожных проб с токсоплазменным антигеном у лиц самых разных контингентов, в том числе и среди умственно отсталых. В действительности роль токсоплазмоза как этиологического фактора умственной отсталости невелика.
Этиология и патогенез. Возбудитель токсоплазмоза — toxoplasma gondii — относится к типу простейших и является внутриклеточным паразитом (простейший паразит).
В организм человека попадает от животных (собаки, кошки, свиньи, крупный рогатый скот), диких животных (лисицы, зайцы, белки и др.) или птиц (голуби, куры и т.д.). Заражение может произойти различным способом (капельным — при уходе за животными, с пищей — через мясо, молоко и пр.).
Врожденный токсоплазмоз является следствием трансплацентарной передачи инфекции от беременной матери к эмбриону или плоду в острой стадии инфекционного процесса у женщин и инфицирует его. Наиболее часто инфицирование плода происходит со 2-го по 6-й месяц беременности. В тяжелых случаях наступает гибель зародыша или плода. В более легких случаях поражение приводит к разнообразным аномалиям развития, и в частности нервной системы.
Клиника.Проявления токсоплазмоза характеризуются чрезвычайным разнообразием в зависимости от времени начала заболевания, типа течения, активности и локализации патологического процесса. В детской практике имеет значение врожденный токсоплазмоз.
Признаки болезни могут проявляться сразу после рождения или в первые недели и месяцы жизни ребенка.
Болезнь иногда может протекать остро по типу менингоэнцефалита (высокая температура, расстройство сознания, судороги, менингеальные явления, параличи и др.). Наряду с поражением центральной нервной системы могут иметь место расстройства со стороны внутренних органов (печень, селезенка, кишечник, легкие). Иногда страдает зрение (атрофия зрительных нервов, изменения в хрусталике и др.).
Болезненный процесс может протекать и в подострой форме. В этих случаях развитие детей сопровождается задержкой. Дети вялы, апатичны. Иногда наблюдается повышенная психомоторная возбудимость.
В тех случаях, когда острая и подострая стадии заканчиваются внутриутробно, ребенок рождается с хроническим токсоплазмозом, для которого характерны грубые неврологические симптомы и выраженное слабоумие.
У таких детей наряду с микроцефалией, гидроцефалией, спастическими параличами и судорогами отмечаются характерные интракраниальные кальцификаты (очаги обызвествления в местах расположения паразита)и поражения органов зрения: хориоретинит, увеит, катаракта, помутнение хрусталика, псевдоколобома желтого пятна, атрофия зрительного нерва, глаукома и микрофтальмия.
При рентгенографии обнаруживаются образовавшиеся кальцификаты (в местах расположения паразита).
При более позднем заражении плода, при инфицировании плода в конце беременности дети могут рождаться без признаков заболевания. Однако первые клинические проявления могут развиться сразу же после рождения или в течение 1—2-го года жизни. В этих случаях острая стадия врожденного токсоплазмоза характеризуется генерализацией процесса и протекает либо как септическое заболевание, либо в форме висцерального токсоплазмоза с высокой температурой, желтухой, сыпью и поражением внутренних органов, либо же в форме токсоплазмозного менингоэнцефалита, лептоменингита и энцефалита.
Токсоплазменный менингоэнцефалит характеризуется высокой температурой тела, адинамией, рвотой, менингеальными симптомами, судорогами и параличами конечностей. В случае выздоровления у детей формируется тяжелая умственная отсталость.
Психическое недоразвитие проявляется с первых месяцев жизни и обычно достигает степени имбецильности и идиотии.
Патоморфологические изменения в головном мозге при врожденном токсоплазмозе характеризуются воспалительно-дистрофическим процессом (очаговый энцефалит или менингоэнцефалит) и последствиями дисциркуляторных нарушений с ишемическими размягчениями вещества мозга вследствие тромбозов и эмболии просвета сосудов токсоплазмами и псевдоцистами.
Диагнозврожденного токсоплазмоза основывается на совокупности клинических и лабораторных данных.
В клинической картине наиболее патогномоничными можно считать два симптома: хориоретинит и кальцификаты в мозге, выявленные рентгенологически; хориоретинит отмечен у 76% больных, кальцификация — у 92%. Но следует помнить, что оба симптома могут появиться в более позднем возрасте. Так, появление хориоретинита при врожденном токсоплазмозе описано даже на 2-м десятилетии жизни.
Для окончательной диагностики заболевания решающее значение имеют специфические серологические реакции и обнаружение токсоплазмы в цереброспинальной жидкости и крови.
При внутриутробном токсоплазмозе и мать, и ребенок первых месяцев жизни могут иметь титр антител 1:256 или чуть ниже. Титр остается положительным в течение нескольких лет. Очень важно отметить, что положительные серологические реакции при сочетании с умственной отсталостью еще не могут считаться доказательством роли токсоплазмоза в повреждении мозга.
Лечение. Применяются препараты пиримидинового ряда — хлоридин при сочетании с сульфаниламидными препаратами, которые усиливают его действие.
Вредности, нарушающие здоровье беременной женщины или действующие непосредственно на плод, могут нарушить психическое развитие ребенка. Число тератогенных факторов, вызывающих нарушения и пороки развития плода, в том числе и умственную отсталость, составляет несколько сотен. Среди них — неполноценное питание будущей матери, ее соматические заболевания, токсикозы, инфекции, а также несовместимость крови. Кроме того, в происхождении умственной отсталости играют роль тяжелые эмоциональные стрессы, вредные физические и химические воздействия.
Внутриутробное развитие плода разделяют на три стадии: стадию зародыша (от оплодотворения до имплантации яйцеклетки в стенку матки — около двух недель); стадию эмбриона (от 2-й до 7-й недели беременности) и стадию фетуса (от 8-й недели и до рождения). Воздействие вредностей на организм беременной женщины в первые две недели после зачатия не сказывается на зародыше, так как он еще не успевает имплантироваться. Если все же это произошло, то его развитие, скорее всего, прекратится. Влияние вредоносных факторов на стадии эмбриона может привести к нарушению формирования ЦНС и внутренних органов, воспрепятствовать закладке конечностей, глаз, ушей, так как при нормальном течении беременности именно между 2-й и 7-й неделями образуются эти части тела. Поражение на стадии фетуса в первую очередь скажется на формировании структур мозга. Таким образом, последствия тератогенного воздействия зависит не только, а иногда не столько от качества вредности, сколько от срока ее действия.
Реакция незрелой нервной ткани на повреждения и болезни отличается от реакции тканей у взрослых. В ответ на вредоносные факторы возникают нарушения развития нейроглии и соединительной ткани, которые обеспечивают жизнедеятельность нейронов. Однако нет прямой зависимости между тяжестью разрушения тканей ЦНС и глубиной психического дефекта. Степень выраженности клинических проявлений определяется временем поражения плода, природой вредоносного фактора, а также возможностями восстановления поврежденной ткани.
Общие соображения о действии разных групп вредностей были высказаны в главе 2. Здесь представлены особенности клинических проявлений синдромов умственной отсталости, возникающих при некоторых наиболее часто встречающихся поражениях плода.
СИНДРОМ УМСТВЕННОЙ ОТСТАЛОСТИ ПРИ ТОКСОПЛАЗМОЗЕ
Токсоплазмоз в качестве причины умственной отсталости описан в 1939 году. Он вызывается одноклеточным паразитом токсоплазмой, которая особенно опасна для плода. Чем раньше он инфицируется, тем более вероятна его гибель, чем позже — тем легче поражения. Среди лиц с тяжелой умственной отсталостью врожденный токсоплазмоз встречается с частотой около 1%.
Клиника. Зараженный плод рождается с активной или скрытой инфекцией. В этом случае у больного отмечаются лихорадка, желтуха, сыпь, а иногда и судорожные припадки. Характерны воспалительные поражения глаз, отложения кальция в тканях мозга. Часто наблюдаются микроцефалия, гидроцефалия, пятнистая пигментация радужной оболочки, пневмония, менингит. В спинномозговой жидкости обнаруживаются высокое содержание белка и нередко — токсоплазмы.
Умственная отсталость при этом синдроме обычно проявляется с первых месяцев жизни и достигает тяжелых степеней.
Патогенез. Токсоплазмы, попав с током крови в тело плода, образуют гранулемы, в центре которых находится паразит, а вокруг мертвые клетки ткани. При проникновении токсоплазм в ЦНС развивается менингит, нередко сопровождающийся гидроцефалией. Подтверждение диагноза возможно при проведении кожной пробы, анализа титра антител в крови.
Терапия. Лечение проводится хлоридином и сульфаниламидами.
СИНДРОМ УМСТВЕННОЙ ОТСТАЛОСТИ ПРИ ЦИТОМЕГАЛИИ
Этот синдром вызывается вирусом слюнных желез, которым дети заражаются внутриутробно. Среди больных с тяжелой умственной отсталостью на долю цитомегалии приходится около 0,3—0,5%. Цитомегалия — причина 10% случаев микроцефалии.
Степень выраженности умственной отсталости определяется временем поражения в пренатальном периоде и тяжестью поражения.
Патогенез. Вирусы, попадающие через плацентарную кровь, вызывают у плода деструктивное воспаление мозга и его оболочек. Они обнаруживаются в тканях, в моче, кроме того, в клетках эпителия появляются характерные тела.
СИНДРОМ УМСТВЕННОЙ ОТСТАЛОСТИ ПРИ ЛИСТЕРИОЗЕ
Заболевание вызывается бактериями, поражающими преимущественно нервные ткани и обладающими способностью проходить плацентарный барьер.
Клиника. Листериоз протекает в форме заражения крови и менингоэнцефалита, проявляясь соответствующими симптомами. По завершении острого периода заболевания остаются признаки грубого органического поражения ЦНС. Его последствиями оказываются тяжелые степени умственной отсталости, сочетающиеся с повышенной возбудимостью, склонностью к аффективным вспышкам.
Патогенез. Симптоматика в значительной степени определяется возникновением специфических гранулем в головном мозге, а также во внутренних органах. В спинномозговой жидкости обнаруживаются признаки, характерные для гнойного менингита.
УМСТВЕННАЯ ОТСТАЛОСТЬ ПРИ ВРОЖДЕННОМ СИФИЛИСЕ (ЮВЕНИЛЬНЫЙ ПАРАЛИЧ)
Симптоматика этого заболевания связана с внутриутробным заражением сифилитической спирохетой.
Патогенез. Спирохеты развиваются в тканях плода. Повреждение тканей связывают с влиянием на них микробных токсинов или с их чрезмерно чувствительной реакцией. Следствием этого являются гуммы, воспаление внутренних стенок сосудов, разрушение или сдавливание нервной ткани.
Терапия. Лечение проводится антибиотиками, препаратами висмута.
УМСТВЕННАЯ ОТСТАЛОСТЬ ПРИ КРАСНУХЕ (РУБЕОЛЯРНАЯ ЭМБРИОПАТИЯ, СИНДРОМ ГРЕГГА-СВАНА)
Этот синдром впервые описан N. Gregg в 1940 году. Он возникает при заболевании матери краснухой в первой трети беременности (50— 80% случаев).
Клиника. Дети рождаются маловесными (на 15—30% легче). В случаев имеется двусторонняя катаракта. У 65% детей — микрофтальмия и другие пороки развития глаз. Вследствие нарушения развития внутреннего уха у 50% детей развивается глухота. Часто встречаются пороки развития зубов. У 50% детей имеется врожденный порок сердца. Микроцефалию обнаруживают у 11 % детей, реже встречаются гидроцефалия, суженная кверху голова и сращения пальцев. Наблюдаются затруднения сосания и глотания, эпилептические припадки, двусторонние или односторонние спастические параличи и парезы. Встречаются большие размеры родничков, расщепление неба, другие пороки лицевого черепа, спинномозговая грыжа, пороки развития костей предплечья, грудной клетки, нижних конечностей. Выявляются также крипторхизм, гипоспадия, двудолевые почки, двурогая матка и др.
Умственная отсталость, наблюдающаяся при этом синдроме, сочетается с нарушением координации движений, двигательной расторможенностью или недостаточной активностью, эмоциональной лабильностью, импульсивностью.
Патогенез. Клиническая картина эмбриопатии зависит от того, с закладкой каких органов плода совпадает инфицирование беременной. Заболевание женщины после 3-месячного срока беременности редко приводит к возникновению пороков у плода. Тератогенное действие краснухи объясняется необычной восприимчивостью эмбриональной ткани к инфекционным агентам. Внутриутробная инфекция приобретает хронический характер, даже после рождения ребенок сравнительно долго выделяет вирусы через дыхательные пути, мочу и кал.
Терапия. Из-за опасности возникновения рубеолярной эмбриопатии многие женщины, узнав о своем заболевании краснухой, прерывают беременность. Эффективность профилактики введением гаммаглобулина оценивается очень различно.
АЛКОГОЛЬНЫЙ СИНДРОМ ПЛОДА (АЛКОГОЛЬНАЯ ЭНЦЕФАЛОПАТИЯ)
Впервые алкогольный синдром плода в 1973 году описали Johns и Smith. 8% всех случаев умственной отсталости обусловлено алкоголизмом родителей. Выраженность синдрома зависит от тяжести материнского алкоголизма и срока воздействия алкоголя на плод. У матерей, страдающих алкоголизмом, в 71% случаев рождаются дети с нарушениями нервно-психического развития, в 37% — с психическим недоразвитием, в 37% — с психопатическими и невротическими расстройствами.
Клиника. У детей обнаруживается низкая масса тела, плохое сосание и глотание, частые срыгивания, отставание в физическом развитии. Треть детей позже начинают ходить. У 32% выявляются пороки сердца, почек, желудочно-кишечного тракта, мочевыделительной системы. Имеются признаки костного дизонтогенеза: задержка развития зон окостенения, диспластичность телосложения, незаращение или раннее закрытие швов черепа, макро- или микроцефалия, короткая шея, недоразвитие верхней и нижней челюсти, гипертелоризм, широкая запавшая переносица, высокое небо, узкие и короткие глазные щели, синдактилия. Для этого синдрома характерны деформация грудной клетки, клинодактилия, гипоплазия ногтей, разболтанность суставов. Нередко встречается эпикант, сосудистые опухоли, асимметрия глазных щелей, косоглазие, нистагм, птоз, мышечная гипотония и иногда припадки.
Задержка психического развития встречается более чем у 25%, психофизический инфантилизм — у 20%, умственная отсталость — также почти у 20% детей. Речь запаздывает у трети детей. Тяжелый алкоголизм матерей приводит к более выраженным степеням умственной отсталости у их детей (дисфорическому и мориоподобному вариантам) по сравнению с детьми, матери которых выпивают меньше. Наряду с другими нарушениями психомоторного развития у них присутствуют плохая память, нарушенное внимание, общая астения, повышенная аффективная возбудимость и раздражительность, двигательная расторможенность и утомляемость. В пубертатном возрасте наряду с легкой умственной отсталостью формируются невротические и патохарактерологические развития. Появляются психопатоподобные (84%), церебрастенические и неврозоподобные (10%) синдромы. Нередки расторможенность влечений, ранняя гиперсексуальность, бродяжничество, воровство.
Патогенез. В прямой зависимости от тяжести алкоголизма отца и матери находятся рождение детей в асфиксии, ослабление сосательного рефлекса, судороги, задержка психомоторного развития, отставание речи. Влияние алкоголизма матери сказывается примерно в 2-3 раза чаще, чем алкоголизм отца. Кроме того, при алкоголизме матери достоверно чаще встречаются недоношенность, переношенность, угрожающие выкидыши, мертворожденность, врожденные уродства. Алкоголь интенсивно действует на клеточные мембраны, на процессы клеточного деления и синтеза ДНК нервных клеток. В первые недели после зачатия он приводит к грубым порокам развития ЦНС. После 10-й недели беременности алкоголь вызывает клеточную дезорганизацию или замедляет клеточную миграцию и нарушает дальнейшее развитие ЦНС. Позже алкоголь нарушает мозговой метаболизм и нейрогенные влияния на эндокринную систему, что вызывает нейроэндокринные расстройства, в частности нарушения роста. Вероятно, в происхождении пороков у плода большую роль играет недостаток цинка в организме матери.
УМСТВЕННАЯ ОТСТАЛОСТЬ, ВЫЗВАННАЯ ГЕМОЛИТИЧЕСКОЙ БОЛЕЗНЬЮ
Гемолитическая болезнь возникает у новорожденных с Rh-несов-местимостью, АБО-несовместимостью и в случае гипербилирубинемии без доказанной несовместимости групп крови матери и ребенка. Подавляющее число больных — мальчики. Частота гемолитической болезни — 1 на 250—300 родов. Клиника. Для биллирубиновой энцефалопатии характерны двигательные расстройства, дефекты и выпадение зубов, нарушения слуха, остроты зрения и умственная отсталость. Неврологические симптомы выявляются в 6 раз чаще, чем в норме. Среди них — глазодвигательные расстройства, повышения тонуса мышц спины, судороги, парезы, параличи, гиперкинезы, атаксия.
Умственная отсталость варьирует от легкой до глубокой степени и встречается в четыре раза чаще, чем у детей, не страдавших гемолитической болезнью. Характерно дисгармоническое развитие интеллекта. Сложная структура психических нарушений обнаруживается у детей с нарушениями слуха. На первый план выступают недостаточность вербального мышления и несостоятельность при выполнении заданий, связанных с речевой переработкой инструкций, при негрубом недоразвитии наглядно-действенного мышления. Затруднения в обучении встречается у двух третей детей. Им свойственна низкая концентрация внимания. Выявляется эмоциональная незрелость, создающая повышенный риск заболевания неврозом. Для этих детей обычно храктер-ны поведенческие нарушения.
Патогенез. Этиология заболевания — иммунологическая несовместимость, связанная с проникновением через плаценту в кровь матери, резус-фактора или другого фактора плода, несовместимого с кровью матери, который провоцирует выработку антител. Антитела, попадая в кровь плода, разрушают эритроциты. Появившийся биллирубин вызывает гемолитическую болезнь новорожденных: отек, тяжелую желтуху и врожденную анемию. Иммунизируется только одна из 25— 30 резус-отрицательных женщин. Этому способствуют аборты, переливание резус-положительной крови, повреждение плаценты. Тяжесть поражения ЦНС зависит не только от уровня биллирубина и продолжительности его действия, но и от состояния эндокринной системы новорожденного, а также от количества белка, способного связывать биллирубин.
Терапия. Обменное переливание крови в первые сутки жизни ребенка.
УМСТВЕННАЯ ОТСТАЛОСТЬ, СВЯЗАННАЯ С РОДОВОЙ ТРАВМОЙ
Под родовыми травмами понимают неизбежные и предотвратимые механические повреждения плода или гипоксию плода во время родов, приводящие к многообразным нарушениям ЦНС. Частота родовых травм — 2—7 на 100 живорожденных.
Клиника. Наибольшее отставание в физическом и нервно-психическом развитии отмечается у детей, перенесших тяжелую асфиксию и родовую травму. У новорожденных наблюдаются угнетение физиологических рефлексов, тремор, судороги, клонус конечностей. У них на 2,5-5 месяца запаздывают моторные навыки (удерживание головы, ползание, ходьба) и первая улыбка, а на 3-6 месяца — первые слова. Часто отмечаются нарушенный тонус мышц, замедленное развитие координации движений, параличи или парезы, сочетающиеся с нарушением черепно-мозговой иннервации. Парез и гипертония мышц ног затрудняют ходьбу, заставляя их передвигаться на носочках. У части детей — гипотония мышц и атетоз. Нередкое явление — судорожные припадки. При перинатальной гипоксии в 30% — задержка психического развития, а в 4% — умственная отсталость. При тяжелой родовой травме с асфиксией наряду с описанной симптоматикой у 25% детей наличествует умственная отсталость. Особенности психических нарушений определяются гипертензионным синдромом, церебральной сосудистой недостаточностью, церебрастенией. Эта мозговая патология приводит к нарушениям поведения, периодически возникающим колебаниям настроения, ослаблению памяти, расстройствам внимания, нарушениям счета в сочетании с нарушением формирования пространственного синтеза.
Патогенез. Под влиянием асфиксии в мозге новорожденного сосуды переполняются кровью, возникает отек тканей, разрывы мелких сосудов и кровоизлияния. Из-за нарушения тканевого обмена разрушаются клетки мозга. При длительной аноксии происходит размягчение, а затем и атрофия коры мозга. Все это предрасполагает к разрывам тканей, происходящим в процессе родов. Таким образом, родовая травма — это переломы костей черепа, разрывы твердой мозговой оболочки и внутричерепные кровоизлияния, возникающие из-за разрыва сосудов. Формирование умственной отсталости при этой патологии связано с недоразвитием мозга и остаточными явлениями перенесенной мозговой травмы (ликвородинамическими, сосудистыми, очаговыми нарушениями).
Терапия. Стимулирующее лечение сочетается с дегидратацией и физиотерапией.
Умственная отсталость, обусловленная
Предшествующей инфекцией или интоксикацией
Краснуха.Заболевание вызывается вирусом краснухи, который проникает в плод в первые три месяца беременности и вызывает тяжелые дефекты развития внутренних органов и головного мозга. Клинически это проявляется врожденными пороками сердца, дефектами глазных яблок, возникновением глухонемоты, гидроцефалии, микроцефалии, а иногда и анэнцефалии и гидроанэнцефалии, которые могут возникнуть и при других видах расстройств.
В неврологическом статусе отмечаются спастические парезы и параличи, слепота, глухота, нарушения речи и др. Выражено резкое отставание психического развития таких больных. Интеллектуальные нарушения проявляются в виде прогрессирующего слабоумия в связи с вторичной атрофией мозгового вещества.
Микроцефалия- заболевание, характеризующееся малыми размерами черепной коробки и мозга, вследствие недоразвития мозгового вещества и раннего заращения родничков и швов черепа.
Клинически заболевание проявляется глубокой умственной отсталостью, спастическими парезами и параличами конечностей, судорожными припадками и резким замедлением психического развития. Обращают на себя внимание некоторые особенности психики микроцефалов: они добродушны и ласковы, однако неожиданно для окружающих у них могут возникать недлительные аффективные вспышки.
Характерен внешний вид больного: голова сужена кверху, низкий и покатый лоб, ресницы длинные, большие оттопыренные уши, не симметрично расположенные, зубы большие и редкие, часто кариозные. Рост черепа больше идет в длину, и высота его мало меняется в течение жизни.
Микроцефалический синдром впервые описан английскими врачами Е. Коккейном (Е. Cochlayne) и Ф. Нэйлом (F. Neil F) в 1936 г.
Анэнцефалия - врожденное недоразвитие черепа и полушарий головного мозга. Обычно сохраняются лишь подкорковые образования, ствол и мозжечок, что обусловливает сохранность лишь простых рефлекторных актов. Продолжительность жизни — не более 10 суток. Частота анэнцефалии - 5-8 случаев на 1000 новорожденных.
Гидроанэнцефалия — врожденное недоразвитие мозга, при котором отсутствуют полностью большие полушария и кости черепа. Пузырь с жидкостью, замещающий головной мозг, покрыт только кожей и мягкими тканями головы. Продолжительность жизни до 3 месяцев. Частота гидроанэнцефалии составляет 1 случай на 18 000 новорожденных.
Врожденный токсоплазмоз — паразитарное заболевание, которое проявляется различными видами врожденных уродств, в том числе и нервной системы, приводящих к тяжелой и глубокой умственной отсталости. Заболевание вызывается токсоплазмой — одноклеточным простейшим организмом, паразитом, которым женщина заражается от домашних или диких животных в период беременности. Передача токсоплазм от матери плоду происходит трансплацентарным путем. Циркулирующие в крови плода токсоплазмы заносятся во все органы и ткани, что обусловливает полиморфизм клинической картины. Поражение плода приводит к выкидышам, мертворождениям, а также к тяжелым поражениям всех органов и систем, вплоть до гидроцефалии и анэнцефалии.
Энцефалиты.Энцефалит — воспаление головного мозга — является одной из наиболее часто встречающихся форм нейроинфекции.
Заболевание обусловлено множеством факторов, в зависимости от которых у детей наиболее часто встречаются следующие клинические формы: клещевой, вирусный, коревой, поствакцинальный.
Клещевой энцефалит.Возбудителем заболевания является вирус, который передается человеку при укусе клеща. В тканях мозга вирус появляется на 2—3 сутки после укуса. Инкубационный период от момента заражения до появления первых симптомов болезни длится 8—20 дней. Клиника заболевания характеризуется острым началом, подъемом температуры, головной болью, однократной рвотой, мышечными и корешковыми болями, слабостью, потерей аппетита, повышенной утомляемостью, адинамией, бледностью кожных покровов, расстройством стула. Как проявление выраженной интоксикации у детей в первые дни болезни отмечается артериальная гипотония в сочетании с тахикардией. В неврологическом статусе выявляется полиморфизм клинической симптоматики: менингиальные симптомы, гемипарезы, бульбарные и псевдобульбарные параличи, другие психические расстройства. По истечении острого периода 10—15 дней заболевание переходит в резидуальную стадию (стадия остаточных явлений), при которой на фоне четкой неврологической картины выявляются различные проявления интеллектуальной недостаточности, от легкой до глубокой степени умственной отсталости.
Профилактика клещевого энцефалита включает в себя уничтожение клещей в зараженных областях и вакцинацию населения, проживающих в этих зонах.
Вирусный энцефалит.Существует множество штаммов нейрови-русов, каждый из которых избранно поражает ту либо иную зону мозга, проявляясь своеобразным течением и клиникой.
Очаговая неврологическая симптоматика в виде гемипарезов, менингиального и гипертензионного синдромов, бульбарных и псевдобульбарных параличей, эпиприпадков и др. выявляется уже в первые дни от начала заболевания на фоне повышения температуры, а зачастую и потери сознания. В остром периоде болезни отмечаются различные психические расстройства.
Нарушения интеллекта проявляются в виде легкой либо умеренной умственной отсталости.
Алкогольный синдром плода.Причиной данной патологии является хронический алкоголизм будущей матери либо однократная ее алкоголизация в период беременности. Алкоголь, оказывая токсическое воздействие на организм плода, с одной стороны, тормозит его нормальное развитие, а с другой - приводит к тяжелым необратимым изменениям еще не сформированных органов и систем, и прежде всего головного мозга, костной системы и внутренних органов.
Клиническая характеристика пороков развития и заболеваний, обусловленных алкогольной интоксикацией, приводится авторами в соответствующих разделах данного пособия.
Никотиновый синдром плода.Табакокурение женщины во время беременности так же, как и употребление алкоголя, оказывает самое пагубное воздействие на развитие плода. Известно, что никотин тормозит маточно-плацентарное кровообращение, приводя к кислородному голоданию мозга.
Наркотический синдром плода.Наркотические вещества и прочие одурманивающие средства, употребляемые будущей матерью во время беременности, оказывают вредное токсическое влияние на организм плода. Так, после рождения у ребенка выявляются различные аномалии развития, задержка психомоторного развития с формированием тяжелой либо глубокой умственной отсталости.
Дата добавления: 2018-02-15 ; просмотров: 367 ;
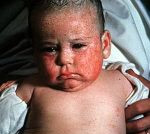
Врожденный токсоплазмоз – это паразитарная патология, которая возникает при трансплацентарном инфицировании ребенка Toxoplasma gondii. У большинства детей протекает бессимптомно. Возможные проявления заболевания: интоксикационный синдром, пятнисто-папулезная сыпь, лимфаденопатия, желтуха, гепатоспленомегалия, отеки нижних конечностей. Часто провоцирует развитие патологий органа зрения, слуха, ЦНС; реже – миокарда, легких и печени. Антенатальная диагностика базируется на проведении биопсии, постнатальная – на совокупности анамнестических и клинико-лабораторных данных (ИФА, ПЦР). Этиотропное лечение врожденного токсоплазмоза проводится при помощи схем на основе препаратов пириметамина и сульфадимезина или спирамицина.
МКБ-10
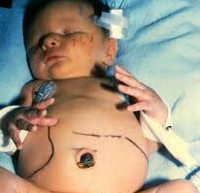
Общие сведения
Врожденный токсоплазмоз – заболевание в педиатрии и неонатологии, возникающее в результате трансплацентарного заражения плода на фоне острой формы токсоплазменной инфекции у матери. Впервые Toxoplasma gondii была описана французами К. Николь и Л. Монсо в 1908 году. В 1939 г. американцы Э. Вольф, Д. Кауэн и Б. Пэйдж подтвердили трансплацентарный механизм передачи возбудителя. Промежуточными хозяевами могут выступать более 400 видов животных. Согласно статистическим данным ВОЗ, число инфицированных токсоплазмой людей в мире составляет порядка 1,5 млрд. человек, в России – около 30% всего населения. Частота врожденной формы 1,5:1000 новорожденных. Даже на фоне лечения средний показатель смертности у детей до 5 лет составляет 12%, осложнения возникают почти у 90%.

Причины врожденного токсоплазмоза
Врожденный токсоплазмоз развивается только при инфицировании матери Toxoplasma gondii во время вынашивания ребенка. Механизм заражения беременной женщины – фекально-оральный. Наиболее распространенные причины: контакт с животными из семейства кошачьих и употребление термически необработанной пищи. Инвазивная форма возбудителя – ооциста – формируется в кишечнике животных и выделяется с калом, после чего может на протяжении 12 и больше месяцев сохранять контагиозность в условиях внешней среды. В крайне редких случаях этиологическим фактором может стать трансплантация контаминированных органов или переливание крови. Заражение плода T. gondii происходит трансплацентарным путем. После рождения ребенка развивается интенсивный гемолиз, возникают геморрагии на слизистых оболочках, расширение камер сердца, пневмония или интерстициальный отек легких, некроз печени и селезенки, увеличение лимфоузлов, воспаление и отек тканей головного мозга, некробиоз сетчатки. При гистологическом исследовании непосредственно пораженных тканей определяется некроз, гранулематозная или диффузная пролиферация ретикулоцитов, инфильтрация плазмоцитами и лимфоцитами, перифокально – множество токсоплазм. Впоследствии на месте некротизированных участков формируется фиброз, переходящий в кальциноз.
В зависимости от периода инфицирования плода врожденный токсоплазмоз может протекать в трех формах:
- Хроническая форма. Заражение происходит в I-II триместрах беременности. Риск передачи возбудителя – 13-18%. При такой форме могут развиваться атрофия головного мозга, гидроцефалия, деформация желудочков мозга, анофтальмия, колобома, атрофия сетчатки, врожденные пороки сердца и других органов и систем.
- Подострая форма. Инфицирование – III триместр. Риск заражения ребенка – 75-85%. Проявления могут включать в себя энцефалит, менингоэнцефалит, очаговый некроз сетчатки, увеит.
- Острая форма. Токсоплазма попадает в организм ребенка непосредственно перед родами. Возможные симптомы: гипертермия, пятнисто-папулезная сыпь, интенсивная желтуха, гепатоспленомегалия, анемия, миокардит, пневмония.
Симптомы врожденного токсоплазмоза
Врожденный токсоплазмоз может проявляться в различные периоды жизни ребенка – от первых дней до нескольких месяцев. Специфических симптомов данное заболевание не имеет. Зачастую присутствующая клиника нечеткая и имитирует другие врожденные патологии. Наиболее вероятные проявления врожденного токсоплазмоза: ухудшение общего состояния, пятнисто-папулезная сыпь различной локализации, генерализованная лимфаденопатия, увеличение печени и селезенки, желтуха, отеки нижних конечностей, субфебрильное повышение температуры тела. Тяжесть симптомов зависит от степени инфицирования токсоплазмами, триместра беременности, в котором произошло инфицирование, и иммунных сил матери. Примерно 70-90% детей не имеют каких-либо проявлений в ранние периоды жизни, но почти у всех спустя некоторое время возникают осложнения. Классический врожденный токсоплазмоз проявляется триадой Сэбина – обструктивная гидроцефалия, хориоретинит и массивное внутричерепное обызвествление. Наблюдается данный комплекс не более чем у 3% детей. Помимо триады, часто возникают миокардит, миозит, гепатит и пневмония. Клинические проявления напрямую зависят от присутствующих патологических изменений. Вероятность развития поздних осложнений на фоне латентного врожденного токсоплазмоза составляет порядка 90%. Период возникновения может быть разным – от нескольких месяцев до нескольких лет. Наиболее часто наблюдается поражение глаз, органа слуха и ЦНС. Самое распространенное осложнение – ретинит (примерно 85% случаев). К другим последствиям перенесенного врожденного токсоплазмоза относят олигофрению, гидроцефалию, повышение внутричерепного давления, острый и хронический энцефалит, эпилепсию, полную глухоту и/или слепоту, микрофтальм, увеит, хроническую гипертермию, редко – шизофрению.
Диагностика врожденного токсоплазмоза
Диагностика врожденного токсоплазмоза может проводиться в антенатальном и постнатальном периоде. Антенатальное исследование подразумевает использование инвазивных методов с дальнейшими лабораторными анализами. Абсолютное показание к их проведению – острый токсоплазмоз матери в сумме с нарушениями развития плода по результатам акушерского УЗИ. Выбор методики исследования зависит от срока беременности. При гестации от 10 недель проводится биопсия хориона, от 16 недель – амниоцентез, от 18 – кордоцентез. Для верификации инфекции полученный материал исследуют при помощи ПЦР. Постнатальная диагностика включает в себя сбор анамнестических данных и проведение клинического и лабораторного исследования. Данная мера является обязательной для всех детей, входящих в группу риска внутриутробного инфицирования. Неспецифическая диагностика и ее результаты зависят от присутствующих симптомов и синдромов. Список исследований может включать в себя ОАК (анемия, тромбоцитопения, лейкоцитоз); рентгенографию ОГК (признаки инфильтрации легких); нейросонографию и КТ головного мозга; биохимическое исследование крови с измерением АЛТ и АСТ, определением СРБ, уровня билирубина и его фракций (все показатели выше нормы); офтальмоскопию (некроз сетчатки); спинномозговую пункцию (признаки воспаления). Специфические методы подразумевают серодиагностику биологических жидкостей методом ИФА, при котором наблюдается возрастание титра антител IgG в 4 и больше раз и высокий уровень IgM на протяжении 10-14 суток. При необходимости проводится ПЦР с целью идентификации ДНК токсоплазмы.
Лечение врожденного токсоплазмоза
Лечение новорожденного с выраженной клинической картиной врожденного токсоплазмоза проводится только в условиях стационара, в отделении патологии новорожденных. Соблюдение специфического режима и рациона не требуется, их коррекция проводится в соответствии с состоянием ребенка. При наличии отягощенного анамнеза матери этиотропную терапию начинают с момента постановки предварительного диагноза. В других случаях перед началом лечения требуется проведения лабораторных методов исследования. Используемые схемы: пириметамин и сульфадимезин на 1-1,5 месяца; спирамицин или другие макролиды на 4-6 недель. В некоторых случаях применяют системные глюкокортикостероиды – преднизолон. Симптоматическое лечение зависит от присутствующих симптомов и синдромов, выявленных педиатром или неонатологом. При стойком повышении внутричерепного давления или развитии гидроцефалии показано хирургическое лечение. При необходимости дальнейшее лечение может проводиться амбулаторно под контролем педиатра, инфекциониста и других специалистов. В таких же условиях проводится терапия субклинической и латентной формы врожденного токсоплазмоза. Решение об отказе от приема препаратов принимается на основе клинико-лабораторных показателей, находящихся в пределах возрастной нормы, и заключения всех лечащих врачей.
Прогноз и профилактика врожденного токсоплазмоза
Прогноз при врожденном токсоплазмозе зависит от триместра, в котором произошло инфицирование плода и тяжести клинических проявлений. При развитии патологии в I триместре может наблюдаться самопроизвольное прерывание беременности и выкидыш или дальнейшее развитие тяжелых форм заболевания, однако аномалии органов при этом не возникают. При адекватной и своевременной терапии прогноз для жизни благоприятный, для выздоровления – сомнительный. Неспецифическая профилактика врожденного токсоплазмоза включает в себя ограничение контакта домашних животных с беременной женщиной, соблюдение гигиенических норм, прием в пищу только термически обработанных продуктов, тщательное мытье овощей и фруктов. При наличии факторов, указывающих на возможное инфицирование матери, проводится специфическая диагностика, направленная на идентификацию T. gondii. При подтверждении диагноза показано немедленное проведение этиотропной терапии. Специфической профилактики врожденного токсоплазмоза не разработано.
Читайте также:


