Отравление красной кровяной солью

| Калий железосинеродистый) | |
|---|---|
 | |
 |
наименование
красное синькали
Гексацианоферрат (III) калия (железосинеродистый калий, феррицианид калия, гексацианоферриат калия, Гмелина соль, красная кровяная соль) — комплексное соединение трёхвалентного железа K3[Fe(CN)6].
Содержание
- 1 История и происхождение названия
- 2 Свойства
- 3 Токсичность
- 4 Получение
- 5 Применение
- 6 Мнемонические правила

История и происхождение названия
Свойства
Тёмно-красные кристаллы с моноклинной решеткой. Водный раствор зеленовато-жёлтого цвета.
В этаноле нерастворим.
Гексацианоферрат(III) калия — очень сильный окислитель, особенно в щелочной среде. Окисляет H2S до S, HI до I2, PbO до PbO2, NH3 до N2 и солей аммония, W до WO4 2− :
На свету происходят следующие обратимые реакции:
С солями Fe 2+ образует темно-синий осадок турнбулевой сини. Уравнение реакции в ионной форме:
С концентрированной серной кислотой реагирует, давая Fe(HSO4)2, KHSO4, NH4HSO4 и CO.
Реагирует с перекисью бария (эта реакция может использоваться для количественного определения BaO2):
В отличие от гексацианоферрата(II) калия, гексацианоферрат(III) калия ядовит.
При взаимодействии с кислотами выделяет весьма токсичный цианистый водород:
K3[Fe(CN)6] + 6HCl → 3KCl + FeCl3 + 6HCN↑
Интересно то, что из гексацианоферрата(III) калия можно получить гексацианоферрат(II) калия с помощью перекиси водорода в щелочной среде:
Однако в нейтральной среде эта реакция протекает в обратную сторону.
Токсичность
Это вещество может раздражать глаза и кожу, ядовит. В очень кислой среде может выделяться циановодород:
6HCl + K3[Fe(CN)6] → 6HCN + FeCl3 + 3KCl 
Получение
Получают гексацианоферрат(III) калия окислением гексацианоферрата(II) калия K4[Fe(CN)6] хлором в солянокислой среде, бромом или другими сильными окислителями, например, перманганатом калия.
Применение
Компонент тонирующих, отбеливающих, усиливающих, ослабляющих растворов в фотографии, электролит в хемотронных приборах, компонент электролитов в гальванопластике, реагент для обнаружения Fe 2+ (см. выше), Li + , Sn 2+ , а также в качестве сильного окислителя.
В почвоведении используют для качественного определения оглеения (солей двухвалентного железа). Химическая реакция описана выше.
Мнемонические правила
Для того, чтобы запомнить формулу красной кровяной соли K3[Fe(CN)6] и не перепутать её с формулой желтой кровяной соли K4[Fe(CN)6], существует несколько мнемонических правил:
[Fe(CN)6] 4–
аммония • бария • железа(II) • железа(III) • калия • кальция • кобальта • магния • марганца • меди(II) • натрия • никеля • олова • свинца • стронция • таллия • цинка • Железистосинеродистая кислота H4[Fe(CN)6]
[Fe(CN)6] 3–
железа(II) • железа(II,III) • калия • кальция • кобальта • меди(I) • натрия • неодима(III) • олова • свинца • Железосинеродистая кислота H3[Fe(CN)6]
Снова о цианидах.
Писали мы о них, и не раз. А потом опять - раскроешь детектив или включишь телевизор и с горечью видишь, как законы химии уступают место законам жанра. Похоже, бесполезно призывать нынешних Чейзов и Конан Дойлов купить себе школьные учебники. Необходимо популярное, понятное руководство по химии веществ, наиболее часто применяемых злодеями против жертв. Так сказать, сборник ляпов с комментариями.
Сразу предупреждаем: здесь вы не найдете информации о том, как синтезировать или где раздобыть цианиды. Читателям и сочинителям детективов это не особенно интересно, а злодеям помогать мы не намерены.
О безвредных цианидах
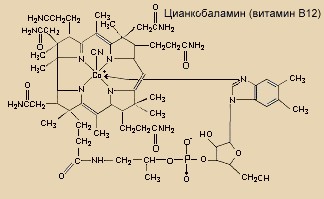
Для начала определимся с термино логией. Цианиды - собирательное название некоторых классов химических соединений, как органических, так и неорганических. Все они содержат цианогруппу, -С N. Таким образом, неорганические цианиды можно рассматривать как производные циана (CN)2 или соли цианистоводородной кислоты HCN. Органические цианиды часто носят название нитрилов, считаясь производными соответствующих органических кислот (к примеру, метилцианид, он же ацетонитрил CH3CN - нитрил уксусной кислоты). Бывают и более сложные органические вещества, содержащие цианогруппу, - например, витамин В12.
Из последнего примера понятно, что не все цианиды - яды. Само по себе наличие цианогруппы в молекуле вещества еще не смертельно. Ядовитым будет лишь такое вещество, которое содержит реакционноспособную цианогруппу. Обычно она связана с молекулой не особенно прочно. Это может быть ионная связь или ковалентная (но не углерод-углеродная). Такая цианогруппа в определенных условиях высвобождается и вмешивается в биохимические процессы, протекающие в организме.
Среди широко распространенных цианидов сравнительно немного настоящих ядов. (Но, как правило, цианидами называют именно их.) Это растворимые цианиды щелочных металлов (калия и натрия), свободный цианистый водород (синильная кислота), дициан, галоидоцианы и некоторые другие производные. А вот известные своей светостойкостью синие краски "берлинская лазурь" и "турнбулева синь", представляющие собой цианидные комплексы железа, абсолютно безвредны.
Почему умер Шееле, а Пуаро остался в живых
Один из распространенных мифов: цианиды убивают потому, что связывают железо, содержащееся в гемоглобине крови, и таким образом лишают ее способности переносить кислород. На самом деле отравляющее действие цианидов основано на том, что они блокируют ферменты тканевого дыхания. Кровь человека, отравленного цианидами, даже венозная, как раз насыщена кислородом до предела и имеет характерный ярко-алый цвет. Но ткани теряют способность усваивать кислород, переносимый кровью, и организм задыхается.
Безвредные
Fe3[Fe(CN)6]2
Ядовитые
Красная кровяная соль
K3[Fe(CN)6]
Na2[Fe(CN)5NO]
Смертельно ядовитые
Некоторые циансодержащие соединения, ядовитые и безвредные
При введении яда непосредственно в кровь или вдыхании газообразных цианидов в больших концентрациях человек может погибнуть в течение нескольких секунд. Малые же концентрации цианидов нейтрализуются определенными защитными механизмами. Впрочем, об этом чуть позже. А теперь рассмотрим подробнее вещества, о которых пойдет речь.
Цианистый водород (синильная кислота), HCN - это бесцветный газ или жидкость (температура кипения +26 o C), хорошо смешивается с водой, спиртом, эфиром. Крайне летуч, крайне ядовит при попадании на кожу, внутрь, в дыхательные пути.
С цианистым водородом в истории химии связан еще один миф: якобы первооткрыватель его, Карл Вильгельм Шееле, погиб в момент открытия. Это, так сказать, полуправда. На самом деле Шееле впервые получил синильную кислоту из желтой кровяной соли в 1782 году, а умер в 1786 году, в возрасте 44 лет. Однако не подлежит сомнению, что Шееле погубили органолептические методы исследования. В XVIII веке было принято пробовать на вкус продукты реакции, а Шееле, помимо цианидов, работал с соединениями ртути и мышьяка.
Чтобы отравить человека, обычно требуется 50 - 60 мг синильной кислоты (других веществ - в пересчете на цианогруппу). В общем, один хороший вдох или щепотка порошка.
Подходящие порошки - это цианистый натрий NaCN и цианистый калий KCN. То и другое - белые кристаллы, хорошо растворимые в воде и спирте (в рюмочке коньяка dosa letalis вполне поместится), гигроскопичны, на воздухе расплываются (особенно цианистый калий). Поскольку синильная кислота слабее угольной, они легко разрушаются углекислым газом, содержащимся в воздухе, с выделением синильной кислоты, поэтому сильно ядовиты не только при приеме внутрь, но также при попадании на кожу или вдыхании паров раствора.
Обо всем этом сочинители детективов часто забывают. Даже Агата Кристи, дама безусловно сведущая в фармакологии. В ее рассказе "Гнездо ос" человек пытается инсценировать собственное убийство (он смертельно болен и, кроме того, желает навлечь обвинение на любовника невесты). Он носит в кармане, в обычном бумажном пакетике, цианистый калий, чтобы подсыпать его себе в чашку. Великий же сыщик Эркюль Пуаро вынимает у него из кармана цианид и подменяет содой. Если бы все происходило на самом деле, очень возможно, что до развязки не дожили бы ни преступник, ни сыщик. По крайней мере, дурноту почувствовали бы оба.
Из галоид цианов наиболее известен хлорциан CICN - бесцветный газ или жидкость (температура кипения +12 о C), растворимый в воде, спирте, эфире. Он чрезвычайно ядовит, по токсичности превосходит цианистый водород. Хлорциан применяют как отравляющее вещество боевого и хозяйственного назначения (именно им уничтожают хвостатых бедолаг-бомжей - отловленных бродячих животных).
Цианиды с солью и сахаром
Но вернемся в светскую, мирную обстановку. Герой подносит бокал к губам и, разумеется, ощущает запах горького миндаля. Опять вранье, точнее, живучий миф. А возник он вот почему. В горьком миндале (как, впрочем, и во многих других косточковых) содержится гликозид амигдалин, который при разрушении зерен расщепляется с образованием глюкозы, синильной кислоты и бензальдегида. Последний и является носителем специфического запаха. Сама синильная кислота пахнет совсем по другому и намного слабее.
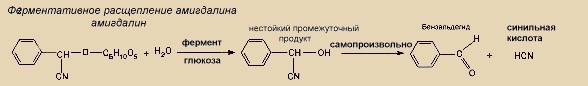
Кстати, отравиться косточками (например, абрикосовыми) действительно можно. Но потребуется их много - что-то около двухсот штук на прием. А поскольку съедают обычно по одной - по мере раскалывания скорлупы - то любители орешков чаще всего отделываются дурнотой и головокружением. Есть и другой путь к бытовому отравлению синильной кислотой из амигдалина и прочей цианосодержащей органики - побыть в одном помещении с большим черемуховым букетом. Если окна закрыты, головная боль гарантирована.
Миф о запахе горького миндаля укоренился настолько прочно, что захватил даже химфак МГУ. Когда я там учился, один шутник из моей группы пугал слабонервных девушек, публично глотая "цианистый калий", сделанный из поваренной соли с маленькой добавкой бензальдегида. Горьким миндалем эта смесь благоухала вовсю, девушки были в шоке.
А после разоблачения этот артист демонстрировал уже мне проглатывание небольших количеств настоящего цианистого калия, насыпанного на увлажненный кусочек сахара. Головной болью потом он мучился. Причем тут сахар, мы расскажем чуть позже.
Так ли страшен цианистый калий?
Стало быть, унюхать цианистый калий герою не удалось. Ну хоть какой-то способ узнать, что ему подсыпали, есть?
В лаборатории синильную кислоту можно определить по ее способности образовывать прочные комплексы с железом, окрашенные в темно-синий цвет (отсюда и ее название). Соответственно реактив для выявления цианида - подкисленный раствор железного купороса (или любой другой соли двухвалентного железа). Но, увы, отраву в чае или коньяке таким способом не опреде лить: с дубильными веществами железо дает интенсивное черное окрашивание.
В сущности, если принята смертельная доза, не будет ни сомнений, ни времени на анализы - удушье, потеря сознания и мгновенная смерть. При меньших дозах наблюдаются все симптомы нехватки кислорода, сильная головная боль, возможна опять-таки потеря сознания.
Однако шансы на спасение у жертвы, как ни странно, неплохие. Если, конечно, герои детектива хоть немного разбираются в химии.
Цианидные отравления (когда речь идет о крохотных дозах) относятся к числу наиболее легко излечимых и создающих минимальное количество осложнений. Лечение основано, как правило, на непосредственном связывании цианидов, попавших в кровь, в нетоксичные соединения. (Разумеется, эффективность антидотов достаточно велика только в первые минуты после отравления.)
Противоцианидные антидоты глотают или вводят внутривенно. Их можно разделить на три основных класса. Первый - сахара (прежде всего глюкоза), необратимо связывающие цианиды в нетоксичные циангидрины. Кстати, этот антидот всегда присутствует в нашей крови, благодаря чему небольшие концентрации цианидов человек может выдерживать некоторое время. Вот почему химикам, работающим с цианидами, рекомендуют держать под языком кусочек сахара или леденец. Это, конечно, только дополнение к обычным средствам безопасности: перчаткам, тяге, защитной маске. К цианидам более устойчивы диабетики, поскольку уровень сахара в их крови выше. Вот, пожалуй, единственная польза, которую человек может получить от гипергликемии. По той же причине, кстати, цианиды менее опасны для птиц, чем для других теплокровных.
Другой антидот, тиосульфат натрия, реагирует с цианидами, превращая их в роданиды, которые так же безвредны. Но особенно интересна третья группа антидотов - вещества, превращающие гемоглобин крови в метгемоглобин. Он не способен переносить кислород, но зато быстро связывает цианиды с образованием цианметгемоглобина, который впоследствии выводится из организма. К этой группе относятся некоторые красители (например, метиленовый синий), органические и неорганические нитриты.
Метгемоглобинобразователи наиболее эффективны из всех антидотов, так как действуют быстрее других, но в то же время они и опасны сами по себе. Как легко догадаться, при их передозировке кровь потеряет способность переносить кислород (то есть произойдет именно то, в чем несправедливо обвиняют цианиды). Кроме того, реакция образования цианметгемоглобина обратима, и со временем часть цианида будет высвобождаться обратно. Поэтому антидоты этой группы применяют обычно в сочетании с антидотами других групп.
В любом случае, если герой подозревает, что его хотят отравить, пусть держит под рукой аптечку с раствором глюкозы и парой ампул амилнитрита, в крайнем случае сойдет и нитроглицерин. (И то и другое - сильные и быстродействующие метгемоглобинобразователи.)
Опять о Распутине
Еще один миф, связанный с цианидами: если злодей переусердствовал и всыпал в чашку много больше смертельной дозы, именно переизбыток и спасает жертву от отравления. Пошел этот миф, вероятно, от того, что из растворов цианистого калия на воздухе выделяется газообразная синильная кислота. Если раствор концентрированный и синильной кислоты много, при вдыхании ее быстро наступает отравление, сопровождающееся потерей сознания. Так что употребитель отравы может просто не успеть ее выпить.
Но все это не имеет ни малейшего отношения к случаю с неудачным отравлением Григория Распутина в 1916 году. Чего только не писали об этой реальной, но тем не менее вполне детективной истории! Высказывалось предположение, что причиной неудачи была именно передозировка цианида. Однако случай явно не тот: отравленное угощение Распутин, по свидетельству очевидцев, съел, а плохо ему стало уже потом. Но почему-то мало кто вспоминает, что травили Распутина не просто цианистым калием, а цианистым калием, подмешанным в кремовые пирожные и портвейн. Иначе говоря, давали ему яд вместе с антидотом, и цианид незамедлительно инактивировался, вступив в реакцию с сахаром. Видимо, в тогдашнем высшем свете химия, в отличие от французского языка или верховой езды, не считалась обязательным элементом образования, так что в итоге пришлось воспользоваться пистолетом.
Напоследок просьба к любителям детективов: если когда-нибудь встретите в любимом жанре хорошие химические ляпы, не забудьте поделиться радостью с "Химией и жизнью". Долой необразованность в рядах писателей!

Поваренная соль — составная часть рациона всех видов животных. У свиней в дозе 0,2-0,5г на 1 кг веса она улучшает аппетит и усвоение поступивших в организм питательных веществ. Но если давать ее в чрезмерно больших дозах или по доведенных до животных нормах после длительного солевого голодания, то у всех видов животных, особенно у свиней и птицы, появляется солевое отравление. Среди пушных зверей к отравлению поваренной солью наиболее чувствительны норки, соболи; несколько слабее реагируют на поваренную соль песцы, лисицы и еноты .
Этиология. В некоторых ЛПХ, КФХ да иногда и сельхозпредприятиях животные страдают хроническим солевым голоданием, в результате неправильного использования поваренной соли, когда ее кладут в кормушки или оставляют на выгульных двориках в виде лизунцов, а также когда владельцы не додают в рационы положенной нормы поваренной соли.
Владельцам животных необходимо знать, что смертельными дозами поваренной соли являются: для крупного рогатого скота 1,5-3кг, для лошадей 1-1,5кг, для овец и свиней 125-250г, для собак 30-60г на голову, для зверей 3-4г на 1 кг веса и для средних по весу кур 4,5г. В тоже время, если в рационе подсвинков содержится недостаточное количество минеральных веществ, то отравление и гибель поросят происходит при дозе соли 0,5-2г на 1кг веса, а жеребят – при 1,5 -2,5г. И наоборот, при достаточно высоком обеспечении подсвинков минеральными веществами подсвинки погибали при дозе соли 9-13г, а жеребята – 6г на 1 кг веса.
У животных солевое отравление наступает при использовании крупных кусков кристаллической соли, плохо растворенных в воде, а у свиней, при скармливание соленой рыбы, соленых огурцов и помидор, отходов столовых, кафе и ресторанов, при скармливании селедочных и мясных рассолов. При скармливании рассолов отравление наступает не только в результате содержания в них высокой концентрации соли, но также из-за наличия токсических продуктов распада белков (птоманны) корма.
Патогенез. Механизм действия поваренной соли на организм животного сводится к резкому нарушению ионного состава крови. Происходит преобладание одновалентных катионов (Na,К) над двухвалентными (Са,Mg) вызывает перевозбуждение нервной системы. В этом отношение действие двухвалентных и одновалентных ионов напоминает собой действие медиаторов (ацетилхолина и адреналина).
При смертельном отравлении свиней содержание натрия в крови у них увеличивается в 1,5-2раза, а в эритроцитах – в 3-5раз (до 150-280мг%); концентрация хлора в плазме и эритроцитах бывает в 1,5-2 раза больше. Во всех органах происходит накопление натрия и хлора. Гемоглобин во время переноса кислорода из легких к тканям находится в соединение с калием. В случае отравления поваренной солью избыточный натрий, заменяет в гемоглобине калий, что влечет за собой нарушение функции гемоглобина в организме, на почве чего развивается кислородное голодание тканей, к нарушению обмена веществ, отеку легких и смерти отравившегося животного от асфиксии.
Клиническая картина. Симптомы острого отравления наступают у животных вскоре после приема корма и сопровождаются:
У свиней симптомы отравления поваренной солью появляется обычно через 12-24часа и характеризуется жаждой, саливацией, учащением дыхания и мышечной дрожью. Повышается температура тела. Во время возбуждения отравившиеся свиньи совершают манежные движения, натыкаются на препятствия. При клиническом осмотре ветеринарный специалист отмечает расширение зрачков, зрение ослаблено или полностью потеряно, нарушена координация движений, наблюдает покраснение или посинение кожи. В течение 3-5 минут тетанические и клонические судороги у животного сменяются угнетением. В результате пареза глотки свиньи отказываются от корма и питья. У отравившихся животных возможна рвота, изо рта выделяется много слюны. Наблюдается понос, иногда в каловых массах находим кровь. Сердечная деятельность ослаблена, пульс слабый, частый, дыхание напряженное. Отравившиеся животные принимают позу сидячей собаки. Смерти животных предшествует их коматозное состояние. При не смертельном отравлении животные выздоравливают в течение нескольких дней.
У крупного рогатого скота отравление поваренной солью протекает в форме гастроэнтерита с усиленной жаждой, рвотой и поносом. В случаях отравления селедочным рассолом к этим симптомам присоединяются скрежетание зубами и тризм жевательных мышц. Стельные коровы абортируют. После нормального отела или аборта у коровы может выпасть матка.
У овец отравление поваренной солью сопровождается сильной жаждой. При клиническом осмотре ветеринарный специалист регистрирует красноту и сухость слизистой оболочки ротовой полости, колики, понос, иногда полиурию. Смерть овец наступает от асфиксии в результате отека легких.
У зверей отравление поваренной солью характеризуется острым гастроэнтеритом, рвотой, поносом. Часто у отравившихся животных возникают эпилептические припадки, во время которых владельцы отмечают сильное слюнотечение. Звери визжат. Температура тела нормальная или ниже нормы.
Птицы при солевом отравлении часто пьют, становятся малоподвижными, вялыми и сидят с опущенными крыльями. При клиническом осмотре отравившейся птицы ветеринарный специалист регистрирует у них понос, судороги, поражение вестибулярного аппарата, которое клинически проявляется перекручиванием шеи, параличом крыльев и ног. Отравившиеся поваренной солью куры почти все время сидят неподвижно на одном месте, безучастны к окружающему, перья у них взъерошены.
Течение болезни, как правило, острое.
Патологоанатомические изменения. При вскрытии павших животных обнаруживаются множественные точечные кровоизлияния, очаговые отеки, некротические изменения тканей. Особенно резко эти изменения выражены в слизистой желудочно-кишечного тракта. Лимфатические узлы увеличены, сочные, иногда геморрагичны. Почки увеличены в объеме, темно-красного цвета, капсула снимается с трудом, граница между корковым и мозговыми слоями не выражена, имеются кровоизлияния. Селезенка и печень увеличены, темно-красные. Легкие увеличены, с явлениями застойной гиперемии и отека. Под эпикардом и эндокардом множественные точечные кровоизлияния, сердечная мышца дряблая. Мочевой пузырь переполнен мочой, его слизистая оболочка гиперемирована. Сосуды оболочки мозга резко инъецированы. Вещество мозга отечное. Кровь светло-красная, не свернувшаяся. У жвачных особенно сильные изменения обнаруживаются в сычуге: слизистая оболочка утолщена, покрасневшая, с множественными кровоизлияниями. У птиц при вскрытии находим признаки острого воспаления пищеварительного тракта, начиная с зоба. Скелетная мускулатура бледная.
Диагноз на отравление животных поваренной солью ставят на основании данных анамнеза, клинической картины отравления, результатов патологоанатомического вскрытия, химико-токсикологического исследования кормов и содержимого желудочно- кишечного тракта.
Дифференциальный диагноз. При проведении дифференциальной диагностики ветеринарный врач должен исключит болезнь Ауески, отравление хлопчатниковым жмыхом, картофелем, гастроэнтериты незаразного, инфекционного и инвазионного происхождения.
Лечение. С целью предупреждения нарушения водного обмена и обезвоживания организма больным животным дают или вводят через зонд и в виде клизм обильное количество воды. Свиньям назначают 5-10%-ный раствор кальция хлорида(1мг/кг массы животного). Внутривенно вводят 40% раствор глюкозы. При отравление хороший лечебный эффект у свиней получают от внутримышечного введения глюконата кальция в дозе 20-30мл.
Жвачным животным внутривенно вводят 10% -ный раствор хлорида кальция: коровам -200мл, овцам 40-50мл. Одновременно с применением кальция, внутривенно вводят 40%-ный раствор глюкозы с кофеином. В дальнейшем отравившимся животным назначают слизистые отвары, легко усвояемые питательные корма.
Профилактика солевых отравлений у животных заключается в том, чтобы владельцы ЛПХ, КФХ и сельхозпредприятий организовали правильное минеральное кормление своих животных. Большое значение имеет содержание в рационе свиней достаточного количества поваренной соли, фосфорных и кальциевых солей (трикальций фосфат, мясо-костная мука и т.д.), витаминов (рыбий жир, морковь, сенная мука, зеленая трава, пророщенный овес). Если свиньи длительное время не получали поваренную соль, то ее первое скармливание начинают с малых доз; так, поросятам – отъемышам ее дают в количестве не более 3-5г на голову в сутки. К соли или солевому корму обязательно примешивают мел или трикальцийфосфат. Скармливать комбикорма, содержащие поваренную соль, необходимо только по назначению. Отходы производства пищевой промышленности, содержащие большое количество соли (рассол и др.), в пищу свиньям не допускаются. Среди обслуживающего персонала необходимо проводить разъяснительную работу о недопустимости скармливания кухонных отходов с большим содержанием поваренной соли.
Зверям нельзя скармливать большое количество соленого мяса. Если другого корма для зверей нет, то соленое мясо следует вымачивать 2-3 суток, меняя за этот срок воду 6-7раз. Проварка мяса позволяет снизить содержание соли в мясе до 2%. Проваренное мясо можно давать из такого расчета, чтобы соли было не больше 5г для лисицы, 2 г для песца и 0,5г для норки. В питьевой воде для кур содержание хлоридов не должно превышать 0,4%, для цыплят – 0,2%.
Попадая через дыхательные пути, они вызывают в крови различные изменения. В одних случаях основным патологическим моментом является переход гемоглобина крови в карбоксигемоглобин. В других - происходят быстрый гемолиз эритроцитов и образование метгемоглобина. Наконец, при некоторых отравлениях происходит образование циангемоглобина. К этой группе, прежде всего, относятся следующие газы: угарный, светильный, водяной, генераторный.
При легком отравлении головная боль, головокружение, общая слабость, тошнота, рвота, угнетение сознания.
Лицо у пострадавшего багрового цвета, в тяжелых случаях отравления кожа пепельно-серая, наблюдаются одышка, сердцебиение, коматозное состояние.
Лечение : в легких случаях ингаляция кислорода, углекислоты с кислородом. Искусственное дыхание. Лобелии по 0,5, камфора, кофеин. Холодное обливание и растирание конечностей. В тяжелых случаях обильное кровопускание - 250-500 мл (венозная кровь ярко-красного цвета). Последующее переливание крови. Можно после кровопускания физиологический раствор в вену. При явлениях возбуждения подкожно 0,0005 бромисто-водородного скополамина. В случае наступления отека легких хлористый кальций внутривенно. Некоторые авторы предлагают терапию тионином. Тионин заменяет дыхательный фермент клеток. Применяется он в виде катализина (0,5% раствор тионина внутривенно по 10 мл).
Отравления, при которых основным патологическим началом является гемолиз эритроцитов, могут вызываться мышьяковистым водородом при изготовлении анилиновых красок, при гальванизации, извлечении и обжигании минеральных руд, наиболее часто при обработке цинка, жести и железа серной или соляной кислотами.
Вдыхаемый мышьяковистый водород через легочные альвеолы попадает в капилляры и разносится по всему кровяному руслу. При попадании в кровь он сразу же проявляет свое гемолитическое действие. Отравление сказывается головной болью, головокружениями, общей слабостью. Появляются повторная рвота желчью, боли в области почек. Через несколько часов обнаруживается кровавая моча (растворенный в плазме крови гемоглобин выводится почками), содержащая гемоглобин, но не красные кровяные тельца (гемоглобинурия). Количество уробилина, уробилиногена в моче значительно увеличено. Возникает возможность и опасность анурии. Уже через несколько часов после отравления появляются резкая желтушная окраска склер, слизистых и кожи, характерный чесночный запах изо рта. Помимо почек гемоглобин выделяется еще и печенью в виде желчных пигментов. Желчный пузырь растянут и болезнен.
Общее самочувствие зависит от тяжести отравления и от состояния нервной системы. В тяжелых случаях отравление проходит с помутнением сознания, гиперестезиями. Иногда возникают схваткообразные боли в животе, болезненность в области печени.
Лечение : в первую очередь постельное содержание даже в легких случаях. Если пульс хорошего наполнения, делают массивное кровопускание. Вдыхание кислорода. Введение глюкозы внутривенно, подкожно и в капельных клизмах. Диатермия области почек.
К ядам, вызывающим образование в крови метгемоглобина, относятся пары анилина, нитробензола и т. п. Метгемоглобин отличается от гемоглобина тем, что прочно соединен с кислородом и не отдает его тканям, в результате чего наступает кислородное голодание, удушение клеток, аноксия. Отравление парами анилина на наших производствах вряд ли возможно. Строгое соблюдение правил техники безопасности устраняет причины, которые могли бы вести к накоплению токсических концентраций паров анилина.
Отравления при всасывании анилина через кожу - редкие случаи.
Симптомы отравления: вначале жалобы на головную боль, головокружение. Далее может наступить бессознательное состояние. Дыхание резко поверхностное. Кожа и слизистые серо-синего цвета. Кровь темно-коричневая, очень вязкая.
Лечение : венепункция для выпускания 300 - 400 мл крови. Это сразу уменьшает вязкость крови и улучшает кровообращение. Введение глюкозы под кожу. Средства, возбуждающие кровообращение и дыхание. Рекомендуют внутривенное вливание 50-100 г 1% раствора метиленовой сини.
К отравлениям, вызывающим образование циан-гемоглобина, относятся обусловленные цианистым калием, другими соединениями, водой горьких миндалей, амигдалином, лавровишневой водой. При всех этих отравлениях происходит удушение клеток, так как циан вступает в соединение с дыхательным ферментом клеток.
Картина отравления следующая: слизистые оболочки ярко красного цвета. Быстро нарастающая одышка. Рвота и потеря сознания, жжение языка, слюнотечение. Зрачки обычно расширены. Изо рта запах миндаля. Могут наступать клонические и топические судороги, коматозное состояние, паралич дыхания. До этого дыхание затрудненное, судорожное, замедленное.
Лечение : искусственное дыхание (лучше вне помещения). Вдыхание кислорода с 5% углекислотой, амилнитрита. Затем внутривенно 10-20 мл 2% раствора азотнокислого натрия или столько же 1% раствора метиленовой сини в 1,8% растворе сернокислого натрия (но не в физиологическом растворе!). После этого в вену 10-20% раствор тиосульфата натрия или под кожу 100-200 мл 3-5% раствора для образования неядовитого роданистого натрия.
Внутривенно 10% глюкоза - от 100 до 300 мл. При венозном застое кровопускание (300-500 мл) с последующим введением в вену физиологического раствора. Под кожу кофеин, лобелии, камфора. Холодные обливания затылка в теплой ванне, холод на голову. Давать нюхать нашатырный спирт либо внутрь 3 - 5 капель.
При отравлении, вызванном сероводородом (клоачный газ), больной жалуется на головную боль, головокружение, тошноту, рвоту, понос, обмороки. Выдыхаемый воздух обладает специфическим запахом. Бессознательное состояние. Расширение зрачков. Цианоз. Отек легких, паралич дыхания, судороги, кома. Смерть может наступить внезапно через несколько секунд или минут.
Лечение : то же, что и при отравлениях синильной кислотой, исключая введение тиосульфата натрия, для которого в данном случае нет никаких показаний.
Кровяные яды при попадании через рот также могут вызывать отравления. Таково, например, отравление бертолетовой солью (хлорновато-кислым калием), которая вызывает гемолиз и образование метгемоглобина. Существует опасность поражения почек.
Во всех случаях отравлений кровяными ядами через рот лечение необходимо начинать с обильного промывания желудка взвесью угля или 0,5% раствором марганцовокислого калия, который окисляет синильную кислоту в неядовитую циановую кислоту. Промывание можно производить 5% раствором тиосульфата натрия (образование неядовитых роданистых соединений). В остальном лечение такое же, как и при отравлении этими ядами через дыхательные пути.
В случае отравления бертолетовой солью необходимо промыть желудок, можно вызвать рвоту (апоморфин). Назначить обильное питье щелочных вод или просто раствора двууглекислой соды, слабительные соли. Кровопускание с последующим введением внутривенно 25 - 30 мл 5% раствора соды. Согревать тело пострадавшего грелками.
Читайте также:
- Можно ли принимать хилак форте при отравлении
- Сколько человек может не есть после отравления
- Пищевые отравление воздействие микроорганизмов на пищевые продукты
- Можно ли отравиться при зарядке аккумулятора
- Снять интоксикацию на дому г нерюнгри
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

